第二章 第2节 物质的微观粒子模型(同步课件 31张PPT)-2024-2025学年八年级科学(浙教版)
文档属性
| 名称 | 第二章 第2节 物质的微观粒子模型(同步课件 31张PPT)-2024-2025学年八年级科学(浙教版) |  | |
| 格式 | pptx | ||
| 文件大小 | 3.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-01-06 10:17:39 | ||
图片预览










文档简介
(共31张PPT)
2.2 物质的微观粒子模型
浙教版八年级科学下册
第二章 微粒的模型与符号
把照相机对着北极星附近的星空进行延时摄影,就会得到一张星星绕北极星运动的轨迹照片。通过这张照片,我们能否推断地球到底是怎样运动的
如果要设计一个飞行器,我们可以先做一个微缩模型(航模)进行试验研究。在对微观粒子的研究中,往往可利用放大的模型来解释小到难以观察的物体。
新课导入
一、构成物质的粒子模型
人们常用模型来表示分子由原子构成,因为这种方式更形象直观。我们曾用蓝球表示氧原子,用白球表示氢原子,用水分子、氧分子和氢分子构成的模型来反映水的电解过程,解释水的电解现象。我们也可以用同样的模型方法来表示各种不同的物质分子。
一、构成物质的粒子模型
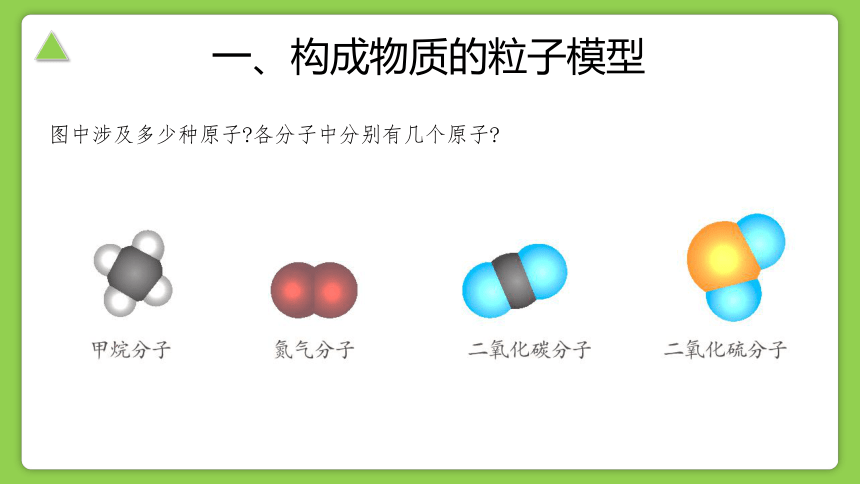
图中涉及多少种原子 各分子中分别有几个原子
一、构成物质的粒子模型
有的物质由分子构成,有的物质由原子直接构成。氢气、氧气、水、甲烷、二氧化碳等物质由分子构成;金属、稀有气体、碳、硅等物质由原子构成。
一、构成物质的粒子模型
①分子的定义
分子是由原子构成的,分子可以直接构成物质。在由分子构成的物质中,分子是保持物质化学性质的最小粒子。
注意:
①“保持”的含义是指构成物质的每一个分子与该物质的化学性质是一致的,分子不变,该物质的化学性质就不变,分子变化了,该物质的化学性质也发生相应改变。
②分子只能保持物质的化学性质,而物质的物理性质(如颜色、气味、状态等)需要大量分子聚集在一起共同体现,单个分子不能体现物质的物理性质。
③“最小”并不是绝对意义上的没有比它更小的粒子的意思,而是指对由分子构成的物质而言,分子是“保持物质化学性质的最小粒子”。
一、构成物质的粒子模型
②分子的性质
a.分子很小:肉眼看不见,需通过扫描隧道显微镜等显微设备来观察。
b.分子在永不停息地做无规则运动:温度升高,分子运动速度加快。如闻到远处的花香;湿衣服变干,且在阳光下干得快等。
一、构成物质的粒子模型
②分子的性质
c.分子之间有空隙:一般来说气体分子间的空隙较大,固体、液体分子间的空隙较小。因此气体容易被压缩,而固体、液体不易被压缩。“两种不同的液体混合后的总体积小于两者的体积之和”可以证明液体分子之间有空隙。
d.同种物质的分子化学性质相同,不同种物质的分子化学性质不同。
一、构成物质的粒子模型
③用分子的观点来解释由分子构成的物质发生的物理变化和化学变化
a.物理变化:分子本身不变,只是构成物质的分子间的距离发生了变化。如水的三态变化。
b.化学变化:分子本身发生变化,变成更小的微粒一-原子,而原子又重新结合成新的分子。如电解水时每个水分子分裂成两个氢原子和一个氧原子,每两个氢原子重新结合成一个氢分子,每两个氧原子重新结合成一个氧分子,即电解水时,水分子变成了氢分子和氧分子。
一、构成物质的粒子模型
(2)不同的分子
①分子种类繁多的原因原子种类和原子数量的搭配构成了丰富多彩的分子世界。
一、构成物质的粒子模型
(2)不同的分子
②分子的构成方式
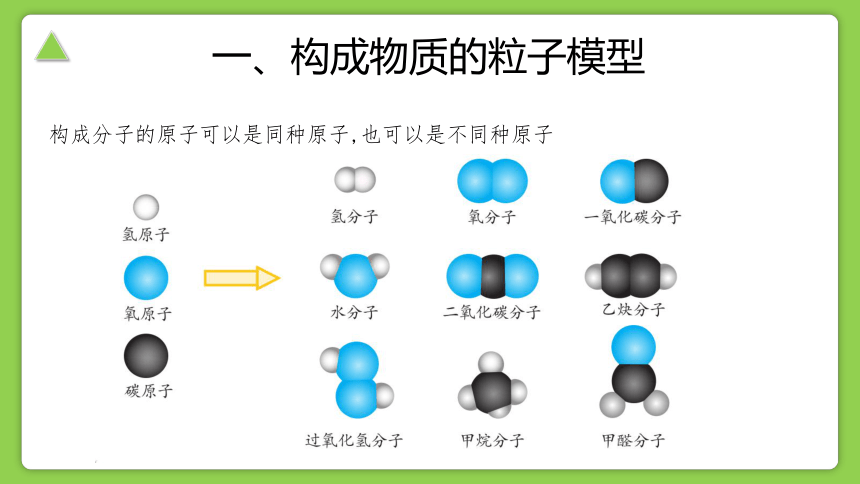
a.同种原子以不同的原子数量结合可以形成很多种分子。如1个氧分子由2个氧原子构成,1个臭氧分子由3个氧原子构成。
b.不同种原子以不同的原子数量结合也可以形成不同的分子。如1个水分子由2个氢原子和1个氧原子构成,1个过氧化氢分子由2个氢原子和2个氧原子构成。
一、构成物质的粒子模型
构成分子的原子可以是同种原子,也可以是不同种原子
一、构成物质的粒子模型
(2)不同的分子
③物质不同,分子构成不同物质的性质是由它自身的结构决定的:结构决定性质,性质反映结构。
一、构成物质的粒子模型
(3)原子
①原子的定义:原子是化学变化中的最小微粒(在化学变化中原子不能再分)。原子也可以直接构成物质。
一、构成物质的粒子模型
(3)原子
②同种原子在直接构成物质时,如果原子的排列方式不同,所形成的物质结构就不同,物质的物理性质也因此而不同。如金刚石和石墨都是由碳原子直接构成的,但由于它们的结构不同,因此物理性质及用途也不同。金刚石坚硬无比,可作钻头和刻刀;而石墨较软且有滑腻感,可用于制作铅笔芯和高温润滑剂。
一、构成物质的粒子模型
③分子和原子的区别与联系
分子 原子
本质区别 在化学变化中,分子可以再分再分 在化学变化中,原子不可以
相同点 ①质量和体积都很小;②都在不停地做无规则运动;③微粒间都有空隙;④同种微粒性质相同,不同种微粒性质不同;⑤都能直接构成物质
联系
思考与讨论
电解水的反应中,从微观的角度分析,什么发生了变化 什么没有变化
电解水的反应中发生了化学变化,水分子在通电条件下变成氢原子和氧原子,两个氢原子构成一个氢分子,两个氧原子构成一个氧分子。整个过程中氢原子和氧原子没有变化,水分子发生了变化。
例1. 图表示氢气和氧气发生的化学反应,下列说法正确的是( )
A.分子是化学变化中的最小微粒
B.每个氢分子由2个氢原子构成
C.每个水分子是由2个氢分子和1个氧原子构成的
D.化学反应前后原子数和分子数均不会发生变化
【答案】B
【解答】由氢分子的构成可知,每个氢分子由2个氢原子构成,故B说法正确;由水分子的构成可知,每个水分子是由2个氢原子和1个氧原子构成的,故C说法不正确;对比反应前后微粒的变化可知,化学反应前后,原子的数目和种类均不会发生改变,分子的种类一定发生改变,分子的数目不一定发生改变,故A、D说法不正确。
二、粒子的大小与质量
分子和原子都有一定的质量和体积。原子和分子的基本性质相同,体积都很小,原子半径一般在10-10米数量级。如碳原子的半径为0.6×10-10米。分子和原子的质量也非常小,1个碳原子的质量约为1.993×10-26千克。
粒子的大小与质量
粒子名称 原子半径 分子或原子质量
氢原子 0.78×10-10m 1.674 ×10-27kg
碳原子 0.77×10-10m 1.993 ×10-26kg
氧原子 0.66×10-10m 2.657 ×10-26kg
氢分子 3.348 ×10-27kg
二氧化碳分子 7.307 ×10-26kg
说明:
不同种类的分子和原子质量不同,体积也不相同。不能认为所有分子的质量和体积一定大于原子的质量和体积,只能理解为分子的质量和体积一定大于构成这种分子的原子的质量和体积。原子的体积(质量)也可以比分子大,例如,一个氧原子的质量约为一个氢分子质量的8倍。
思考与讨论:
已知一粒米的质量约为2.1×10-5千克,如果等分这粒米,要分多少次才能把它分到10-27千克。
74次
例2.下列叙述中正确的是( )
A.分子是由原子构成的,因此分子的质量一定比原子大
B.分子是由原子构成的,因此分子的体积一定比原子大
C.1个氢原子的质量大约为1粒米质量的1%
D.分子的质量和体积一定比构成它的原子的质量和体积大
【答案】D
【解答】分子的质量和体积一定比构成它的原子的质量和体积大,如氢分子的质量和体积肯定比构成它的氢原子的质量和体积大,但分子的质量和体积并不一定比所有原子的质量和体积大,例如,一个氧原子的质量大约是一个氢分子质量的8倍。氢原子的质量在10-27千克的数量级,一粒米的质量在10-5千克的数量级,两者的质量差距远远大于1%。
下列各图中●和〇分别表示氢原子和氧原子,其中能表示保持H2O化学性质的微粒是( )
课堂小练习
【答案】A
【解析】A、能表示水分子,能保持H2O化学性质的,故A符合题意;B、该图是氢分子和氧分子的混合气体,不能保持H2O化学性质,故B不符合题意;C、该图是氢气,不能保持H2O化学性质,故C不符合题意;D、该图表示氢原子和氧原子,不能保持H2O化学性质,故D不符合题意。故选:A。
两只分别装有空气和二氧化氮气体的玻璃瓶,瓶口相对中间用玻璃板隔开,如图甲。装置的微观模型用图乙表示,其中“●“代表空气粒子,“〇“代表二氧化氮分子。抽去玻璃板,紧贴瓶口,一段时间后瓶中微粒分布情况可表示为( )
【答案】A
【解析】空气分子和二氧化氮分子都在不停地运动,打开玻璃板后,空气分子会进入二氧化氮分子中间空隙,而二氧化氮分子会进入空气分子的空隙,从而使右边颜色变浅,左边颜色变深。当达到一定时间后,左右两个瓶子内的分子分布均匀,即两边的颜色是一致的。故选A。
课堂小练习
推理是初中科学常用的思维方法。下列推理正确的是( )
①离子是带电荷的微粒,所以带电荷的微粒一定是离子;
②同种元素质子数相同,所以质子数相同的微粒一定是同一种元素;
③单质中只含一种元素,所以由一种元素组成的物质一定是单质
A.只有① B.只有②
C.只有③ D.①②③都不正确
课堂小练习
【答案】D
【解析】①离子是带电荷的微粒,带电荷的微粒不一定是离子,也可能是质子等,故推理错误。②同种元素质子数相同,但质子数相同的微粒不一定是同一种元素,如水分子和氖原子,故推理错误。③单质中只含一种元素,但由同种元素组成的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物、金刚石和石墨的混合物等,故推理错误。故①②③都不正确。
故选:D。
课堂小练习
【答案】A
【解析】A、氯化钠是含有金属元素和非金属元素的化合物,是由钠离子和氯离子构成的,故选项正确。B、氢气属于气态非金属单质,是由氢分子构成的,故选项错误。C、二氧化硫是由非金属元素组成的化合物,是由二氧化硫分子构成的,故选项错误。D、银属于金属单质,是由银原子直接构成的,故选项错误。
故选:A。
构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是( )
A.氯化钠 B.氢气 C.二氧化硫 D.金属银
课堂小练习
【答案】C
【解析】A、H2O2中含有氢元素,分子中含有氢原子,但不含有氢分子,故A错误。
B、H2O中含有氢元素,分子中含有氢原子,但不含有氢分子,故B错误;
C、H2由大量的氢气分子构成,故C正确;
D、Ca(OH)2中含有氢元素,分子中含有氢原子,但不含有氢分子,故D错误;
故选:C。
下列物质中含有氢分子的是( )
A.H2O2 B.H2O C.H2 D.Ca(OH)2
课堂小练习
最近,科学家制造出了含4个氧原子的新型“氧分子”,而一个氧气分子是由2个氧原子构成的,针对以上事实,下列说法中错误的是( )
A.新型“氧分子”与氧气分子都是由氧原子构成的
B.每个新型“氧分子”与每个氧气分子含有氧原子个数不同
C.氧气分子与新型“氧分子”的化学性质应该有不同之处
D.一个新型“氧分子”由2个氧气分子构成
【答案】D
【解析】A、氧分子是由两个氧原子构成的,新型“氧分子”是由4个氧原子构成的,故A说法正确;B、4个氧原子的新型“氧分子”,而氧分子是由2个氧原子构成的,故B说法正确;C、同种分子性质相同,不同分子性质不同,故C说法正确;D、新型“氧分子”是由4个氧原子构成,不是由2个氧气分子构成,故D说法错误。
故选:D。
课堂小练习
西溪湿地以独特的风光和生态环境,形成了极富吸引力的湿地景观旅游资源。湿地空气质量优良率高,参与空气质量评价的污染物主要为细颗粒物、可吸入颗粒物、二氧化硫、二氧化氮、臭氧、一氧化碳等六项,其中SO2、NO2、CO这三种分子中都含有( )
A.氧分子 B.氧元素 C.氧原子 D.氧气
【答案】C
【解析】A、氧气是由氧分子构成的,SO2、NO2、CO这三种分子中均不含氧分子,故A不合题意;
B、分子是由原子构成的,因此SO2、NO2、CO这三种分子中均含氧原子,而不是氧元素,故B不合题意;
C、分子是由原子构成的,因此SO2、NO2、CO这三种分子中均含氧原子,故C符合题意;
D、SO2、NO2、CO这三种分子中均含氧原子,不含氧气,故D不合题意。
故选:C。
课堂小结
2.2 物质的微观粒子模型
浙教版八年级科学下册
第二章 微粒的模型与符号
把照相机对着北极星附近的星空进行延时摄影,就会得到一张星星绕北极星运动的轨迹照片。通过这张照片,我们能否推断地球到底是怎样运动的
如果要设计一个飞行器,我们可以先做一个微缩模型(航模)进行试验研究。在对微观粒子的研究中,往往可利用放大的模型来解释小到难以观察的物体。
新课导入
一、构成物质的粒子模型
人们常用模型来表示分子由原子构成,因为这种方式更形象直观。我们曾用蓝球表示氧原子,用白球表示氢原子,用水分子、氧分子和氢分子构成的模型来反映水的电解过程,解释水的电解现象。我们也可以用同样的模型方法来表示各种不同的物质分子。
一、构成物质的粒子模型
图中涉及多少种原子 各分子中分别有几个原子
一、构成物质的粒子模型
有的物质由分子构成,有的物质由原子直接构成。氢气、氧气、水、甲烷、二氧化碳等物质由分子构成;金属、稀有气体、碳、硅等物质由原子构成。
一、构成物质的粒子模型
①分子的定义
分子是由原子构成的,分子可以直接构成物质。在由分子构成的物质中,分子是保持物质化学性质的最小粒子。
注意:
①“保持”的含义是指构成物质的每一个分子与该物质的化学性质是一致的,分子不变,该物质的化学性质就不变,分子变化了,该物质的化学性质也发生相应改变。
②分子只能保持物质的化学性质,而物质的物理性质(如颜色、气味、状态等)需要大量分子聚集在一起共同体现,单个分子不能体现物质的物理性质。
③“最小”并不是绝对意义上的没有比它更小的粒子的意思,而是指对由分子构成的物质而言,分子是“保持物质化学性质的最小粒子”。
一、构成物质的粒子模型
②分子的性质
a.分子很小:肉眼看不见,需通过扫描隧道显微镜等显微设备来观察。
b.分子在永不停息地做无规则运动:温度升高,分子运动速度加快。如闻到远处的花香;湿衣服变干,且在阳光下干得快等。
一、构成物质的粒子模型
②分子的性质
c.分子之间有空隙:一般来说气体分子间的空隙较大,固体、液体分子间的空隙较小。因此气体容易被压缩,而固体、液体不易被压缩。“两种不同的液体混合后的总体积小于两者的体积之和”可以证明液体分子之间有空隙。
d.同种物质的分子化学性质相同,不同种物质的分子化学性质不同。
一、构成物质的粒子模型
③用分子的观点来解释由分子构成的物质发生的物理变化和化学变化
a.物理变化:分子本身不变,只是构成物质的分子间的距离发生了变化。如水的三态变化。
b.化学变化:分子本身发生变化,变成更小的微粒一-原子,而原子又重新结合成新的分子。如电解水时每个水分子分裂成两个氢原子和一个氧原子,每两个氢原子重新结合成一个氢分子,每两个氧原子重新结合成一个氧分子,即电解水时,水分子变成了氢分子和氧分子。
一、构成物质的粒子模型
(2)不同的分子
①分子种类繁多的原因原子种类和原子数量的搭配构成了丰富多彩的分子世界。
一、构成物质的粒子模型
(2)不同的分子
②分子的构成方式
a.同种原子以不同的原子数量结合可以形成很多种分子。如1个氧分子由2个氧原子构成,1个臭氧分子由3个氧原子构成。
b.不同种原子以不同的原子数量结合也可以形成不同的分子。如1个水分子由2个氢原子和1个氧原子构成,1个过氧化氢分子由2个氢原子和2个氧原子构成。
一、构成物质的粒子模型
构成分子的原子可以是同种原子,也可以是不同种原子
一、构成物质的粒子模型
(2)不同的分子
③物质不同,分子构成不同物质的性质是由它自身的结构决定的:结构决定性质,性质反映结构。
一、构成物质的粒子模型
(3)原子
①原子的定义:原子是化学变化中的最小微粒(在化学变化中原子不能再分)。原子也可以直接构成物质。
一、构成物质的粒子模型
(3)原子
②同种原子在直接构成物质时,如果原子的排列方式不同,所形成的物质结构就不同,物质的物理性质也因此而不同。如金刚石和石墨都是由碳原子直接构成的,但由于它们的结构不同,因此物理性质及用途也不同。金刚石坚硬无比,可作钻头和刻刀;而石墨较软且有滑腻感,可用于制作铅笔芯和高温润滑剂。
一、构成物质的粒子模型
③分子和原子的区别与联系
分子 原子
本质区别 在化学变化中,分子可以再分再分 在化学变化中,原子不可以
相同点 ①质量和体积都很小;②都在不停地做无规则运动;③微粒间都有空隙;④同种微粒性质相同,不同种微粒性质不同;⑤都能直接构成物质
联系
思考与讨论
电解水的反应中,从微观的角度分析,什么发生了变化 什么没有变化
电解水的反应中发生了化学变化,水分子在通电条件下变成氢原子和氧原子,两个氢原子构成一个氢分子,两个氧原子构成一个氧分子。整个过程中氢原子和氧原子没有变化,水分子发生了变化。
例1. 图表示氢气和氧气发生的化学反应,下列说法正确的是( )
A.分子是化学变化中的最小微粒
B.每个氢分子由2个氢原子构成
C.每个水分子是由2个氢分子和1个氧原子构成的
D.化学反应前后原子数和分子数均不会发生变化
【答案】B
【解答】由氢分子的构成可知,每个氢分子由2个氢原子构成,故B说法正确;由水分子的构成可知,每个水分子是由2个氢原子和1个氧原子构成的,故C说法不正确;对比反应前后微粒的变化可知,化学反应前后,原子的数目和种类均不会发生改变,分子的种类一定发生改变,分子的数目不一定发生改变,故A、D说法不正确。
二、粒子的大小与质量
分子和原子都有一定的质量和体积。原子和分子的基本性质相同,体积都很小,原子半径一般在10-10米数量级。如碳原子的半径为0.6×10-10米。分子和原子的质量也非常小,1个碳原子的质量约为1.993×10-26千克。
粒子的大小与质量
粒子名称 原子半径 分子或原子质量
氢原子 0.78×10-10m 1.674 ×10-27kg
碳原子 0.77×10-10m 1.993 ×10-26kg
氧原子 0.66×10-10m 2.657 ×10-26kg
氢分子 3.348 ×10-27kg
二氧化碳分子 7.307 ×10-26kg
说明:
不同种类的分子和原子质量不同,体积也不相同。不能认为所有分子的质量和体积一定大于原子的质量和体积,只能理解为分子的质量和体积一定大于构成这种分子的原子的质量和体积。原子的体积(质量)也可以比分子大,例如,一个氧原子的质量约为一个氢分子质量的8倍。
思考与讨论:
已知一粒米的质量约为2.1×10-5千克,如果等分这粒米,要分多少次才能把它分到10-27千克。
74次
例2.下列叙述中正确的是( )
A.分子是由原子构成的,因此分子的质量一定比原子大
B.分子是由原子构成的,因此分子的体积一定比原子大
C.1个氢原子的质量大约为1粒米质量的1%
D.分子的质量和体积一定比构成它的原子的质量和体积大
【答案】D
【解答】分子的质量和体积一定比构成它的原子的质量和体积大,如氢分子的质量和体积肯定比构成它的氢原子的质量和体积大,但分子的质量和体积并不一定比所有原子的质量和体积大,例如,一个氧原子的质量大约是一个氢分子质量的8倍。氢原子的质量在10-27千克的数量级,一粒米的质量在10-5千克的数量级,两者的质量差距远远大于1%。
下列各图中●和〇分别表示氢原子和氧原子,其中能表示保持H2O化学性质的微粒是( )
课堂小练习
【答案】A
【解析】A、能表示水分子,能保持H2O化学性质的,故A符合题意;B、该图是氢分子和氧分子的混合气体,不能保持H2O化学性质,故B不符合题意;C、该图是氢气,不能保持H2O化学性质,故C不符合题意;D、该图表示氢原子和氧原子,不能保持H2O化学性质,故D不符合题意。故选:A。
两只分别装有空气和二氧化氮气体的玻璃瓶,瓶口相对中间用玻璃板隔开,如图甲。装置的微观模型用图乙表示,其中“●“代表空气粒子,“〇“代表二氧化氮分子。抽去玻璃板,紧贴瓶口,一段时间后瓶中微粒分布情况可表示为( )
【答案】A
【解析】空气分子和二氧化氮分子都在不停地运动,打开玻璃板后,空气分子会进入二氧化氮分子中间空隙,而二氧化氮分子会进入空气分子的空隙,从而使右边颜色变浅,左边颜色变深。当达到一定时间后,左右两个瓶子内的分子分布均匀,即两边的颜色是一致的。故选A。
课堂小练习
推理是初中科学常用的思维方法。下列推理正确的是( )
①离子是带电荷的微粒,所以带电荷的微粒一定是离子;
②同种元素质子数相同,所以质子数相同的微粒一定是同一种元素;
③单质中只含一种元素,所以由一种元素组成的物质一定是单质
A.只有① B.只有②
C.只有③ D.①②③都不正确
课堂小练习
【答案】D
【解析】①离子是带电荷的微粒,带电荷的微粒不一定是离子,也可能是质子等,故推理错误。②同种元素质子数相同,但质子数相同的微粒不一定是同一种元素,如水分子和氖原子,故推理错误。③单质中只含一种元素,但由同种元素组成的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物、金刚石和石墨的混合物等,故推理错误。故①②③都不正确。
故选:D。
课堂小练习
【答案】A
【解析】A、氯化钠是含有金属元素和非金属元素的化合物,是由钠离子和氯离子构成的,故选项正确。B、氢气属于气态非金属单质,是由氢分子构成的,故选项错误。C、二氧化硫是由非金属元素组成的化合物,是由二氧化硫分子构成的,故选项错误。D、银属于金属单质,是由银原子直接构成的,故选项错误。
故选:A。
构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是( )
A.氯化钠 B.氢气 C.二氧化硫 D.金属银
课堂小练习
【答案】C
【解析】A、H2O2中含有氢元素,分子中含有氢原子,但不含有氢分子,故A错误。
B、H2O中含有氢元素,分子中含有氢原子,但不含有氢分子,故B错误;
C、H2由大量的氢气分子构成,故C正确;
D、Ca(OH)2中含有氢元素,分子中含有氢原子,但不含有氢分子,故D错误;
故选:C。
下列物质中含有氢分子的是( )
A.H2O2 B.H2O C.H2 D.Ca(OH)2
课堂小练习
最近,科学家制造出了含4个氧原子的新型“氧分子”,而一个氧气分子是由2个氧原子构成的,针对以上事实,下列说法中错误的是( )
A.新型“氧分子”与氧气分子都是由氧原子构成的
B.每个新型“氧分子”与每个氧气分子含有氧原子个数不同
C.氧气分子与新型“氧分子”的化学性质应该有不同之处
D.一个新型“氧分子”由2个氧气分子构成
【答案】D
【解析】A、氧分子是由两个氧原子构成的,新型“氧分子”是由4个氧原子构成的,故A说法正确;B、4个氧原子的新型“氧分子”,而氧分子是由2个氧原子构成的,故B说法正确;C、同种分子性质相同,不同分子性质不同,故C说法正确;D、新型“氧分子”是由4个氧原子构成,不是由2个氧气分子构成,故D说法错误。
故选:D。
课堂小练习
西溪湿地以独特的风光和生态环境,形成了极富吸引力的湿地景观旅游资源。湿地空气质量优良率高,参与空气质量评价的污染物主要为细颗粒物、可吸入颗粒物、二氧化硫、二氧化氮、臭氧、一氧化碳等六项,其中SO2、NO2、CO这三种分子中都含有( )
A.氧分子 B.氧元素 C.氧原子 D.氧气
【答案】C
【解析】A、氧气是由氧分子构成的,SO2、NO2、CO这三种分子中均不含氧分子,故A不合题意;
B、分子是由原子构成的,因此SO2、NO2、CO这三种分子中均含氧原子,而不是氧元素,故B不合题意;
C、分子是由原子构成的,因此SO2、NO2、CO这三种分子中均含氧原子,故C符合题意;
D、SO2、NO2、CO这三种分子中均含氧原子,不含氧气,故D不合题意。
故选:C。
课堂小结
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
