3.4二氧化碳
图片预览


文档简介
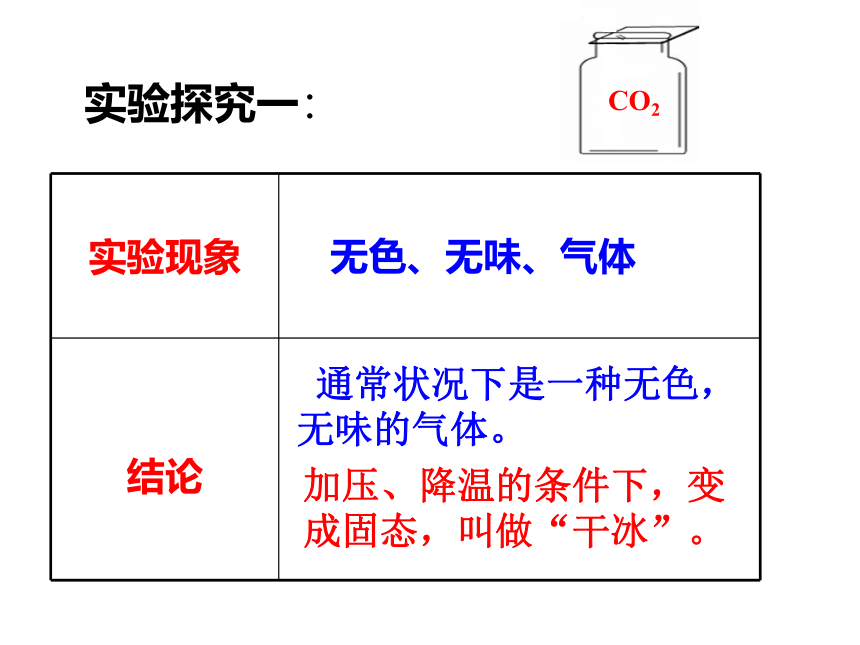
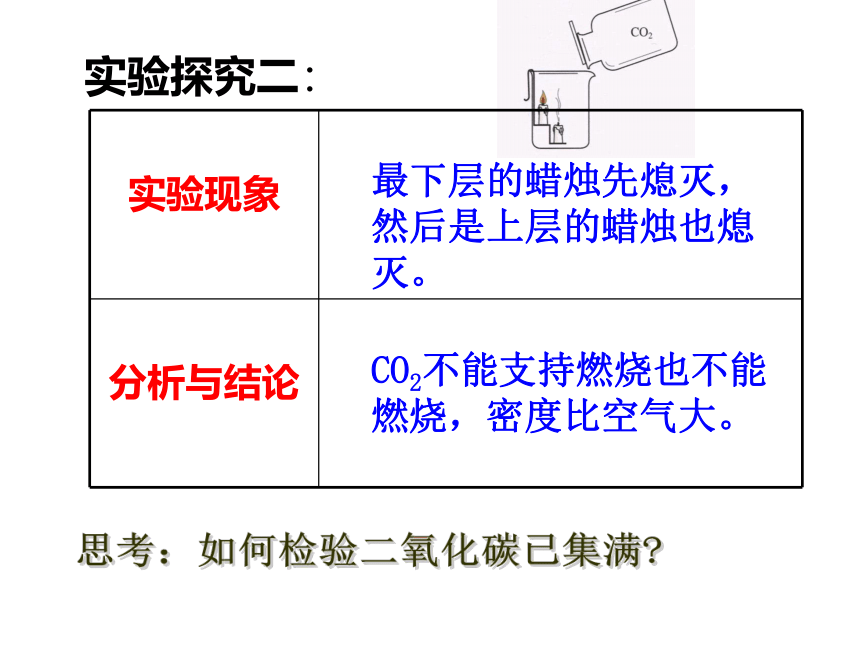
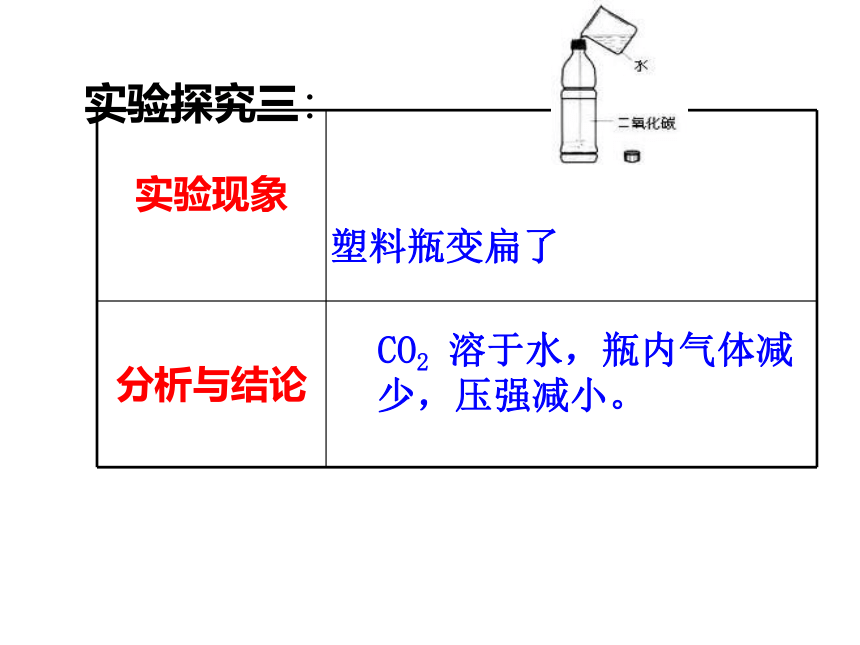
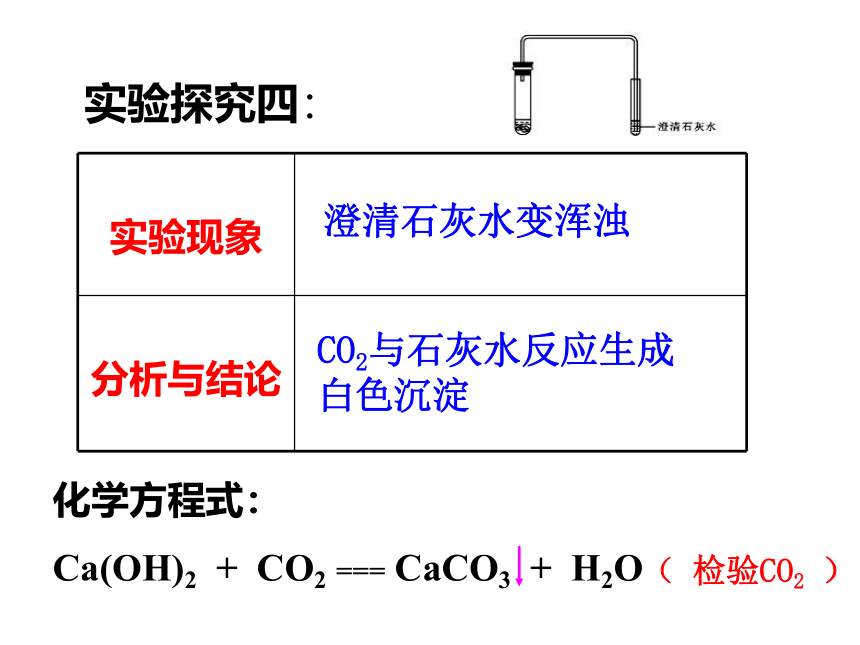
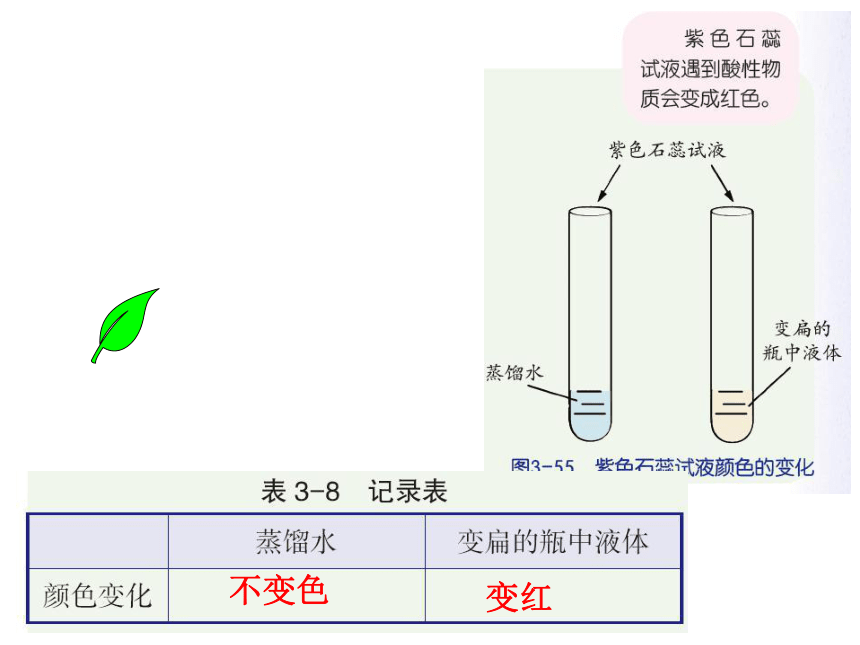
课件19张PPT。自然界中的二氧化碳二氧化碳气体由大量二氧化碳分子构成。二氧化碳分子由一个碳原子和两个氧子构成。CO2本身没有毒性。CO2 实验探究一: 通常状况下是一种无色,无味的气体。无色、无味、气体CO2加压、降温的条件下,变成固态,叫做“干冰”。 实验探究二: 最下层的蜡烛先熄灭,然后是上层的蜡烛也熄灭。CO2不能支持燃烧也不能燃烧,密度比空气大。思考:如何检验二氧化碳已集满? 实验探究三: 塑料瓶变扁了CO2 溶于水,瓶内气体减少,压强减小。 实验探究四: 澄清石灰水变浑浊CO2与石灰水反应生成白色沉淀( 检验CO2 )变红不变色二氧化碳的性质气态 无色 无味 比空气大 能溶于水一般情况下不能燃烧,也不支持燃烧4.无毒,但不能供给呼吸一 、实验室制取二氧化碳的反应原理实验1:稀盐酸与大理石(或石灰石)反应
现象分析有大量气泡产生,大理石逐渐溶解该反应在常温下进行,反应速度适中,便于控制。大理石与稀盐酸反应生成了碳酸和氯化钙:
CaCO3+2HCl=CaCl2+H2CO3碳酸很不稳定,分解成水和二氧化碳:H2CO3=H2O+CO2总反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2实验2:稀硫酸与大理石(或石灰石)反应现象分析刚开始有大量气泡产生,一时间后,气泡逐渐
减少 ,反应逐渐停止。虽然该反应能生成二氧化碳:
CaCO3+H2SO4==CaSO4+H2O+CO2
但生成的CaSO4微溶于水,覆盖在大理石表面,
形成一层薄膜,使大理石与酸不能接触,反应难
以进行。结论实验室制取二氧化碳不能用稀硫酸代替稀盐酸
实验室制取气体的装置气体发生装置气体收集装置反应物的状态固体和固体反应固体和液体反应液体和液体反应反应条件(是否需要加热、加催化剂等)。。。设计实验室制取气体的装置排空气法密度比空气的大——向上排空气法密度比空气的小——向下排空气法排水法(不易溶于水、不与水发生反应)实验室制取二氧化碳的操作步骤连接仪器
①检查气密性
②加大理石
③加稀盐酸
④收集气体
⑤1、怎样检验生成的气体是二氧化碳?答:将生成的气体通入澄清的石灰水,石灰水变浑浊,证明生成的气体 是二氧化碳。讨论2、怎样检验二氧化碳是否收集满?答:用燃着的木条接近集气瓶口,如果木条熄灭,证明已满。课堂练习 下图为实验室制取二氧化碳的装置图,有哪些
错误?为什么?请改正?C课堂练习1 实验室制取氧气的发生装置应选择______,收集装置应选择______。
3 实验室制取二氧化碳的发生装置应选择______,收集装置应选择______。
AD EB CDFCa + Cl=CaCl2+ + CO2↑CO3CO3 课堂小结1)反应原理2)装置图3)收集方法4)检验方法二氧化碳
实验室制法向上排空气法将气体通入澄清石灰水或向集气瓶倒入少量澄清石灰水,澄清石灰水变浑浊2H2HH2O 二氧化碳的应用
现象分析有大量气泡产生,大理石逐渐溶解该反应在常温下进行,反应速度适中,便于控制。大理石与稀盐酸反应生成了碳酸和氯化钙:
CaCO3+2HCl=CaCl2+H2CO3碳酸很不稳定,分解成水和二氧化碳:H2CO3=H2O+CO2总反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2实验2:稀硫酸与大理石(或石灰石)反应现象分析刚开始有大量气泡产生,一时间后,气泡逐渐
减少 ,反应逐渐停止。虽然该反应能生成二氧化碳:
CaCO3+H2SO4==CaSO4+H2O+CO2
但生成的CaSO4微溶于水,覆盖在大理石表面,
形成一层薄膜,使大理石与酸不能接触,反应难
以进行。结论实验室制取二氧化碳不能用稀硫酸代替稀盐酸
实验室制取气体的装置气体发生装置气体收集装置反应物的状态固体和固体反应固体和液体反应液体和液体反应反应条件(是否需要加热、加催化剂等)。。。设计实验室制取气体的装置排空气法密度比空气的大——向上排空气法密度比空气的小——向下排空气法排水法(不易溶于水、不与水发生反应)实验室制取二氧化碳的操作步骤连接仪器
①检查气密性
②加大理石
③加稀盐酸
④收集气体
⑤1、怎样检验生成的气体是二氧化碳?答:将生成的气体通入澄清的石灰水,石灰水变浑浊,证明生成的气体 是二氧化碳。讨论2、怎样检验二氧化碳是否收集满?答:用燃着的木条接近集气瓶口,如果木条熄灭,证明已满。课堂练习 下图为实验室制取二氧化碳的装置图,有哪些
错误?为什么?请改正?C课堂练习1 实验室制取氧气的发生装置应选择______,收集装置应选择______。
3 实验室制取二氧化碳的发生装置应选择______,收集装置应选择______。
AD EB CDFCa + Cl=CaCl2+ + CO2↑CO3CO3 课堂小结1)反应原理2)装置图3)收集方法4)检验方法二氧化碳
实验室制法向上排空气法将气体通入澄清石灰水或向集气瓶倒入少量澄清石灰水,澄清石灰水变浑浊2H2HH2O 二氧化碳的应用
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
