2.5表示元素的符号(第2课时) 同步练习(含解析)
文档属性
| 名称 | 2.5表示元素的符号(第2课时) 同步练习(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 256.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-01-07 00:00:00 | ||
图片预览




文档简介
2.5表示元素的符号(第二课时)
一、选择题
1.碘盐中含有一定量的碘酸钾。我省实施新的碘盐含碘量标准,碘盐中碘含量从每千克 35 毫克降至 25 毫克。这里的“碘”是指( )
A.碘原子 B.碘分子 C.碘元素 D.碘单质
2.下列元素符号中书写正确的是( )
A.MG B.CA C.Fe D.f
3.锆被誉为原子时代的“第一号金属”,广泛应用于航空航天、精密铸造等领域。如图是锆元素在元素周期表中的信息,从中不能直接获得该元素的信息是( )
A.原子半径 B.元素符号
C.元素名称 D.相对原子质量
4.5G时代已经来临,高纯度单质硅(Si)是制作芯片的材料,如图是硅元素在元素周期表中的信息,则该硅原子的核外电子数为( )
A.14 B.15 C.28 D.29
5.钷可为航天器提供动力。钷元素在元素周期表中的信息如图所示,下列说法错误的是( )
A.钷的原子序数为61 B.钷的元素符号为Pm,钷是非金属
C.钷原子的核外电子数为61 D.钷元素的相对原子质量为145
6.下列关于Hg的说法不正确的是( )
A.表示一个汞原子
B.表示汞这种物质
C.表示汞这种元素
D.表示一个汞分子
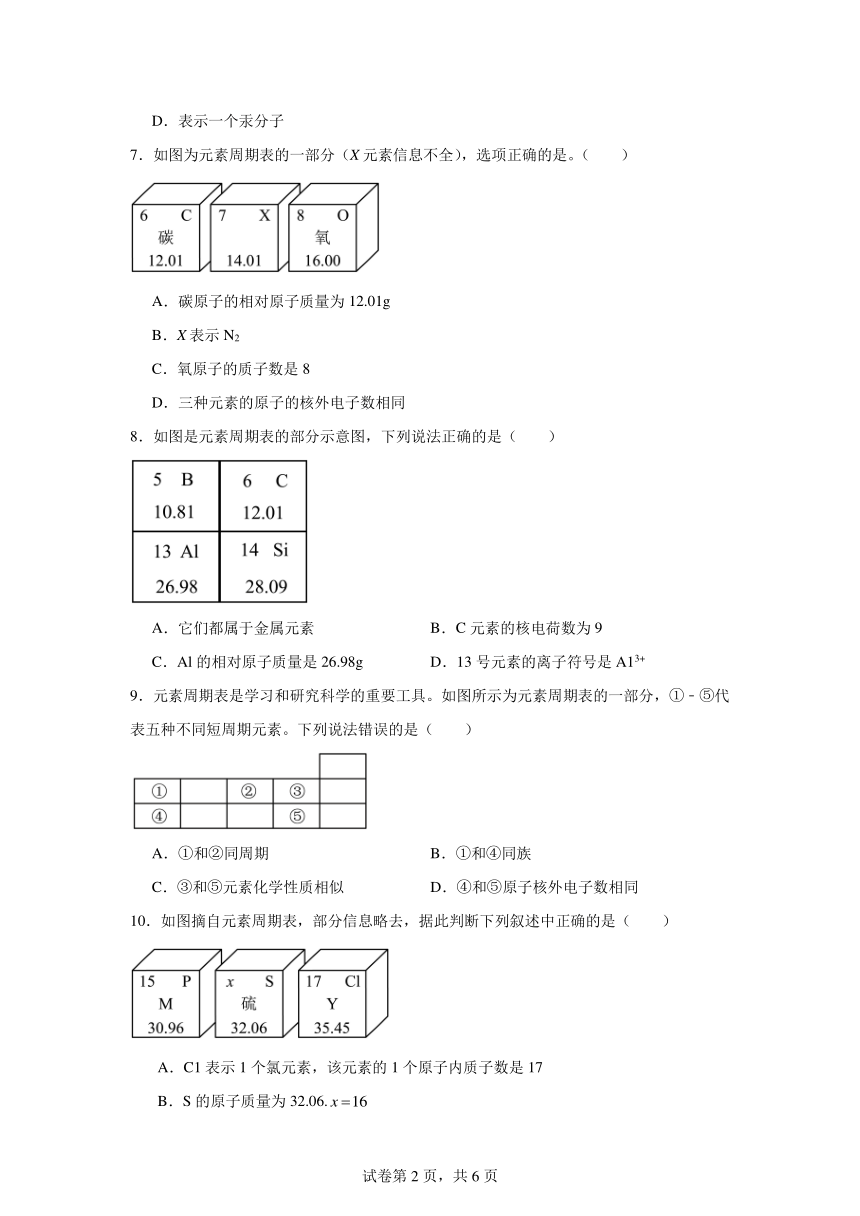
7.如图为元素周期表的一部分(X元素信息不全),选项正确的是。( )
A.碳原子的相对原子质量为12.01g
B.X表示N2
C.氧原子的质子数是8
D.三种元素的原子的核外电子数相同
8.如图是元素周期表的部分示意图,下列说法正确的是( )
A.它们都属于金属元素 B.C元素的核电荷数为9
C.Al的相对原子质量是26.98g D.13号元素的离子符号是A13+
9.元素周期表是学习和研究科学的重要工具。如图所示为元素周期表的一部分,①﹣⑤代表五种不同短周期元素。下列说法错误的是( )
A.①和②同周期 B.①和④同族
C.③和⑤元素化学性质相似 D.④和⑤原子核外电子数相同
10.如图摘自元素周期表,部分信息略去,据此判断下列叙述中正确的是( )
A.C1表示1个氯元素,该元素的1个原子内质子数是17
B.S的原子质量为32.06.
C.三种都是非金属元素,它们分别形成的单质常温下均是固态
D.三种元素在周期表中属于同一周期
11.下列化学用语,通常只表示微观意义,而不表示宏观意义的是 。
A.Ca B.N C.2N D.He
12.法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是( )
A.该粒子不显电性
B.该粒子质量数为4
C.与氢元素的质子数相同
D.该粒子质量比氢原子大
13.在元素周期表中的下列四种元素,属于金属元素的是( )
A. B.
C. D.
14.下列符号,既表示一种元素,又能表示该元素的一个原子,还能表示该元素组成的单质的是 ()
A.N2 B.3Fe C.Al D.H
15.由同种元素组成的物质一定不是( )
A.纯净物 B.单质 C.化合物 D.混合物
二、填空题
16.写出元素符号或元素名称
(1)N (2)镁 (3)Al (4)磷 (5)Cl (6)铁 (7)铜 (8)Ag
17.化学符号“Cu”能表示多种意义(1) ;(2) ;(3)
18.请写出下列符号的含义或根据要求写出符号:
(1)3H: 。
(2)Cl: 。
(3)Fe: 。
(4)氧元素: 。
(5)5个铝原子: 。
(6)n个钠原子: 。
19.元素周期表中,同一周期从左到右,元素原子的质子数逐渐 (增加或减少),同一族元素的 (化学或物理)性质都很相似。
20.合成化学元素113号(Nh)、115号(Mc 镆)。
(1)其中,“115号(Mc)”中115表示原子的 。
(2)镆的相对原子质量是288,其中子数为 。
21.默写1~20号元素的符号
1 2 3 4 5 6 7 8 9 10
He Li Be B F Ne
11 12 13 14 15 16 17 18 19 20
Si P Ar K
22.人类在探索物质世界和微观世界的历史长河中,充满了智慧。请你回答相关问题。
(1)下面的科学家中最早发现电子的是 (填字母)。
A.道尔顿 B.汤姆森 C.卢瑟福 D.门捷列夫
(2)原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,科学家都运用了 来表达他们的理论成果。
(3)碳—12、碳—13、碳—14都是碳元素的原子,它们的主要差别在于 。
(4)人们很早就意识到物质都是由几种亘古不变的基本成分“元素”组成的。如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?你的观点及依据是 。
23.元素周期表是学习科学的重要工具,下表是元素周期表的部分信息。请分析表中信息,回答下列问题。
(1)硫元素的原子序数是 。
(2)第15号元素属于 元素(填“金属”或“非金属”)。
(3)下列各组元素不具有相似化学性质的是 (填字母)。
A.Li 和Na B.Be 和 Mg C.Al 和 Si D.F 和 Cl
24.2019年是“国际化学元素周期表年”,以纪念俄国化学家门捷列夫在1869年发明第一张元素周期表150周年。门捷列夫将当时已知的63种元素依据相对原子质量大小并以表的形式排列,将相似化学性质的元素放在同一列中,制成了元素周期表的雏形。
(1)钔的质子数为101,中子数为157,相对原子质量为258,则其核外电子数为 ;
(2)在1869年之前,许多化学家就对当时已知的元素进行排列。但国际上公认把发明元素周期律的桂冠戴在了门捷列夫的头上,你推测可能的原因是 。
A.门捷列夫按照相对原子质量排列元素,这也是现在元素周期表元素排列的标准
B.门捷列夫以“相似化学性质的元素放同一列”原则修正一些元素的相对原子质量
C.门捷列夫发明的元素周期表完全是他的独创,并不需要吸收别人的研究成果
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实
E.门捷列夫当时在科学界威望极高,他的发明成果更能让人信服
25.化学元素组成万物。人们很早就意识到物质都是由几种亘古不变的基本成分——“元素”组成的。
(1)古人曾认为水是组成物质的元素之一。在你学过的知识中能说明“水不是元素“的实验事实是 ;
(2)现代化学对“元素"做了科学定义,图甲是两个微粒的结构模型示意图,小科认为这两个微粒不属于同种元素,你认为他的依据是 ;
(3)1869年,俄国化学家门捷列夫在前人研究的基础上制作出第一张元素周期表,图乙是元素周期表的部分内容,表中空白格处元素原子的质子数为 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 C C A A B D C D D D
题号 11 12 13 14 15
答案 C C A C C
1.C
【详解】试题分析:元素是具有相同核电荷数的同一类原子的总称。题中的碘指的是碘元素。
考点:元素的概念;人体的元素组成与元素对人体健康的重要作用。
点评:本题主要考查了日常生活用品中的元素组成问题。
2.C
【详解】元素符号的书写要满足“一大二小”的要求,即:只有一个字母时要大写,有两个字母时第一个字母大写,第二个字母小写,故选C。
3.A
【详解】A、根据元素周期表中的一格可知,不能直接体现原子半径,故选项正确;
B、根据元素周期表中的一格可知,字母表示该元素的元素符号,能直接体现,故选项错误;
C、根据元素周期表中的一格可知,中间的汉字表示该元素的元素名称,能直接体现,故选项错误;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,能直接体现,故选项错误。
故选A。
4.A
【详解】根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为14;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为14。故选A。
5.B
【详解】A、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为61,故选项说法正确;
B、根据元素周期表中的一格可知,字母表示该元素的元素符号,钷的元素符号为Pm, 钷带“钅”字旁,属于金属元素,故选项说法错误;
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为61;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为61,故选项说法正确;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为145,故选项说法正确。
故选B。
6.D
【分析】元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义。
【详解】A、Hg属于金属元素,可表示一个汞原子,故选项说法正确。
B、Hg属于金属元素,可表示汞这一纯净物,故选项说法正确。
C、Hg属于金属元素,可表示汞元素,故选项说法正确。
D、Hg属于金属单质,是由汞原子直接构成的,故选项说法错误。
故选D。
7.C
【详解】A、元素信息图中最下方的数字是原子的相对原子质量,由图可知,碳原子的相对原子质量为12.01,选项错误;
B、原子序数为7的元素为氮元素,其元素符号为N,即X为N,选项错误;
C、元素信息图左上角的数字为原子序数,原子序数等于原子的质子数,由图可知,氧原子的质子数是8,选项正确;
D、碳原子核外电子数为6,氮原子核外电子数为7,氧原子核外电子数为8,三种元素的原子核外电子数不相同,选项错误;
故选C。
8.D
【详解】A、铝(Al)元素名称都有“钅”字偏旁,属于金属元素,B(硼)、C(碳)、Si(硅)元素名称都有“石”字旁,属于固态非金属元素属于非金属元素,故A错误;
B、根据碳元素周期表中的一格可知,左上角的数字为6,表示原子序数为6;根据原子序数=核电荷数,则该元素的原子核电荷数为6,错误;
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为26.98,相对原子质量单位是“1”,不是“克”,错误;
D、13号元素为铝元素,核外电子排布为2,8,3,最外层电子数为3,在化学反应中容易失去3个电子形成带3个单位正电荷的铝离子,离子符号是Al3+,正确;
故选D。
9.D
【详解】A、由图可知,①和②位于元素周期表中的同一横行,属于同周期,选项正确;
B、由图可知,①和④位于元素周期表中的同一纵行,属于同族,选项正确;
C、由图可知,③和⑤位于元素周期表中的同一纵行,属于同族,其最外层电子数相同,元素化学性质相似,选项正确;
D、由图可知,④和⑤位于元素周期表中的同一横行,属于同周期,其核外电子层数相同,选项错误;
故选D。
10.D
【详解】A、元素是个宏观概念,只讲种类、不讲个数,Cl可以表示1个氯原子,但不能表示1个氯元素,错误;
B、S的相对原子质量为32.06,而不是原子的实际质量,错误;
C、氯元素形成的单质是氯气,常温下是气态,错误;
D、磷、硫、氯在元素周期表中位于同一横行,属于同一周期,正确。
故选D。
11.C
【详解】元素符号的意义是:表示一种元素;表示这种元素的一个原子。对于由原子直接构成的物质,元素符号还表示这种物质。元素符号既有宏观意义,还有微观意义,但元素符号前有数字,就只表示几个原子,只有微观意义,没有宏观意义。Ca、N、He既有宏观意义,还有微观意义,而2N只有微观意义表示2个氮原子,没有宏观意义。故选C。
12.C
【详解】A.该粒子只由四个中子构成,中子不带电,故该粒子不显电性,故A正确;
B.质量数=质子数+中子数=0+4=4,故B正确;
C.该粒子只含有中子,不含有质子,故C错误;
D.该粒子的质量为4,氢原子的质量为1,故D正确,
故选C。
13.A
【分析】金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头,据此进行解答即可.
【详解】A、钠带“钅”字旁,属于金属元素,故选项正确。
B、硫带“石”字旁,属于固态非金属元素,故选项错误。
C、氩带“气”字旁,属于稀有气体元素,故选项错误。
D、氧带“气”字旁,属于气态非金属元素,故选项错误。
故选A。
14.C
【详解】元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义.
A、该符号是氮气的化学式,不是元素符号,故选项不符合题意.
B、该符号可表示3个铁原子,不是元素符号,故选项不符合题意.
C、Al属于金属元素,可表示铝元素,表示一个铝原子,还能表示铝这一单质,故选项符合题意.
D、H属于气态非金属元素,可表示氢元素,表示一个氢原子,但不能表示一种物质,故选项不符合题意.
故选C.
15.C
【详解】由同种元素组成的物质可能是单质、纯净物、混合物,但是一定不是化合物,因为化合物是由不同种元素组成的纯净物。
故选C。
16. 氮 Mg 铝 P 氯 Fe Cu 银
【详解】(1)N的元素名称为;氮;
(2)镁的元素符号为:Mg;
(3)Al的元素名称为:铝;
(4)磷的元素符号为:P;
(5)Cl的元素名称为:氯;
(6)铁的元素符号为:Fe;
(7)铜的元素符号为:Cu;
(8)Ag的元素名称为:银;
17. 铜这种物质 铜元素 一个铜原子
【详解】化学符号“Cu”的意义有:宏观上表示铜这种物质,表示铜元素;微观上表示一个铜原子。
故答案为(1)铜这种物质;(2)铜元素;(3)一个铜原子。
18.3个氢原子 氯元素、一个氯原子 铁元素、一个铁原子、铁单质 O 5Al nNa
【详解】(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,所以3H表示3个氢原子;
(2)元素符号既能表示某元素,也能表示某元素的一个原子,所以Cl表示氯元素、一个氯原子;
(3)元素符号既能表示某元素,也能表示某元素的一个原子,金属元素和部分固态非金属以及稀有气体的元素符号还能表示这种物质,所以Fe表示铁元素、一个铁原子,还表示铁单质;
(4)书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写,氧元素表示为O;
(5)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,5个铝原子表示为5Al;(6)由上分析可知n个钠原子表示为nNa。
19. 增加 化学
【详解】(1)元素周期表中,从左向右元素原子质子数逐渐增加,故填增加;
(2)同族元素最外层电子数相同,由于化学性质与最外层电子数有关,故同族元素的化学性质相似,故填化学。
20. 原子序数 173
【详解】(1)“115号(Mc)”中115表示原子的原子序数;
(2)原子中核电荷数=核内质子数=核外电子数,镆的原子序数是115,其核内质子数为115;镆的相对原子质量是288,相对原子质量≈质子数+中子数,其中子数为288-115=173。
21. H C N O Na Mg Al S Cl Ca
【分析】由一个字母表示的元素符号大写,由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
【详解】根据元素周期表的背诵要求本题考查的是前20号元素的默写,前二十号元素依次是:氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩钾钙,故填:H,C,N,O,Na,Mg,Al,S,Cl,Ca。
22. B 模型 中子数不同 不属于同种元素,因为质子数不同
【详解】(1)汤姆森最早发现电子的存在。
(2)原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,科学家都运用了模型来表达他们的理论成果。
(3)碳-12、碳-13、碳-14都是碳元素的原子,互为同位素,它们的主要差别在于中子数不同。
(4)由原子中质子数等于核外电子数,可知这两个微粒核内的质子数不同,所以不属于同种元素。
23. 16 非金属 C
【详解】根据元素周期表的一格可知,元素周期表的一格左上方的数字表示元素的原子序数,所以硫元素的原子序数是16。故填:16。
根据元素周期表可知,第15号元素是磷元素,磷是石字旁,所以磷元素属于非金属元素。故填:非金属。
在原子中,最外层电子数相同,化学性质相似,根据元素周期表可知,同族元素最外层电子数相同,即同族元素具有相似化学性质。
A、Li 和Na 是同族元素具有相似化学性质。A不符合题意;
B、Be 和 Mg 是同族元素具有相似化学性质。B不符合题意;
C、Al 和 Si 不是同族元素不具有相似化学性质。C符合题意;
D、F 和 Cl是同族元素具有相似化学性质。D不符合题意。
综上所述:选择C。故填:C。
24. 101 BD
【详解】(1)在原子中,质子数=核电荷数=原子序数=核外电子数,钔的质子数为101,根据核外电子数等于质子数可知,它的核外电子数为101。
(2)A.元素周期表是按照原子序数,也就是原子里面的质子数的大小进行排列的,故A错误;
B.门捷列夫发现了“相似化学性质的元素放同一列”原则,据此对已经发现的元素的相对原子质量进行了修正,故B正确;
C.门捷列夫得到的元素周期表并不是他独创的,而是在前面大量科学家的研究结果之上,再加上自己的仔细研究才得到的,故C错误;
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实,故D正确;
D.在科学界,科学家的荣誉都是建立在实实在在的研究成果之上的,和他本身的威望没有多大关系,故D错误。
故选BD。
25. 水电解生成氢气和氧气 质子数不同 31
【详解】(1)能够证明“水不是元素”的实验事实为:水电解生成氢气和氧气;
(2)元素是具有相同核电荷数的同一类原子的统称,而质子数等于核电荷数,所以区别是否是同种元素的关键是质子数。依据是:质子数不同;
(3)在元素周期表中,元素名称左上角的数字为该元素的原子序数,因此表格中元素锗的原子序数为32,那么它左边的元素原子的原子序数为:32-1=31。因为质子数=原子序数,所以空白格处原子的质子数为31。
答案第1页,共2页
答案第1页,共2页
一、选择题
1.碘盐中含有一定量的碘酸钾。我省实施新的碘盐含碘量标准,碘盐中碘含量从每千克 35 毫克降至 25 毫克。这里的“碘”是指( )
A.碘原子 B.碘分子 C.碘元素 D.碘单质
2.下列元素符号中书写正确的是( )
A.MG B.CA C.Fe D.f
3.锆被誉为原子时代的“第一号金属”,广泛应用于航空航天、精密铸造等领域。如图是锆元素在元素周期表中的信息,从中不能直接获得该元素的信息是( )
A.原子半径 B.元素符号
C.元素名称 D.相对原子质量
4.5G时代已经来临,高纯度单质硅(Si)是制作芯片的材料,如图是硅元素在元素周期表中的信息,则该硅原子的核外电子数为( )
A.14 B.15 C.28 D.29
5.钷可为航天器提供动力。钷元素在元素周期表中的信息如图所示,下列说法错误的是( )
A.钷的原子序数为61 B.钷的元素符号为Pm,钷是非金属
C.钷原子的核外电子数为61 D.钷元素的相对原子质量为145
6.下列关于Hg的说法不正确的是( )
A.表示一个汞原子
B.表示汞这种物质
C.表示汞这种元素
D.表示一个汞分子
7.如图为元素周期表的一部分(X元素信息不全),选项正确的是。( )
A.碳原子的相对原子质量为12.01g
B.X表示N2
C.氧原子的质子数是8
D.三种元素的原子的核外电子数相同
8.如图是元素周期表的部分示意图,下列说法正确的是( )
A.它们都属于金属元素 B.C元素的核电荷数为9
C.Al的相对原子质量是26.98g D.13号元素的离子符号是A13+
9.元素周期表是学习和研究科学的重要工具。如图所示为元素周期表的一部分,①﹣⑤代表五种不同短周期元素。下列说法错误的是( )
A.①和②同周期 B.①和④同族
C.③和⑤元素化学性质相似 D.④和⑤原子核外电子数相同
10.如图摘自元素周期表,部分信息略去,据此判断下列叙述中正确的是( )
A.C1表示1个氯元素,该元素的1个原子内质子数是17
B.S的原子质量为32.06.
C.三种都是非金属元素,它们分别形成的单质常温下均是固态
D.三种元素在周期表中属于同一周期
11.下列化学用语,通常只表示微观意义,而不表示宏观意义的是 。
A.Ca B.N C.2N D.He
12.法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是( )
A.该粒子不显电性
B.该粒子质量数为4
C.与氢元素的质子数相同
D.该粒子质量比氢原子大
13.在元素周期表中的下列四种元素,属于金属元素的是( )
A. B.
C. D.
14.下列符号,既表示一种元素,又能表示该元素的一个原子,还能表示该元素组成的单质的是 ()
A.N2 B.3Fe C.Al D.H
15.由同种元素组成的物质一定不是( )
A.纯净物 B.单质 C.化合物 D.混合物
二、填空题
16.写出元素符号或元素名称
(1)N (2)镁 (3)Al (4)磷 (5)Cl (6)铁 (7)铜 (8)Ag
17.化学符号“Cu”能表示多种意义(1) ;(2) ;(3)
18.请写出下列符号的含义或根据要求写出符号:
(1)3H: 。
(2)Cl: 。
(3)Fe: 。
(4)氧元素: 。
(5)5个铝原子: 。
(6)n个钠原子: 。
19.元素周期表中,同一周期从左到右,元素原子的质子数逐渐 (增加或减少),同一族元素的 (化学或物理)性质都很相似。
20.合成化学元素113号(Nh)、115号(Mc 镆)。
(1)其中,“115号(Mc)”中115表示原子的 。
(2)镆的相对原子质量是288,其中子数为 。
21.默写1~20号元素的符号
1 2 3 4 5 6 7 8 9 10
He Li Be B F Ne
11 12 13 14 15 16 17 18 19 20
Si P Ar K
22.人类在探索物质世界和微观世界的历史长河中,充满了智慧。请你回答相关问题。
(1)下面的科学家中最早发现电子的是 (填字母)。
A.道尔顿 B.汤姆森 C.卢瑟福 D.门捷列夫
(2)原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,科学家都运用了 来表达他们的理论成果。
(3)碳—12、碳—13、碳—14都是碳元素的原子,它们的主要差别在于 。
(4)人们很早就意识到物质都是由几种亘古不变的基本成分“元素”组成的。如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?你的观点及依据是 。
23.元素周期表是学习科学的重要工具,下表是元素周期表的部分信息。请分析表中信息,回答下列问题。
(1)硫元素的原子序数是 。
(2)第15号元素属于 元素(填“金属”或“非金属”)。
(3)下列各组元素不具有相似化学性质的是 (填字母)。
A.Li 和Na B.Be 和 Mg C.Al 和 Si D.F 和 Cl
24.2019年是“国际化学元素周期表年”,以纪念俄国化学家门捷列夫在1869年发明第一张元素周期表150周年。门捷列夫将当时已知的63种元素依据相对原子质量大小并以表的形式排列,将相似化学性质的元素放在同一列中,制成了元素周期表的雏形。
(1)钔的质子数为101,中子数为157,相对原子质量为258,则其核外电子数为 ;
(2)在1869年之前,许多化学家就对当时已知的元素进行排列。但国际上公认把发明元素周期律的桂冠戴在了门捷列夫的头上,你推测可能的原因是 。
A.门捷列夫按照相对原子质量排列元素,这也是现在元素周期表元素排列的标准
B.门捷列夫以“相似化学性质的元素放同一列”原则修正一些元素的相对原子质量
C.门捷列夫发明的元素周期表完全是他的独创,并不需要吸收别人的研究成果
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实
E.门捷列夫当时在科学界威望极高,他的发明成果更能让人信服
25.化学元素组成万物。人们很早就意识到物质都是由几种亘古不变的基本成分——“元素”组成的。
(1)古人曾认为水是组成物质的元素之一。在你学过的知识中能说明“水不是元素“的实验事实是 ;
(2)现代化学对“元素"做了科学定义,图甲是两个微粒的结构模型示意图,小科认为这两个微粒不属于同种元素,你认为他的依据是 ;
(3)1869年,俄国化学家门捷列夫在前人研究的基础上制作出第一张元素周期表,图乙是元素周期表的部分内容,表中空白格处元素原子的质子数为 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 C C A A B D C D D D
题号 11 12 13 14 15
答案 C C A C C
1.C
【详解】试题分析:元素是具有相同核电荷数的同一类原子的总称。题中的碘指的是碘元素。
考点:元素的概念;人体的元素组成与元素对人体健康的重要作用。
点评:本题主要考查了日常生活用品中的元素组成问题。
2.C
【详解】元素符号的书写要满足“一大二小”的要求,即:只有一个字母时要大写,有两个字母时第一个字母大写,第二个字母小写,故选C。
3.A
【详解】A、根据元素周期表中的一格可知,不能直接体现原子半径,故选项正确;
B、根据元素周期表中的一格可知,字母表示该元素的元素符号,能直接体现,故选项错误;
C、根据元素周期表中的一格可知,中间的汉字表示该元素的元素名称,能直接体现,故选项错误;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,能直接体现,故选项错误。
故选A。
4.A
【详解】根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为14;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为14。故选A。
5.B
【详解】A、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为61,故选项说法正确;
B、根据元素周期表中的一格可知,字母表示该元素的元素符号,钷的元素符号为Pm, 钷带“钅”字旁,属于金属元素,故选项说法错误;
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为61;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为61,故选项说法正确;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为145,故选项说法正确。
故选B。
6.D
【分析】元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义。
【详解】A、Hg属于金属元素,可表示一个汞原子,故选项说法正确。
B、Hg属于金属元素,可表示汞这一纯净物,故选项说法正确。
C、Hg属于金属元素,可表示汞元素,故选项说法正确。
D、Hg属于金属单质,是由汞原子直接构成的,故选项说法错误。
故选D。
7.C
【详解】A、元素信息图中最下方的数字是原子的相对原子质量,由图可知,碳原子的相对原子质量为12.01,选项错误;
B、原子序数为7的元素为氮元素,其元素符号为N,即X为N,选项错误;
C、元素信息图左上角的数字为原子序数,原子序数等于原子的质子数,由图可知,氧原子的质子数是8,选项正确;
D、碳原子核外电子数为6,氮原子核外电子数为7,氧原子核外电子数为8,三种元素的原子核外电子数不相同,选项错误;
故选C。
8.D
【详解】A、铝(Al)元素名称都有“钅”字偏旁,属于金属元素,B(硼)、C(碳)、Si(硅)元素名称都有“石”字旁,属于固态非金属元素属于非金属元素,故A错误;
B、根据碳元素周期表中的一格可知,左上角的数字为6,表示原子序数为6;根据原子序数=核电荷数,则该元素的原子核电荷数为6,错误;
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为26.98,相对原子质量单位是“1”,不是“克”,错误;
D、13号元素为铝元素,核外电子排布为2,8,3,最外层电子数为3,在化学反应中容易失去3个电子形成带3个单位正电荷的铝离子,离子符号是Al3+,正确;
故选D。
9.D
【详解】A、由图可知,①和②位于元素周期表中的同一横行,属于同周期,选项正确;
B、由图可知,①和④位于元素周期表中的同一纵行,属于同族,选项正确;
C、由图可知,③和⑤位于元素周期表中的同一纵行,属于同族,其最外层电子数相同,元素化学性质相似,选项正确;
D、由图可知,④和⑤位于元素周期表中的同一横行,属于同周期,其核外电子层数相同,选项错误;
故选D。
10.D
【详解】A、元素是个宏观概念,只讲种类、不讲个数,Cl可以表示1个氯原子,但不能表示1个氯元素,错误;
B、S的相对原子质量为32.06,而不是原子的实际质量,错误;
C、氯元素形成的单质是氯气,常温下是气态,错误;
D、磷、硫、氯在元素周期表中位于同一横行,属于同一周期,正确。
故选D。
11.C
【详解】元素符号的意义是:表示一种元素;表示这种元素的一个原子。对于由原子直接构成的物质,元素符号还表示这种物质。元素符号既有宏观意义,还有微观意义,但元素符号前有数字,就只表示几个原子,只有微观意义,没有宏观意义。Ca、N、He既有宏观意义,还有微观意义,而2N只有微观意义表示2个氮原子,没有宏观意义。故选C。
12.C
【详解】A.该粒子只由四个中子构成,中子不带电,故该粒子不显电性,故A正确;
B.质量数=质子数+中子数=0+4=4,故B正确;
C.该粒子只含有中子,不含有质子,故C错误;
D.该粒子的质量为4,氢原子的质量为1,故D正确,
故选C。
13.A
【分析】金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头,据此进行解答即可.
【详解】A、钠带“钅”字旁,属于金属元素,故选项正确。
B、硫带“石”字旁,属于固态非金属元素,故选项错误。
C、氩带“气”字旁,属于稀有气体元素,故选项错误。
D、氧带“气”字旁,属于气态非金属元素,故选项错误。
故选A。
14.C
【详解】元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义.
A、该符号是氮气的化学式,不是元素符号,故选项不符合题意.
B、该符号可表示3个铁原子,不是元素符号,故选项不符合题意.
C、Al属于金属元素,可表示铝元素,表示一个铝原子,还能表示铝这一单质,故选项符合题意.
D、H属于气态非金属元素,可表示氢元素,表示一个氢原子,但不能表示一种物质,故选项不符合题意.
故选C.
15.C
【详解】由同种元素组成的物质可能是单质、纯净物、混合物,但是一定不是化合物,因为化合物是由不同种元素组成的纯净物。
故选C。
16. 氮 Mg 铝 P 氯 Fe Cu 银
【详解】(1)N的元素名称为;氮;
(2)镁的元素符号为:Mg;
(3)Al的元素名称为:铝;
(4)磷的元素符号为:P;
(5)Cl的元素名称为:氯;
(6)铁的元素符号为:Fe;
(7)铜的元素符号为:Cu;
(8)Ag的元素名称为:银;
17. 铜这种物质 铜元素 一个铜原子
【详解】化学符号“Cu”的意义有:宏观上表示铜这种物质,表示铜元素;微观上表示一个铜原子。
故答案为(1)铜这种物质;(2)铜元素;(3)一个铜原子。
18.3个氢原子 氯元素、一个氯原子 铁元素、一个铁原子、铁单质 O 5Al nNa
【详解】(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,所以3H表示3个氢原子;
(2)元素符号既能表示某元素,也能表示某元素的一个原子,所以Cl表示氯元素、一个氯原子;
(3)元素符号既能表示某元素,也能表示某元素的一个原子,金属元素和部分固态非金属以及稀有气体的元素符号还能表示这种物质,所以Fe表示铁元素、一个铁原子,还表示铁单质;
(4)书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写,氧元素表示为O;
(5)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,5个铝原子表示为5Al;(6)由上分析可知n个钠原子表示为nNa。
19. 增加 化学
【详解】(1)元素周期表中,从左向右元素原子质子数逐渐增加,故填增加;
(2)同族元素最外层电子数相同,由于化学性质与最外层电子数有关,故同族元素的化学性质相似,故填化学。
20. 原子序数 173
【详解】(1)“115号(Mc)”中115表示原子的原子序数;
(2)原子中核电荷数=核内质子数=核外电子数,镆的原子序数是115,其核内质子数为115;镆的相对原子质量是288,相对原子质量≈质子数+中子数,其中子数为288-115=173。
21. H C N O Na Mg Al S Cl Ca
【分析】由一个字母表示的元素符号大写,由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
【详解】根据元素周期表的背诵要求本题考查的是前20号元素的默写,前二十号元素依次是:氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩钾钙,故填:H,C,N,O,Na,Mg,Al,S,Cl,Ca。
22. B 模型 中子数不同 不属于同种元素,因为质子数不同
【详解】(1)汤姆森最早发现电子的存在。
(2)原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,科学家都运用了模型来表达他们的理论成果。
(3)碳-12、碳-13、碳-14都是碳元素的原子,互为同位素,它们的主要差别在于中子数不同。
(4)由原子中质子数等于核外电子数,可知这两个微粒核内的质子数不同,所以不属于同种元素。
23. 16 非金属 C
【详解】根据元素周期表的一格可知,元素周期表的一格左上方的数字表示元素的原子序数,所以硫元素的原子序数是16。故填:16。
根据元素周期表可知,第15号元素是磷元素,磷是石字旁,所以磷元素属于非金属元素。故填:非金属。
在原子中,最外层电子数相同,化学性质相似,根据元素周期表可知,同族元素最外层电子数相同,即同族元素具有相似化学性质。
A、Li 和Na 是同族元素具有相似化学性质。A不符合题意;
B、Be 和 Mg 是同族元素具有相似化学性质。B不符合题意;
C、Al 和 Si 不是同族元素不具有相似化学性质。C符合题意;
D、F 和 Cl是同族元素具有相似化学性质。D不符合题意。
综上所述:选择C。故填:C。
24. 101 BD
【详解】(1)在原子中,质子数=核电荷数=原子序数=核外电子数,钔的质子数为101,根据核外电子数等于质子数可知,它的核外电子数为101。
(2)A.元素周期表是按照原子序数,也就是原子里面的质子数的大小进行排列的,故A错误;
B.门捷列夫发现了“相似化学性质的元素放同一列”原则,据此对已经发现的元素的相对原子质量进行了修正,故B正确;
C.门捷列夫得到的元素周期表并不是他独创的,而是在前面大量科学家的研究结果之上,再加上自己的仔细研究才得到的,故C错误;
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实,故D正确;
D.在科学界,科学家的荣誉都是建立在实实在在的研究成果之上的,和他本身的威望没有多大关系,故D错误。
故选BD。
25. 水电解生成氢气和氧气 质子数不同 31
【详解】(1)能够证明“水不是元素”的实验事实为:水电解生成氢气和氧气;
(2)元素是具有相同核电荷数的同一类原子的统称,而质子数等于核电荷数,所以区别是否是同种元素的关键是质子数。依据是:质子数不同;
(3)在元素周期表中,元素名称左上角的数字为该元素的原子序数,因此表格中元素锗的原子序数为32,那么它左边的元素原子的原子序数为:32-1=31。因为质子数=原子序数,所以空白格处原子的质子数为31。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
