第3节 化学方程式 第1课时质量守恒定律与化学方程式(PDF版,含答案)
文档属性
| 名称 | 第3节 化学方程式 第1课时质量守恒定律与化学方程式(PDF版,含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-02-14 00:00:00 | ||
图片预览

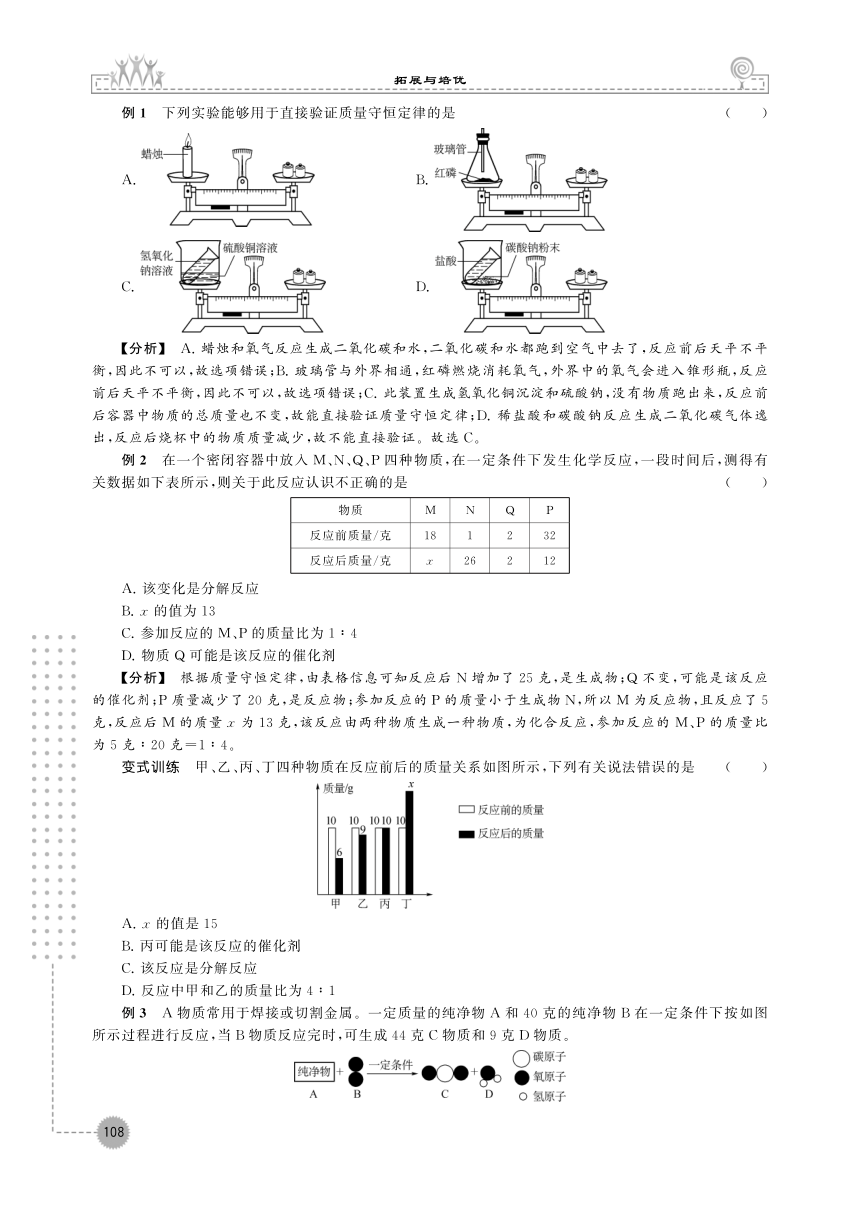

文档简介
料学八年级下册
第3节
化学方程式
第1课时质量守恒定律与化学方程式
思维点击
一、质量守恒定律
1.概念:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律就叫做
质量守恒定律。
2.对概念的理解
(1)质量守恒定律只适用于化学反应,不能用于物理变化。例如,将3g水加热变成3g水蒸气,这一变
化前后质量虽然相等,但这是物理变化,不能说它遵守质量守恒定律。
(2)质量守恒定律指的是“质量守恒”,不包括其他方面的守恒,如对反应物和生成物均是气体的反应来
说,反应前后的总质量守恒,但是其体积却不一定守恒。
(3)质量守恒定律中的第一个“质量”二字,是指“参加”化学反应的反应物的质量,不是所有反应物质量
的任意简单相加。
例如,2g氢气与8g氧气在点燃的条件下,并非生成10g水,而是1g氢气与8g氧气参加反应,生成9g水。
(4)很多化学反应中有气体或沉淀生成,因此“生成的各物质质量总和”包括了固态、液态和气态三种状
态的物质,不能把生成的特别是逸散到空气中的气态物质计算在“总质量”之外而误认为化学反应不遵循质
量守恒定律。
3.实验验证:有气体参加或生成的实验必须在密闭容器里进行。
如:(1)有气体生成的实验没密闭,天平会不平衡(生成的气体逸散到空气中)。
(2)有气体参加的实验没密闭,天平会不平衡(没有称量参加反应的气体)。
4.微观实质
(1)化学反应的实质是在化学反应过程中,参加反应的各物质(反应物)的原子,重新组合而生成其他物
质(生成物)的过程。由分子构成的物质在化学反应中的变化过程可表示为:
分子分翠原子熏新粗合分子来集新物质
(2)质量守恒的原因是在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子本身的质量
也没有改变,所以,反应前后的质量总和必然相等。例如,水通电分解生成氢气和氧气,从微观角度看:当水
分子分解时,生成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子。
【拓展】质量守恒定律的延伸和拓展理解:
质量守恒定律要抓住“六个不变”“两个一定变”“两个可能变”。
反应前后的总质量不变
宏观
元素的种类不变
元素的质量不变
六个不变
原子的种类不变
微观
原子的数目不变
原子的质量不变
物质的种类一定变
两个一定变
构成物质的分子种类一定变
分子的总数可能变
两个可能变
元素的化合价可能变
107
第3节
化学方程式
第1课时质量守恒定律与化学方程式
思维点击
一、质量守恒定律
1.概念:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律就叫做
质量守恒定律。
2.对概念的理解
(1)质量守恒定律只适用于化学反应,不能用于物理变化。例如,将3g水加热变成3g水蒸气,这一变
化前后质量虽然相等,但这是物理变化,不能说它遵守质量守恒定律。
(2)质量守恒定律指的是“质量守恒”,不包括其他方面的守恒,如对反应物和生成物均是气体的反应来
说,反应前后的总质量守恒,但是其体积却不一定守恒。
(3)质量守恒定律中的第一个“质量”二字,是指“参加”化学反应的反应物的质量,不是所有反应物质量
的任意简单相加。
例如,2g氢气与8g氧气在点燃的条件下,并非生成10g水,而是1g氢气与8g氧气参加反应,生成9g水。
(4)很多化学反应中有气体或沉淀生成,因此“生成的各物质质量总和”包括了固态、液态和气态三种状
态的物质,不能把生成的特别是逸散到空气中的气态物质计算在“总质量”之外而误认为化学反应不遵循质
量守恒定律。
3.实验验证:有气体参加或生成的实验必须在密闭容器里进行。
如:(1)有气体生成的实验没密闭,天平会不平衡(生成的气体逸散到空气中)。
(2)有气体参加的实验没密闭,天平会不平衡(没有称量参加反应的气体)。
4.微观实质
(1)化学反应的实质是在化学反应过程中,参加反应的各物质(反应物)的原子,重新组合而生成其他物
质(生成物)的过程。由分子构成的物质在化学反应中的变化过程可表示为:
分子分翠原子熏新粗合分子来集新物质
(2)质量守恒的原因是在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子本身的质量
也没有改变,所以,反应前后的质量总和必然相等。例如,水通电分解生成氢气和氧气,从微观角度看:当水
分子分解时,生成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子。
【拓展】质量守恒定律的延伸和拓展理解:
质量守恒定律要抓住“六个不变”“两个一定变”“两个可能变”。
反应前后的总质量不变
宏观
元素的种类不变
元素的质量不变
六个不变
原子的种类不变
微观
原子的数目不变
原子的质量不变
物质的种类一定变
两个一定变
构成物质的分子种类一定变
分子的总数可能变
两个可能变
元素的化合价可能变
107
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
