3.4 二氧化碳(同步课件 31张PPT)--2024-2025学年浙教版科学八年级下册
文档属性
| 名称 | 3.4 二氧化碳(同步课件 31张PPT)--2024-2025学年浙教版科学八年级下册 |  | |
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-03-26 18:15:38 | ||
图片预览









文档简介
(共31张PPT)
浙教版八年级科学下册
第三章 生命与空气
3.4 二氧化碳
二氧化碳(carbon dioxide)在空气中含量不多,约占 0.04%。然而,就是这些含量很低的 CO2,对自然界的作用却不可小看。你知道它有哪些重要作用吗?
一、自然界中的二氧化碳
1.二氧化碳的构成和组成
(1)二氧化碳气体是由大量二氧化碳分子构成的,其化学式为 CO2。
(2)每个二氧化碳分子由1个碳原子和2个氧原子构成。
(3)二氧化碳由碳元素和氧元素组成,其中碳元素的化合价为+4价。
一、自然界中的二氧化碳
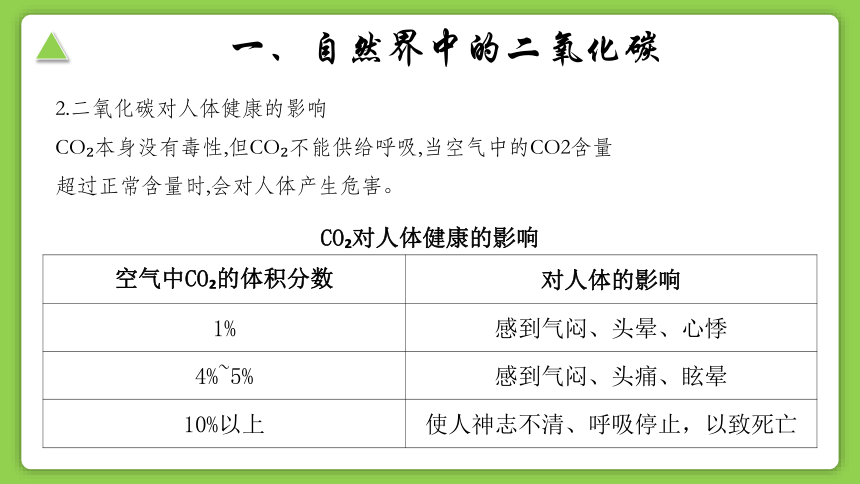
2.二氧化碳对人体健康的影响
CO 本身没有毒性,但CO 不能供给呼吸,当空气中的CO2含量
超过正常含量时,会对人体产生危害。
CO 对人体健康的影响 空气中CO 的体积分数 对人体的影响
1% 感到气闷、头晕、心悸
4%~5% 感到气闷、头痛、眩晕
10%以上 使人神志不清、呼吸停止,以致死亡
为什么冬天虽然天气寒冷,但教室还是应当适时开窗通风?
人呼吸产生CO2,CO 不能供给呼吸,含量超过正常含量时对人体有害,开窗通风能使教室内空气清新,降低教室内CO 的含量。
二、二氧化碳的性质
二氧化碳与人的健康关系密切。对于二氧化碳,你还知道些什么?
1.观察一瓶二氧化碳气体,它的颜色、状态和气味是怎样的?
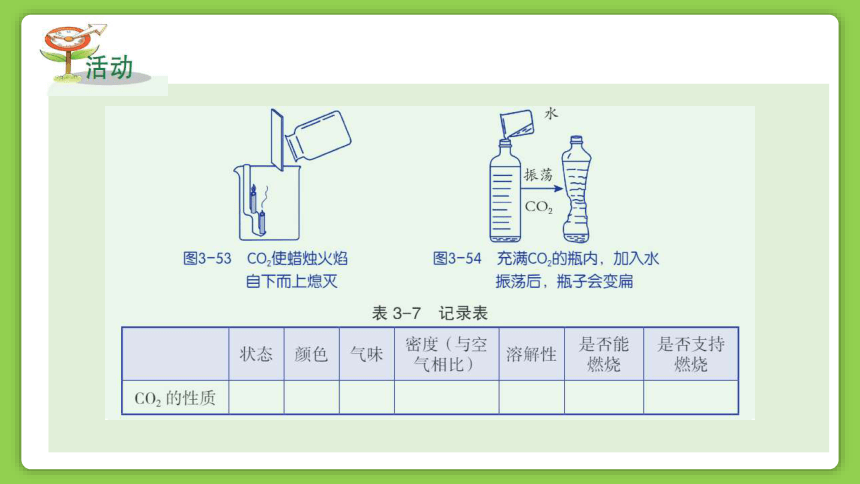
2.如图 3-53 所示,向烧杯里倾倒二氧化碳。注意观察蜡烛火焰的变化。由此你能得出什么结论?
3.如图 3-54 所示,在一个充满二氧化碳的软塑料瓶里,迅速倒入少量蒸馏水,立即将瓶塞塞紧振荡,观察有什么现象。
由此你能得出什么结论?
实验装置 实验内容 实验现象 实验分析
观察一瓶 CO 气体的颜色、状态和气味 CO 气体没有颜色、没有气味 通常状况下,CO 是无色、无味的气体
向烧杯里缓慢倾倒CO2,观察蜡烛火焰的变化 两支蜡烛自下而上,依次熄灭 一般情况下,CO2,不燃烧,也不支持燃烧,且密度比空气的大。倾倒时会在烧杯底部先聚集较多的CO ,使下方蜡烛首先接触到较多的CO2而先熄灭,上方蜡烛后接触到较多的CO2而后熄灭
在一个充满 CO 的软塑料瓶里,迅速倒入少量蒸馏水,立即将瓶塞塞紧振荡,观察现象 塑料瓶变瘪 部分 CO 溶于水使瓶内气体减少,导致瓶内气体压强减小,在外界大气压强的作用下,瓶子变瘪
2.二氧化碳的物理性质
(1)通常状况下,CO 有如下物理性质:
状态 颜色 气味 密度(与空气相比) 溶解性
气态 无色 无味 比空气的大 能溶于水
说明
①CO 的密度大约是空气密度的1.5倍,因此能像倒液体那样从一个容器向另一个容器倾倒。②通常1体积水中能溶解1体积的 CO ,增大压强可使其溶解得更多。
(2)在加压降温的情况下,CO2能变成无色液体,甚至变成雪状固体。通常把固体 CO 叫做“干冰”,干冰易升华吸热。
CO2 溶于水的过程中,有没有发生化学变化呢?
CO 溶于水的过程中,CO 以分子形式存在,属于物理变化;CO 与水反应生成H2CO3,属于化学变化。
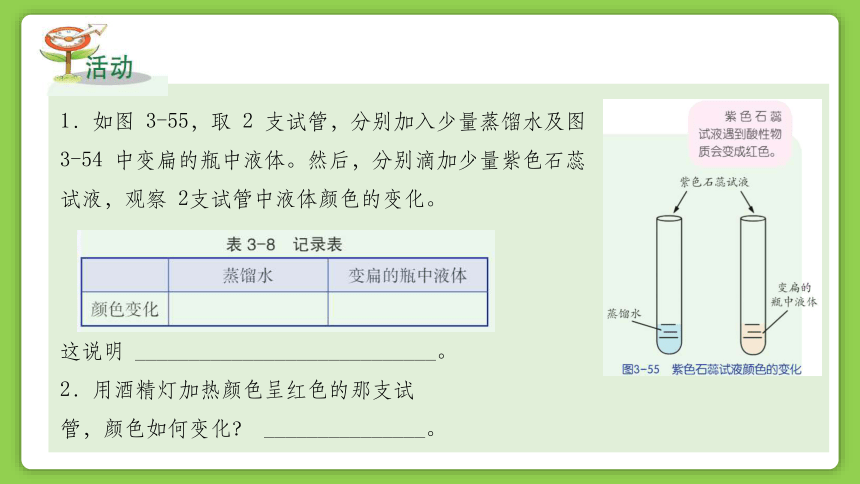
1.如图 3-55,取 2 支试管,分别加入少量蒸馏水及图 3-54 中变扁的瓶中液体。然后,分别滴加少量紫色石蕊试液,观察 2支试管中液体颜色的变化。
这说明 ____________________________。
2.用酒精灯加热颜色呈红色的那支试
管,颜色如何变化? _______________。
3.二氧化碳的化学性质
实验1 实验2
实验 步骤 取2支试管,分别加入少量蒸馏水及前面活 动中变扁的瓶中液体,然后,分别滴加少量紫 色石蕊试液,观察2支试管中液体颜色的变化 用酒精灯加热颜
色呈红色的那支
试管,观察液体
颜色的变化
实验 现象 滴入蒸馏水中的紫色石蕊试液不变色,滴入 变扁瓶中液体的紫色石蕊试液变红色 红色的石蕊试液
重新变为紫色
化学方 程式
(2)二氧化碳与澄清石灰水反应
实验操作 把CO 通入澄清石灰水[Ca(OH) 水溶液]中
实验现象 生成白色沉淀,澄清石灰水变浑浊
现象分析 CO 与Ca(OH) 反应,生成了难溶于水的物质,故澄清石灰
水变浑浊
化学方程式 CO +Ca(OH) =CaCO ↓+H O→这一反应常用来检验CO
示例 用熟石灰[Ca(OH)2]抹墙,墙壁会变白变硬;长期存放石灰水的试剂瓶,瓶壁有白色固体,石灰水表面有一层白膜;鸡蛋放入石灰水中可以保存较长时间,这些都是因为Ca(OH)2,与CO 反应生成了CaCO 沉淀
归纳总结
二氧化碳的化学性质
(1)一般情况下,二氧化碳不燃烧,也不支持燃烧,不能供给呼吸。
(2)二氧化碳能与水反应生成碳酸:CO2+H2O=H2CO3。
(3)二氧化碳能使澄清石灰水变浑浊:CO +Ca(OH) =CaCO3+H2O
三、二氧化碳的制取
实验室常用大理石或石灰石(主要成分为碳酸钙)与稀盐酸反应来制取二氧化碳气体。
1.药品的选择
药品 现象
稀盐酸与块状大理石 产生气泡,速率适中
浓盐酸与块状大理石 剧烈反应,迅速产生大量气泡,并伴有白雾
稀硫酸与块状大理石 刚开始时产生气泡,后来速率减慢并逐渐停止
稀盐酸与碳酸钠粉末(或纯碳酸钙) 剧烈反应,迅速产生大量气泡
通过上述对比分析可知,实验室制取二氧化碳的药品宜选用稀盐酸和大理石(或石灰石,主要成分都是碳酸钙)。
1.如果在实验室中制取二氧化碳气体,你选择的装置是表 3-9 中的
_____________。
2.怎样检查气体发生装置的气密性?
3.组装好你选择的发生装置和收集装置,制取一瓶二氧化碳气体。
4.在确定气体发生装置时,应该考虑哪些因素?在确定气体收集装置时,
又应该考虑哪些因素
二氧化碳的制取和性质研究
1.初步学会实验室制取二氧化碳装置的装配和连接方法。
2.初步学会实验室制取二氧化碳的方法,学习用向上排空气法收集气体。
3.初步学会用块状固体和液体反应制取气体的方法。
二氧化碳的制取和性质研究
石灰石(或大理石),稀盐酸,澄清石灰
水,紫色石蕊试液,蒸馏水,锥形瓶,烧杯,
双孔橡皮塞,橡皮管,玻璃导管,集气瓶,
玻璃片,蜡烛,木条,火柴,铁皮架。
实验室制取C O2,选用石灰石(或大理石)为原料,则不能选 用稀硫酸。因为生成的硫酸钙是微溶性物质,它会包裹在石灰石表面,使酸液不能与石灰石接触,从而使反应中止。
二氧化碳的制取和性质研究
1.制取二氧化碳。
(1)按图 3-58 组装好制取二氧化碳的简易装置,
检查装置的气密性。
(2)在锥形瓶中加入几小块大理石,塞紧带有
长颈漏斗和导管的橡皮塞。
(3)把气体导管插入集气瓶中,导管口应处在接近集气瓶的瓶底处。
二氧化碳的制取和性质研究
(4)通过长颈漏斗加入适
量的稀盐酸,锥形瓶中立刻有气体产生。
(5)片刻后,把燃着的火柴放到集气瓶口的上方,如果火柴很快熄灭,说明集气瓶中已经收集满二氧化碳气体,盖好毛玻璃片,将集气瓶口向上放在桌子上备用。
二氧化碳的制取和性质研究
2.试验二氧化碳性质。
(1)把一支短蜡烛固定在烧杯中的铁皮架上,点燃。如图 3-59 所示,拿起集满二氧化碳的集气瓶,向烧杯中缓缓倾倒二氧化碳,观察到的现象是 ___________
二氧化碳的制取和性质研究
(2)如图 3-60 所示,取一支试管,注
入少量澄清石灰水,通入二氧化碳,观察
到的现象是 ______________________________________________________。
(3)另取一支试管,加入 2 毫升蒸馏水,滴入 1~2 滴石蕊试液,为 ________ 色,通入二氧化碳气体,溶液颜色变为 _________ 色。
二氧化碳的制取和性质研究
图 3-61 是某学生设计的实验室制取并收集二氧化碳气体的装置图。指出装置中的错误之处,并说明原因。
四、二氧化碳的应用
CO 的性质 CO 的用途
能溶于水(物理性质) 生产汽水等碳酸饮料
干冰(固态CO )升华吸热(物理性质) 作为制冷剂,用于人工降雨,
制造舞台云雾效果等
一般情况下,不燃烧,也不支持燃烧(化学性质),密度比空气的大(物理性质) 用来灭火
参与植物光合作用(化学性质), 作为气体肥料,提高光合作
用的强度和效率
能用CO 、H O、NaCl等生产纯碱(Na CO ) (化学性质) 作为化工产品的原料
二氧化碳的下列用途没有利用其化学性质的是( )
A.干冰用于人工降雨
B.二氧化碳用于灭火
C.二氧化碳作为气体肥料
D.二氧化碳用于制纯碱
解析:干冰用于人工降雨,利用了干冰升华时吸热的性质,属于物理性质。
答案:A
课堂小结
如图是实验室制取气体的常用装置。实验小组同学想要制取并收集一瓶干燥的二氧化碳气体,可选择下列装置中的发生装置: ;收集装置: ;干燥装置: 。(请选出所有可能的答案,用所给字母填空)
课堂小练习
【解答】解:实验室常用大理石(或石灰石)和稀盐酸反应制取二氧化碳,属于固、液常温型,并要在后面接干燥装置,应该选的发生装置是B;二氧化碳的密度比空气大,能溶于水,要收集干燥的二氧化碳要用装置E;二氧化碳能和氢氧化钠反应,二氧化碳不和浓硫酸反应,浓硫酸具有吸水性,可用浓硫酸干燥二氧化碳,所以干燥装置是G。故答案为:B;E;G。
正确规范的操作是实验成功的关键,下列实验操作符合规范的是( )
课堂小练习
【解答】解:A.配制溶液时应将固体放入烧杯中配制,不可在量筒中配制,故A操作错误;
B.因为氧气的密度比水小,所以收集氧气时,应从短导管进入,将水从长导管排出,故B操作正确;
C.二氧化碳验满的方法是将燃着的木条放在集气瓶口,故C操作错误;
D.测pH时,应将待测液滴在pH试纸上,而不是将pH试纸伸入待测液中,这样操作会污染试剂,故D操作错误。
故选:B。
小金利用如图装置研究二氧化碳的性质。注射器内装有足量稀盐酸,硬质玻璃管中有四个棉球,其中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。下列关于实验过程及现象的分析,不合理的是( )
A.若把稀盐酸换成稀硫酸则反应速度太慢,可能会影响实验结论
B.若把大理石换成碳酸钠则反应速度太快,可能会影响实验结论
C.通过①②或③④现象的比较,均能得出二氧化碳溶于水呈酸性
D.通过①④或②③现象的比较,均能得出二氧化碳密度大于空气
课堂小练习
【解答】解:A、稀硫酸和大理石反应,生成硫酸钙,微溶于水的硫酸钙覆盖在石灰石的表面,阻碍反应进一步进行,可能会影响实验结论;B、碳酸钠与稀盐酸反应速率过快,可能会影响实验结论;
C、①④处棉球会变成红色,②③处干燥的棉球不变色,所以通过①②或③④现象的比较,均能得出二氧化碳溶于水呈酸性;D、①④处棉球会变成红色,②③处干燥的棉球不变色,故通过①④能得出二氧化碳密度大于空气,而②③不能得出二氧化碳密度大于空气。故选:D。
浙教版八年级科学下册
第三章 生命与空气
3.4 二氧化碳
二氧化碳(carbon dioxide)在空气中含量不多,约占 0.04%。然而,就是这些含量很低的 CO2,对自然界的作用却不可小看。你知道它有哪些重要作用吗?
一、自然界中的二氧化碳
1.二氧化碳的构成和组成
(1)二氧化碳气体是由大量二氧化碳分子构成的,其化学式为 CO2。
(2)每个二氧化碳分子由1个碳原子和2个氧原子构成。
(3)二氧化碳由碳元素和氧元素组成,其中碳元素的化合价为+4价。
一、自然界中的二氧化碳
2.二氧化碳对人体健康的影响
CO 本身没有毒性,但CO 不能供给呼吸,当空气中的CO2含量
超过正常含量时,会对人体产生危害。
CO 对人体健康的影响 空气中CO 的体积分数 对人体的影响
1% 感到气闷、头晕、心悸
4%~5% 感到气闷、头痛、眩晕
10%以上 使人神志不清、呼吸停止,以致死亡
为什么冬天虽然天气寒冷,但教室还是应当适时开窗通风?
人呼吸产生CO2,CO 不能供给呼吸,含量超过正常含量时对人体有害,开窗通风能使教室内空气清新,降低教室内CO 的含量。
二、二氧化碳的性质
二氧化碳与人的健康关系密切。对于二氧化碳,你还知道些什么?
1.观察一瓶二氧化碳气体,它的颜色、状态和气味是怎样的?
2.如图 3-53 所示,向烧杯里倾倒二氧化碳。注意观察蜡烛火焰的变化。由此你能得出什么结论?
3.如图 3-54 所示,在一个充满二氧化碳的软塑料瓶里,迅速倒入少量蒸馏水,立即将瓶塞塞紧振荡,观察有什么现象。
由此你能得出什么结论?
实验装置 实验内容 实验现象 实验分析
观察一瓶 CO 气体的颜色、状态和气味 CO 气体没有颜色、没有气味 通常状况下,CO 是无色、无味的气体
向烧杯里缓慢倾倒CO2,观察蜡烛火焰的变化 两支蜡烛自下而上,依次熄灭 一般情况下,CO2,不燃烧,也不支持燃烧,且密度比空气的大。倾倒时会在烧杯底部先聚集较多的CO ,使下方蜡烛首先接触到较多的CO2而先熄灭,上方蜡烛后接触到较多的CO2而后熄灭
在一个充满 CO 的软塑料瓶里,迅速倒入少量蒸馏水,立即将瓶塞塞紧振荡,观察现象 塑料瓶变瘪 部分 CO 溶于水使瓶内气体减少,导致瓶内气体压强减小,在外界大气压强的作用下,瓶子变瘪
2.二氧化碳的物理性质
(1)通常状况下,CO 有如下物理性质:
状态 颜色 气味 密度(与空气相比) 溶解性
气态 无色 无味 比空气的大 能溶于水
说明
①CO 的密度大约是空气密度的1.5倍,因此能像倒液体那样从一个容器向另一个容器倾倒。②通常1体积水中能溶解1体积的 CO ,增大压强可使其溶解得更多。
(2)在加压降温的情况下,CO2能变成无色液体,甚至变成雪状固体。通常把固体 CO 叫做“干冰”,干冰易升华吸热。
CO2 溶于水的过程中,有没有发生化学变化呢?
CO 溶于水的过程中,CO 以分子形式存在,属于物理变化;CO 与水反应生成H2CO3,属于化学变化。
1.如图 3-55,取 2 支试管,分别加入少量蒸馏水及图 3-54 中变扁的瓶中液体。然后,分别滴加少量紫色石蕊试液,观察 2支试管中液体颜色的变化。
这说明 ____________________________。
2.用酒精灯加热颜色呈红色的那支试
管,颜色如何变化? _______________。
3.二氧化碳的化学性质
实验1 实验2
实验 步骤 取2支试管,分别加入少量蒸馏水及前面活 动中变扁的瓶中液体,然后,分别滴加少量紫 色石蕊试液,观察2支试管中液体颜色的变化 用酒精灯加热颜
色呈红色的那支
试管,观察液体
颜色的变化
实验 现象 滴入蒸馏水中的紫色石蕊试液不变色,滴入 变扁瓶中液体的紫色石蕊试液变红色 红色的石蕊试液
重新变为紫色
化学方 程式
(2)二氧化碳与澄清石灰水反应
实验操作 把CO 通入澄清石灰水[Ca(OH) 水溶液]中
实验现象 生成白色沉淀,澄清石灰水变浑浊
现象分析 CO 与Ca(OH) 反应,生成了难溶于水的物质,故澄清石灰
水变浑浊
化学方程式 CO +Ca(OH) =CaCO ↓+H O→这一反应常用来检验CO
示例 用熟石灰[Ca(OH)2]抹墙,墙壁会变白变硬;长期存放石灰水的试剂瓶,瓶壁有白色固体,石灰水表面有一层白膜;鸡蛋放入石灰水中可以保存较长时间,这些都是因为Ca(OH)2,与CO 反应生成了CaCO 沉淀
归纳总结
二氧化碳的化学性质
(1)一般情况下,二氧化碳不燃烧,也不支持燃烧,不能供给呼吸。
(2)二氧化碳能与水反应生成碳酸:CO2+H2O=H2CO3。
(3)二氧化碳能使澄清石灰水变浑浊:CO +Ca(OH) =CaCO3+H2O
三、二氧化碳的制取
实验室常用大理石或石灰石(主要成分为碳酸钙)与稀盐酸反应来制取二氧化碳气体。
1.药品的选择
药品 现象
稀盐酸与块状大理石 产生气泡,速率适中
浓盐酸与块状大理石 剧烈反应,迅速产生大量气泡,并伴有白雾
稀硫酸与块状大理石 刚开始时产生气泡,后来速率减慢并逐渐停止
稀盐酸与碳酸钠粉末(或纯碳酸钙) 剧烈反应,迅速产生大量气泡
通过上述对比分析可知,实验室制取二氧化碳的药品宜选用稀盐酸和大理石(或石灰石,主要成分都是碳酸钙)。
1.如果在实验室中制取二氧化碳气体,你选择的装置是表 3-9 中的
_____________。
2.怎样检查气体发生装置的气密性?
3.组装好你选择的发生装置和收集装置,制取一瓶二氧化碳气体。
4.在确定气体发生装置时,应该考虑哪些因素?在确定气体收集装置时,
又应该考虑哪些因素
二氧化碳的制取和性质研究
1.初步学会实验室制取二氧化碳装置的装配和连接方法。
2.初步学会实验室制取二氧化碳的方法,学习用向上排空气法收集气体。
3.初步学会用块状固体和液体反应制取气体的方法。
二氧化碳的制取和性质研究
石灰石(或大理石),稀盐酸,澄清石灰
水,紫色石蕊试液,蒸馏水,锥形瓶,烧杯,
双孔橡皮塞,橡皮管,玻璃导管,集气瓶,
玻璃片,蜡烛,木条,火柴,铁皮架。
实验室制取C O2,选用石灰石(或大理石)为原料,则不能选 用稀硫酸。因为生成的硫酸钙是微溶性物质,它会包裹在石灰石表面,使酸液不能与石灰石接触,从而使反应中止。
二氧化碳的制取和性质研究
1.制取二氧化碳。
(1)按图 3-58 组装好制取二氧化碳的简易装置,
检查装置的气密性。
(2)在锥形瓶中加入几小块大理石,塞紧带有
长颈漏斗和导管的橡皮塞。
(3)把气体导管插入集气瓶中,导管口应处在接近集气瓶的瓶底处。
二氧化碳的制取和性质研究
(4)通过长颈漏斗加入适
量的稀盐酸,锥形瓶中立刻有气体产生。
(5)片刻后,把燃着的火柴放到集气瓶口的上方,如果火柴很快熄灭,说明集气瓶中已经收集满二氧化碳气体,盖好毛玻璃片,将集气瓶口向上放在桌子上备用。
二氧化碳的制取和性质研究
2.试验二氧化碳性质。
(1)把一支短蜡烛固定在烧杯中的铁皮架上,点燃。如图 3-59 所示,拿起集满二氧化碳的集气瓶,向烧杯中缓缓倾倒二氧化碳,观察到的现象是 ___________
二氧化碳的制取和性质研究
(2)如图 3-60 所示,取一支试管,注
入少量澄清石灰水,通入二氧化碳,观察
到的现象是 ______________________________________________________。
(3)另取一支试管,加入 2 毫升蒸馏水,滴入 1~2 滴石蕊试液,为 ________ 色,通入二氧化碳气体,溶液颜色变为 _________ 色。
二氧化碳的制取和性质研究
图 3-61 是某学生设计的实验室制取并收集二氧化碳气体的装置图。指出装置中的错误之处,并说明原因。
四、二氧化碳的应用
CO 的性质 CO 的用途
能溶于水(物理性质) 生产汽水等碳酸饮料
干冰(固态CO )升华吸热(物理性质) 作为制冷剂,用于人工降雨,
制造舞台云雾效果等
一般情况下,不燃烧,也不支持燃烧(化学性质),密度比空气的大(物理性质) 用来灭火
参与植物光合作用(化学性质), 作为气体肥料,提高光合作
用的强度和效率
能用CO 、H O、NaCl等生产纯碱(Na CO ) (化学性质) 作为化工产品的原料
二氧化碳的下列用途没有利用其化学性质的是( )
A.干冰用于人工降雨
B.二氧化碳用于灭火
C.二氧化碳作为气体肥料
D.二氧化碳用于制纯碱
解析:干冰用于人工降雨,利用了干冰升华时吸热的性质,属于物理性质。
答案:A
课堂小结
如图是实验室制取气体的常用装置。实验小组同学想要制取并收集一瓶干燥的二氧化碳气体,可选择下列装置中的发生装置: ;收集装置: ;干燥装置: 。(请选出所有可能的答案,用所给字母填空)
课堂小练习
【解答】解:实验室常用大理石(或石灰石)和稀盐酸反应制取二氧化碳,属于固、液常温型,并要在后面接干燥装置,应该选的发生装置是B;二氧化碳的密度比空气大,能溶于水,要收集干燥的二氧化碳要用装置E;二氧化碳能和氢氧化钠反应,二氧化碳不和浓硫酸反应,浓硫酸具有吸水性,可用浓硫酸干燥二氧化碳,所以干燥装置是G。故答案为:B;E;G。
正确规范的操作是实验成功的关键,下列实验操作符合规范的是( )
课堂小练习
【解答】解:A.配制溶液时应将固体放入烧杯中配制,不可在量筒中配制,故A操作错误;
B.因为氧气的密度比水小,所以收集氧气时,应从短导管进入,将水从长导管排出,故B操作正确;
C.二氧化碳验满的方法是将燃着的木条放在集气瓶口,故C操作错误;
D.测pH时,应将待测液滴在pH试纸上,而不是将pH试纸伸入待测液中,这样操作会污染试剂,故D操作错误。
故选:B。
小金利用如图装置研究二氧化碳的性质。注射器内装有足量稀盐酸,硬质玻璃管中有四个棉球,其中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。下列关于实验过程及现象的分析,不合理的是( )
A.若把稀盐酸换成稀硫酸则反应速度太慢,可能会影响实验结论
B.若把大理石换成碳酸钠则反应速度太快,可能会影响实验结论
C.通过①②或③④现象的比较,均能得出二氧化碳溶于水呈酸性
D.通过①④或②③现象的比较,均能得出二氧化碳密度大于空气
课堂小练习
【解答】解:A、稀硫酸和大理石反应,生成硫酸钙,微溶于水的硫酸钙覆盖在石灰石的表面,阻碍反应进一步进行,可能会影响实验结论;B、碳酸钠与稀盐酸反应速率过快,可能会影响实验结论;
C、①④处棉球会变成红色,②③处干燥的棉球不变色,所以通过①②或③④现象的比较,均能得出二氧化碳溶于水呈酸性;D、①④处棉球会变成红色,②③处干燥的棉球不变色,故通过①④能得出二氧化碳密度大于空气,而②③不能得出二氧化碳密度大于空气。故选:D。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
