3.1空气与氧气 第2课时(课件 24张PPT)
文档属性
| 名称 | 3.1空气与氧气 第2课时(课件 24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 23.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-04-28 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
1
新课导入
(1)班里来了一位新同学,如果你想认识他,你会从哪些方面认识他?
(2)你用哪些方法认识这位新同学?
特点
观察法、实验法
如何认识“氧气”?
特点
性质
3.1.2 空气与氧气
【核心概念】
1.物质的结构与性质
【学习内容与要求】
1.2 空气与水是重要的物质
⑤认识氧气的主要性质。
1.科学观念:认识氧气的物理性质和化学性质,能与许多物质发生反应,了解燃烧时的一些特殊的实验现象,认识氧化物的概念。
2.科学思维:初步具有现象描述及表达能力;学习从具体到抽象、从个别到一般的归纳方法。
3.探究实践:培养学生对实验的观察、分析判断能力及动手实验能力﹔学会闻气体;会分析实验信息并从中归纳得出结论。
4.态度责任:培养学生对知识与生活密切联系的意识,养成实事求是、尊重科学、尊重事物发展规律的科学态度。
2
核心概念与素养
3
新知探究
1.1 氧气的颜色、状态和气味
任务一:知识氧气的物理性质
从哪些角度认识氧气的的物理性质?
物理性质
颜色:无色……
状态:固态、液态、气态
气味:无味、刺激性气味、臭鸡蛋气味……
沸点、熔点、凝固点、
硬度:质地硬、质地软
导电性、导热性、延展性
密度
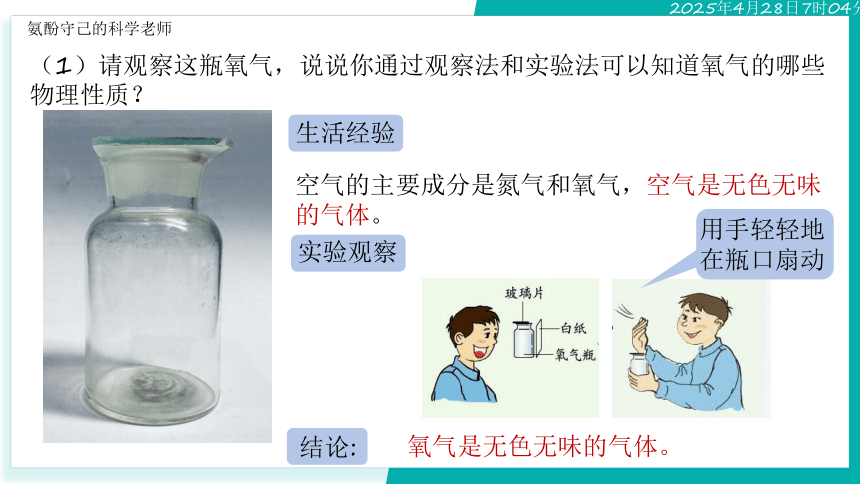
(1)请观察这瓶氧气,说说你通过观察法和实验法可以知道氧气的哪些物理性质?
生活经验
空气的主要成分是氮气和氧气,空气是无色无味的气体。
氧气是无色无味的气体。
实验观察
用手轻轻地在瓶口扇动
结论:
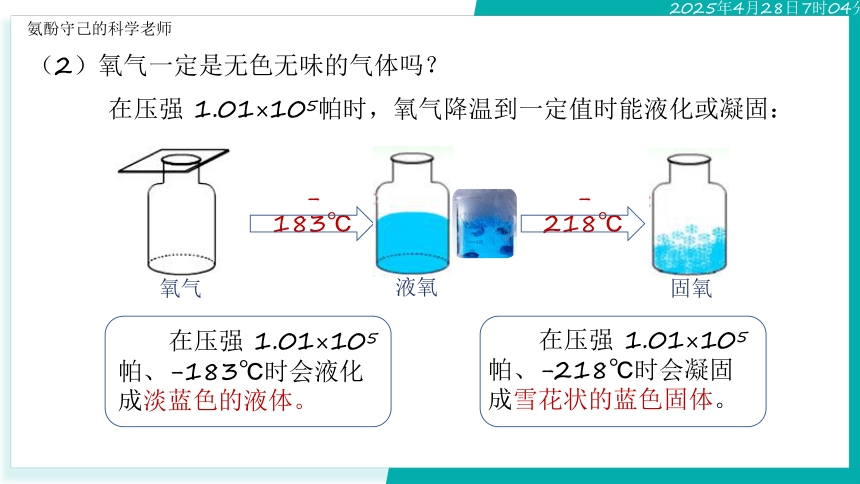
(2)氧气一定是无色无味的气体吗?
氧气
在压强 1.01×105帕时,氧气降温到一定值时能液化或凝固:
-183℃
固氧
-218℃
在压强 1.01×105帕、-183℃时会液化成淡蓝色的液体。
在压强 1.01×105帕、-218℃时会凝固成雪花状的蓝色固体。
液氧
1.2 氧气的溶解度
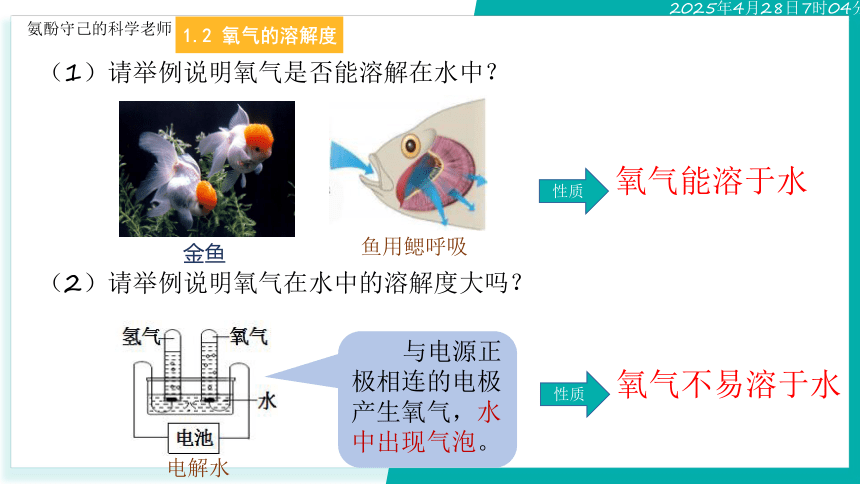
(1)请举例说明氧气是否能溶解在水中?
(2)请举例说明氧气在水中的溶解度大吗?
金鱼
鱼用鳃呼吸
电解水
与电源正极相连的电极产生氧气,水中出现气泡。
性质
氧气能溶于水
性质
氧气不易溶于水
(1)你能设计实验测量氧气在水中的溶解度吗?
如何表示溶解度?
一定温度下,100g水中能溶解物质的最大质量
如何表示溶解度?
一定温度下,1升水中能溶解气体的最大体积
常温下1 升水中大约能溶解30 毫升的氧气。
性质
1.3 氧气的密度
(1)如图,将氧气倾倒入右侧容器内后,观察到杠杆右端向下倾斜的现象,说明氧气的密度大小和空气的密度大小存在怎么的关系?
(2)盛有氧气的集气瓶应该如何放置?
标准状况下氧气的密度为1.429克/升,空气密度1.293 克/ 升。
氧气的密度比空气略大。
正放
倒放
2.1 助燃性
任务二:知识氧气的化学性质
带火星的木条复燃
性质
氧气能支持燃烧(助燃性)
用带火星的木条检验氧气
性质
用途
决定
用带火星的木条靠近待检验气体,若木条复燃,则证明是氧气
4.木炭燃烧的实验如图所示。下列有关说法正确的是( )
A.①中木炭发出耀眼的白光
B.②中氧气为无色气体,
密度比空气小
C.③中澄清石灰水变浑浊
D.对比①②现象可证明,氧气具有可燃性
C
b本
SO2
硫在空气中剧烈燃烧,发出淡蓝色火焰,生成刺激性气味的气体,并放出大量的热
硫在氧气中剧烈燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,并放出大量的热
硫是黄色的粉末状固体
2.2 与硫反应
(1)硫在空气中(氧气中)燃烧是物理变化还是化学变化?并说明理由。
(2)你能写出这个化学反应的文字表达式吗?
(3)若用黄球表示硫原子,用蓝球表示氧原子,你能表示硫在氧气中燃烧的实质吗?
化学变化
+
氧气
二氧化硫
点燃
硫
(S) (O2) (SO2)
====
点燃
反应物
生成物
(反应)条件
+
2.3 与铁反应
剧烈燃烧,火星四射
放出大量
黑
思考:为什么要将“四氧化三铁”五个字去掉?
(1)请写出铁在氧气中燃烧的文字表达式和化学式
(2)为什么在化学式中Fe前要加数字“2”?
铁
+
氧气
点燃
四氧化三铁
3Fe
+
2O2
点燃
Fe3O4
=======
化学变化的实质是分子分解成原子,原子重新组合成新的分子。化学反应前后原子的种类和数目保持不变
1.关于铁在氧气里燃烧的实验,你能回答下列问题吗?
(1)氧气与金属反应时在容器底部垫一层细沙的原因是什么?
(2)火柴在这里的作用是什么?
(3)将铁丝绕成螺旋状,这样做的目的是什么?
(4)在火柴快要燃尽时才放进集气瓶的目的是什么?
防止高温熔融物溅落炸裂瓶底
引燃
防止火柴燃烧消耗过多的氧气使铁丝不能顺利燃烧。
螺旋状是增加铁丝的受热面积和与氧气的接触面积。
通过以上实验可以看出,氧气是一种化学性质比较活泼的气体,会与许多物质发生反应。
+
氧气
二氧化硫
点燃
硫
铁
+
氧气
点燃
四氧化三铁
磷
+
氧气
点燃
五氧化二磷
镁
+
氧气
点燃
氧化镁
+
O2
SO2
点燃
S
Fe
+
O2
点燃
Fe3O4
P
+
O2
点燃
P2O5
Mg
+
O2
点燃
MgO
碳
+
氧气
点燃
二氧化碳
C
+
O2
点燃
CO2
硫在空气和氧气里燃烧
铁丝在氧气里燃烧
氧气的浓度不同。
空气中氧气只占空气体积的21%,其浓度比纯氧中浓度低;反应物浓度越大,反应越剧烈。
3.下列有关实验现象的描述错误的是( )
A.铁丝在氧气中燃烧,火星四射,生成黑色固体
B.红磷在空气中燃烧,产生大量白烟
C.木炭在氧气中燃烧,发出白光,放出热量
D.硫在氧气中燃烧,发出淡蓝色火焰,生成具有刺激性气味的气体
D
3.1 氧化物
任务三:知识氧化物
请写出下列物质的化学式。它们在组成元素上有什么共同点?
物质名称 化学式
二氧化硫
四氧化三铁
五氧化二磷
氧化镁
SO2
Fe3O4
P2O5
MgO
由两种元素组成,其中一种元素是氧元素的化合物。
是氧化物。
物质
混合物
纯净物
不同物质简单的组成
单质
一种元素组成
化合物
不同元素组成
氧化物
=另一元素+氧元素
其他
2.分类是学习科学的方法之一。下列物质属于氧化物的是( )
A.氧气
B.水
C.纯碱(Na2CO3)
D.氢氧化钙[Ca(OH)2]
B
11.分析硫、碳、铁丝三种物质在氧气中的燃烧,回答问题。
(1)从操作角度:三种物质都要自上而下________(填“快速”或“缓慢”)伸入盛有氧气的集气瓶中。铁丝燃烧实验中,需要在铁丝下端的火柴快要燃尽时再将铁丝伸入充满氧气的集气瓶中,其目的是
缓慢
______________________________________________________。
(2)从现象角度:在空气中点燃硫时,观察到淡黄色固体熔化后,燃烧发出________色火焰,在氧气中,硫燃烧得更旺。碳在氧气中比在空气中燃烧得更旺。铁丝在空气中不燃烧,在氧气中剧烈燃烧,火星四射并生成黑色的固体,此黑色的固体物质是_______________(填物质名称)。
(3)从装置角度:物质燃烧实验时,集气瓶底是否放入水及放入水的原因各不相同,铁丝燃烧时,集气瓶底放入少许水的目的是
__________________________________。
防止火柴燃烧消耗过多的氧气,使铁丝燃烧现象不明显
淡蓝
四氧化三铁
防止高温熔化物溅落炸裂集气瓶
1
新课导入
(1)班里来了一位新同学,如果你想认识他,你会从哪些方面认识他?
(2)你用哪些方法认识这位新同学?
特点
观察法、实验法
如何认识“氧气”?
特点
性质
3.1.2 空气与氧气
【核心概念】
1.物质的结构与性质
【学习内容与要求】
1.2 空气与水是重要的物质
⑤认识氧气的主要性质。
1.科学观念:认识氧气的物理性质和化学性质,能与许多物质发生反应,了解燃烧时的一些特殊的实验现象,认识氧化物的概念。
2.科学思维:初步具有现象描述及表达能力;学习从具体到抽象、从个别到一般的归纳方法。
3.探究实践:培养学生对实验的观察、分析判断能力及动手实验能力﹔学会闻气体;会分析实验信息并从中归纳得出结论。
4.态度责任:培养学生对知识与生活密切联系的意识,养成实事求是、尊重科学、尊重事物发展规律的科学态度。
2
核心概念与素养
3
新知探究
1.1 氧气的颜色、状态和气味
任务一:知识氧气的物理性质
从哪些角度认识氧气的的物理性质?
物理性质
颜色:无色……
状态:固态、液态、气态
气味:无味、刺激性气味、臭鸡蛋气味……
沸点、熔点、凝固点、
硬度:质地硬、质地软
导电性、导热性、延展性
密度
(1)请观察这瓶氧气,说说你通过观察法和实验法可以知道氧气的哪些物理性质?
生活经验
空气的主要成分是氮气和氧气,空气是无色无味的气体。
氧气是无色无味的气体。
实验观察
用手轻轻地在瓶口扇动
结论:
(2)氧气一定是无色无味的气体吗?
氧气
在压强 1.01×105帕时,氧气降温到一定值时能液化或凝固:
-183℃
固氧
-218℃
在压强 1.01×105帕、-183℃时会液化成淡蓝色的液体。
在压强 1.01×105帕、-218℃时会凝固成雪花状的蓝色固体。
液氧
1.2 氧气的溶解度
(1)请举例说明氧气是否能溶解在水中?
(2)请举例说明氧气在水中的溶解度大吗?
金鱼
鱼用鳃呼吸
电解水
与电源正极相连的电极产生氧气,水中出现气泡。
性质
氧气能溶于水
性质
氧气不易溶于水
(1)你能设计实验测量氧气在水中的溶解度吗?
如何表示溶解度?
一定温度下,100g水中能溶解物质的最大质量
如何表示溶解度?
一定温度下,1升水中能溶解气体的最大体积
常温下1 升水中大约能溶解30 毫升的氧气。
性质
1.3 氧气的密度
(1)如图,将氧气倾倒入右侧容器内后,观察到杠杆右端向下倾斜的现象,说明氧气的密度大小和空气的密度大小存在怎么的关系?
(2)盛有氧气的集气瓶应该如何放置?
标准状况下氧气的密度为1.429克/升,空气密度1.293 克/ 升。
氧气的密度比空气略大。
正放
倒放
2.1 助燃性
任务二:知识氧气的化学性质
带火星的木条复燃
性质
氧气能支持燃烧(助燃性)
用带火星的木条检验氧气
性质
用途
决定
用带火星的木条靠近待检验气体,若木条复燃,则证明是氧气
4.木炭燃烧的实验如图所示。下列有关说法正确的是( )
A.①中木炭发出耀眼的白光
B.②中氧气为无色气体,
密度比空气小
C.③中澄清石灰水变浑浊
D.对比①②现象可证明,氧气具有可燃性
C
b本
SO2
硫在空气中剧烈燃烧,发出淡蓝色火焰,生成刺激性气味的气体,并放出大量的热
硫在氧气中剧烈燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,并放出大量的热
硫是黄色的粉末状固体
2.2 与硫反应
(1)硫在空气中(氧气中)燃烧是物理变化还是化学变化?并说明理由。
(2)你能写出这个化学反应的文字表达式吗?
(3)若用黄球表示硫原子,用蓝球表示氧原子,你能表示硫在氧气中燃烧的实质吗?
化学变化
+
氧气
二氧化硫
点燃
硫
(S) (O2) (SO2)
====
点燃
反应物
生成物
(反应)条件
+
2.3 与铁反应
剧烈燃烧,火星四射
放出大量
黑
思考:为什么要将“四氧化三铁”五个字去掉?
(1)请写出铁在氧气中燃烧的文字表达式和化学式
(2)为什么在化学式中Fe前要加数字“2”?
铁
+
氧气
点燃
四氧化三铁
3Fe
+
2O2
点燃
Fe3O4
=======
化学变化的实质是分子分解成原子,原子重新组合成新的分子。化学反应前后原子的种类和数目保持不变
1.关于铁在氧气里燃烧的实验,你能回答下列问题吗?
(1)氧气与金属反应时在容器底部垫一层细沙的原因是什么?
(2)火柴在这里的作用是什么?
(3)将铁丝绕成螺旋状,这样做的目的是什么?
(4)在火柴快要燃尽时才放进集气瓶的目的是什么?
防止高温熔融物溅落炸裂瓶底
引燃
防止火柴燃烧消耗过多的氧气使铁丝不能顺利燃烧。
螺旋状是增加铁丝的受热面积和与氧气的接触面积。
通过以上实验可以看出,氧气是一种化学性质比较活泼的气体,会与许多物质发生反应。
+
氧气
二氧化硫
点燃
硫
铁
+
氧气
点燃
四氧化三铁
磷
+
氧气
点燃
五氧化二磷
镁
+
氧气
点燃
氧化镁
+
O2
SO2
点燃
S
Fe
+
O2
点燃
Fe3O4
P
+
O2
点燃
P2O5
Mg
+
O2
点燃
MgO
碳
+
氧气
点燃
二氧化碳
C
+
O2
点燃
CO2
硫在空气和氧气里燃烧
铁丝在氧气里燃烧
氧气的浓度不同。
空气中氧气只占空气体积的21%,其浓度比纯氧中浓度低;反应物浓度越大,反应越剧烈。
3.下列有关实验现象的描述错误的是( )
A.铁丝在氧气中燃烧,火星四射,生成黑色固体
B.红磷在空气中燃烧,产生大量白烟
C.木炭在氧气中燃烧,发出白光,放出热量
D.硫在氧气中燃烧,发出淡蓝色火焰,生成具有刺激性气味的气体
D
3.1 氧化物
任务三:知识氧化物
请写出下列物质的化学式。它们在组成元素上有什么共同点?
物质名称 化学式
二氧化硫
四氧化三铁
五氧化二磷
氧化镁
SO2
Fe3O4
P2O5
MgO
由两种元素组成,其中一种元素是氧元素的化合物。
是氧化物。
物质
混合物
纯净物
不同物质简单的组成
单质
一种元素组成
化合物
不同元素组成
氧化物
=另一元素+氧元素
其他
2.分类是学习科学的方法之一。下列物质属于氧化物的是( )
A.氧气
B.水
C.纯碱(Na2CO3)
D.氢氧化钙[Ca(OH)2]
B
11.分析硫、碳、铁丝三种物质在氧气中的燃烧,回答问题。
(1)从操作角度:三种物质都要自上而下________(填“快速”或“缓慢”)伸入盛有氧气的集气瓶中。铁丝燃烧实验中,需要在铁丝下端的火柴快要燃尽时再将铁丝伸入充满氧气的集气瓶中,其目的是
缓慢
______________________________________________________。
(2)从现象角度:在空气中点燃硫时,观察到淡黄色固体熔化后,燃烧发出________色火焰,在氧气中,硫燃烧得更旺。碳在氧气中比在空气中燃烧得更旺。铁丝在空气中不燃烧,在氧气中剧烈燃烧,火星四射并生成黑色的固体,此黑色的固体物质是_______________(填物质名称)。
(3)从装置角度:物质燃烧实验时,集气瓶底是否放入水及放入水的原因各不相同,铁丝燃烧时,集气瓶底放入少许水的目的是
__________________________________。
防止火柴燃烧消耗过多的氧气,使铁丝燃烧现象不明显
淡蓝
四氧化三铁
防止高温熔化物溅落炸裂集气瓶
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
