八下第三章空气与生命复习(1)
图片预览





文档简介
(共21张PPT)
第三章
空气与生命复习(1)
空
气
的
组
成
成
分
氧
气
二氧化碳
氮
气
稀有气体
其他气体
(21%)
(78%)
(0.03%)
(0.94%)
(0.03%)
氧气性质
物理性质:
化学性质:
常温下无色、无味、呈气态
密度比空气大,
不易溶于水。
比较活泼
S
+
O2
SO2
点燃
明亮的蓝紫色火焰,
生成具有刺激性气味的气体
现象:
氧化反应
氧化物
由两种元素构成,其中一种元素是氧的化合物
你能说说氧气有什么用途
助燃
供给呼吸
不同点
剧烈氧化
缓慢氧化
相同点
氧化反应
碳
磷
铁丝
说一说
反应现象
写一写
化学方程式
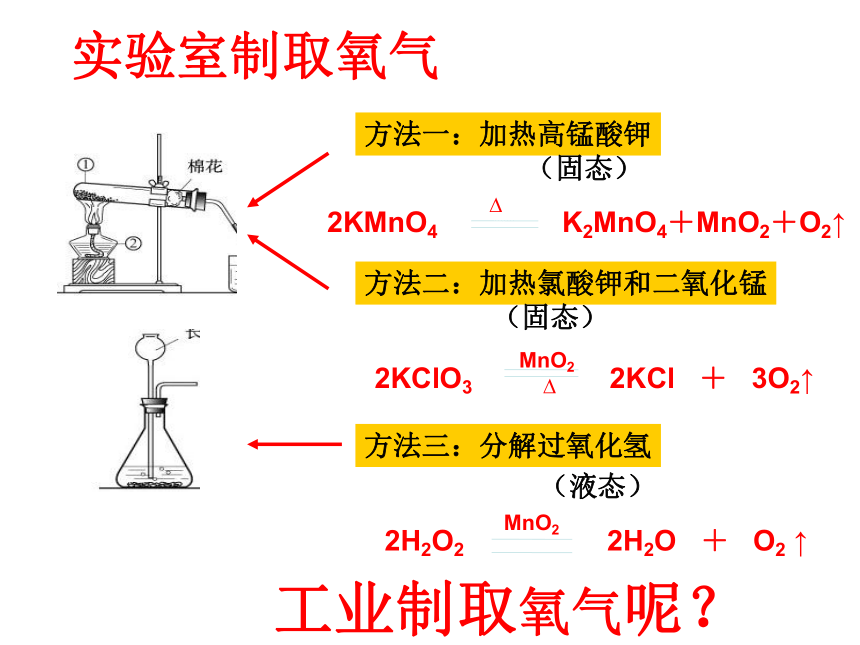
实验室制取氧气
2KMnO4
K2MnO4+MnO2+O2↑
2KClO3
2KCl
+
3O2↑
MnO2
MnO2
2H2O2
2H2O
+
O2
↑
方法一:加热高锰酸钾
方法二:加热氯酸钾和二氧化锰
方法三:分解过氧化氢
(固态)
(固态)
(液态)
工业制取氧气呢?
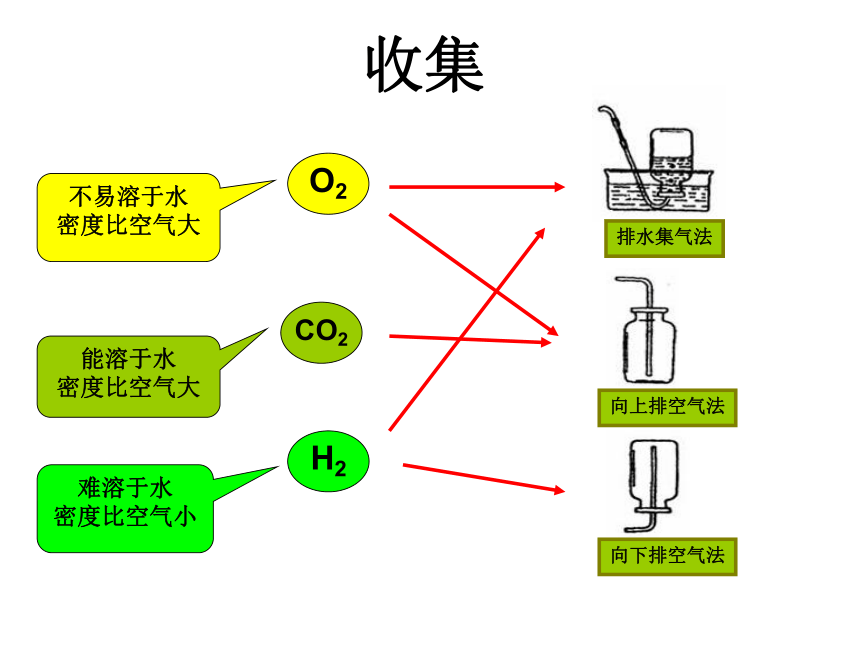
收集
不易溶于水
密度比空气大
能溶于水
密度比空气大
难溶于水
密度比空气小
O2
CO2
H2
排水集气法
向上排空气法
向下排空气法
O2
O2
空气
空气
O2
O2
水
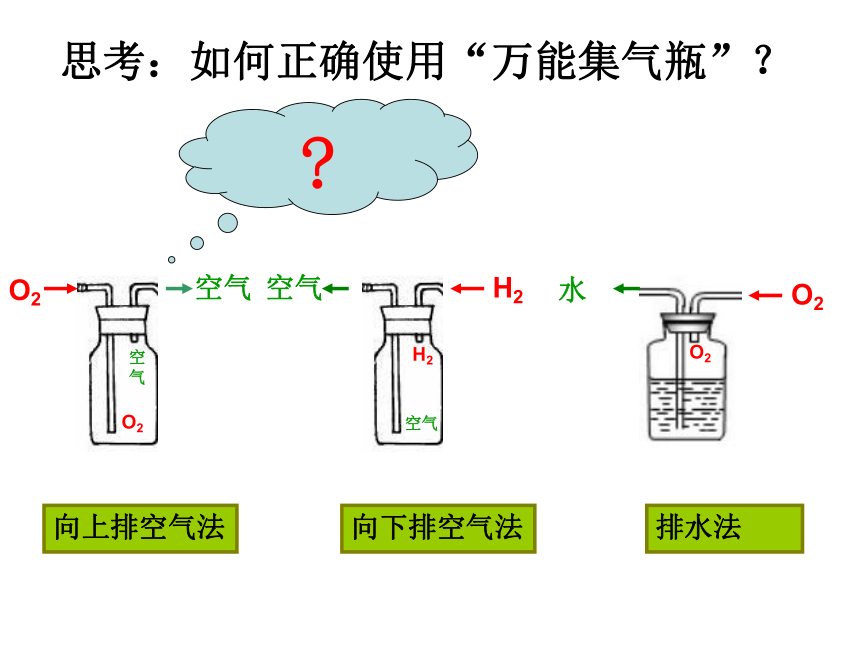
思考:如何正确使用“万能集气瓶”?
H2
空气
空气
H2
向上排空气法
向下排空气法
排水法
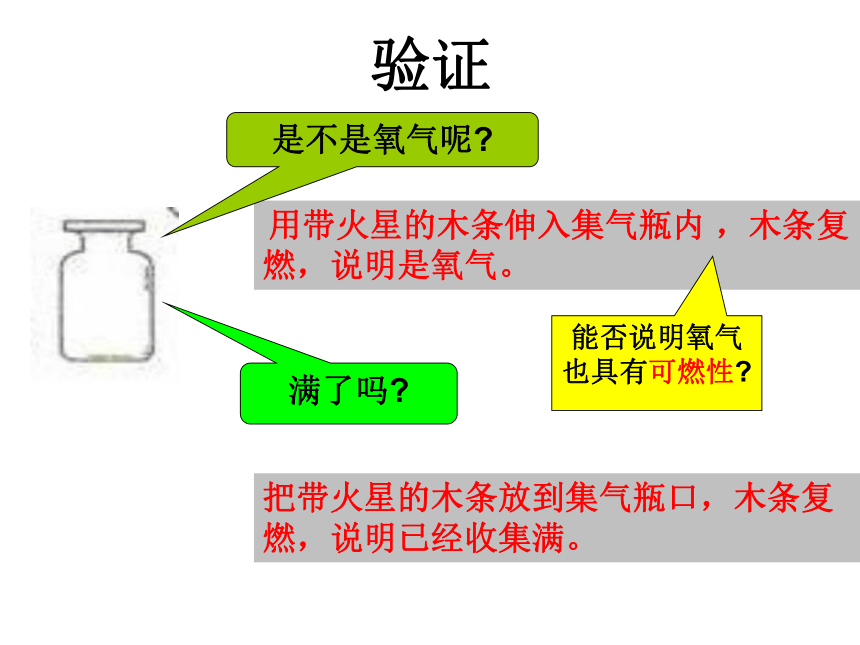
验证
用带火星的木条伸入集气瓶内
,木条复燃,说明是氧气。
把带火星的木条放到集气瓶口,木条复燃,说明已经收集满。
是不是氧气呢
满了吗
能否说明氧气也具有可燃性
科技小讨论
冥王星表面大气的主要成分是甲烷,甲烷是一种可燃性气体,美国计划向冥王星发射探测火箭,有人认为这样做很危险,因为火箭喷出的
火焰会点燃冥王星上的甲烷,你认同吗?
燃烧条件
可燃物
助燃剂(氧气)
温度达到着火点
灭火
同时满足
方法一
降低着火点
方法二
隔绝氧气
×
使温度降到
着火点以下
参加反应的各物质质量总和等于反应后生成的各物质的质量总和。
即在化学反应前后原子的种类和数目不变
内容
质量守恒定律
化学方程式
遵守
1、下列物质属于氧化物的是(
)
A.氧气
B.干冰
C.氯酸钾
D.过氧化氢溶液
2、实验室制取气体选择收集方法时,下列性质:①颜色;②密度;③溶解性;④可燃性;⑤能否与水反应,必须考虑的是(
)
A.①②③
B.②③④
C.③④⑤
D.②③⑤
3.
小红在餐厅看到服务员用盖子熄灭酒精灯火锅,该灭火方法的主要原理是
(
)
A.清除可燃物
B.降低可燃物的着火点
C.使可燃物的温度降到着火
D.隔绝空气
B
D
D
4、下列是实验室常用仪器装置图
A.
B.
C.
D.
E
(1)
实验室利用高锰酸钾加热分解制O2,用E装置收集氧气,停止加热前,必须先
。
(2)
实验室制取CO2应选择装置A,此实验中分液漏斗中应放的物质是
,判断CO2已收集满的方法是
。
(3)
已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,在实验室中常采用熟石灰固体和氯化铵固体混合加热的方法来制取,则应选择的发生装置及收集装置是
。
将导管从水槽中移出
稀盐酸
将点燃的木条伸到集气瓶口,观察其是否熄灭
B和D
5.某化合物完全燃烧,消耗了氧气9.6克,同时生成二氧化碳8.8克、水5.4克,则该化合物
(
)
A、只含有C、H两种元素
B、一定含C、H两种元素,可能含O元素
C、一定含C、H、O
三种元素
D、一定含C、O两种元素,可能含H元素
C
6.某有机物R,其燃烧的化学方程式为:
R+3O2
点燃
2CO2+3H2O,则R的化学式是(
)
A、C2H6
B、C2H6O
C、C2H4
D、C2H4O
7.在化学反应:
4NH3+5O2=====
4X+6
H2O中,
X的分子式是
(
)
A、N2O
B、NO2
C、NO
D、N2O3
B
C
8.在化学反应A+B===C+2D中,10克A与14克B恰好完全反应,生成16克C。若使5克A与足量的B反应,可生成D的质量为
(
)
A、4克
B、8克
C、12克
D、16克
9.在化学反应A+B===C+D中,已知25克A与10克B恰好完全反应,生成5克C。当反应有12克D生成时,参加反应的A的质量为
(
)
A、5克
B、10克
C、20克
D、25克
A
B
计算
1、实验室用过氧化氢制取氧气,现欲制氧气3.2克?问:需过氧化氢多少克?
解:
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
X
32
3.2
X
=
6.8g
68
32
解题步聚
写出方程式
对应数据比
列出比例式
算出答案
设需过氧化氢的质量为X
2、实验室用过氧化氢制取氧气,现欲制氧气2.24升
(氧气在常温下的密度为1.429克/升)。问:需过氧化氢多少克?
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
32
解:
m
=
ρv
=1.429x2.24
=
3.2g
68
X
32
3.2
X
=
6.8g
设需过氧化氢的质量为X
3、如图所示,实验室用过氧化氢制取氧气,烧瓶内的物质的质量在完全反应前后如右图所示,问:实验前加入过氧化氢多少克?
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
32
68
X
32
3.2
X
=
6.8g
解:
氧气质量=100
–
96.8
=
3.2g
设需过氧化氢的质量为X
4、实验室用100克过氧化氢溶液制取氧气,完全反应后生成氧气3.2克。问:原过氧化氢溶液的质量分数是多少?
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
32
68
X
32
3.2
X
=
6.8g
解:
6.8
100
100%
6.8%
设需过氧化氢的质量为X
作业:作业本复习题
第三章
空气与生命复习(1)
空
气
的
组
成
成
分
氧
气
二氧化碳
氮
气
稀有气体
其他气体
(21%)
(78%)
(0.03%)
(0.94%)
(0.03%)
氧气性质
物理性质:
化学性质:
常温下无色、无味、呈气态
密度比空气大,
不易溶于水。
比较活泼
S
+
O2
SO2
点燃
明亮的蓝紫色火焰,
生成具有刺激性气味的气体
现象:
氧化反应
氧化物
由两种元素构成,其中一种元素是氧的化合物
你能说说氧气有什么用途
助燃
供给呼吸
不同点
剧烈氧化
缓慢氧化
相同点
氧化反应
碳
磷
铁丝
说一说
反应现象
写一写
化学方程式
实验室制取氧气
2KMnO4
K2MnO4+MnO2+O2↑
2KClO3
2KCl
+
3O2↑
MnO2
MnO2
2H2O2
2H2O
+
O2
↑
方法一:加热高锰酸钾
方法二:加热氯酸钾和二氧化锰
方法三:分解过氧化氢
(固态)
(固态)
(液态)
工业制取氧气呢?
收集
不易溶于水
密度比空气大
能溶于水
密度比空气大
难溶于水
密度比空气小
O2
CO2
H2
排水集气法
向上排空气法
向下排空气法
O2
O2
空气
空气
O2
O2
水
思考:如何正确使用“万能集气瓶”?
H2
空气
空气
H2
向上排空气法
向下排空气法
排水法
验证
用带火星的木条伸入集气瓶内
,木条复燃,说明是氧气。
把带火星的木条放到集气瓶口,木条复燃,说明已经收集满。
是不是氧气呢
满了吗
能否说明氧气也具有可燃性
科技小讨论
冥王星表面大气的主要成分是甲烷,甲烷是一种可燃性气体,美国计划向冥王星发射探测火箭,有人认为这样做很危险,因为火箭喷出的
火焰会点燃冥王星上的甲烷,你认同吗?
燃烧条件
可燃物
助燃剂(氧气)
温度达到着火点
灭火
同时满足
方法一
降低着火点
方法二
隔绝氧气
×
使温度降到
着火点以下
参加反应的各物质质量总和等于反应后生成的各物质的质量总和。
即在化学反应前后原子的种类和数目不变
内容
质量守恒定律
化学方程式
遵守
1、下列物质属于氧化物的是(
)
A.氧气
B.干冰
C.氯酸钾
D.过氧化氢溶液
2、实验室制取气体选择收集方法时,下列性质:①颜色;②密度;③溶解性;④可燃性;⑤能否与水反应,必须考虑的是(
)
A.①②③
B.②③④
C.③④⑤
D.②③⑤
3.
小红在餐厅看到服务员用盖子熄灭酒精灯火锅,该灭火方法的主要原理是
(
)
A.清除可燃物
B.降低可燃物的着火点
C.使可燃物的温度降到着火
D.隔绝空气
B
D
D
4、下列是实验室常用仪器装置图
A.
B.
C.
D.
E
(1)
实验室利用高锰酸钾加热分解制O2,用E装置收集氧气,停止加热前,必须先
。
(2)
实验室制取CO2应选择装置A,此实验中分液漏斗中应放的物质是
,判断CO2已收集满的方法是
。
(3)
已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,在实验室中常采用熟石灰固体和氯化铵固体混合加热的方法来制取,则应选择的发生装置及收集装置是
。
将导管从水槽中移出
稀盐酸
将点燃的木条伸到集气瓶口,观察其是否熄灭
B和D
5.某化合物完全燃烧,消耗了氧气9.6克,同时生成二氧化碳8.8克、水5.4克,则该化合物
(
)
A、只含有C、H两种元素
B、一定含C、H两种元素,可能含O元素
C、一定含C、H、O
三种元素
D、一定含C、O两种元素,可能含H元素
C
6.某有机物R,其燃烧的化学方程式为:
R+3O2
点燃
2CO2+3H2O,则R的化学式是(
)
A、C2H6
B、C2H6O
C、C2H4
D、C2H4O
7.在化学反应:
4NH3+5O2=====
4X+6
H2O中,
X的分子式是
(
)
A、N2O
B、NO2
C、NO
D、N2O3
B
C
8.在化学反应A+B===C+2D中,10克A与14克B恰好完全反应,生成16克C。若使5克A与足量的B反应,可生成D的质量为
(
)
A、4克
B、8克
C、12克
D、16克
9.在化学反应A+B===C+D中,已知25克A与10克B恰好完全反应,生成5克C。当反应有12克D生成时,参加反应的A的质量为
(
)
A、5克
B、10克
C、20克
D、25克
A
B
计算
1、实验室用过氧化氢制取氧气,现欲制氧气3.2克?问:需过氧化氢多少克?
解:
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
X
32
3.2
X
=
6.8g
68
32
解题步聚
写出方程式
对应数据比
列出比例式
算出答案
设需过氧化氢的质量为X
2、实验室用过氧化氢制取氧气,现欲制氧气2.24升
(氧气在常温下的密度为1.429克/升)。问:需过氧化氢多少克?
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
32
解:
m
=
ρv
=1.429x2.24
=
3.2g
68
X
32
3.2
X
=
6.8g
设需过氧化氢的质量为X
3、如图所示,实验室用过氧化氢制取氧气,烧瓶内的物质的质量在完全反应前后如右图所示,问:实验前加入过氧化氢多少克?
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
32
68
X
32
3.2
X
=
6.8g
解:
氧气质量=100
–
96.8
=
3.2g
设需过氧化氢的质量为X
4、实验室用100克过氧化氢溶液制取氧气,完全反应后生成氧气3.2克。问:原过氧化氢溶液的质量分数是多少?
2H2O2
2H2O
+
O2↑
MnO2
X
3.2
68
32
68
X
32
3.2
X
=
6.8g
解:
6.8
100
100%
6.8%
设需过氧化氢的质量为X
作业:作业本复习题
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
