《饮食中的有机化合物第二课时》课件3
图片预览






文档简介
课件26张PPT。第3章 重要的有机化合物
第3节 饮食中的有机化合物
第2课时 乙 酸
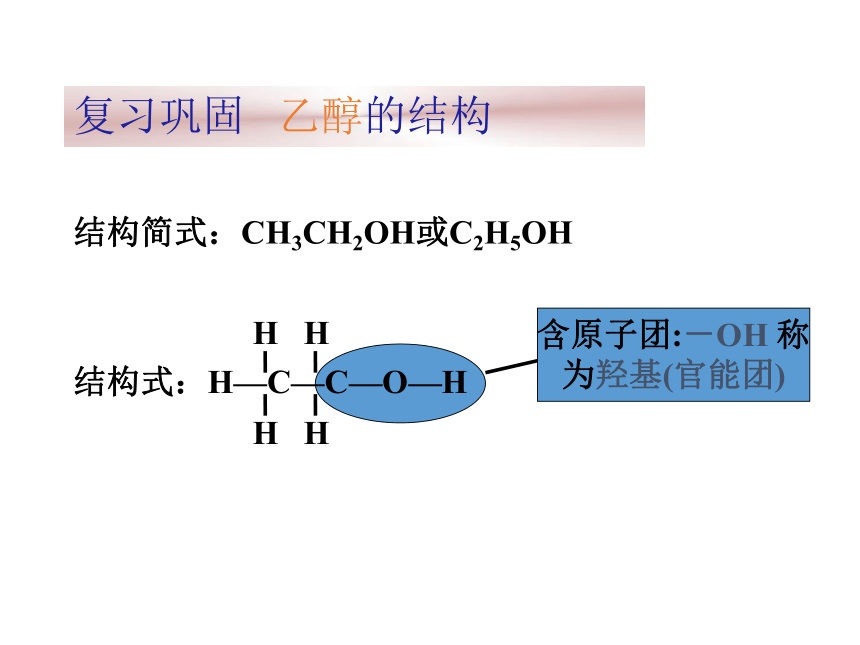
复习巩固 乙醇的结构结构简式:CH3CH2OH或C2H5OH含原子团:-OH 称
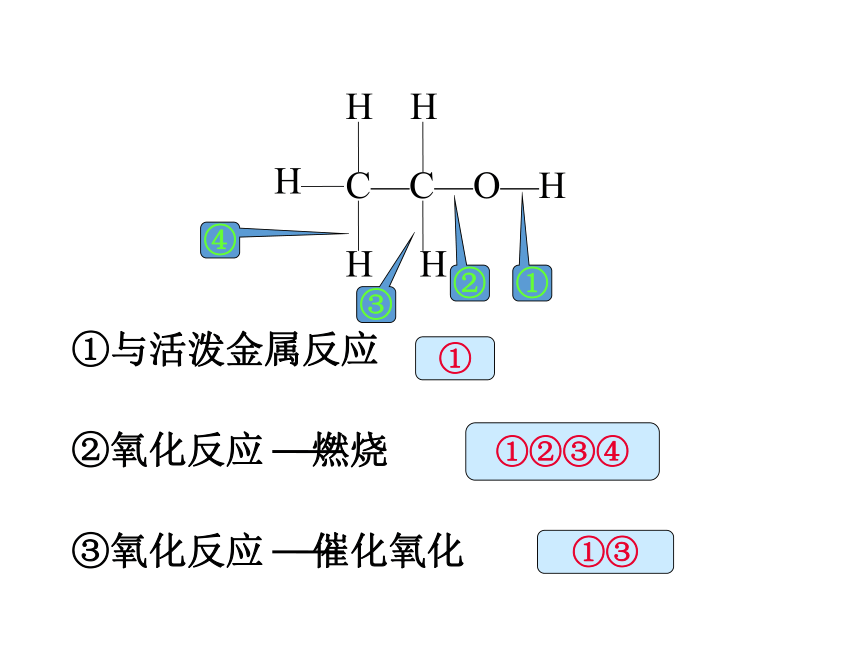
为羟基(官能团)①②③④①③①化学方程式说明:乙基-C2H5对羟基-O-H键有影响,乙醇具有氧化性;其他如K、Mg、Al 等也能把羟基里的氢置换(或取代)出来 。
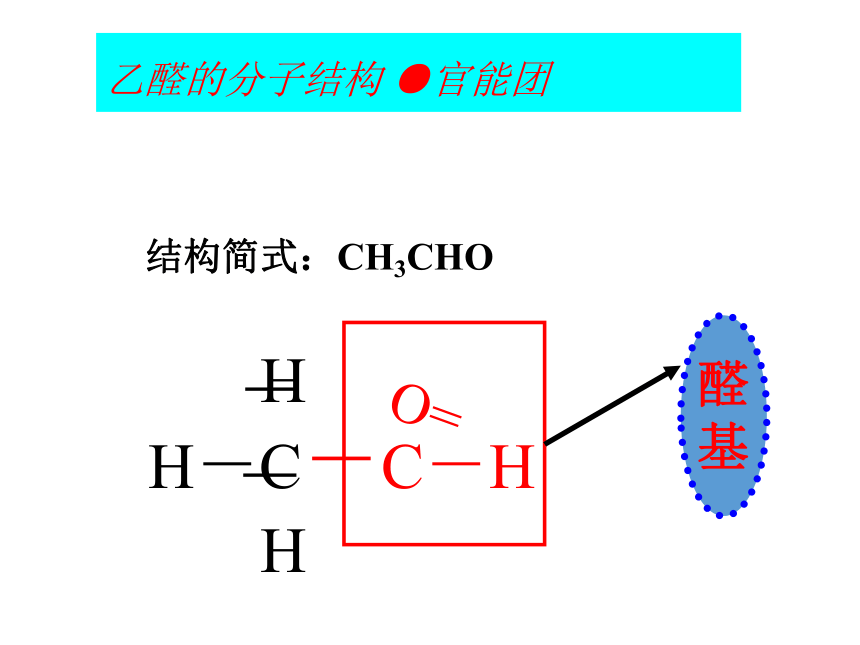
2(-OH ) H2↑1. 与活泼金属反应 (断①键) 2. 燃烧 ( ①②③④键全断) 3. 催化氧化 (断①③)乙醛的分子结构 ●官能团醛
基结构简式:CH3CHO学习目标1、掌握乙酸的结构和化学性质;
2、了解乙酸的物理性质、用途;
3、掌握酯化反应的原理、实质。乙 酸乙酸结构物理性质化学性质知识总结乙酸的物理性质颜 色 :无色强烈刺激性气味液体117.90C乙酸是食醋的主要成分,俗称醋酸。沸 点 :熔 点 :16.60C当温度低于16.6时,乙酸就凝结成像冰一样的晶体,因此无水乙酸又称为冰醋酸。溶解性:易溶于水和酒精气 味 :状 态 :观察与思考乙酸的结构分子式:C2H4O2结构简式:CH3COOH含原子团:-COOH
称为羧基 乙酸在溶于水时能够电离出CHCOO-和H+ ,因而乙酸具有一定的酸性。请你根据现有的化学药品设计实验方案:
(1)证明乙酸的酸性;
(2)证明乙酸是弱酸。联接1联接2乙酸在水溶液中的电离方程式:CH3COOH CH3COO— + H+总 结:
1.乙酸是一种常见的有机酸,它能使指示剂变色,能与活泼金属,碱及盐等物质反应,具有酸的通性。
2.乙酸的酸性比碳酸强。 家庭中常用食醋浸泡有水垢[主要成分是CaCO3和MgOH)2 ]暖瓶或水壶,以清除水垢。请写出有关反应的化学方程式。
迁移 应用 在试管里加入3mL乙醇,然后一边摇动一边慢
慢加入2mL浓硫酸和2mL乙酸,加入2-3块小脆瓷
片;按图连接好装置,用酒精灯小心均匀的加热使
馆3-5min,将产生的蒸汽经导管通到饱和碳酸钠溶
液的液面上,观察现象。思 考:(1)浓硫酸的作用?(2)为什么用饱和的Na2CO3溶液收集乙酸乙酯?催化剂(提高反应速率)、吸水剂(促进反应向生成乙酸乙酯的反应方向进行,提高产率)①中和挥发出来的乙酸
②吸收挥发出来的乙醇
③降低乙酸乙酯的溶解度(3)加热的目的?①提高反应速率
②使生成的乙酸乙酯挥发,有利于收集
③提高乙醇、乙酸的转化率(4)导管的作用是什么?能不能将导管插到液面以下?为什么?导管作用是导气、冷凝。不能将导管插到液面以下,防止发生倒吸。注意点: 1、加药品的顺序:先加乙醇,再加浓硫酸,然后加乙酸。
2、试管要上倾450,使液体受热面积大。
3、导管末端不能插入溶液中,防止受热不均发生液体倒吸。
4、不能用NaOH代替Na2CO3,因为NaOH碱性太强,使乙酸乙酯水解。
5、加碎瓷片的作用:防止爆沸。实验现象:实验结论:饱和碳酸钠溶液的液面上有无色透明的
油状液体产生,并可闻到香味。在浓硫酸存在、加热的条件下,乙酸和
乙醇发生反应,生成无色、透明、不溶
于水、有香味的油状液体。该油状液体
是乙酸乙酯。酯化反应的化学方程式:乙酸乙酯酯化反应像乙酸和乙醇这样生成酯和水的反应称为酯化反应,它是可逆的反应
①与金属,碱等反应显酸性②与乙醇反应①②问题讨论1、乙酸比乙醇的相对分子质量大多少?
2、相对分子质量相同的酸和醇之间有什么关系?
3、制取乙酸乙酯中需加入浓硫酸冰醋酸和乙醇各2ml,正确加入顺序?
4、实验中加热试管的目的是什么?1.关于乙酸的下列说法中不正确的是( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
2. 酯化反应属于( )
A.中和反应 B.不可逆反应
C.离子反应 D.取代反应课堂练习DD3.下列物质的溶液中,不易被氧化,不易被分解且能存放在玻璃试剂瓶中的是( )
A.氢氟酸 B.次氯酸 C.碳酸 D.醋酸4.下列4.物质中最难电离出H+的是( )
A.CH3COOH B.C2H5OH C.H2O D.H2CO3
5.胆固醇是人体必需的生物活性物质,分子式为 C25H46O,有一种胆固醇酯是液晶材料,分子式为C32H50O2,生成这种胆固醇酯的酸是( )
A. C6H13COOH B. C6H5COOH
C. C7H15COOH D. C6H5CH2COOHDBB6.巴豆酸的结构简式为CH3—CH=CH—COOH。现有①氯化氢、②溴水、③纯碱溶液、④丁醇、⑤酸性高锰酸钾溶液,判断在一定条件下,能与巴豆酸反应的物质是( )
A.仅②④⑤ B.仅①③④
C.仅①②③④ D.全部 D方案⑶:往NaOH溶液中先加入酚酞试剂,再加入乙酸,若红色消失证明酸、碱反应已发生。方案⑴:往紫色石蕊试液中加入乙酸。方案⑷:往Na2CO3粉末中加入乙酸。方案⑵:往镁粉中加入乙酸。证明弱酸的方案证明是弱酸方案:
方案⑴:取同浓度、同体积的盐酸和醋酸溶液,分别与足量的金属锌反应,观察反应产生气体的快慢。
方案⑵:取同浓度的盐酸和醋酸溶液,分别用PH试纸测试,看酸性的强弱。
第3节 饮食中的有机化合物
第2课时 乙 酸
复习巩固 乙醇的结构结构简式:CH3CH2OH或C2H5OH含原子团:-OH 称
为羟基(官能团)①②③④①③①化学方程式说明:乙基-C2H5对羟基-O-H键有影响,乙醇具有氧化性;其他如K、Mg、Al 等也能把羟基里的氢置换(或取代)出来 。
2(-OH ) H2↑1. 与活泼金属反应 (断①键) 2. 燃烧 ( ①②③④键全断) 3. 催化氧化 (断①③)乙醛的分子结构 ●官能团醛
基结构简式:CH3CHO学习目标1、掌握乙酸的结构和化学性质;
2、了解乙酸的物理性质、用途;
3、掌握酯化反应的原理、实质。乙 酸乙酸结构物理性质化学性质知识总结乙酸的物理性质颜 色 :无色强烈刺激性气味液体117.90C乙酸是食醋的主要成分,俗称醋酸。沸 点 :熔 点 :16.60C当温度低于16.6时,乙酸就凝结成像冰一样的晶体,因此无水乙酸又称为冰醋酸。溶解性:易溶于水和酒精气 味 :状 态 :观察与思考乙酸的结构分子式:C2H4O2结构简式:CH3COOH含原子团:-COOH
称为羧基 乙酸在溶于水时能够电离出CHCOO-和H+ ,因而乙酸具有一定的酸性。请你根据现有的化学药品设计实验方案:
(1)证明乙酸的酸性;
(2)证明乙酸是弱酸。联接1联接2乙酸在水溶液中的电离方程式:CH3COOH CH3COO— + H+总 结:
1.乙酸是一种常见的有机酸,它能使指示剂变色,能与活泼金属,碱及盐等物质反应,具有酸的通性。
2.乙酸的酸性比碳酸强。 家庭中常用食醋浸泡有水垢[主要成分是CaCO3和MgOH)2 ]暖瓶或水壶,以清除水垢。请写出有关反应的化学方程式。
迁移 应用 在试管里加入3mL乙醇,然后一边摇动一边慢
慢加入2mL浓硫酸和2mL乙酸,加入2-3块小脆瓷
片;按图连接好装置,用酒精灯小心均匀的加热使
馆3-5min,将产生的蒸汽经导管通到饱和碳酸钠溶
液的液面上,观察现象。思 考:(1)浓硫酸的作用?(2)为什么用饱和的Na2CO3溶液收集乙酸乙酯?催化剂(提高反应速率)、吸水剂(促进反应向生成乙酸乙酯的反应方向进行,提高产率)①中和挥发出来的乙酸
②吸收挥发出来的乙醇
③降低乙酸乙酯的溶解度(3)加热的目的?①提高反应速率
②使生成的乙酸乙酯挥发,有利于收集
③提高乙醇、乙酸的转化率(4)导管的作用是什么?能不能将导管插到液面以下?为什么?导管作用是导气、冷凝。不能将导管插到液面以下,防止发生倒吸。注意点: 1、加药品的顺序:先加乙醇,再加浓硫酸,然后加乙酸。
2、试管要上倾450,使液体受热面积大。
3、导管末端不能插入溶液中,防止受热不均发生液体倒吸。
4、不能用NaOH代替Na2CO3,因为NaOH碱性太强,使乙酸乙酯水解。
5、加碎瓷片的作用:防止爆沸。实验现象:实验结论:饱和碳酸钠溶液的液面上有无色透明的
油状液体产生,并可闻到香味。在浓硫酸存在、加热的条件下,乙酸和
乙醇发生反应,生成无色、透明、不溶
于水、有香味的油状液体。该油状液体
是乙酸乙酯。酯化反应的化学方程式:乙酸乙酯酯化反应像乙酸和乙醇这样生成酯和水的反应称为酯化反应,它是可逆的反应
①与金属,碱等反应显酸性②与乙醇反应①②问题讨论1、乙酸比乙醇的相对分子质量大多少?
2、相对分子质量相同的酸和醇之间有什么关系?
3、制取乙酸乙酯中需加入浓硫酸冰醋酸和乙醇各2ml,正确加入顺序?
4、实验中加热试管的目的是什么?1.关于乙酸的下列说法中不正确的是( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
2. 酯化反应属于( )
A.中和反应 B.不可逆反应
C.离子反应 D.取代反应课堂练习DD3.下列物质的溶液中,不易被氧化,不易被分解且能存放在玻璃试剂瓶中的是( )
A.氢氟酸 B.次氯酸 C.碳酸 D.醋酸4.下列4.物质中最难电离出H+的是( )
A.CH3COOH B.C2H5OH C.H2O D.H2CO3
5.胆固醇是人体必需的生物活性物质,分子式为 C25H46O,有一种胆固醇酯是液晶材料,分子式为C32H50O2,生成这种胆固醇酯的酸是( )
A. C6H13COOH B. C6H5COOH
C. C7H15COOH D. C6H5CH2COOHDBB6.巴豆酸的结构简式为CH3—CH=CH—COOH。现有①氯化氢、②溴水、③纯碱溶液、④丁醇、⑤酸性高锰酸钾溶液,判断在一定条件下,能与巴豆酸反应的物质是( )
A.仅②④⑤ B.仅①③④
C.仅①②③④ D.全部 D方案⑶:往NaOH溶液中先加入酚酞试剂,再加入乙酸,若红色消失证明酸、碱反应已发生。方案⑴:往紫色石蕊试液中加入乙酸。方案⑷:往Na2CO3粉末中加入乙酸。方案⑵:往镁粉中加入乙酸。证明弱酸的方案证明是弱酸方案:
方案⑴:取同浓度、同体积的盐酸和醋酸溶液,分别与足量的金属锌反应,观察反应产生气体的快慢。
方案⑵:取同浓度的盐酸和醋酸溶液,分别用PH试纸测试,看酸性的强弱。
