空气与生命(空气、氧气复习)
图片预览





文档简介
课件34张PPT。
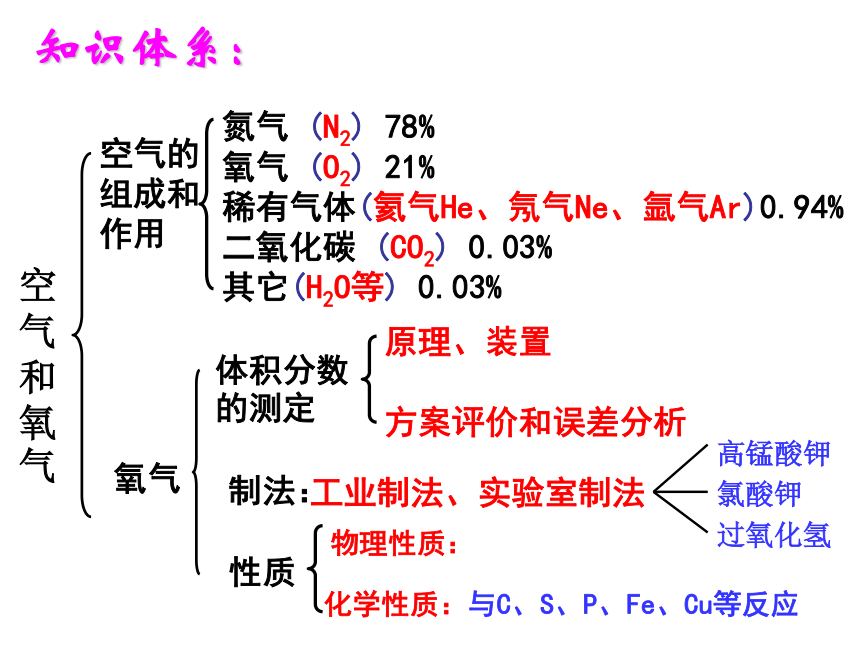
空气和氧气
空气的
组成和作用氧气制法:体积分数的测定知识体系:工业制法、实验室制法性质常见知识点填空举例——空气组成及作用:
1、空气中各组分气体按体积计算:氧气占 ;氮气占 ;二氧化碳占 ;稀有气体占 。
举例说明空气中存在:氧气 ,二氧化碳 ,水蒸气 。
2、空气中氧气的主要作用有 。
二氧化碳的主要用途有 。
举例说明氮气的作用 。
例举稀有气体主要有 ,
它的主要用途包括 ;
写出其中氦气、氖气的化学式 、 。
21%78%0.04%0.93%燃烧,生物能呼吸植物能光合作用雨、露、雪、雾等 防腐;保护气;制化肥农药;冷冻剂氦气、氖气、氩气、氪气、氙气He Ne供生物呼吸、支持燃烧等供生物光合作用、制干冰、灭火等制作霓虹灯、保护气、医学麻醉剂等
1、用于制造氮肥、作瓜果蔬菜保护气的是 。
2、 能代替氢气填充气球的稀有气体是 。
3、量多时会造成温室效应的是 。
4、能支持燃烧、供给呼吸的是 。
我会应用N2Heco2o2捕捉空气,你
有哪些方法?
方法1:用一个集气瓶装满水,在教室里倒掉
方法2:用一只注射器在教室里抽气(这个可以取一定体积 的气体)
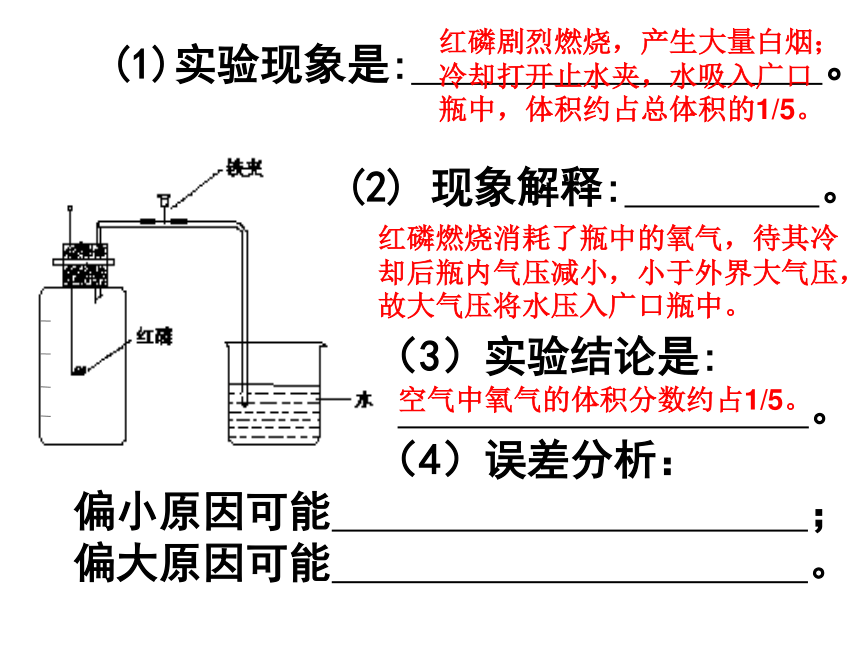
方法3:用一个挤扁了的塑料袋在教室里兜一袋子就可以了1、原理:利用物质的燃烧消耗密闭容器内的氧气,空气减少的体积即为其中所含氧气体积。3、装置2、可燃物的选择条件:①能消耗空气中的氧气。②不产生其它气体(用水时)。(1)实验现象是: 。红磷剧烈燃烧,产生大量白烟;冷却打开止水夹,水吸入广口瓶中,体积约占总体积的1/5。 (3)实验结论是:
。
(4)误差分析:
偏小原因可能 ;
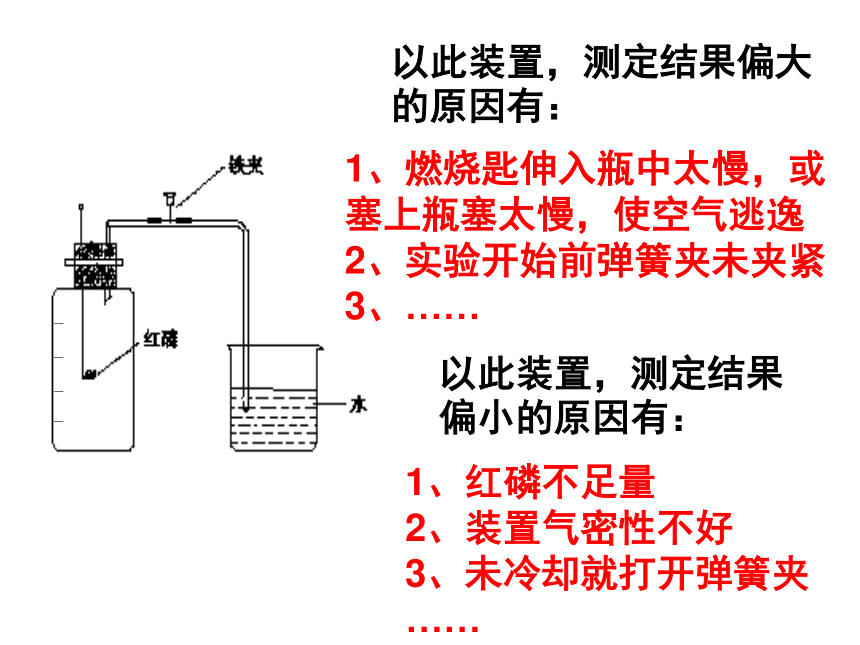
偏大原因可能 。红磷燃烧消耗了瓶中的氧气,待其冷却后瓶内气压减小,小于外界大气压,故大气压将水压入广口瓶中。(2) 现象解释: 。空气中氧气的体积分数约占1/5。以此装置,测定结果偏大的原因有:以此装置,测定结果偏小的原因有:1、燃烧匙伸入瓶中太慢,或塞上瓶塞太慢,使空气逃逸
2、实验开始前弹簧夹未夹紧
3、……1、红磷不足量
2、装置气密性不好
3、未冷却就打开弹簧夹
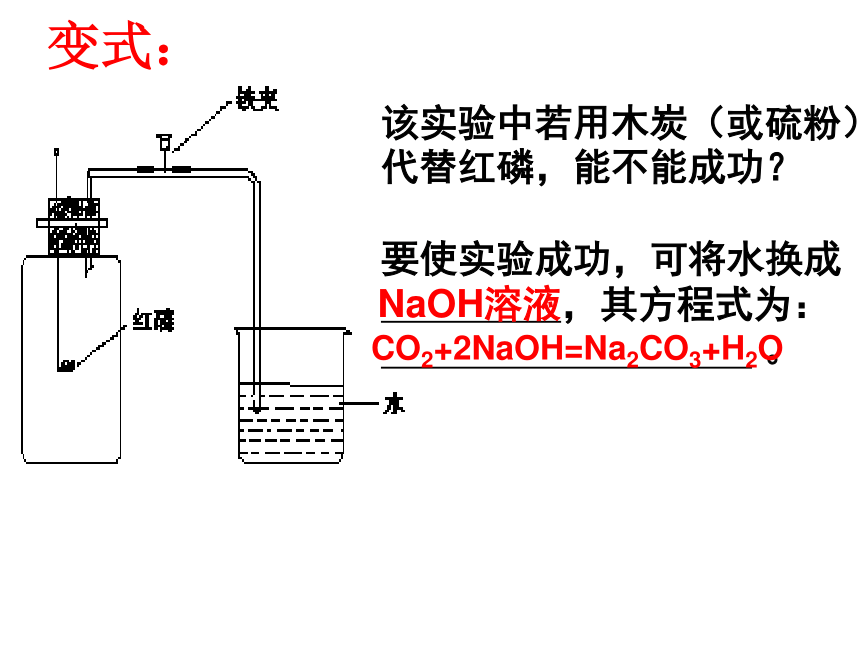
……该实验中若用木炭(或硫粉)代替红磷,能不能成功?
要使实验成功,可将水换成
,其方程式为:
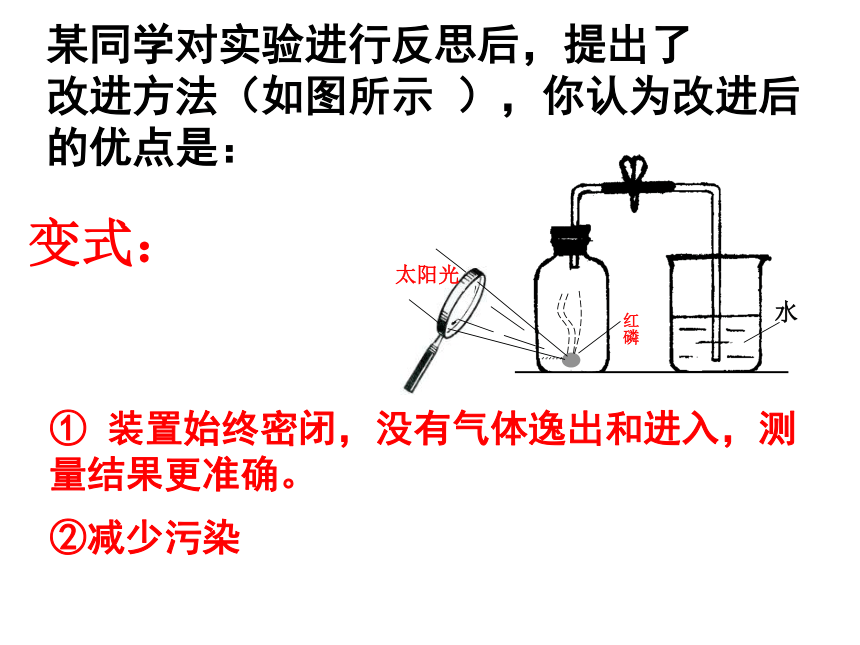
。变式:NaOH溶液CO2+2NaOH=Na2CO3+H2O某同学对实验进行反思后,提出了
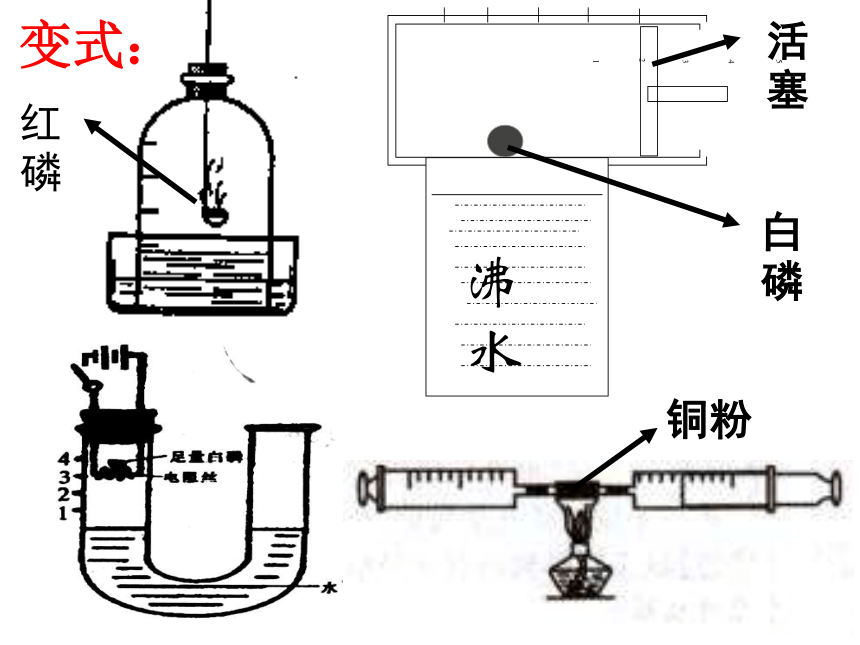
改进方法(如图所示 ),你认为改进后的优点是:① 装置始终密闭,没有气体逸出和进入,测量结果更准确。②减少污染变式:铜粉变式:O2C、S、P、Fe、Mg、
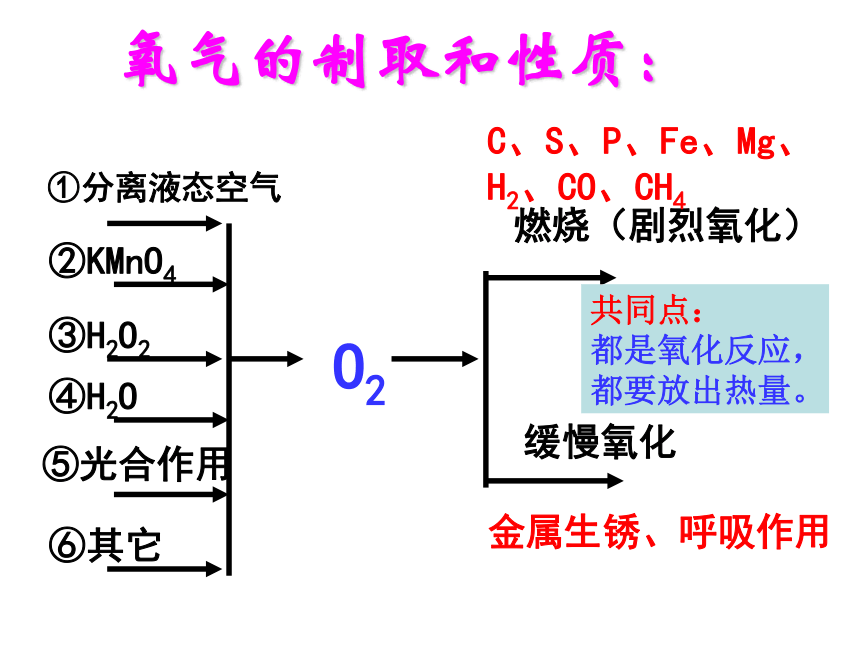
H2、CO、CH4金属生锈、呼吸作用氧气的制取和性质:共同点:
都是氧化反应,
都要放出热量。1、氧气的制备:(1)工业上制取氧气:分离液态空气法利用液态空气中液态氮和液态氧的沸点不同,液态氮先汽化,剩下就是氧气。例:将一根燃烧的木条放在盛满液态空气的保温瓶口,打开瓶盖时,木条 (填熄灭
或更旺)理由是 。熄灭液态空气中氮气先汽化,不支持燃烧2、氧气的实验室制法: 药品:KMnO4、KClO3或H2O2溶液 原理:
装置:比较过氧化氢和高锰酸钾固体制氧气的利弊:从两个方面考虑:
(1)反应的条件。
(2)药品的状态。
在选择发生装置时要考虑哪些因素?适用于反应物是固体且需加热
适用于反应物有两种(固体+液体)且不需加热
KMnO4制O2(制NH3)H2O2制O2(制CO2、H2)指出下列制取O2装置中错误:高锰酸钾制氧气的步骤:注意:(1)要先 后 ;
(2)集气什么时候开始?什么时候结束?变式:这些装置各有什么优点?例:(2015黑龙江省龙东地区)在课外小实验中,小强同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(如图所示)。请回答该实验设计的优点。(答出三点即可)节约资源、降低成本、节约药品、废物利用、减少污染保护环境、操作方便、可控制反应的发生和停止等(答案合理即可)在选择集气装置时要考虑哪些因素?从两个方面考虑:
(1)生成气体的密度(能否与空气反应)。
(2)生成气体的溶解性(能否与水反应)。气体不与水反应,且难溶于水气体密度比空气大气体密度比空气小排水法或排空气法集气可以定量测出收集到的气体体积常见题型:1、能用⑴⑵⑶装置收集的气体分别具有什么性质?
2、用⑷装置收集氢气由 端通入氢气,用⑸装置收集氧气由 端通入氧气
3、氨气是一种极易溶于水的气体,收集氨气可选
择 装置
4、在⑷装置中储存了一瓶氧气,欲将其中的氧气取出,你的措施是 。
bd3或4将水从a导管通入集气瓶例1. (2015乌鲁木齐)在医院里给病人输氧时,用到类似如右图所示的装置。下列有关说法中不正确的是
( )
A. 使用该装置可用来观测氧气输出的速率
B. b导管连接病人吸入氧气的塑料管
C. 使用该装置可用来观测是否有氧气输出
D. b导管应连接供给氧气的钢瓶B例2(2015上海)不能达到相应实验目的的装置是( )B氧气的物理性质氧气的化学性质问题:
有一瓶未知气体,可能是空气、氧气和二氧化碳,你有什么办法可以快速地鉴别它?将燃着的木条伸入瓶中,如果燃烧更旺则是氧气,如果熄灭则是二氧化碳,如果没有明显变化则是空气。1.木炭在氧气中燃烧的现象_____________________________________________ 。 发出白光,放出热量,生成一种无色无味的气体2.硫在氧气中燃烧的现象_____________________________________________ 。 硫在氧气中剧烈燃烧,发出明亮的蓝紫色火焰
氧气的化学性质思考:如何证明生成二氧化碳?注意:与硫在空气中燃烧有区别?3.镁带燃烧的现象____________________________________________________________________
发出耀眼的白光、放出热量、产生白烟或白色固体。4.铁丝在氧气中燃烧实验的现象________________________________________
铁丝剧烈燃烧,火星四射,生成一种黑色固体。思考:如何证明铁丝与氧气发生了化学变化?思考:做硫(或磷)、铁丝在氧气中燃烧实验时,集气瓶底部都需留些水,两瓶中的水作用分别是什么?硫或磷燃烧实验中:水用于吸收产生的二氧化硫或五氧化二磷,防止污染环境。
铁丝燃烧实验中:以防生成火热的熔化物跌落,引起瓶底炸裂。燃烧和灭火1、燃烧的三个条件:2、灭火原理:a.火灾隔离带——转移可燃物b. CO2灭火——隔绝空气c. 高压水枪灭火——降低温度到
可燃物着火点以下支持燃烧供给呼吸我会总结1.与非金属反应
(C、S、P、H2)2.与金属反应
(Mg、Fe、Al、Cu)3.与化合物反应
(CO、CH4)A、B、C三种元素,A元素的单质是最清洁的燃料;B元素的单质能在C元素的单质中剧烈燃烧,火星四射,生成黑色固体;B元素的单质是目前世界上年产量最高的金属。写出A、B、C三种元素的名称或符号:A___________、B___________、C___________;
写出B、C二种元素组成的一种化合物的化学式:_______________________。 H(氢) Fe(铁) O(氧) FeO(或Fe2O3、Fe3O4) 典例示范:小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧,于是设计了如下图所示的装置进行实验探究,请你结合实验过程回答下列问题。(1)集气瓶底预先铺少量沙子的目的是 ________________________________________________;
(2)铝丝在空气中不能被点燃,引燃铝丝的办法是:________________________________________________________________________;
防止反应生成的固体物质溅落瓶底,致使集气瓶炸裂铝丝下端系一根火柴,点燃火柴,待火柴即将燃尽时,将铝丝伸入集满氧气的集气瓶中
拓展延伸(3)用正确方法引燃铝丝,伸入装有氧气的集气瓶中后,未观察到铝丝发生剧烈燃烧现象,可能的原因是 __________________________
___________________________。
(4)写出铝在氧气中燃烧的化学方程式
__________________________。
①铝丝表面 有氧化膜②氧气浓度不够
空气和氧气
空气的
组成和作用氧气制法:体积分数的测定知识体系:工业制法、实验室制法性质常见知识点填空举例——空气组成及作用:
1、空气中各组分气体按体积计算:氧气占 ;氮气占 ;二氧化碳占 ;稀有气体占 。
举例说明空气中存在:氧气 ,二氧化碳 ,水蒸气 。
2、空气中氧气的主要作用有 。
二氧化碳的主要用途有 。
举例说明氮气的作用 。
例举稀有气体主要有 ,
它的主要用途包括 ;
写出其中氦气、氖气的化学式 、 。
21%78%0.04%0.93%燃烧,生物能呼吸植物能光合作用雨、露、雪、雾等 防腐;保护气;制化肥农药;冷冻剂氦气、氖气、氩气、氪气、氙气He Ne供生物呼吸、支持燃烧等供生物光合作用、制干冰、灭火等制作霓虹灯、保护气、医学麻醉剂等
1、用于制造氮肥、作瓜果蔬菜保护气的是 。
2、 能代替氢气填充气球的稀有气体是 。
3、量多时会造成温室效应的是 。
4、能支持燃烧、供给呼吸的是 。
我会应用N2Heco2o2捕捉空气,你
有哪些方法?
方法1:用一个集气瓶装满水,在教室里倒掉
方法2:用一只注射器在教室里抽气(这个可以取一定体积 的气体)
方法3:用一个挤扁了的塑料袋在教室里兜一袋子就可以了1、原理:利用物质的燃烧消耗密闭容器内的氧气,空气减少的体积即为其中所含氧气体积。3、装置2、可燃物的选择条件:①能消耗空气中的氧气。②不产生其它气体(用水时)。(1)实验现象是: 。红磷剧烈燃烧,产生大量白烟;冷却打开止水夹,水吸入广口瓶中,体积约占总体积的1/5。 (3)实验结论是:
。
(4)误差分析:
偏小原因可能 ;
偏大原因可能 。红磷燃烧消耗了瓶中的氧气,待其冷却后瓶内气压减小,小于外界大气压,故大气压将水压入广口瓶中。(2) 现象解释: 。空气中氧气的体积分数约占1/5。以此装置,测定结果偏大的原因有:以此装置,测定结果偏小的原因有:1、燃烧匙伸入瓶中太慢,或塞上瓶塞太慢,使空气逃逸
2、实验开始前弹簧夹未夹紧
3、……1、红磷不足量
2、装置气密性不好
3、未冷却就打开弹簧夹
……该实验中若用木炭(或硫粉)代替红磷,能不能成功?
要使实验成功,可将水换成
,其方程式为:
。变式:NaOH溶液CO2+2NaOH=Na2CO3+H2O某同学对实验进行反思后,提出了
改进方法(如图所示 ),你认为改进后的优点是:① 装置始终密闭,没有气体逸出和进入,测量结果更准确。②减少污染变式:铜粉变式:O2C、S、P、Fe、Mg、
H2、CO、CH4金属生锈、呼吸作用氧气的制取和性质:共同点:
都是氧化反应,
都要放出热量。1、氧气的制备:(1)工业上制取氧气:分离液态空气法利用液态空气中液态氮和液态氧的沸点不同,液态氮先汽化,剩下就是氧气。例:将一根燃烧的木条放在盛满液态空气的保温瓶口,打开瓶盖时,木条 (填熄灭
或更旺)理由是 。熄灭液态空气中氮气先汽化,不支持燃烧2、氧气的实验室制法: 药品:KMnO4、KClO3或H2O2溶液 原理:
装置:比较过氧化氢和高锰酸钾固体制氧气的利弊:从两个方面考虑:
(1)反应的条件。
(2)药品的状态。
在选择发生装置时要考虑哪些因素?适用于反应物是固体且需加热
适用于反应物有两种(固体+液体)且不需加热
KMnO4制O2(制NH3)H2O2制O2(制CO2、H2)指出下列制取O2装置中错误:高锰酸钾制氧气的步骤:注意:(1)要先 后 ;
(2)集气什么时候开始?什么时候结束?变式:这些装置各有什么优点?例:(2015黑龙江省龙东地区)在课外小实验中,小强同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(如图所示)。请回答该实验设计的优点。(答出三点即可)节约资源、降低成本、节约药品、废物利用、减少污染保护环境、操作方便、可控制反应的发生和停止等(答案合理即可)在选择集气装置时要考虑哪些因素?从两个方面考虑:
(1)生成气体的密度(能否与空气反应)。
(2)生成气体的溶解性(能否与水反应)。气体不与水反应,且难溶于水气体密度比空气大气体密度比空气小排水法或排空气法集气可以定量测出收集到的气体体积常见题型:1、能用⑴⑵⑶装置收集的气体分别具有什么性质?
2、用⑷装置收集氢气由 端通入氢气,用⑸装置收集氧气由 端通入氧气
3、氨气是一种极易溶于水的气体,收集氨气可选
择 装置
4、在⑷装置中储存了一瓶氧气,欲将其中的氧气取出,你的措施是 。
bd3或4将水从a导管通入集气瓶例1. (2015乌鲁木齐)在医院里给病人输氧时,用到类似如右图所示的装置。下列有关说法中不正确的是
( )
A. 使用该装置可用来观测氧气输出的速率
B. b导管连接病人吸入氧气的塑料管
C. 使用该装置可用来观测是否有氧气输出
D. b导管应连接供给氧气的钢瓶B例2(2015上海)不能达到相应实验目的的装置是( )B氧气的物理性质氧气的化学性质问题:
有一瓶未知气体,可能是空气、氧气和二氧化碳,你有什么办法可以快速地鉴别它?将燃着的木条伸入瓶中,如果燃烧更旺则是氧气,如果熄灭则是二氧化碳,如果没有明显变化则是空气。1.木炭在氧气中燃烧的现象_____________________________________________ 。 发出白光,放出热量,生成一种无色无味的气体2.硫在氧气中燃烧的现象_____________________________________________ 。 硫在氧气中剧烈燃烧,发出明亮的蓝紫色火焰
氧气的化学性质思考:如何证明生成二氧化碳?注意:与硫在空气中燃烧有区别?3.镁带燃烧的现象____________________________________________________________________
发出耀眼的白光、放出热量、产生白烟或白色固体。4.铁丝在氧气中燃烧实验的现象________________________________________
铁丝剧烈燃烧,火星四射,生成一种黑色固体。思考:如何证明铁丝与氧气发生了化学变化?思考:做硫(或磷)、铁丝在氧气中燃烧实验时,集气瓶底部都需留些水,两瓶中的水作用分别是什么?硫或磷燃烧实验中:水用于吸收产生的二氧化硫或五氧化二磷,防止污染环境。
铁丝燃烧实验中:以防生成火热的熔化物跌落,引起瓶底炸裂。燃烧和灭火1、燃烧的三个条件:2、灭火原理:a.火灾隔离带——转移可燃物b. CO2灭火——隔绝空气c. 高压水枪灭火——降低温度到
可燃物着火点以下支持燃烧供给呼吸我会总结1.与非金属反应
(C、S、P、H2)2.与金属反应
(Mg、Fe、Al、Cu)3.与化合物反应
(CO、CH4)A、B、C三种元素,A元素的单质是最清洁的燃料;B元素的单质能在C元素的单质中剧烈燃烧,火星四射,生成黑色固体;B元素的单质是目前世界上年产量最高的金属。写出A、B、C三种元素的名称或符号:A___________、B___________、C___________;
写出B、C二种元素组成的一种化合物的化学式:_______________________。 H(氢) Fe(铁) O(氧) FeO(或Fe2O3、Fe3O4) 典例示范:小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧,于是设计了如下图所示的装置进行实验探究,请你结合实验过程回答下列问题。(1)集气瓶底预先铺少量沙子的目的是 ________________________________________________;
(2)铝丝在空气中不能被点燃,引燃铝丝的办法是:________________________________________________________________________;
防止反应生成的固体物质溅落瓶底,致使集气瓶炸裂铝丝下端系一根火柴,点燃火柴,待火柴即将燃尽时,将铝丝伸入集满氧气的集气瓶中
拓展延伸(3)用正确方法引燃铝丝,伸入装有氧气的集气瓶中后,未观察到铝丝发生剧烈燃烧现象,可能的原因是 __________________________
___________________________。
(4)写出铝在氧气中燃烧的化学方程式
__________________________。
①铝丝表面 有氧化膜②氧气浓度不够
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
