原子结构的模型(一)[下学期]
图片预览






文档简介
课件19张PPT。(第一课时)第3节 原子结构的模型思考 在上一节中用实心的圆球模型代表原子从而表示出分子结构模型。那么实心球模型能否代表原子的真实结构吗? 原子结构模型是科学家根据自己
的认识,对原子结构的形象描摹
。一种模型代表了人类对原子结
构认识的一个阶段。人类认识原
子的历史是漫长的,也是无止境
的。下面介绍的几种原子结构模
型简明形象地表示出了人类对原
子结构认识逐步深化的演变过程。
1.道尔顿原子模型(1803年) 3.卢瑟福原子模型(1911年) 2.汤姆森原子模型(1904年) 4.波尔原子模型(1913年) 5.现代模型(20世纪20年代以来) 实心球模型西瓜模型(布丁模型)行星模型分层模型电子云模型道尔顿原子模型一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。近代科学原子论 英国化学家道尔顿
(J.Dalton , 1766~1844)(最早提出原子理论)汤姆生原子模型原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)电子是种带负电、有一定质量的微粒,普遍存在于各种原子之中。
汤姆生原子模型:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了电荷,从而形成了中性原子。英国物理学家汤姆生
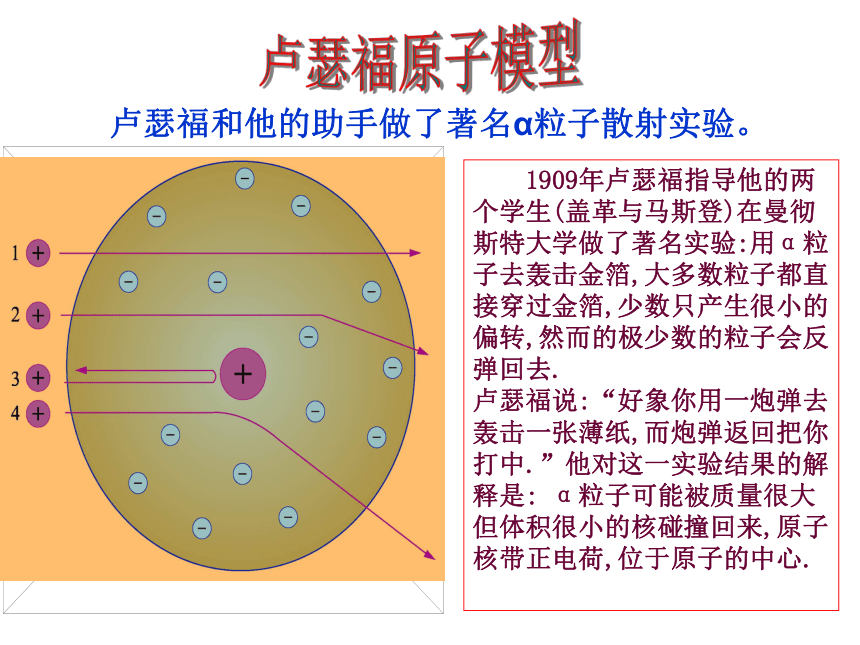
(J.J.Thomson ,1856~1940) 卢瑟福和他的助手做了著名α粒子散射实验。卢瑟福原子模型 1909年卢瑟福指导他的两个学生(盖革与马斯登)在曼彻斯特大学做了著名实验:用α粒子去轰击金箔,大多数粒子都直接穿过金箔,少数只产生很小的偏转,然而的极少数的粒子会反弹回去.
卢瑟福说:“好象你用一炮弹去轰击一张薄纸,而炮弹返回把你打中.”他对这一实验结果的解释是: α粒子可能被质量很大但体积很小的核碰撞回来,原子核带正电荷,位于原子的中心.卢瑟福原子模型(又称行星原子模型):原子是由居于原子中心的带正电的原子核和核外带负电的电子构成。原子核的质量几乎等于原子的全部质量,电子在原子核外空间绕核做高速运动。就像行星环绕太阳运转一样。根据实验,卢瑟福在1911年提出原子有核模型。原子是由一个居中心的带正电荷的原子核与带负电荷的核外电子构成的。 卢瑟福发现了原子核 电子在原子核外空间的一定轨道上分层绕核做高速的圆周运动。波尔原子模型丹麦物理学家波尔
(N.Bohr,1885~1962)试验中发现,电子出现在不同区域的次数不同,像“云雾”一样。 电子云模型 二、原子的结构:
?
1、原子: 原子核: 带正电荷
(不显电性) 核外电子:带负电荷
原子核所带正电荷数与核外电子所带负
电荷数相等,整个原子不显电性。
2、原子核大小与核外电子运动范围
(原子大小)的比较。
?
原子的半径:10-10米原子核有多大?原子核的半径:10-15—10-14米碳原子结构的行星模型三、揭开原子核的秘密
1、原子核是由更小的两种粒子质子
和中子构成的。
一个电子带一个单位的负电荷,
一个质子带一个单位的正电荷,
中子不带电。
核电荷数:原子核所带的电荷数(即质子数)
原子内部结构原子核中子质子电子原子的质量主要集中在原子核上。
分析下表:在一个原子中哪些数目总是相等的?(1)核电荷数=质子数=核外电子数。
(2)中子数不一定等于质子数。
(3)原子内可以没有中子。
质子和中子都是由更微小的粒子
--夸克构成 水的微观层次分析一杯水--水分子-- 氧原子 氧原子核 质子
氢原子 核外电子 中子 夸克
的认识,对原子结构的形象描摹
。一种模型代表了人类对原子结
构认识的一个阶段。人类认识原
子的历史是漫长的,也是无止境
的。下面介绍的几种原子结构模
型简明形象地表示出了人类对原
子结构认识逐步深化的演变过程。
1.道尔顿原子模型(1803年) 3.卢瑟福原子模型(1911年) 2.汤姆森原子模型(1904年) 4.波尔原子模型(1913年) 5.现代模型(20世纪20年代以来) 实心球模型西瓜模型(布丁模型)行星模型分层模型电子云模型道尔顿原子模型一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。近代科学原子论 英国化学家道尔顿
(J.Dalton , 1766~1844)(最早提出原子理论)汤姆生原子模型原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)电子是种带负电、有一定质量的微粒,普遍存在于各种原子之中。
汤姆生原子模型:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了电荷,从而形成了中性原子。英国物理学家汤姆生
(J.J.Thomson ,1856~1940) 卢瑟福和他的助手做了著名α粒子散射实验。卢瑟福原子模型 1909年卢瑟福指导他的两个学生(盖革与马斯登)在曼彻斯特大学做了著名实验:用α粒子去轰击金箔,大多数粒子都直接穿过金箔,少数只产生很小的偏转,然而的极少数的粒子会反弹回去.
卢瑟福说:“好象你用一炮弹去轰击一张薄纸,而炮弹返回把你打中.”他对这一实验结果的解释是: α粒子可能被质量很大但体积很小的核碰撞回来,原子核带正电荷,位于原子的中心.卢瑟福原子模型(又称行星原子模型):原子是由居于原子中心的带正电的原子核和核外带负电的电子构成。原子核的质量几乎等于原子的全部质量,电子在原子核外空间绕核做高速运动。就像行星环绕太阳运转一样。根据实验,卢瑟福在1911年提出原子有核模型。原子是由一个居中心的带正电荷的原子核与带负电荷的核外电子构成的。 卢瑟福发现了原子核 电子在原子核外空间的一定轨道上分层绕核做高速的圆周运动。波尔原子模型丹麦物理学家波尔
(N.Bohr,1885~1962)试验中发现,电子出现在不同区域的次数不同,像“云雾”一样。 电子云模型 二、原子的结构:
?
1、原子: 原子核: 带正电荷
(不显电性) 核外电子:带负电荷
原子核所带正电荷数与核外电子所带负
电荷数相等,整个原子不显电性。
2、原子核大小与核外电子运动范围
(原子大小)的比较。
?
原子的半径:10-10米原子核有多大?原子核的半径:10-15—10-14米碳原子结构的行星模型三、揭开原子核的秘密
1、原子核是由更小的两种粒子质子
和中子构成的。
一个电子带一个单位的负电荷,
一个质子带一个单位的正电荷,
中子不带电。
核电荷数:原子核所带的电荷数(即质子数)
原子内部结构原子核中子质子电子原子的质量主要集中在原子核上。
分析下表:在一个原子中哪些数目总是相等的?(1)核电荷数=质子数=核外电子数。
(2)中子数不一定等于质子数。
(3)原子内可以没有中子。
质子和中子都是由更微小的粒子
--夸克构成 水的微观层次分析一杯水--水分子-- 氧原子 氧原子核 质子
氢原子 核外电子 中子 夸克
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
