第七节元素符号表示的量[下学期]
图片预览








文档简介
课件24张PPT。第七节 元素符号表示的量一个碳原子的质量是:
0.00000000000000000000000001993千克 即1.993×10ˉ27千克
一个氧原子的质量是:
0.00000000000000000000000002657千克 即2.657×10ˉ26千克
一个铁原子的质量是:
0.00000000000000000000000009288千克 即9.288×10ˉ26千克1个碳原子的质量:1.993×10-26千克,
其1/12是1.993×10-26千克≈1.66×10-27千克,则氧的相对原子质量=
即原子的相对原子质量=一、相对原子质量 以C-12质量的1/12作为标准,其他原子的质量跟它相比所得的值,就是该原子的相对原子质量。
练一练:
一个铁原子的质量是9.288×10-26千克,
一个氢原子的质量是1.674×10-27千克,
一个碳原子的质量是1.993×10-26千克,
计算铁、氢、碳的相对原子质量。相对原子质量不是原子的真实
质量,而是一个比值,它的SI单位
是1,符号是1(单位1一般不写出)。
计算采用相对原子质量的近似值。
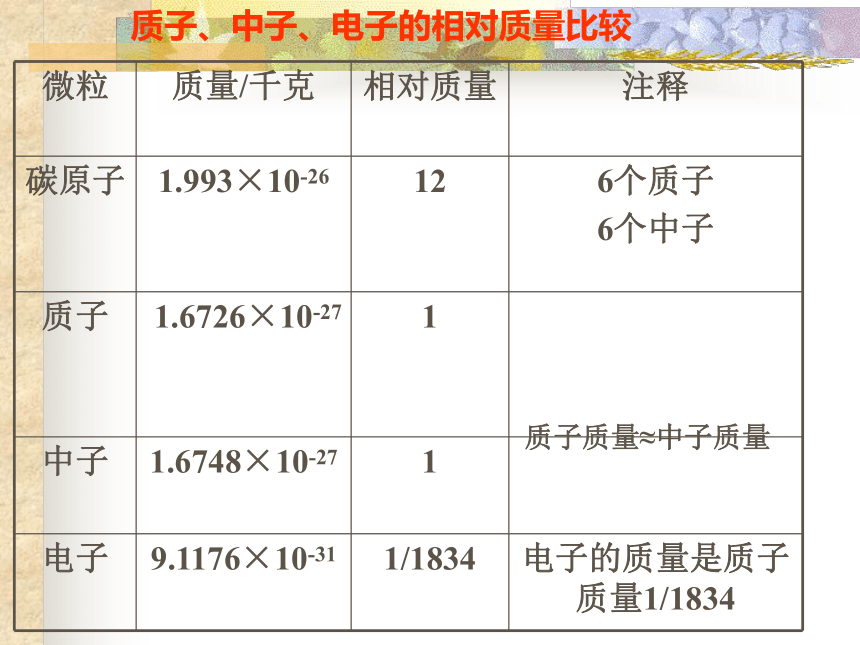
质子、中子、电子的相对质量比较质子质量≈中子质量1、质子和中子的质量大约相等,且都约等于一种碳原子 的质量的1/12; 2、 电子的质量很小,相对可以忽略,原子的质量几乎集中在原子核上相对原子质量的近似计算公式:相对原子质量 ≈质子数+中子数
氢 1 0 1 1 8 8 16 钠 11 11 11镁 12 12 24氯 17 17 35铝 13 14 13铁 26 26 56C表示碳元素表示一个碳原子表示碳元素的质量二、相对分子质量 一个分子中各原子的相对原子质量的总和就是该分子的相对分子质量。CO2二氧化碳这种物质(1个)二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成二氧化碳的相对分子质量为:12+2×16=44练一练:计算下列分子的相对分子量。
氯化钠 MgO P2O5 水 H3PO4
三.元素的质量比及质量分数计算
2、某元素的质量分数=
×100%
1、 元素的质量比=化学式中各原子的相对原子质量乘以其原子个数所得积的最简比3、化合物里含某元素的质量=化合物的质量×化合物里某元素的质量分数1、水的化学式是H2O,求
H2O中氢元素和氧元素的
质量比.解:H:O=(1×2):16=1:8答:H2O中氢元素和氧元素的质量比是1:8。
2.求H2SO4中各元素的质量比?解:H:S:O=(1×2):(32×1):(16×4)=1:16:32答 :H2SO4中各元素的质量比是1:16:32。
3.求:化肥碳酸氢铵NH4HCO3中氮元素的质量分数.解:M=14+1×4+1+12+16×3=79氮元素的质量分数=
×100%
=14 ×100%=18 %
79
4.计算CO2里所含氧元素和
碳元素的质量分数。5、计算物质中氮元素质量分数:
NH4HCO3
NH4Cl CO(NH2)2
6: “9.11事件发生不久,在美国又出现了炭疽病。这种病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%。其化学式
C17H18N3O3 。它由___ 种元素组成,每个分子中含有___ 个原子,其相对分子质量是__ ,其中氧元素的质量分数是____,元素间的质量比是_____.7、计算5吨氧化铁中含铁多少吨。
解:氧化铁的化学式是Fe2O3
氧化铁的相对分子质量是:
56×2+16×3=160
?
5吨氧化铁中所含铁的质量是:
5×70%=3.5(吨)
答:5吨氧化铁中含铁3.5吨。
0.00000000000000000000000001993千克 即1.993×10ˉ27千克
一个氧原子的质量是:
0.00000000000000000000000002657千克 即2.657×10ˉ26千克
一个铁原子的质量是:
0.00000000000000000000000009288千克 即9.288×10ˉ26千克1个碳原子的质量:1.993×10-26千克,
其1/12是1.993×10-26千克≈1.66×10-27千克,则氧的相对原子质量=
即原子的相对原子质量=一、相对原子质量 以C-12质量的1/12作为标准,其他原子的质量跟它相比所得的值,就是该原子的相对原子质量。
练一练:
一个铁原子的质量是9.288×10-26千克,
一个氢原子的质量是1.674×10-27千克,
一个碳原子的质量是1.993×10-26千克,
计算铁、氢、碳的相对原子质量。相对原子质量不是原子的真实
质量,而是一个比值,它的SI单位
是1,符号是1(单位1一般不写出)。
计算采用相对原子质量的近似值。
质子、中子、电子的相对质量比较质子质量≈中子质量1、质子和中子的质量大约相等,且都约等于一种碳原子 的质量的1/12; 2、 电子的质量很小,相对可以忽略,原子的质量几乎集中在原子核上相对原子质量的近似计算公式:相对原子质量 ≈质子数+中子数
氢 1 0 1 1 8 8 16 钠 11 11 11镁 12 12 24氯 17 17 35铝 13 14 13铁 26 26 56C表示碳元素表示一个碳原子表示碳元素的质量二、相对分子质量 一个分子中各原子的相对原子质量的总和就是该分子的相对分子质量。CO2二氧化碳这种物质(1个)二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成二氧化碳的相对分子质量为:12+2×16=44练一练:计算下列分子的相对分子量。
氯化钠 MgO P2O5 水 H3PO4
三.元素的质量比及质量分数计算
2、某元素的质量分数=
×100%
1、 元素的质量比=化学式中各原子的相对原子质量乘以其原子个数所得积的最简比3、化合物里含某元素的质量=化合物的质量×化合物里某元素的质量分数1、水的化学式是H2O,求
H2O中氢元素和氧元素的
质量比.解:H:O=(1×2):16=1:8答:H2O中氢元素和氧元素的质量比是1:8。
2.求H2SO4中各元素的质量比?解:H:S:O=(1×2):(32×1):(16×4)=1:16:32答 :H2SO4中各元素的质量比是1:16:32。
3.求:化肥碳酸氢铵NH4HCO3中氮元素的质量分数.解:M=14+1×4+1+12+16×3=79氮元素的质量分数=
×100%
=14 ×100%=18 %
79
4.计算CO2里所含氧元素和
碳元素的质量分数。5、计算物质中氮元素质量分数:
NH4HCO3
NH4Cl CO(NH2)2
6: “9.11事件发生不久,在美国又出现了炭疽病。这种病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%。其化学式
C17H18N3O3 。它由___ 种元素组成,每个分子中含有___ 个原子,其相对分子质量是__ ,其中氧元素的质量分数是____,元素间的质量比是_____.7、计算5吨氧化铁中含铁多少吨。
解:氧化铁的化学式是Fe2O3
氧化铁的相对分子质量是:
56×2+16×3=160
?
5吨氧化铁中所含铁的质量是:
5×70%=3.5(吨)
答:5吨氧化铁中含铁3.5吨。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
