元素符号表示的量[下学期]
图片预览










文档简介
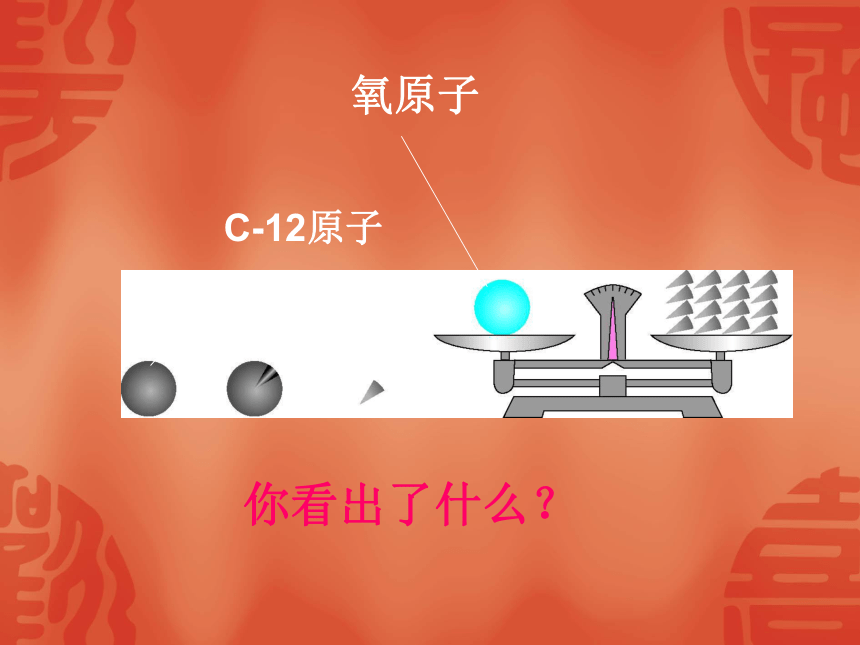
课件45张PPT。第七节元素符号表示的量为什么要制订国际千克原器?某一物体的质量是国际千克原器的2倍,它的质量是多少?(2千克)如果它的质量是国际千克原器的1/2,它的质量又是多少?0.5千克原子非常小,它有质量吗?(有)各种原子的质量一样大吗?(不一样)你知道它们的大小吗?相对原子质量的规定一个碳原子的质量是:
0.00000000000000000000000001993千克 即1.993×10-26千克
一个氧原子的质量是:
0.00000000000000000000000002657千克 即2.657×10-26千克 一个铁原子的质量是:
0.00000000000000000000000009288千克 即9.288×10-26千克一个氢原子的质量是:
0.000000000000000000000000001674千克 即1、674×10-27千克氢原子:1.674×10-27千克氧原子:2.657×10-26千克那么你能算出一个水(二氧化碳、氧化铁)分子的质量吗?1.674×10-27×2+2.657×10-26
=2.992×10-26千克这样计算起来方便吗?碳原子:1.993×10-26千克铁原子9.288×10-26千克我们已经知道国际上规定采用相对原子质量来表示原子的质量关系以什么作为标准呢?把一个C-12原子的质量分为12等分则一份质量为
1.993×10-26×1/12=1.661×10-27千克C-12原子质量×1/12 即1.661×10-27千克1个碳原子的质量:1.993×10-26千克,
其1/12是1.993×10-26千克≈1.66×10-27千克,则氧的相对原子质量=
即原子的相对原子质量=练一练:
一个铁原子的质量是9.288×10-26千克,
一个氢原子的质量是1.674×10-27千克,
一个碳原子的质量是1.993×10-26千克,
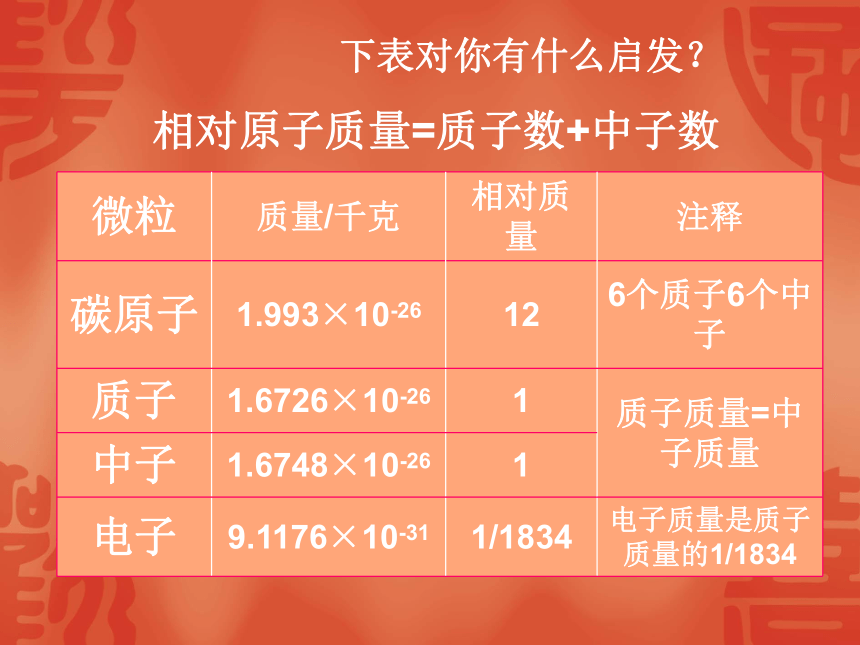
计算铁、氢、碳的相对原子质量。其他原子的质量跟它相比所得的比值,就是该原子的相对原子质量。如氧原子:2.657×10-261.661×10-27=16氢原子:1.674×10-271.661×10-27=1你认为C-12原子的相对原子质量是多少?(12)你看出了什么?氧原子C-12原子下表对你有什么启发?相对原子质量=质子数+中子数我们要用到某原子的相对质量,是否都需要进行计算? 1、从元素周期表(附录5)中查出下列元素的相对原子质量:
Ca_________ Al_________
Cl_________ Ag__________
2、从相对原子质量表(附录3)查出下列元素的相对原子质量:
H_________ C_________
O________ Cl__________练一练:如何查出元素的相对原子质量?元素周期表相对原子质量表你能查出钾和氯的相对原子质量吗?3935.5分子是由原子构成的,一个分子的质量是各原子质量的总和分子的质量也很小,能用相对质量来表示吗?相对分子质量一个分子中各原子的相对原子质量总和如何计算呢?先思考H2O可表示哪些含义呢?构成化学式的意义相对原子质量H C N O Na Mg Al P S Cl K Ca Fe Cu Zn Ag Ba求水的相对分子质量1.写出化学式H2O2.查有关相对原子质量3.求出各元素的相对原子质量总和1×2+16=18H2SO4的相对分子质量=1×2+32+16×4=981 12 14 16 23 24 27 31 32 35.5 39 40 56 64 65 108 137已知:C—12 O—16 H—1 N—14 Ca—40 S—32
求出下列相对分子质量:
CH4_____ H2O_____ Ca(OH)2_____
CO(NH2)2_____ (NH4)2SO4______
3H2O_____ 4CO2_____ 5Mg(OH)2_____练一练:思考什么物质的相对分子质量最小?H2二氧化碳分子· · · · · · · · ·…………………………………CO2CO2气体
氧原子氧原子
碳原子氧元素碳元素⑵⑴⑶⑷一个化学式(如CO2)给你传递了什么信息?
读图
相对分子质量为44(5)CO2二氧化碳这种物质一个二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成(1)(2)(3)(4)二氧化碳的相对分子质量为44(5)练一练“9.11事件”发生不久,在美国又出现了炭疽病.次病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%.其化学式为C17H18N3O3;它由____种元素组成,每个分子中含有___个原子,其相对分子质量是______441312第7节 元素符号表示的量(2)课前复习想一想:1.相对原子质量是以什么为标准的?以一个C-12原子的质量的1/12作为标准2.相对分子质量是指什么?相对分子质量是指一个分子中各原子的
相对原子质量的总和3.化学式的意义:CO2二氧化碳这种物质(1个)二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成(1)(2)(3)(4)(5)相对分子质量求下列物质的相对分子质量:1.三氧化硫(SO3)的相对分子质量
2.氧化钙(CaO)的相对分子质量
=40 ×1+16 ×1=56=32×1+16 ×3=80
3.磷酸(H3PO4)的相对原子质量=1×3+31×1+16×4=984.五氧化二磷(P2O5)的相对原子质量=31 ×2+16 ×5=142(5)尿素CO(NH2)2的相对分子质量=14×1+16×1+(14×1+1×2)×2
=60(6)硫酸铜晶体(CuSO4.5H2O)的
相对分子质量=64×1+32×1+16×4+5(1×2+16)
=250根据化学式可以计算相对分子质量,
还可以有哪些计算呢?一、根据化学式还可以计算组成物质的
各元素的质量比例如:求水中氢元素和氧元素的质量比;解:H:O=(1 × 2):(16 × 1)=1:8练一练:1.求:SO2中硫元素和氧元素的质量比解:(32 ×1):(16 × 2)=2.求化肥碳酸氢氨(NH4HCO3)
的相对分子质量及各元素的质量比解:NH4HCO3的相对分子质量=14 × 1+1 × 5+12 × 1+16 × 3
=79N:H:C:O=(14 × 1):(1 × 5)
:(12 × 1):(16 × 3)=14:5:12:48二、根据化学式还可以计算物质中
某一元素的质量分数例如:求化肥碳酸氢氨(NH4HCO3)
中氮元素的质量分数解:NH4HCO3的相对分子质量=79氮元素的质量分数=NNH4HCO3=1479=18%结论:元素的质量分数=分子中该元素的原子个数
× 该元素相对原子质量相对分子质量×100%计算硝酸铵(NH4NO3)中氮元素的质量分数(NH4NO3)中氮元素的质量分数=
2NNH4NO3=2 × 1414 × 2+1 × 4+16 × 3=2880=35%氮肥是含氮元素的物质,如碳酸氢铵
( NH4HCO3 ),尿素 [CO(NH2)2]
硫酸铵[( NH4 )2SO4],硝酸铵( NH4NO3 ),
求各种化肥中的氮元素的质量分数.三、可以计算出一定质量的某物质中
元素的质量例如:计算36克水中氢元素和氧元素的质量解:氢元素的质量=36 × 2HH2O=36 ×218=4克氧元素的质量=36 ×H2OO=36 ×1618=32克某市场中硫酸铵和尿素两种化肥,每千克的售价分别为1.3元和1.8元,根据它们含氮的比例买哪种化肥更经济?讨论解:每千克硫酸铵中含氮元素的质量=1千克2N(NH4 )2SO4×=1千克×28132=0.212千克每千克尿素中含氮元素的质量=1千克×2NCO(NH2)2=1千克×2860=0.46千克元素符号表示的量(三)综合应用
某元素的质量分数=
×100% 元素的质量比=化学式中各原子的相对原子质量乘以其原子个数所得积的最简比化合物里含某元素的质量=化合物的质量×化合物里某 元素的质量分数 课前复习巩固练习填表例题(1、2):见书P40例题3: “9.11事件发生不久,在美国又出现了炭疽病。次病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%。其化学式为
C17H18N3O3 。它由___种元素组成,每个分子中含有___个原子,其相对分子质量是__,其中氧元素的质量分数是____,元素间的质量比是_____.例题4 某氮的氧化物里,氮元素和氧元素的质量比为7:20,则该氮的氧化物的化学式为( )
设氮的氧化物的化学式为NxOy
化学式为N2O5 例题5 多少克四氧化三铁里的含铁量跟320g氧化铁里的含铁量相当?
方法①设四氧化三铁的质量为x,则
x× ×100% = 320× ×100%
x =309.3(g)
方法②:按化学式的关系式解题: 2Fe3O4—3Fe2O3 464 480
x 320 464:x = 480:320 x=309.3(g)
答:四氧化三铁的质量为309.3g例题6 常温下,乙烷(C2H6)气体和酒精(C2H6O)蒸气的混合物中,氧元素的质量分数为a%,则该混合物中碳元素的质量分数是( )
解析 混合物中,O%=a%则C、H%=(100—a)%, 由化学式C2H6、C2H6O可知混合物中 碳、氢元素的质量之比等于1:4, 所以C%= % 3.元素的质量比及质量分数计算
组成某物质的元素的质量等于该物质中此元素的所有原子的总和,即原子量×原子个数。 举例:①某氧化物的化学式为 ,其中氮元素和氧元素的质量比为7:4,此氧化物化学式中X与Y的比为______,此化学式是________。
②X、Y两元素的原子量比是7:2,在它们组成的化合物中,X与Y元素的质量比为7:3,试写出此化合物的化学式________。 ③要使其中含相同质量的氧元素,则 的质量比是________。
④当两种物质中硫元素的质量比是2:3时,这两种物质的质量比是_______;氧元素的质量比是________。
⑤某碳氢化合物中,碳元素与氢元素的质量比为3:1,则其化学式中碳原子与氢原子的个数比是_________。⑥某碳、氢、氧组成的化合物中,碳、氢、氧三元素的质量比为6:1:8,则该化合物的式量是___________。
⑦医药上用的阿斯匹林的组成里含4.5%的氢,35.5%的氧,60%的碳,其式量为180。阿斯匹林的化学式为 ,那么x、y、z的比为_______。
⑧在课本例题计算化肥硝酸铵(NH4NO3)中氮元素的质量分数后,可以补充以下例题:为满足生产需要,要使每公顷地增加2 kg的氮元素,问在50 hm2地上应施加硝酸铵肥料多少千克? 若改施碳酸氢铵(NH4HCO3),问需碳酸氢铵肥料多少千克?
⑨X与Y两种元素的原子量之比为7:2,它们形成的一种化合物中X元素的质量分数为70%,则这种化合物的化学式可能是( ) ⑩经分析测得在2.5克的某铜矿中含有0.5克氧化铜,计算在这种铜矿中含铜元素的质量分数?
11甲乙两种化合物都是由XY两种元素组成的,甲物质中含X元素为50%,乙物质中含X元素为40%,若甲的化学式为 ,则乙的化学式为( )
12黄铜矿(主要成分为 ),其中含硫的质量分数为32.16%,求其中含铁元素的质量分数。
0.00000000000000000000000001993千克 即1.993×10-26千克
一个氧原子的质量是:
0.00000000000000000000000002657千克 即2.657×10-26千克 一个铁原子的质量是:
0.00000000000000000000000009288千克 即9.288×10-26千克一个氢原子的质量是:
0.000000000000000000000000001674千克 即1、674×10-27千克氢原子:1.674×10-27千克氧原子:2.657×10-26千克那么你能算出一个水(二氧化碳、氧化铁)分子的质量吗?1.674×10-27×2+2.657×10-26
=2.992×10-26千克这样计算起来方便吗?碳原子:1.993×10-26千克铁原子9.288×10-26千克我们已经知道国际上规定采用相对原子质量来表示原子的质量关系以什么作为标准呢?把一个C-12原子的质量分为12等分则一份质量为
1.993×10-26×1/12=1.661×10-27千克C-12原子质量×1/12 即1.661×10-27千克1个碳原子的质量:1.993×10-26千克,
其1/12是1.993×10-26千克≈1.66×10-27千克,则氧的相对原子质量=
即原子的相对原子质量=练一练:
一个铁原子的质量是9.288×10-26千克,
一个氢原子的质量是1.674×10-27千克,
一个碳原子的质量是1.993×10-26千克,
计算铁、氢、碳的相对原子质量。其他原子的质量跟它相比所得的比值,就是该原子的相对原子质量。如氧原子:2.657×10-261.661×10-27=16氢原子:1.674×10-271.661×10-27=1你认为C-12原子的相对原子质量是多少?(12)你看出了什么?氧原子C-12原子下表对你有什么启发?相对原子质量=质子数+中子数我们要用到某原子的相对质量,是否都需要进行计算? 1、从元素周期表(附录5)中查出下列元素的相对原子质量:
Ca_________ Al_________
Cl_________ Ag__________
2、从相对原子质量表(附录3)查出下列元素的相对原子质量:
H_________ C_________
O________ Cl__________练一练:如何查出元素的相对原子质量?元素周期表相对原子质量表你能查出钾和氯的相对原子质量吗?3935.5分子是由原子构成的,一个分子的质量是各原子质量的总和分子的质量也很小,能用相对质量来表示吗?相对分子质量一个分子中各原子的相对原子质量总和如何计算呢?先思考H2O可表示哪些含义呢?构成化学式的意义相对原子质量H C N O Na Mg Al P S Cl K Ca Fe Cu Zn Ag Ba求水的相对分子质量1.写出化学式H2O2.查有关相对原子质量3.求出各元素的相对原子质量总和1×2+16=18H2SO4的相对分子质量=1×2+32+16×4=981 12 14 16 23 24 27 31 32 35.5 39 40 56 64 65 108 137已知:C—12 O—16 H—1 N—14 Ca—40 S—32
求出下列相对分子质量:
CH4_____ H2O_____ Ca(OH)2_____
CO(NH2)2_____ (NH4)2SO4______
3H2O_____ 4CO2_____ 5Mg(OH)2_____练一练:思考什么物质的相对分子质量最小?H2二氧化碳分子· · · · · · · · ·…………………………………CO2CO2气体
氧原子氧原子
碳原子氧元素碳元素⑵⑴⑶⑷一个化学式(如CO2)给你传递了什么信息?
读图
相对分子质量为44(5)CO2二氧化碳这种物质一个二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成(1)(2)(3)(4)二氧化碳的相对分子质量为44(5)练一练“9.11事件”发生不久,在美国又出现了炭疽病.次病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%.其化学式为C17H18N3O3;它由____种元素组成,每个分子中含有___个原子,其相对分子质量是______441312第7节 元素符号表示的量(2)课前复习想一想:1.相对原子质量是以什么为标准的?以一个C-12原子的质量的1/12作为标准2.相对分子质量是指什么?相对分子质量是指一个分子中各原子的
相对原子质量的总和3.化学式的意义:CO2二氧化碳这种物质(1个)二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成(1)(2)(3)(4)(5)相对分子质量求下列物质的相对分子质量:1.三氧化硫(SO3)的相对分子质量
2.氧化钙(CaO)的相对分子质量
=40 ×1+16 ×1=56=32×1+16 ×3=80
3.磷酸(H3PO4)的相对原子质量=1×3+31×1+16×4=984.五氧化二磷(P2O5)的相对原子质量=31 ×2+16 ×5=142(5)尿素CO(NH2)2的相对分子质量=14×1+16×1+(14×1+1×2)×2
=60(6)硫酸铜晶体(CuSO4.5H2O)的
相对分子质量=64×1+32×1+16×4+5(1×2+16)
=250根据化学式可以计算相对分子质量,
还可以有哪些计算呢?一、根据化学式还可以计算组成物质的
各元素的质量比例如:求水中氢元素和氧元素的质量比;解:H:O=(1 × 2):(16 × 1)=1:8练一练:1.求:SO2中硫元素和氧元素的质量比解:(32 ×1):(16 × 2)=2.求化肥碳酸氢氨(NH4HCO3)
的相对分子质量及各元素的质量比解:NH4HCO3的相对分子质量=14 × 1+1 × 5+12 × 1+16 × 3
=79N:H:C:O=(14 × 1):(1 × 5)
:(12 × 1):(16 × 3)=14:5:12:48二、根据化学式还可以计算物质中
某一元素的质量分数例如:求化肥碳酸氢氨(NH4HCO3)
中氮元素的质量分数解:NH4HCO3的相对分子质量=79氮元素的质量分数=NNH4HCO3=1479=18%结论:元素的质量分数=分子中该元素的原子个数
× 该元素相对原子质量相对分子质量×100%计算硝酸铵(NH4NO3)中氮元素的质量分数(NH4NO3)中氮元素的质量分数=
2NNH4NO3=2 × 1414 × 2+1 × 4+16 × 3=2880=35%氮肥是含氮元素的物质,如碳酸氢铵
( NH4HCO3 ),尿素 [CO(NH2)2]
硫酸铵[( NH4 )2SO4],硝酸铵( NH4NO3 ),
求各种化肥中的氮元素的质量分数.三、可以计算出一定质量的某物质中
元素的质量例如:计算36克水中氢元素和氧元素的质量解:氢元素的质量=36 × 2HH2O=36 ×218=4克氧元素的质量=36 ×H2OO=36 ×1618=32克某市场中硫酸铵和尿素两种化肥,每千克的售价分别为1.3元和1.8元,根据它们含氮的比例买哪种化肥更经济?讨论解:每千克硫酸铵中含氮元素的质量=1千克2N(NH4 )2SO4×=1千克×28132=0.212千克每千克尿素中含氮元素的质量=1千克×2NCO(NH2)2=1千克×2860=0.46千克元素符号表示的量(三)综合应用
某元素的质量分数=
×100% 元素的质量比=化学式中各原子的相对原子质量乘以其原子个数所得积的最简比化合物里含某元素的质量=化合物的质量×化合物里某 元素的质量分数 课前复习巩固练习填表例题(1、2):见书P40例题3: “9.11事件发生不久,在美国又出现了炭疽病。次病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%。其化学式为
C17H18N3O3 。它由___种元素组成,每个分子中含有___个原子,其相对分子质量是__,其中氧元素的质量分数是____,元素间的质量比是_____.例题4 某氮的氧化物里,氮元素和氧元素的质量比为7:20,则该氮的氧化物的化学式为( )
设氮的氧化物的化学式为NxOy
化学式为N2O5 例题5 多少克四氧化三铁里的含铁量跟320g氧化铁里的含铁量相当?
方法①设四氧化三铁的质量为x,则
x× ×100% = 320× ×100%
x =309.3(g)
方法②:按化学式的关系式解题: 2Fe3O4—3Fe2O3 464 480
x 320 464:x = 480:320 x=309.3(g)
答:四氧化三铁的质量为309.3g例题6 常温下,乙烷(C2H6)气体和酒精(C2H6O)蒸气的混合物中,氧元素的质量分数为a%,则该混合物中碳元素的质量分数是( )
解析 混合物中,O%=a%则C、H%=(100—a)%, 由化学式C2H6、C2H6O可知混合物中 碳、氢元素的质量之比等于1:4, 所以C%= % 3.元素的质量比及质量分数计算
组成某物质的元素的质量等于该物质中此元素的所有原子的总和,即原子量×原子个数。 举例:①某氧化物的化学式为 ,其中氮元素和氧元素的质量比为7:4,此氧化物化学式中X与Y的比为______,此化学式是________。
②X、Y两元素的原子量比是7:2,在它们组成的化合物中,X与Y元素的质量比为7:3,试写出此化合物的化学式________。 ③要使其中含相同质量的氧元素,则 的质量比是________。
④当两种物质中硫元素的质量比是2:3时,这两种物质的质量比是_______;氧元素的质量比是________。
⑤某碳氢化合物中,碳元素与氢元素的质量比为3:1,则其化学式中碳原子与氢原子的个数比是_________。⑥某碳、氢、氧组成的化合物中,碳、氢、氧三元素的质量比为6:1:8,则该化合物的式量是___________。
⑦医药上用的阿斯匹林的组成里含4.5%的氢,35.5%的氧,60%的碳,其式量为180。阿斯匹林的化学式为 ,那么x、y、z的比为_______。
⑧在课本例题计算化肥硝酸铵(NH4NO3)中氮元素的质量分数后,可以补充以下例题:为满足生产需要,要使每公顷地增加2 kg的氮元素,问在50 hm2地上应施加硝酸铵肥料多少千克? 若改施碳酸氢铵(NH4HCO3),问需碳酸氢铵肥料多少千克?
⑨X与Y两种元素的原子量之比为7:2,它们形成的一种化合物中X元素的质量分数为70%,则这种化合物的化学式可能是( ) ⑩经分析测得在2.5克的某铜矿中含有0.5克氧化铜,计算在这种铜矿中含铜元素的质量分数?
11甲乙两种化合物都是由XY两种元素组成的,甲物质中含X元素为50%,乙物质中含X元素为40%,若甲的化学式为 ,则乙的化学式为( )
12黄铜矿(主要成分为 ),其中含硫的质量分数为32.16%,求其中含铁元素的质量分数。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
