空气与生命复习课[下学期]
图片预览




文档简介
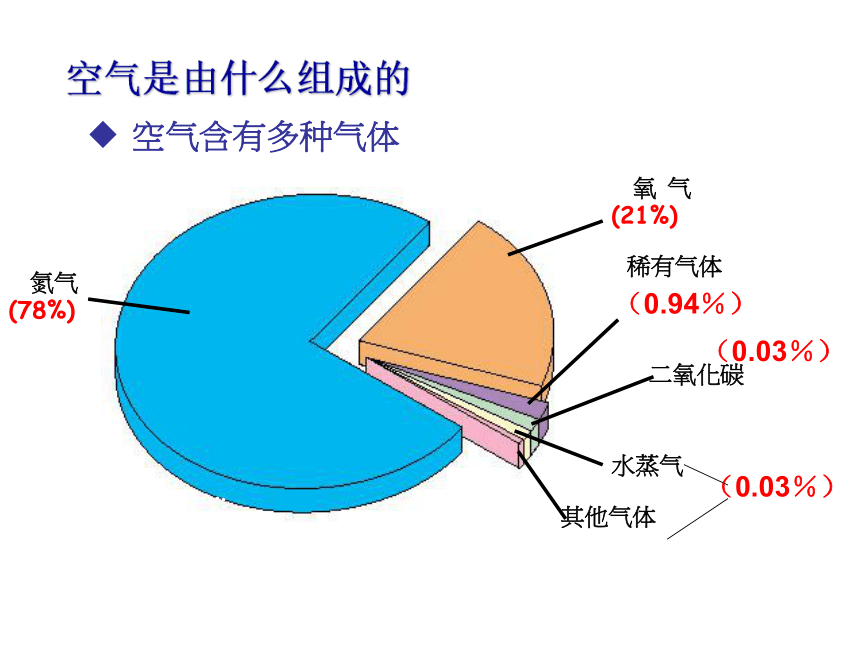
课件39张PPT。空气你认为包装袋中充的可能是什么气体?阐述你的理由。1、现有四瓶无色气体:空气、氧气、二氧化碳、氮气。你怎样将它们一一鉴别出来?用燃烧的木条,正常燃烧的是空气,烧的更加旺的是氧气,熄灭的是氮气和二氧化碳,再用澄清的石灰水辨别出二氧化碳空气是由什么组成的空气含有多种气体其他气体二氧化碳(0.94%)
(0.03%)
(0.03%)
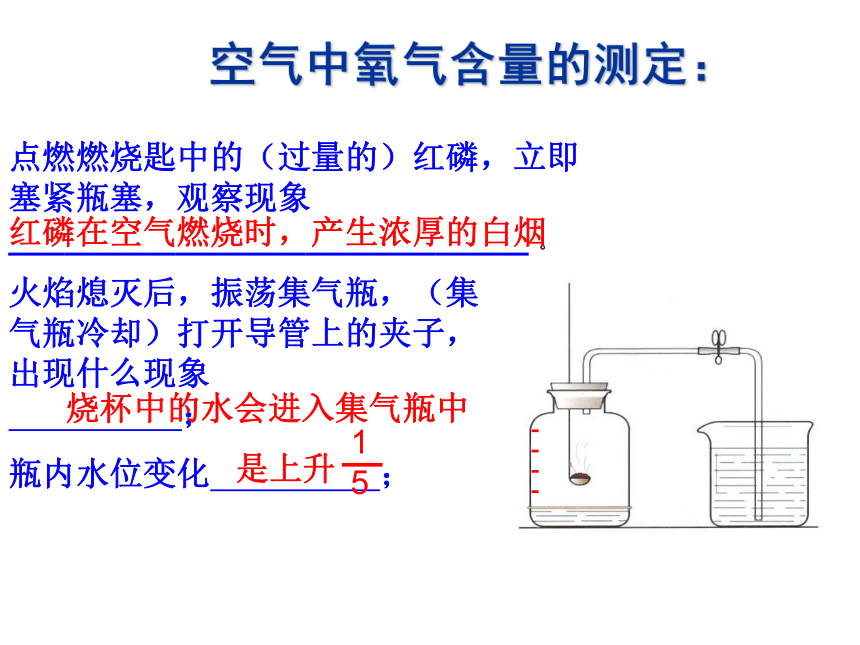
点燃燃烧匙中的(过量的)红磷,立即塞紧瓶塞,观察现象____________________________ 。红磷在空气燃烧时,产生浓厚的白烟 火焰熄灭后,振荡集气瓶,(集气瓶冷却)打开导管上的夹子,出现什么现象 ;
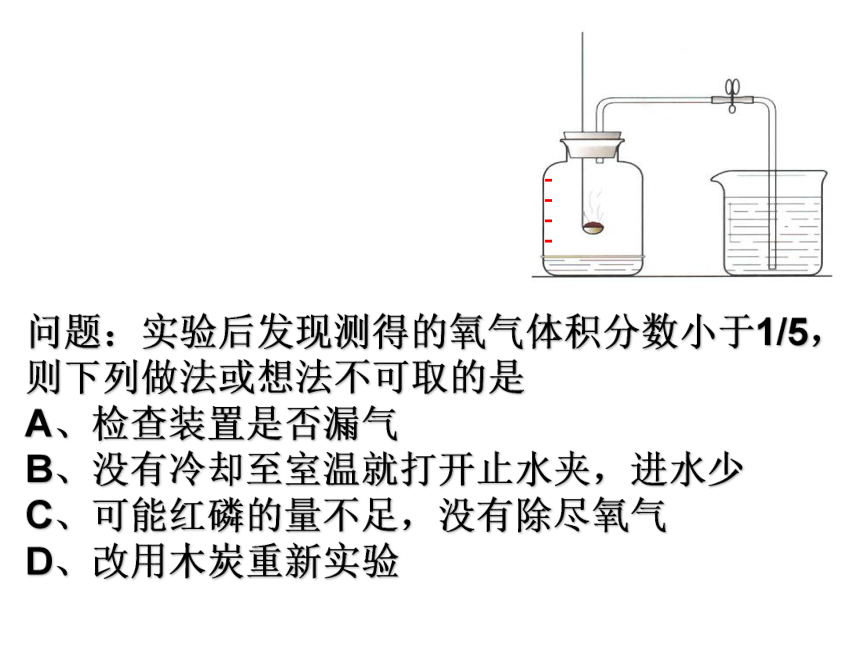
瓶内水位变化 ;烧杯中的水会进入集气瓶中 是上升空气中氧气含量的测定:问题:实验后发现测得的氧气体积分数小于1/5,
则下列做法或想法不可取的是
A、检查装置是否漏气
B、没有冷却至室温就打开止水夹,进水少
C、可能红磷的量不足,没有除尽氧气
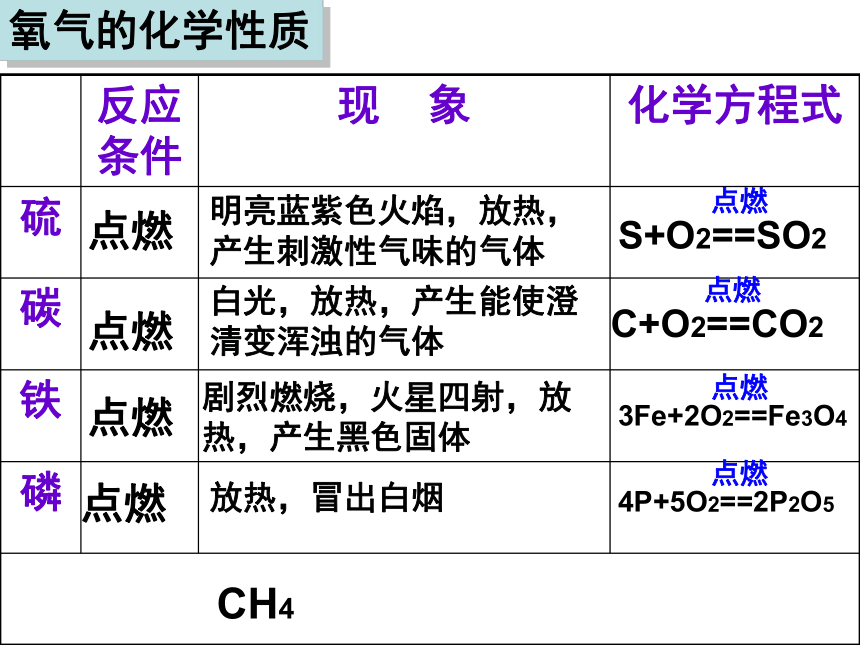
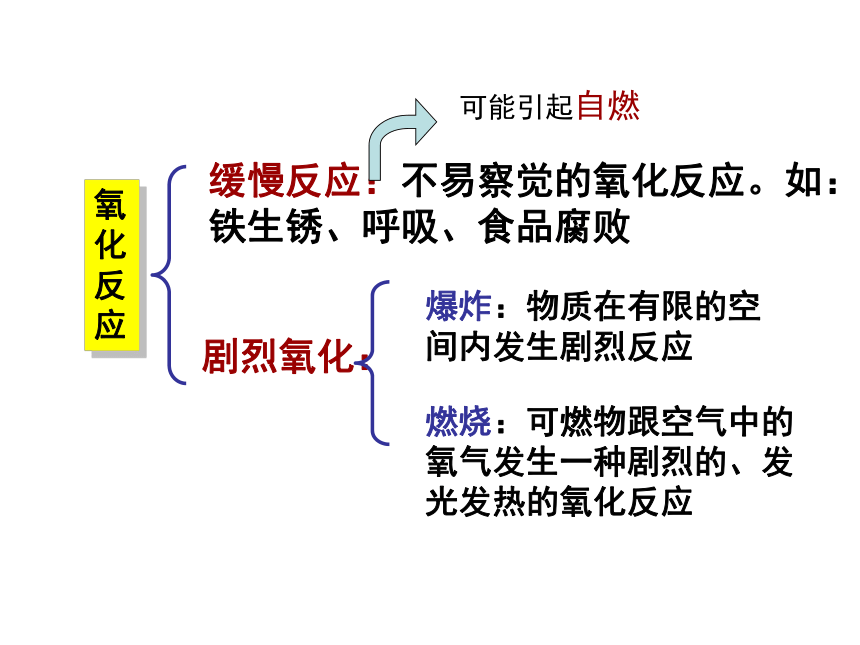
D、改用木炭重新实验根据作用指出气体的名称稀有气体(0.94%)按体积算氮气(78%)氧气(21%)其他气体(1%)二氧化碳(0.03%)水蒸气等其他杂质(0.03%)冲入灯泡延长使用寿命,用于食品防腐、保鲜,液态氮可作冷冻剂,是制作化肥、炸药的原料供给生物呼吸,支持燃料的燃烧用作保护气,制成各种用途的霓虹灯光合作用原料,用于制造纯碱、尿素、汽水饮料利用氮气的什么性质?氧气的化学性质点燃点燃点燃点燃明亮蓝紫色火焰,放热,产生刺激性气味的气体白光,放热,产生能使澄清变浑浊的气体剧烈燃烧,火星四射,放热,产生黑色固体放热,冒出白烟CH4氧化反应 缓慢反应:不易察觉的氧化反应。如:铁生锈、呼吸、食品腐败剧烈氧化:爆炸:物质在有限的空间内发生剧烈反应燃烧:可燃物跟空气中的氧气发生一种剧烈的、发光发热的氧化反应可能引起自燃燃烧的条件可燃物
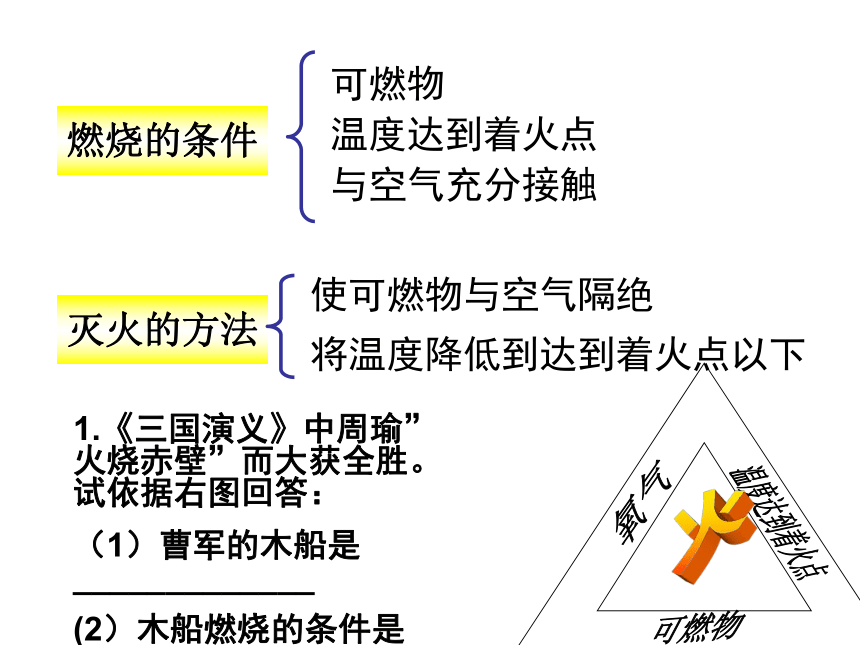
温度达到着火点
与空气充分接触灭火的方法使可燃物与空气隔绝
将温度降低到达到着火点以下 1.《三国演义》中周瑜”火烧赤壁”而大获全胜。试依据右图回答:
(1)曹军的木船是_____________
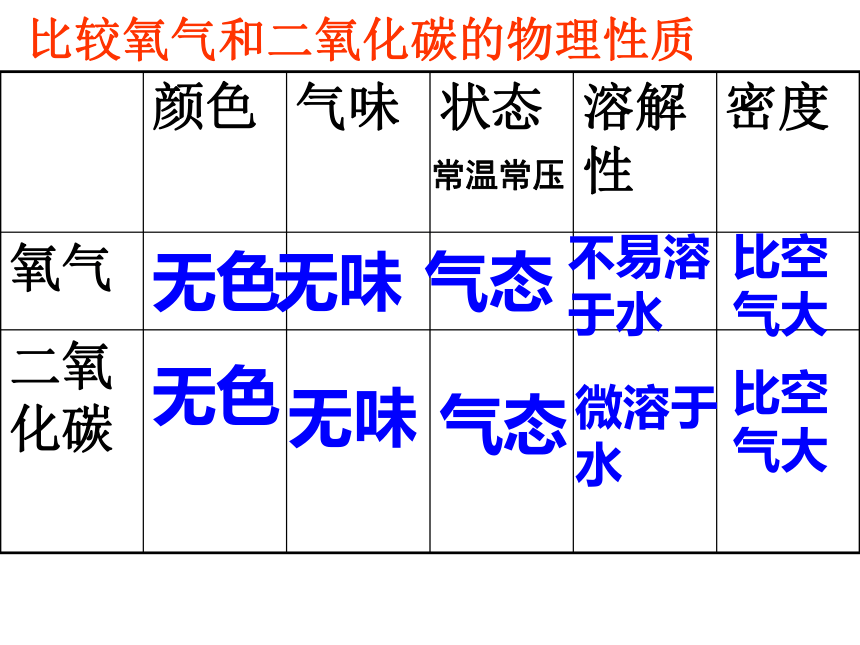
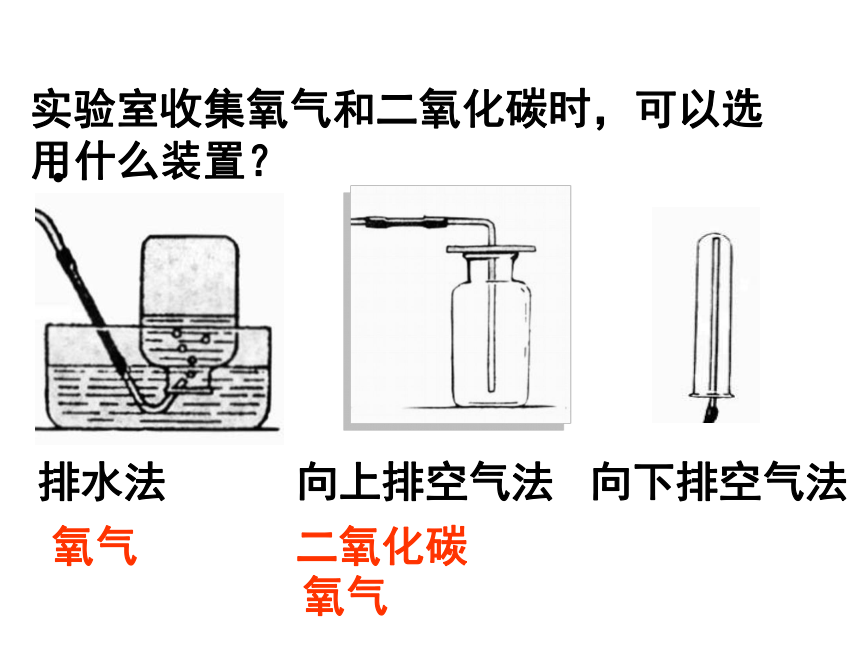
(2)木船燃烧的条件是____________________比较氧气和二氧化碳的物理性质无色无味气态常温常压不易溶于水比空气大无色无味气态微溶于水比空气大 实验室收集氧气和二氧化碳时,可以选用什么装置?排水法向上排空气法向下排空气法氧气二氧化碳氧气实验室制取O2和CO2CaCO3+2HCl=H2O+CaCl2+CO2↑排水法向上排空气法向上排空气法用带火星的木条伸到集气瓶口
用燃烧的木条伸到集气瓶口实验室用的少量氧气的制取和收集方法二:加热高锰酸钾(氯酸钾)法方法一:分解双氧水法比较两种装置有什么不同?方法2:加热高锰酸钾法查、装、定、点、收、取、灭试管口应略低于试管底(试管口略向下倾斜)铁夹夹在离管口约1/3至1/4处收集满氧气后,要先从水槽中移出导管,再熄灭酒精灯实验时,试管口要塞一团棉花指出错误之处1. 二氧化碳不能燃烧,也不支持燃烧。二氧化碳的化学性质二氧化碳的密度比空气大二氧化碳微溶于水2、二氧化碳跟水能反应二氧化碳的化学性质CO2+H2O=H2CO3浑浊二氧化碳的化学性质CO2 + Ca(OH)2 = CaCO3 ↓+ H2O
碳酸钙检验
二氧化碳
CO2 + 2NaOH = Na2CO3+ H2O 如果将二氧化碳通入到烧碱溶液中,是否也可以观察到浑浊的现象?讨论:为什么久置石灰水的试剂瓶内壁总是出现白膜?怎样才能除去白膜?用化学方程式来表示CO2+ Ca(OH)2 = H2O +CaCO3 ↓2HCl+CaCO3 = H2O + CO2 ↑ + CaCl2实验室有时用硫化亚铁(FeS)固体和稀硫酸在常温下反应,生成硫酸亚铁同时,得到一种无色,有刺激性气味,可溶于水的气体,经测定该气体的密度比空气的密度大.
试根据以上叙述及下图填空:
(1)叙述该气体物理性质有______
无色,刺激性气味,可溶于水,密度比空气大 (2)制取该气体应选_____装置,收集装置___;
(3)反应前容器里物质的总质量为10克,反应后物质的质量为8克,则生成气体的质量
____克AACDBDE1.内容:在化学反应中,参加化学反应的物质的质量总和等于反应后生成的各物质的质量总和。一.质量守恒定律2.微观解释:反应前后原子的种类和数目既没有改变也没有增减,原子的质量没有变化,所以,化学反应前后各物质的质量总和必然相等。4个磷原子 10个氧原子4个磷原子 10个氧原子
4P+5O2 ??????2P2O5点燃甲同学认为2克氢气和8克氧气反应能生成10克水,符合质量守恒定律的观点;
乙同学认为1克的冰融化成1克水, 遵循了质量守恒定律;
丙同学根据“铁生锈后质量会增加”,推断出质量守恒定律也有例外.
你认为三位同学的观点正确吗?
思考题1、加热A克氯酸钾和B克二氧化锰的混合物,反应后称得残留物的质量总和为C克,则生成氧气的质量为____
2、在化学反应A+B=C+D中,若20克A和10克B正好完全反应生成5克C,则4克A和___ 克B正好反应___克D。若D的相对分子质量为75,则A的相对分子质量为____
A+B-C2560练习:3. CO俗称“无形杀手”,用物质X可以测定空气受CO污染的程度,X与CO反应的化学方程式为:X+5CO==I2+5CO2,根据生成CO2的质量,可测定CO含量,请你写出X的化学式_________.I2O5练习: 4.在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
反应后密闭容器中A的质量为____________;
此基本的反应类型是_____________ 练习: 8、把干燥纯净的KClO3和MnO2的混合物13.32克,加热至不再产生气体为止,称量剩余物质量为9.48克,求①生成氧气的质量;②剩余物质各是什么?质量分别是多少克?分析 MnO2作为催化剂在反应前后其质量和化学性质都不改变,所以13.32g-9.48g=3.84g, 这3.84g就是放出O2的质量,这也是解本题的关键.
解 根据质量守恒定律
mO2 = 13.32g – 9.48g = 3.84g
设生成物中KCl质量为xg
2KClO3=====2KCl+3O2↑
149 96
x 3.84g
∴ x=5.96g
MnO2的质量 9.48g – 5.96g = 3.52g
答:氧气的质量为3.84g,剩余物为KCl和MnO2质量分别为5.96g和3.52g.
MnO2149X963.84g=练习:有一不纯的锌片15.25克,跟足量的稀硫酸完全反应(杂质不参加反应),生成0.4克氢气,求此锌片中含锌的质量分数.
(反应化学方程式是:
Zn + H2SO4 === ZnSO4 + H2↑)光合作用的表达式:
二氧化碳+水===有机物(淀粉)氧气
光叶绿体 呼吸作用的表达式:有机物+氧气===二氧化碳+水+能量酶联系:光合作用为呼吸作用提供 和
呼吸作用为光合作用提供 和
有机物氧气二氧化碳水光合作用所需要的能量是呼吸作用释放的能量,
呼吸作用释放的能量是光合作用储存在有机物中的能量。光合作用和呼吸作用的区别叶绿体
活细胞是否吸进CO2
呼出O2吸进O2
呼出CO2制造有机物
储藏能量
分解有机物
释放能量问题:
如何设计实验验证光合作用必需
要光?原理:
设置对照实验,一组光照,一组无光处理,其它条件保持一致。比较两者产生淀粉的情况来验证猜测。设计实验验证光合作用必需要光实验步骤:
1、取一盆植物,选取合适叶片,遮光处理。
2、放在暗处24小时。
3、光照几小时。
4、酒精脱色,清水漂洗。
5、碘液检测。问题:何种现象可验证光合作用
必需要光?遮光处理不变蓝,光照处理变蓝2、解释新疆的哈密瓜
为什么特别甜?新疆温差大,白天光照强复述吸气和呼气的变化碳循环和氧循环生物呼吸物质燃烧 植物
光合作用 植物
光合作用物质燃烧生物呼吸微生物分解作用
(0.03%)
(0.03%)
点燃燃烧匙中的(过量的)红磷,立即塞紧瓶塞,观察现象____________________________ 。红磷在空气燃烧时,产生浓厚的白烟 火焰熄灭后,振荡集气瓶,(集气瓶冷却)打开导管上的夹子,出现什么现象 ;
瓶内水位变化 ;烧杯中的水会进入集气瓶中 是上升空气中氧气含量的测定:问题:实验后发现测得的氧气体积分数小于1/5,
则下列做法或想法不可取的是
A、检查装置是否漏气
B、没有冷却至室温就打开止水夹,进水少
C、可能红磷的量不足,没有除尽氧气
D、改用木炭重新实验根据作用指出气体的名称稀有气体(0.94%)按体积算氮气(78%)氧气(21%)其他气体(1%)二氧化碳(0.03%)水蒸气等其他杂质(0.03%)冲入灯泡延长使用寿命,用于食品防腐、保鲜,液态氮可作冷冻剂,是制作化肥、炸药的原料供给生物呼吸,支持燃料的燃烧用作保护气,制成各种用途的霓虹灯光合作用原料,用于制造纯碱、尿素、汽水饮料利用氮气的什么性质?氧气的化学性质点燃点燃点燃点燃明亮蓝紫色火焰,放热,产生刺激性气味的气体白光,放热,产生能使澄清变浑浊的气体剧烈燃烧,火星四射,放热,产生黑色固体放热,冒出白烟CH4氧化反应 缓慢反应:不易察觉的氧化反应。如:铁生锈、呼吸、食品腐败剧烈氧化:爆炸:物质在有限的空间内发生剧烈反应燃烧:可燃物跟空气中的氧气发生一种剧烈的、发光发热的氧化反应可能引起自燃燃烧的条件可燃物
温度达到着火点
与空气充分接触灭火的方法使可燃物与空气隔绝
将温度降低到达到着火点以下 1.《三国演义》中周瑜”火烧赤壁”而大获全胜。试依据右图回答:
(1)曹军的木船是_____________
(2)木船燃烧的条件是____________________比较氧气和二氧化碳的物理性质无色无味气态常温常压不易溶于水比空气大无色无味气态微溶于水比空气大 实验室收集氧气和二氧化碳时,可以选用什么装置?排水法向上排空气法向下排空气法氧气二氧化碳氧气实验室制取O2和CO2CaCO3+2HCl=H2O+CaCl2+CO2↑排水法向上排空气法向上排空气法用带火星的木条伸到集气瓶口
用燃烧的木条伸到集气瓶口实验室用的少量氧气的制取和收集方法二:加热高锰酸钾(氯酸钾)法方法一:分解双氧水法比较两种装置有什么不同?方法2:加热高锰酸钾法查、装、定、点、收、取、灭试管口应略低于试管底(试管口略向下倾斜)铁夹夹在离管口约1/3至1/4处收集满氧气后,要先从水槽中移出导管,再熄灭酒精灯实验时,试管口要塞一团棉花指出错误之处1. 二氧化碳不能燃烧,也不支持燃烧。二氧化碳的化学性质二氧化碳的密度比空气大二氧化碳微溶于水2、二氧化碳跟水能反应二氧化碳的化学性质CO2+H2O=H2CO3浑浊二氧化碳的化学性质CO2 + Ca(OH)2 = CaCO3 ↓+ H2O
碳酸钙检验
二氧化碳
CO2 + 2NaOH = Na2CO3+ H2O 如果将二氧化碳通入到烧碱溶液中,是否也可以观察到浑浊的现象?讨论:为什么久置石灰水的试剂瓶内壁总是出现白膜?怎样才能除去白膜?用化学方程式来表示CO2+ Ca(OH)2 = H2O +CaCO3 ↓2HCl+CaCO3 = H2O + CO2 ↑ + CaCl2实验室有时用硫化亚铁(FeS)固体和稀硫酸在常温下反应,生成硫酸亚铁同时,得到一种无色,有刺激性气味,可溶于水的气体,经测定该气体的密度比空气的密度大.
试根据以上叙述及下图填空:
(1)叙述该气体物理性质有______
无色,刺激性气味,可溶于水,密度比空气大 (2)制取该气体应选_____装置,收集装置___;
(3)反应前容器里物质的总质量为10克,反应后物质的质量为8克,则生成气体的质量
____克AACDBDE1.内容:在化学反应中,参加化学反应的物质的质量总和等于反应后生成的各物质的质量总和。一.质量守恒定律2.微观解释:反应前后原子的种类和数目既没有改变也没有增减,原子的质量没有变化,所以,化学反应前后各物质的质量总和必然相等。4个磷原子 10个氧原子4个磷原子 10个氧原子
4P+5O2 ??????2P2O5点燃甲同学认为2克氢气和8克氧气反应能生成10克水,符合质量守恒定律的观点;
乙同学认为1克的冰融化成1克水, 遵循了质量守恒定律;
丙同学根据“铁生锈后质量会增加”,推断出质量守恒定律也有例外.
你认为三位同学的观点正确吗?
思考题1、加热A克氯酸钾和B克二氧化锰的混合物,反应后称得残留物的质量总和为C克,则生成氧气的质量为____
2、在化学反应A+B=C+D中,若20克A和10克B正好完全反应生成5克C,则4克A和___ 克B正好反应___克D。若D的相对分子质量为75,则A的相对分子质量为____
A+B-C2560练习:3. CO俗称“无形杀手”,用物质X可以测定空气受CO污染的程度,X与CO反应的化学方程式为:X+5CO==I2+5CO2,根据生成CO2的质量,可测定CO含量,请你写出X的化学式_________.I2O5练习: 4.在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
反应后密闭容器中A的质量为____________;
此基本的反应类型是_____________ 练习: 8、把干燥纯净的KClO3和MnO2的混合物13.32克,加热至不再产生气体为止,称量剩余物质量为9.48克,求①生成氧气的质量;②剩余物质各是什么?质量分别是多少克?分析 MnO2作为催化剂在反应前后其质量和化学性质都不改变,所以13.32g-9.48g=3.84g, 这3.84g就是放出O2的质量,这也是解本题的关键.
解 根据质量守恒定律
mO2 = 13.32g – 9.48g = 3.84g
设生成物中KCl质量为xg
2KClO3=====2KCl+3O2↑
149 96
x 3.84g
∴ x=5.96g
MnO2的质量 9.48g – 5.96g = 3.52g
答:氧气的质量为3.84g,剩余物为KCl和MnO2质量分别为5.96g和3.52g.
MnO2149X963.84g=练习:有一不纯的锌片15.25克,跟足量的稀硫酸完全反应(杂质不参加反应),生成0.4克氢气,求此锌片中含锌的质量分数.
(反应化学方程式是:
Zn + H2SO4 === ZnSO4 + H2↑)光合作用的表达式:
二氧化碳+水===有机物(淀粉)氧气
光叶绿体 呼吸作用的表达式:有机物+氧气===二氧化碳+水+能量酶联系:光合作用为呼吸作用提供 和
呼吸作用为光合作用提供 和
有机物氧气二氧化碳水光合作用所需要的能量是呼吸作用释放的能量,
呼吸作用释放的能量是光合作用储存在有机物中的能量。光合作用和呼吸作用的区别叶绿体
活细胞是否吸进CO2
呼出O2吸进O2
呼出CO2制造有机物
储藏能量
分解有机物
释放能量问题:
如何设计实验验证光合作用必需
要光?原理:
设置对照实验,一组光照,一组无光处理,其它条件保持一致。比较两者产生淀粉的情况来验证猜测。设计实验验证光合作用必需要光实验步骤:
1、取一盆植物,选取合适叶片,遮光处理。
2、放在暗处24小时。
3、光照几小时。
4、酒精脱色,清水漂洗。
5、碘液检测。问题:何种现象可验证光合作用
必需要光?遮光处理不变蓝,光照处理变蓝2、解释新疆的哈密瓜
为什么特别甜?新疆温差大,白天光照强复述吸气和呼气的变化碳循环和氧循环生物呼吸物质燃烧 植物
光合作用 植物
光合作用物质燃烧生物呼吸微生物分解作用
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
