第二章复习(二)[下学期]
图片预览






文档简介
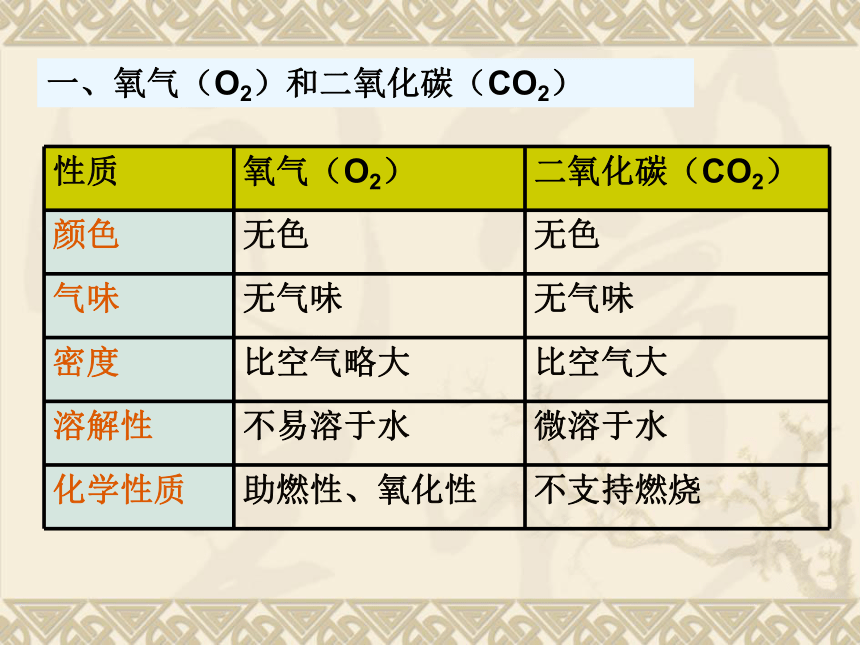
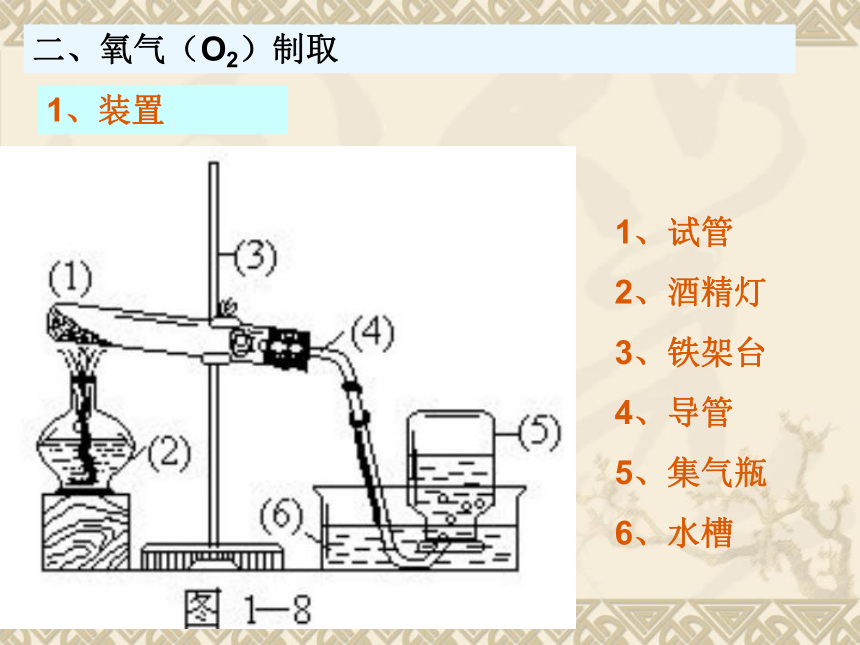
课件20张PPT。第二章复习(二)梅山小班 李森伟一、氧气(O2)和二氧化碳(CO2)二、氧气(O2)制取1、试管
2、酒精灯
3、铁架台
4、导管
5、集气瓶
6、水槽1、装置2、注意事项(1)试管口略向下斜:
(2)实验结束时,先移出导管,再熄灭酒精灯:
(3)试管口塞一团棉花:
(4)用外焰加热:
(5)先要均匀受热:
(6)气泡连续时才能收集:
(7)氧气集满后,应正放在桌面上:3、制取的原理2KClO3=====2KCl+3O2↑
2KMnO4===K2MnO4+MnO2+O2↑MnO24、收集方法排水法
向上排空气法不易溶于水
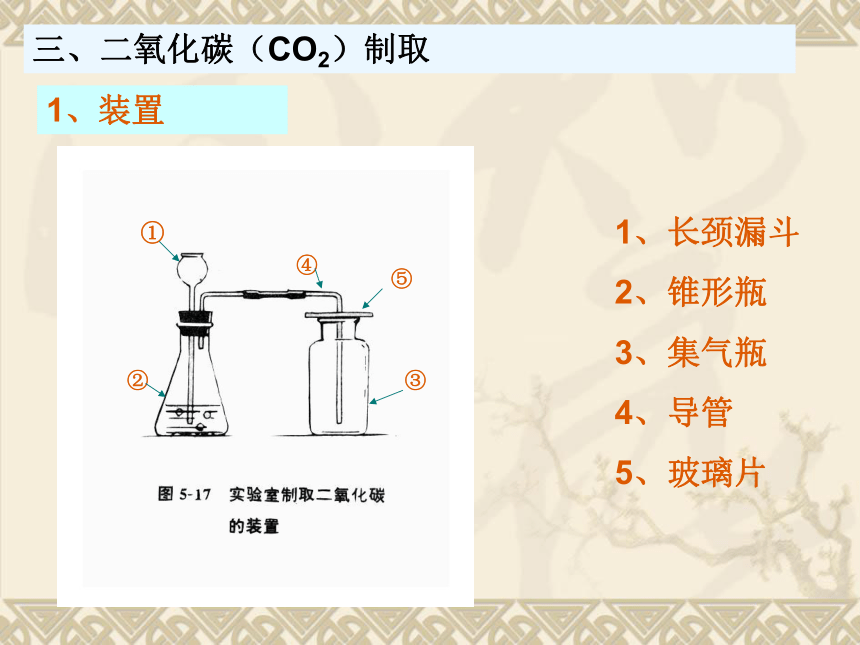
密度比空气大1、长颈漏斗
2、锥形瓶
3、集气瓶
4、导管
5、玻璃片1、装置三、二氧化碳(CO2)制取①②③④⑤2、注意事项(1)长颈漏斗下端口应伸到液面以下:
(2)伸入集气瓶的导管口应接近瓶底:
(3)不能用排水法收集:
(4)检验二氧化碳是否集满,应把燃着的木条放在集气瓶口的上方:
(5)二氧化碳集满后,应正放在桌面上:3、制取的原理CaCO3+2HCl==CaCl2+H2O+CO2↑ 4、收集方法向上排空气法密度比空气大不能用排水法收集的原因是:二氧化碳会与水反应
CO2+H2O==H2CO3
H2CO3===H2O+CO2↑ 1.关于催化剂的说法正确的是 [ ] A.用等质量的氯酸钾和高锰酸钾分别制取氧气,前者生成氧气多是因为加入了二氧化锰 B.催化剂不参加化学反应 C.催化剂能改变其它物质的化学反应速度 D.二氧化锰是所有化学反应的催化剂
2.制取和收集氧气时,都要用到的一组仪器是[ ] A.集气瓶,量筒,铁架台,试管 B.集气瓶,试管,铁架台,导管 C.酒精灯,蒸发皿,试管,铁架台 D.铁架台,试管,漏斗,导管 CB3.能用排水法收集的气体,应具备的性质是式 [ ] A.没有颜色 B.密度比空气小 C.难溶于水 D.易溶于水
4.实验室用高锰酸钾制氧气时,错误的操作是[ ] A.检查装置的气密性时,先对试管加热,过一会儿把导管放入水里,没有看到气泡逸出,说明装置漏气 B.固定在铁夹上的试管,试管口应略向下倾斜 C.加热时,先使酒精灯在试管下方来回移动,使试管均匀受热,然后再对准高锰酸钾所在部位加热 D.排水法收集氧气后,应先把导管移出水面,再停止加热 CA5.下列叙述正确的是 [ ] A.用带火星的木条插入到集气瓶中检验内氧气是否已满 B.食盐水蒸发得到固体食盐和水蒸气是分解反应 C.把氯酸钾和高锰酸钾混合加热,比单独加热氯酸钾制出氧气的速率快 D.因为氧气比水轻,所以可以用排水法收集
6.下列现象可用氧气的物理性质解释的是 [ ] A.白磷在40℃时即可燃烧,烈日下白磷不经点燃就可燃烧 B.红色的铜经加热表面生成黑色的氧化铜 C.实验室制取氧气时,最好用排水法而不用向上排空气法收集 D.氧气可使带火星的木条燃烧 CC7.下列说法正确的是 [ ] A.氯酸钾中含有氧气,加热时即可放出 B.从空气中可以得到氮气和氧气,这个变化是分解反应 C.凡是含氧的物质都可以作为实验室制氧气的原料 D.实验室用氯酸钾制氧气时发生了化学反应
9.收集氧气时,检验集气瓶已收集满氧气的方法是 [ ] A.把带火星的木条伸到集气瓶底部 B.把带火星的木条放到集气瓶口 C.向集气瓶中倒入少量石灰水 D.在集气瓶口闻气味 DB14.在实验室制取氧气主要分为以下七步。请按操作的先后顺序,把序号填在括号内。
第( )步:给试管加热 第( )步:检查装置的气密性 第( )步:用铁架台上的铁夹把试管固定在铁
架台上 第( )步:将氯酸钾和二氧化锰放入试管中,
用带导管的塞子塞紧 第( )步:用排水集气法收集一瓶氧气 第( )步:用灯帽盖灭酒精灯 第( )步:将导管从水槽内拿出来123456715.判断正误
(1)工业上主要是用分离液态空气的方法制取大量氧气,这个过程属于分解反应。 ( )
(2)加热含有氧的化合物就一定会产生氧气。( )
(3)加热氯酸钾和二氧化锰的混合物制取氧气的化学反应属于化合反应类型,因为反应物是两种。 ( )
(4)催化剂在化学反应中质量和化学性质都不改变。( )
(5)因为氧气能够支持燃烧,所以空气里所含氧气越丰富,可燃物燃烧就越强烈。 ( )
(6)使燃着的木条熄灭的无色气体一定是二氧化碳气。 ( )
(7)从氯酸钾制氧气后的剩余固体中分离出的二氧化锰,质量和化学性质都没有改变 ( )
(8)污染空气的气体,主要是二氧化硫、二氧化氮、一氧化碳等 ( )
(9)氧化反应是指物质跟氧气发生的反应 ( )
(10)食盐水蒸发后得到食盐和水蒸气,所以食盐水蒸发是分解反应。 ( )1、把点燃的蜡烛伸进干燥的有氧气的集气瓶里,待燃烧停止,冷却后,集气瓶壁出现 ,说明燃烧生成了 ,向瓶里倒入澄清的石灰水,石灰水变 ,说明蜡烛燃烧还生成了 。25、实验室制取氧气的操作有:①用排水法收集气体,②把药品装入大试管,③给试管加热,④检查气密性,⑤熄灭酒精灯停止加热,⑥将导管移出水面,⑦用铁夹把装置固定在铁架台上。将操作正确顺序用数字代号排列起来______________。 26、炎热的夏季,你一定想喝一杯冰水解暑。某冷饮店出售一种特制的冰水,由服务员在水中加入一些雪状的物质,该物质一放入水中立即冒出大量气泡,很快就得到一杯清凉可口的冰水,饮用时有碳酸饮料的口感。
(1)请你判断雪状的物质是________________;
(2)请你设计两个实验分别验证这种物质的成分30、某生在实验室用高锰酸钾
(2KMnO4 K2MnO4+MnO2+O2↑)来制取氧气,他在加热操作前,已经完成的实验步骤如图所示,回答:
(2)审视图示,请分别指出该生在加热前的
操作中的三个明显错误:
①__________ ②____________ ③_____________
(3)加热前,测得试管及内部高锰酸钾的总质量21.6克,完全反应后冷却到室温,测得试管及内部固体的总质量为20克,则生成的氧气质量为____________克。 29、如图是制取和验证CO2化学性质的装置图,
试回答下列问题:
(1)写出有标号的仪器名称: a______ b______c_____
(2)装置1是制取CO2装置,内装的药品是:
(写名称)________和_______。反应现象_____________
(3)用装置2来检验CO2,则盛放的试剂名称是__________,反应现象_____________。
(4)用装置3证明CO2与水反应生成碳酸,则装置3中除水外还应加入的试剂是:_______________,实验现象是___________________
(5)装置4中放有燃着的高低不同的蜡烛,观察到的现象是______________________这个现象说明CO2具有的性质是___________________、_____________________21、①纯净的氮气是无色、无味的气体;②在放电条件下,N2跟O2能直接化合生成无色的NO气体;③NO气体不溶于水,在常温下易跟空气中的O2化合,生成红棕色NO2气体;④NO2气体有毒,易溶于水,溶于水后生成HNO3和NO;⑤生成的HNO3随雨水淋洒在大地上,同土壤中的矿物相作用,形成可溶性硝酸盐。试填写下列空白:
(1)氮气的物理性质是____________________
(2)实验室制取NO气体宜用________________法收集(3)写出NO2跟水作用的化学方程式______________________ 32、煤是重要的化工原料,用煤作燃料,不仅是极大的浪费,而且因煤中含有硫,燃烧后生成的二氧化硫会造成空气污染。某工厂用煤作燃料,每天燃烧含硫2%的煤4800千克。
(1)试计算每天该厂排放到空气中的二氧化硫为多少千克?
(2)该厂废气中二氧化硫的含量可根据下列反应测定:SO2+2H2O+I2==H2SO4+2HI。现取该厂废气样品500mL,用溶质的质量分数为2*10-9(即0.0000002%)的碘溶液200克与废气中二氧化硫恰好完全反应.试计算该厂排放的废气是否符合国家规定的工业废气排放标准(废气中二氧化硫的含量不得超过0.15mg/m3)
(3)用煤作燃料,你认为用什么方法可以减少二氧化硫对空气的污染.
2、酒精灯
3、铁架台
4、导管
5、集气瓶
6、水槽1、装置2、注意事项(1)试管口略向下斜:
(2)实验结束时,先移出导管,再熄灭酒精灯:
(3)试管口塞一团棉花:
(4)用外焰加热:
(5)先要均匀受热:
(6)气泡连续时才能收集:
(7)氧气集满后,应正放在桌面上:3、制取的原理2KClO3=====2KCl+3O2↑
2KMnO4===K2MnO4+MnO2+O2↑MnO24、收集方法排水法
向上排空气法不易溶于水
密度比空气大1、长颈漏斗
2、锥形瓶
3、集气瓶
4、导管
5、玻璃片1、装置三、二氧化碳(CO2)制取①②③④⑤2、注意事项(1)长颈漏斗下端口应伸到液面以下:
(2)伸入集气瓶的导管口应接近瓶底:
(3)不能用排水法收集:
(4)检验二氧化碳是否集满,应把燃着的木条放在集气瓶口的上方:
(5)二氧化碳集满后,应正放在桌面上:3、制取的原理CaCO3+2HCl==CaCl2+H2O+CO2↑ 4、收集方法向上排空气法密度比空气大不能用排水法收集的原因是:二氧化碳会与水反应
CO2+H2O==H2CO3
H2CO3===H2O+CO2↑ 1.关于催化剂的说法正确的是 [ ] A.用等质量的氯酸钾和高锰酸钾分别制取氧气,前者生成氧气多是因为加入了二氧化锰 B.催化剂不参加化学反应 C.催化剂能改变其它物质的化学反应速度 D.二氧化锰是所有化学反应的催化剂
2.制取和收集氧气时,都要用到的一组仪器是[ ] A.集气瓶,量筒,铁架台,试管 B.集气瓶,试管,铁架台,导管 C.酒精灯,蒸发皿,试管,铁架台 D.铁架台,试管,漏斗,导管 CB3.能用排水法收集的气体,应具备的性质是式 [ ] A.没有颜色 B.密度比空气小 C.难溶于水 D.易溶于水
4.实验室用高锰酸钾制氧气时,错误的操作是[ ] A.检查装置的气密性时,先对试管加热,过一会儿把导管放入水里,没有看到气泡逸出,说明装置漏气 B.固定在铁夹上的试管,试管口应略向下倾斜 C.加热时,先使酒精灯在试管下方来回移动,使试管均匀受热,然后再对准高锰酸钾所在部位加热 D.排水法收集氧气后,应先把导管移出水面,再停止加热 CA5.下列叙述正确的是 [ ] A.用带火星的木条插入到集气瓶中检验内氧气是否已满 B.食盐水蒸发得到固体食盐和水蒸气是分解反应 C.把氯酸钾和高锰酸钾混合加热,比单独加热氯酸钾制出氧气的速率快 D.因为氧气比水轻,所以可以用排水法收集
6.下列现象可用氧气的物理性质解释的是 [ ] A.白磷在40℃时即可燃烧,烈日下白磷不经点燃就可燃烧 B.红色的铜经加热表面生成黑色的氧化铜 C.实验室制取氧气时,最好用排水法而不用向上排空气法收集 D.氧气可使带火星的木条燃烧 CC7.下列说法正确的是 [ ] A.氯酸钾中含有氧气,加热时即可放出 B.从空气中可以得到氮气和氧气,这个变化是分解反应 C.凡是含氧的物质都可以作为实验室制氧气的原料 D.实验室用氯酸钾制氧气时发生了化学反应
9.收集氧气时,检验集气瓶已收集满氧气的方法是 [ ] A.把带火星的木条伸到集气瓶底部 B.把带火星的木条放到集气瓶口 C.向集气瓶中倒入少量石灰水 D.在集气瓶口闻气味 DB14.在实验室制取氧气主要分为以下七步。请按操作的先后顺序,把序号填在括号内。
第( )步:给试管加热 第( )步:检查装置的气密性 第( )步:用铁架台上的铁夹把试管固定在铁
架台上 第( )步:将氯酸钾和二氧化锰放入试管中,
用带导管的塞子塞紧 第( )步:用排水集气法收集一瓶氧气 第( )步:用灯帽盖灭酒精灯 第( )步:将导管从水槽内拿出来123456715.判断正误
(1)工业上主要是用分离液态空气的方法制取大量氧气,这个过程属于分解反应。 ( )
(2)加热含有氧的化合物就一定会产生氧气。( )
(3)加热氯酸钾和二氧化锰的混合物制取氧气的化学反应属于化合反应类型,因为反应物是两种。 ( )
(4)催化剂在化学反应中质量和化学性质都不改变。( )
(5)因为氧气能够支持燃烧,所以空气里所含氧气越丰富,可燃物燃烧就越强烈。 ( )
(6)使燃着的木条熄灭的无色气体一定是二氧化碳气。 ( )
(7)从氯酸钾制氧气后的剩余固体中分离出的二氧化锰,质量和化学性质都没有改变 ( )
(8)污染空气的气体,主要是二氧化硫、二氧化氮、一氧化碳等 ( )
(9)氧化反应是指物质跟氧气发生的反应 ( )
(10)食盐水蒸发后得到食盐和水蒸气,所以食盐水蒸发是分解反应。 ( )1、把点燃的蜡烛伸进干燥的有氧气的集气瓶里,待燃烧停止,冷却后,集气瓶壁出现 ,说明燃烧生成了 ,向瓶里倒入澄清的石灰水,石灰水变 ,说明蜡烛燃烧还生成了 。25、实验室制取氧气的操作有:①用排水法收集气体,②把药品装入大试管,③给试管加热,④检查气密性,⑤熄灭酒精灯停止加热,⑥将导管移出水面,⑦用铁夹把装置固定在铁架台上。将操作正确顺序用数字代号排列起来______________。 26、炎热的夏季,你一定想喝一杯冰水解暑。某冷饮店出售一种特制的冰水,由服务员在水中加入一些雪状的物质,该物质一放入水中立即冒出大量气泡,很快就得到一杯清凉可口的冰水,饮用时有碳酸饮料的口感。
(1)请你判断雪状的物质是________________;
(2)请你设计两个实验分别验证这种物质的成分30、某生在实验室用高锰酸钾
(2KMnO4 K2MnO4+MnO2+O2↑)来制取氧气,他在加热操作前,已经完成的实验步骤如图所示,回答:
(2)审视图示,请分别指出该生在加热前的
操作中的三个明显错误:
①__________ ②____________ ③_____________
(3)加热前,测得试管及内部高锰酸钾的总质量21.6克,完全反应后冷却到室温,测得试管及内部固体的总质量为20克,则生成的氧气质量为____________克。 29、如图是制取和验证CO2化学性质的装置图,
试回答下列问题:
(1)写出有标号的仪器名称: a______ b______c_____
(2)装置1是制取CO2装置,内装的药品是:
(写名称)________和_______。反应现象_____________
(3)用装置2来检验CO2,则盛放的试剂名称是__________,反应现象_____________。
(4)用装置3证明CO2与水反应生成碳酸,则装置3中除水外还应加入的试剂是:_______________,实验现象是___________________
(5)装置4中放有燃着的高低不同的蜡烛,观察到的现象是______________________这个现象说明CO2具有的性质是___________________、_____________________21、①纯净的氮气是无色、无味的气体;②在放电条件下,N2跟O2能直接化合生成无色的NO气体;③NO气体不溶于水,在常温下易跟空气中的O2化合,生成红棕色NO2气体;④NO2气体有毒,易溶于水,溶于水后生成HNO3和NO;⑤生成的HNO3随雨水淋洒在大地上,同土壤中的矿物相作用,形成可溶性硝酸盐。试填写下列空白:
(1)氮气的物理性质是____________________
(2)实验室制取NO气体宜用________________法收集(3)写出NO2跟水作用的化学方程式______________________ 32、煤是重要的化工原料,用煤作燃料,不仅是极大的浪费,而且因煤中含有硫,燃烧后生成的二氧化硫会造成空气污染。某工厂用煤作燃料,每天燃烧含硫2%的煤4800千克。
(1)试计算每天该厂排放到空气中的二氧化硫为多少千克?
(2)该厂废气中二氧化硫的含量可根据下列反应测定:SO2+2H2O+I2==H2SO4+2HI。现取该厂废气样品500mL,用溶质的质量分数为2*10-9(即0.0000002%)的碘溶液200克与废气中二氧化硫恰好完全反应.试计算该厂排放的废气是否符合国家规定的工业废气排放标准(废气中二氧化硫的含量不得超过0.15mg/m3)
(3)用煤作燃料,你认为用什么方法可以减少二氧化硫对空气的污染.
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
