核外电子排布[下学期]
图片预览






文档简介
课件23张PPT。 核外电子排布的知识宏观物体与电子的对比:1.对比质量
电子的质量:9.10×10-31kg
2.对比速度
如炮弹2km/s; 人造卫星7.8km/s; 宇宙飞船11km/s
氢原子核外电子:2.2×105km/s
3.对比运动范围
原子半径:n×10-10m
乒乓球半径:4×10-2m
电子运动视频1.什么叫原子?它的结构是怎样的?
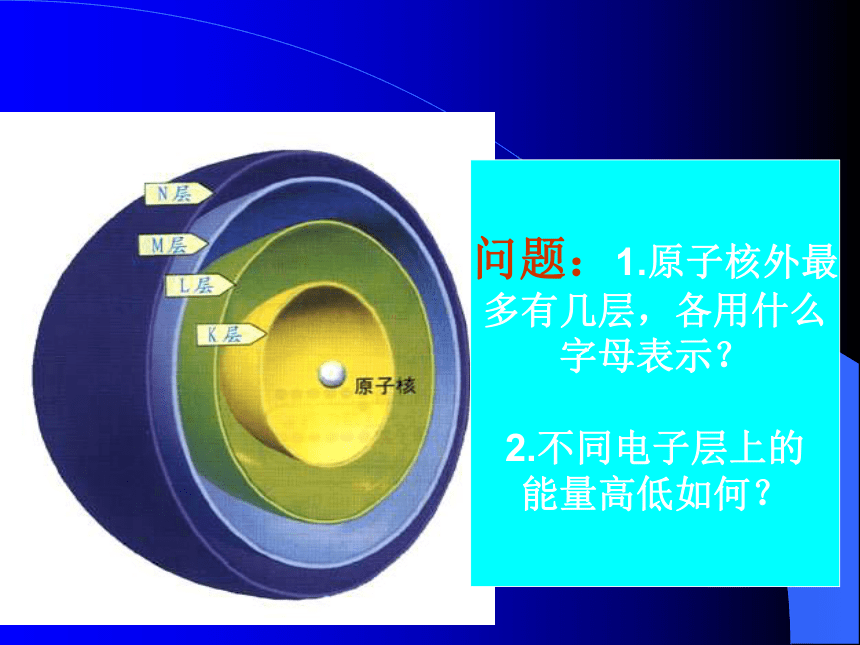
2.原子为什么会呈电中性?思考:原子原子核质子中子核外电子核电荷数= =核外电子数核内质子数复习玻尔电子模型 核外电子是处在一定的轨道上饶核运行的。就太阳系的行星饶太阳运行一样;在核外运行的电子按能量的高低分层排步。问题:1.原子核外最
多有几层,各用什么
字母表示?
2.不同电子层上的
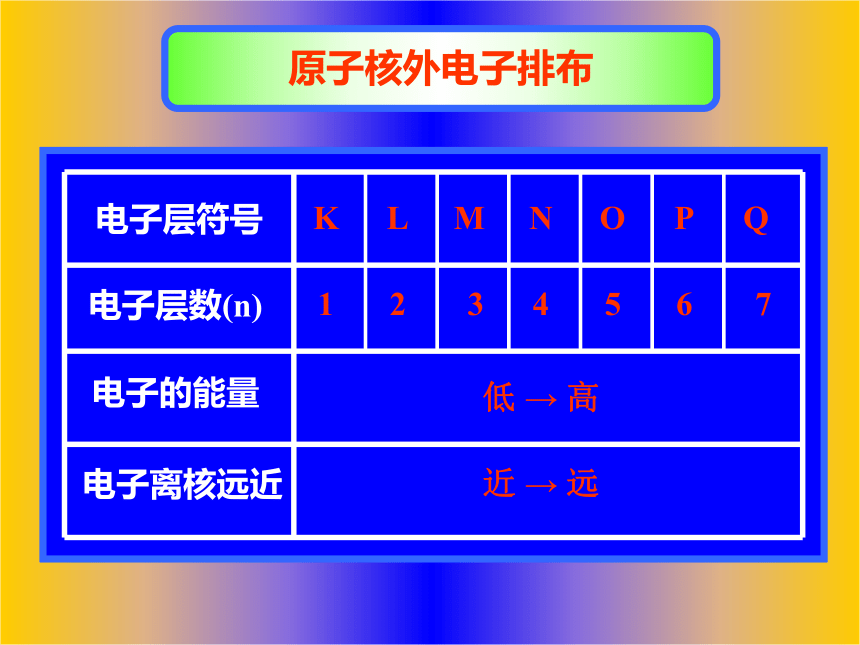
能量高低如何?小结:原子核外电子是分层排布的(1)“电子层”表示运动着的电子离核远近的不同*由进到远:第一 、二、三、四、五、六、七层 K 、 L、 M、 N、 O、 P、 Q*由进到远: 电子(层)的能量由低到高能量最低原理 在核外电子排布中,电子总是尽量最先占有能量最低的轨道
只有能量最低的轨道被占满后,电子才能依次占有能量较高的轨道,这就是所谓能量最低原理。 原子核外电子排布KLMNOPQ1234567低 → 高 近 → 远 核外电子排布规律1)核外电子总是尽先排布在能量最低的电子层里,然后再由里往外,依次排布在能量逐步升高的电子层里。 2)各电子层最多容纳的电子数目是2n2,即K层2个,L层8个,M层18个,N层32个。 最外层电子数目不超过8个(K层为最外层时不超过2个) 次外层电子数目不超过18个。2.原子结构示意图表示原子氧原子(O)氢原子(H)原子结构示意图的含义:镁原子(Mg )原子核质子数电子层该层上的电子数第一层 倒数第一层 最外层 次外层
试画出氧原子,磷原子,钠离子,氯离子,氖原子的结构示意图
核电荷数为1~18的元素的原子结构示意图金属元素非金属元素稀有气体元素最外层电子数
一般少于4个最外层电子数
一般多于4个最外层电子数
以达到最多(2
个或8个)说明: 1. 化学反应的实质是原子的重新组 合,在组合过程中,元素的原子总是力求使自身的结构趋于或达到稳定结构。 2.稳定结构是指类似于稀有气体元素原子的最外层电子数达到最多(2个或8个)的结构。思考: 稀有气体元素的原子已经达到了稳定结构,金属元素的原子和非金属元素的原子怎样才能达到稳定结构呢?得失电子稀有气体元素原子电子层排布元素的原子最外层电数与元素性质的关系 课堂练习一(1) 1.原子核外电子是按电子的__________、________排布的。 2.稀有气体元素的原子最外电子层一般有_______电子,(氦有______个电子)化学性质比较________,一般情况下不跟其它物质____________。
3.某元素的原子核内有17个质子,核外共有_________个电子,最外层有_______个电子,在化学反应中易_____个电子。 课堂练习一(2) 4.金属元素在化学反应中 ( ) A.易得电子 B.易失电子 C.易导电 D.不易得失电子 5.钠原子失去一个电子后发生变化的是 ( ) A.电子层数 B.原子量 C.质子数 D.中子数 6.与元素的化学性质关系最密切的是 ( ) A.中子数 B.电子数 C.最外层电子数 D.核外电子层数 讨论完成下表:少于4易失电子不稳定较活泼多于4不稳定易得电子较活泼2或8稳定不易得失较稳定三类不同元素的原子结构特点与化学性质的关系结论:元素的化学性质与最外层电子数关系密切最外层电子数决定化学性质练习:1.复述本课所学重点内容
2.完成课后习题
3.从核电荷数、质子数、中子数、核外电子(数)、最外层电子数中选折填充:
(1)决定元素种类的是 ;
(2)与元素化学性质十分密切的是 ;
(3)不带电的微粒是 ;
(4)决定原子质量的是 和 ;
(5)一定相等的是 和 。核电荷数或质子数最外层电子数中子质子数中子数核电荷数质子数练习 X、Y、Z 三种元素,其核电荷数均小于20,
X原子最外层电子数是次外层电子数的 2 倍,Y原子的次外层电子数是最外层电子数的 2 倍,Z原子的次外层电子数是最外层电子数的 4 倍,
则三种元素分别是:END
电子的质量:9.10×10-31kg
2.对比速度
如炮弹2km/s; 人造卫星7.8km/s; 宇宙飞船11km/s
氢原子核外电子:2.2×105km/s
3.对比运动范围
原子半径:n×10-10m
乒乓球半径:4×10-2m
电子运动视频1.什么叫原子?它的结构是怎样的?
2.原子为什么会呈电中性?思考:原子原子核质子中子核外电子核电荷数= =核外电子数核内质子数复习玻尔电子模型 核外电子是处在一定的轨道上饶核运行的。就太阳系的行星饶太阳运行一样;在核外运行的电子按能量的高低分层排步。问题:1.原子核外最
多有几层,各用什么
字母表示?
2.不同电子层上的
能量高低如何?小结:原子核外电子是分层排布的(1)“电子层”表示运动着的电子离核远近的不同*由进到远:第一 、二、三、四、五、六、七层 K 、 L、 M、 N、 O、 P、 Q*由进到远: 电子(层)的能量由低到高能量最低原理 在核外电子排布中,电子总是尽量最先占有能量最低的轨道
只有能量最低的轨道被占满后,电子才能依次占有能量较高的轨道,这就是所谓能量最低原理。 原子核外电子排布KLMNOPQ1234567低 → 高 近 → 远 核外电子排布规律1)核外电子总是尽先排布在能量最低的电子层里,然后再由里往外,依次排布在能量逐步升高的电子层里。 2)各电子层最多容纳的电子数目是2n2,即K层2个,L层8个,M层18个,N层32个。 最外层电子数目不超过8个(K层为最外层时不超过2个) 次外层电子数目不超过18个。2.原子结构示意图表示原子氧原子(O)氢原子(H)原子结构示意图的含义:镁原子(Mg )原子核质子数电子层该层上的电子数第一层 倒数第一层 最外层 次外层
试画出氧原子,磷原子,钠离子,氯离子,氖原子的结构示意图
核电荷数为1~18的元素的原子结构示意图金属元素非金属元素稀有气体元素最外层电子数
一般少于4个最外层电子数
一般多于4个最外层电子数
以达到最多(2
个或8个)说明: 1. 化学反应的实质是原子的重新组 合,在组合过程中,元素的原子总是力求使自身的结构趋于或达到稳定结构。 2.稳定结构是指类似于稀有气体元素原子的最外层电子数达到最多(2个或8个)的结构。思考: 稀有气体元素的原子已经达到了稳定结构,金属元素的原子和非金属元素的原子怎样才能达到稳定结构呢?得失电子稀有气体元素原子电子层排布元素的原子最外层电数与元素性质的关系 课堂练习一(1) 1.原子核外电子是按电子的__________、________排布的。 2.稀有气体元素的原子最外电子层一般有_______电子,(氦有______个电子)化学性质比较________,一般情况下不跟其它物质____________。
3.某元素的原子核内有17个质子,核外共有_________个电子,最外层有_______个电子,在化学反应中易_____个电子。 课堂练习一(2) 4.金属元素在化学反应中 ( ) A.易得电子 B.易失电子 C.易导电 D.不易得失电子 5.钠原子失去一个电子后发生变化的是 ( ) A.电子层数 B.原子量 C.质子数 D.中子数 6.与元素的化学性质关系最密切的是 ( ) A.中子数 B.电子数 C.最外层电子数 D.核外电子层数 讨论完成下表:少于4易失电子不稳定较活泼多于4不稳定易得电子较活泼2或8稳定不易得失较稳定三类不同元素的原子结构特点与化学性质的关系结论:元素的化学性质与最外层电子数关系密切最外层电子数决定化学性质练习:1.复述本课所学重点内容
2.完成课后习题
3.从核电荷数、质子数、中子数、核外电子(数)、最外层电子数中选折填充:
(1)决定元素种类的是 ;
(2)与元素化学性质十分密切的是 ;
(3)不带电的微粒是 ;
(4)决定原子质量的是 和 ;
(5)一定相等的是 和 。核电荷数或质子数最外层电子数中子质子数中子数核电荷数质子数练习 X、Y、Z 三种元素,其核电荷数均小于20,
X原子最外层电子数是次外层电子数的 2 倍,Y原子的次外层电子数是最外层电子数的 2 倍,Z原子的次外层电子数是最外层电子数的 4 倍,
则三种元素分别是:END
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
