碳和碳的化合物[下学期]
图片预览

文档简介
课题 第七单元 氢和碳
课时教学目标 1、掌握碳及的性质、用途2、掌握CO2的制取、性质、用途
课时教学重 难 点 二氧化碳的性质、制取和用途
教学媒体准 备 多媒体课件
时间 教 师 活 动 设计 学生活动
复习本点:2、碳的还原性:(1)还原金属氧化物: C + 2CuO===Cu + CO2 3C + 2Fe2O3===4Fe +3CO2(2)还原非金属氧化物: C + CO2 === 2CO C + H2O ===CO +H2例1、 为了增加汽车轮胎的耐磨性,常在制轮胎的橡胶中加入耐磨物质是( ) A、石墨粉 B、活性炭 C、木炭粉 D、炭黑 知识点复习回顾
课 时 授 课 计 划 授课日期 年 月日星期
时间 教 师 活 动 设 计 学生活动
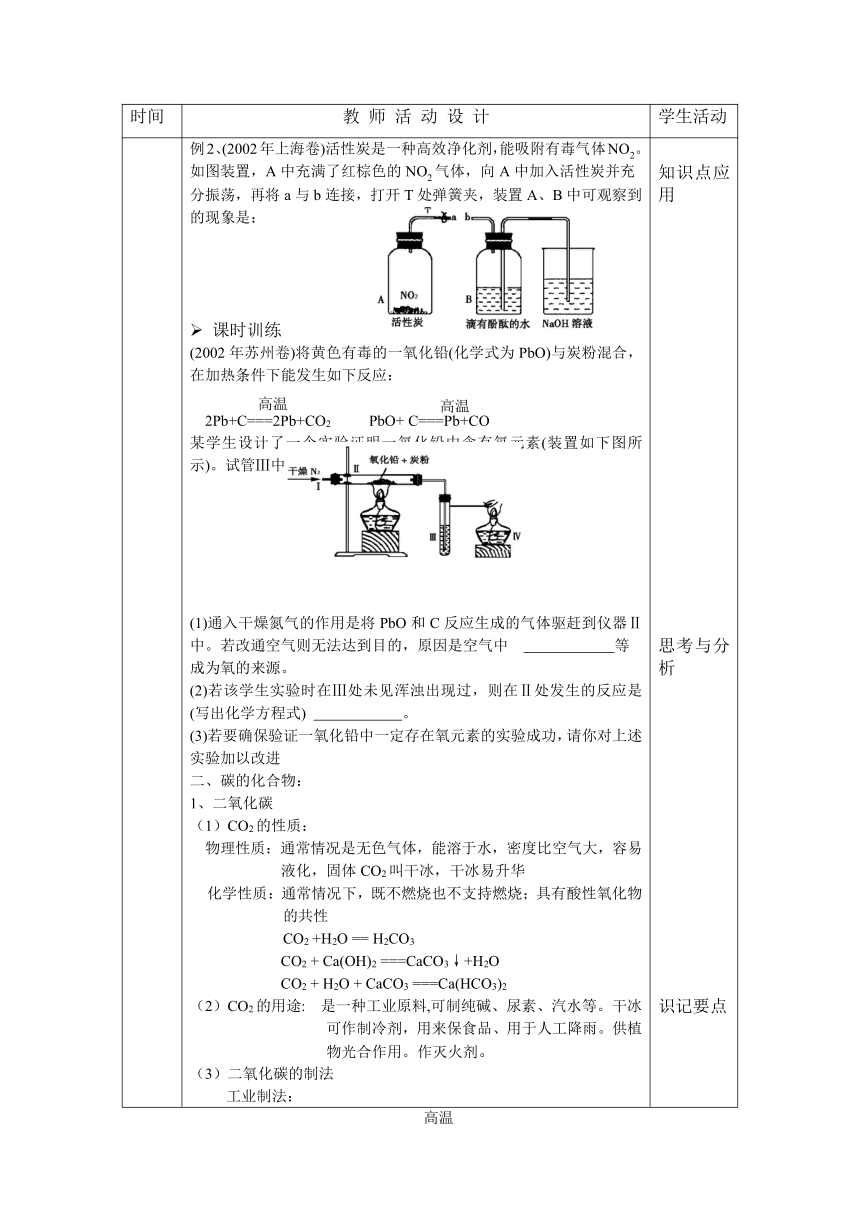
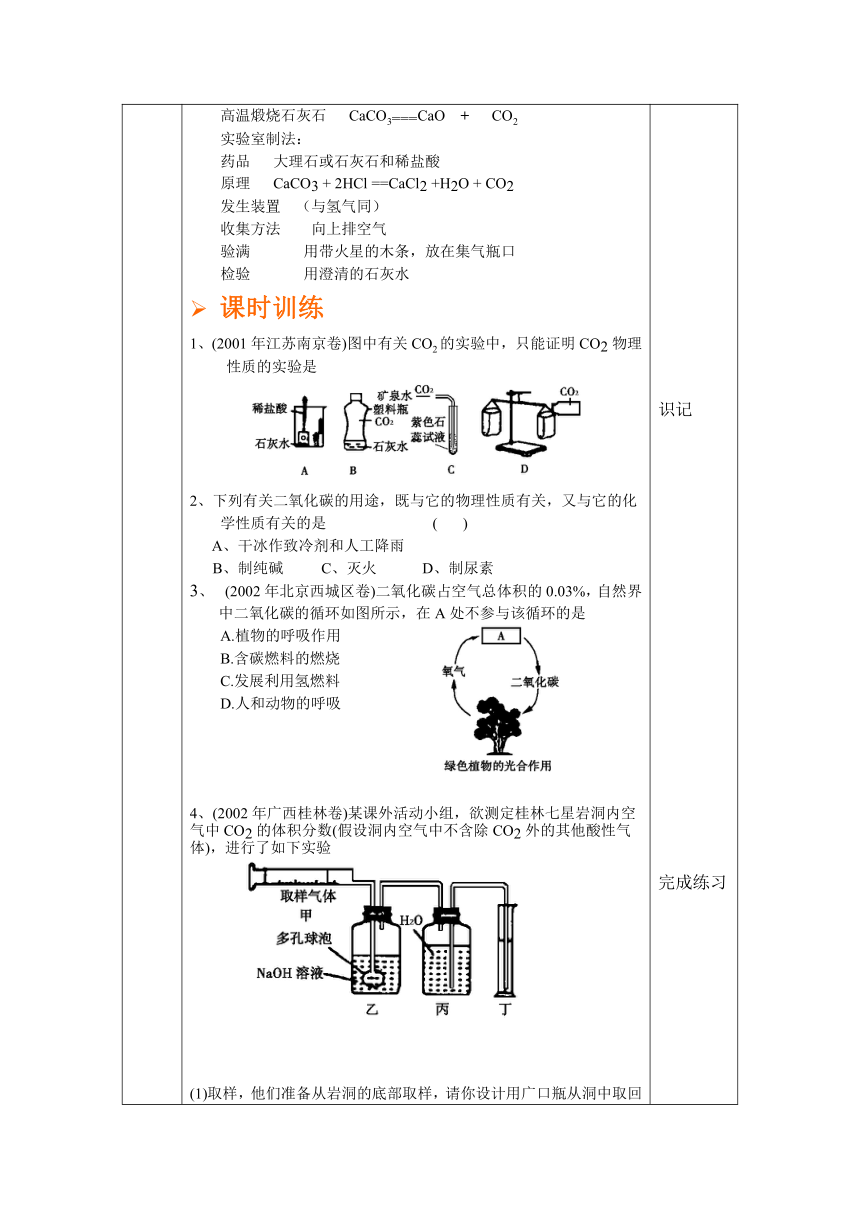
例2、(2002年上海卷)活性炭是一种高效净化剂,能吸附有毒气体NO2。如图装置,A中充满了红棕色的NO2气体,向A中加入活性炭并充分振荡,再将a与b连接,打开T处弹簧夹,装置A、B中可观察到的现象是: 课时训练(2002年苏州卷)将黄色有毒的一氧化铅(化学式为PbO)与炭粉混合,在加热条件下能发生如下反应:2Pb+C===2Pb+CO2 PbO+ C===Pb+CO某学生设计了一个实验证明一氧化铅中含有氧元素(装置如下图所示)。试管Ⅲ中盛放澄清石灰水(1)通入干燥氮气的作用是将PbO和C反应生成的气体驱赶到仪器Ⅱ中。若改通空气则无法达到目的,原因是空气中 等成为氧的来源。(2)若该学生实验时在Ⅲ处未见浑浊出现过,则在Ⅱ处发生的反应是(写出化学方程式) 。(3)若要确保验证一氧化铅中一定存在氧元素的实验成功,请你对上述实验加以改进二、碳的化合物:1、二氧化碳(1)CO2的性质: 物理性质:通常情况是无色气体,能溶于水,密度比空气大,容易液化,固体CO2叫干冰,干冰易升华化学性质:通常情况下,既不燃烧也不支持燃烧;具有酸性氧化物的共性 CO2 +H2O == H2CO3 CO2 + Ca(OH)2 ===CaCO3↓+H2O CO2 + H2O + CaCO3 ===Ca(HCO3)2(2)CO2的用途: 是一种工业原料,可制纯碱、尿素、汽水等。干冰可作制冷剂,用来保食品、用于人工降雨。供植物光合作用。作灭火剂。(3)二氧化碳的制法工业制法:高温煅烧石灰石 CaCO3===CaO + CO2 实验室制法: 药品 大理石或石灰石和稀盐酸原理 CaCO3 + 2HCl ==CaCl2 +H2O + CO2发生装置 (与氢气同) 收集方法 向上排空气验满 用带火星的木条,放在集气瓶口检验 用澄清的石灰水 课时训练1、(2001年江苏南京卷)图中有关CO2的实验中,只能证明CO2物理性质的实验是2、下列有关二氧化碳的用途,既与它的物理性质有关,又与它的化学性质有关的是 ( ) A、干冰作致冷剂和人工降雨 B、制纯碱 C、灭火 D、制尿素3、 (2002年北京西城区卷)二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环的是 A.植物的呼吸作用 B.含碳燃料的燃烧C.发展利用氢燃料 D.人和动物的呼吸4、(2002年广西桂林卷)某课外活动小组,欲测定桂林七星岩洞内空气中CO2的体积分数(假设洞内空气中不含除CO2外的其他酸性气体),进行了如下实验(1)取样,他们准备从岩洞的底部取样,请你设计用广口瓶从洞中取回一瓶空气样品的方法:(2)测定,用150 mL的注射器从广口瓶抽取100 mL气样,按图所示的装置进行实验。问:①乙装置中NaOH溶液的作用是 ②实验结束后,量筒内水的体积为99 mL,此数据的体积数是(用序号填写):A、CO2; B、N2和O2的混合气体;C、空气中除CO2外的所有气体;(3)计算洞底空气中CO2的体积分数为;(4)为营造更好的旅游环境,降低洞内CO2的含量,你认为应采取的措施有。5.(2002年安徽卷)“南极的冰化了”,这是中央电视台2002年5月22日“东方时空”中的一个节目标题,说的是南极一块叫“拉伸B”的冰架发生坍塌,其撕裂的面积比上海市还大。这是大自然又一次发生的警告:地球正在变暖!温室效应的影响已经不容忽视。(1)造成温室效应的主要原因是 . (2)为了减缓温室效应,我们每个人都可以从自己身边做起,比如说使用双面纸张。双面使用纸张和减缓温室效应的关系是 .(3)请再举出一件你可以做到的有利于减缓温室效应的事情 知识点应用思考与分析识记要点识记完成练习完成练习
教后录
课 时 授 课 计 划 授课日期 年 月日星期
课题 第七单元 氢和碳
课时教学目标 1、掌握CO的性质、用途2、能对三种还原剂C、H2、CO进行比较3、掌握碳酸盐(CaCO3)的性质、鉴定4、了解碳的有机物
课时教学重 难 点 CO的性质,三种还原剂比较
教学媒体准 备 多媒体课件
时间 教 师 活 动 设计 学生活动
复习要点:2、一氧化碳(1)一氧化碳的性质物理性质:通常情况下无色、无味的气体,密度比空气略小,难溶于水。化学性质:可燃性 2CO + O2====2CO2 还原性 CO +CuO===Cu +CO2 yCO + FexOy ===xFe +yCO2毒 性 CO有剧毒 (2)一氧化碳对空气的污染 目前全世界人为排放出的CO总量每年约为几亿吨。其中,一半以上来自汽车排放的废气,其余主要来自煤等燃料的燃烧和石油炼制、钢铁冶炼等。森林火灾、生物的腐烂等过程也产生一氧化碳。三种还原剂——C、H2、CO比较1)、物质类别: C、H2 是非金属单质,CO是化合物 2)、物理性质木炭为黑色固体,不溶于水H2、CO都是无色、无味的气体,难溶于水,CO的密度比空气略小,H2是最轻的气体3)、化学性质: C、H2、CO都可燃性、还原性。CO有剧毒4)、H2还原氧化铜的实验比较: 仪器装置 实验操作注意事项 实验现象反应速度3、碳酸钙的性质、石灰石的用途及碳酸盐的鉴定(1)、碳酸钙的物理性质: 纯净的碳酸钙是白色粉末,难溶于水。碳酸钙在自然界中主要以大理石、石灰石和白垩的形式存在。大理石是自然界中比较纯净的碳酸钙;石灰石是自然界中含杂质较多的碳酸钙;白垩产于海洋中,是比较纯净的碳酸钙。
时间 教师活动设计 学生活动
(2)、碳酸钙的化学性质碳酸钙与盐酸反应:碳酸钙在高温下分解碳酸钙和碳酸氢钙之间可以互相转化(3)、石灰石、大理石的用途:它们都是重要的建筑材料。天安门的华表、人民大会堂的不少柱子都是用大理石做的。石灰石也是建筑上常用的石料。工业上用石灰石制生石灰,同时得到副产品二氧化碳。把粉碎的石灰石和粘土按适当比率混合,再加强热,就制得水泥4、碳酸盐的鉴定试剂:稀盐酸和澄清石灰水原理:碳酸盐中都含有碳酸根,碳酸根遇到酸中的氢离子,会生成二氧化碳气体。即: 2H+ + CO32- == CO2 +H2O例如:CaCO3+2HCl = CaCl2+H2O+CO2↑ Na2CO3+2HCl = 2NaCl+H2O+CO2↑ 方法:取少量待测液于试管中,向其中滴加稀盐酸或稀硝酸,将生成的气体通入澄清石灰水中。现象:有大量气泡产生,澄清石灰水变浑浊5、碳的有机物(1)甲烷 CH4 俗称 沼气 甲烷是无色、无味的气体,密度比空气小,极难溶于水,可以燃烧 CH4 + 2O2 ===CO2 + 2H2O (2)乙醇 C2H5OH 俗称 酒精乙醇是无色透明、具有特殊气味的液体。易挥发,能与水以任意比互溶,能溶解多种有机化合物。有可燃性 C2H5OH + 3O2===2CO2 + 3H2O (3)甲醇 有毒,饮后会使人眼睛失明,饮用大量时会使人 死亡。因此,绝对禁止饮用工业酒精,也绝不允许用工业酒 精来配酒出售(4)乙酸 CH3COOH 俗称 醋酸醋酸是无色透明、具有酸味的液体。易挥发,16 ℃时变为冰样固体也称冰醋酸醋酸具有酸的通性:
教后录
高温
高温
高温
高温
高温
高温
高温
高温
点燃
点燃
点燃
课时教学目标 1、掌握碳及的性质、用途2、掌握CO2的制取、性质、用途
课时教学重 难 点 二氧化碳的性质、制取和用途
教学媒体准 备 多媒体课件
时间 教 师 活 动 设计 学生活动
复习本点:2、碳的还原性:(1)还原金属氧化物: C + 2CuO===Cu + CO2 3C + 2Fe2O3===4Fe +3CO2(2)还原非金属氧化物: C + CO2 === 2CO C + H2O ===CO +H2例1、 为了增加汽车轮胎的耐磨性,常在制轮胎的橡胶中加入耐磨物质是( ) A、石墨粉 B、活性炭 C、木炭粉 D、炭黑 知识点复习回顾
课 时 授 课 计 划 授课日期 年 月日星期
时间 教 师 活 动 设 计 学生活动
例2、(2002年上海卷)活性炭是一种高效净化剂,能吸附有毒气体NO2。如图装置,A中充满了红棕色的NO2气体,向A中加入活性炭并充分振荡,再将a与b连接,打开T处弹簧夹,装置A、B中可观察到的现象是: 课时训练(2002年苏州卷)将黄色有毒的一氧化铅(化学式为PbO)与炭粉混合,在加热条件下能发生如下反应:2Pb+C===2Pb+CO2 PbO+ C===Pb+CO某学生设计了一个实验证明一氧化铅中含有氧元素(装置如下图所示)。试管Ⅲ中盛放澄清石灰水(1)通入干燥氮气的作用是将PbO和C反应生成的气体驱赶到仪器Ⅱ中。若改通空气则无法达到目的,原因是空气中 等成为氧的来源。(2)若该学生实验时在Ⅲ处未见浑浊出现过,则在Ⅱ处发生的反应是(写出化学方程式) 。(3)若要确保验证一氧化铅中一定存在氧元素的实验成功,请你对上述实验加以改进二、碳的化合物:1、二氧化碳(1)CO2的性质: 物理性质:通常情况是无色气体,能溶于水,密度比空气大,容易液化,固体CO2叫干冰,干冰易升华化学性质:通常情况下,既不燃烧也不支持燃烧;具有酸性氧化物的共性 CO2 +H2O == H2CO3 CO2 + Ca(OH)2 ===CaCO3↓+H2O CO2 + H2O + CaCO3 ===Ca(HCO3)2(2)CO2的用途: 是一种工业原料,可制纯碱、尿素、汽水等。干冰可作制冷剂,用来保食品、用于人工降雨。供植物光合作用。作灭火剂。(3)二氧化碳的制法工业制法:高温煅烧石灰石 CaCO3===CaO + CO2 实验室制法: 药品 大理石或石灰石和稀盐酸原理 CaCO3 + 2HCl ==CaCl2 +H2O + CO2发生装置 (与氢气同) 收集方法 向上排空气验满 用带火星的木条,放在集气瓶口检验 用澄清的石灰水 课时训练1、(2001年江苏南京卷)图中有关CO2的实验中,只能证明CO2物理性质的实验是2、下列有关二氧化碳的用途,既与它的物理性质有关,又与它的化学性质有关的是 ( ) A、干冰作致冷剂和人工降雨 B、制纯碱 C、灭火 D、制尿素3、 (2002年北京西城区卷)二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环的是 A.植物的呼吸作用 B.含碳燃料的燃烧C.发展利用氢燃料 D.人和动物的呼吸4、(2002年广西桂林卷)某课外活动小组,欲测定桂林七星岩洞内空气中CO2的体积分数(假设洞内空气中不含除CO2外的其他酸性气体),进行了如下实验(1)取样,他们准备从岩洞的底部取样,请你设计用广口瓶从洞中取回一瓶空气样品的方法:(2)测定,用150 mL的注射器从广口瓶抽取100 mL气样,按图所示的装置进行实验。问:①乙装置中NaOH溶液的作用是 ②实验结束后,量筒内水的体积为99 mL,此数据的体积数是(用序号填写):A、CO2; B、N2和O2的混合气体;C、空气中除CO2外的所有气体;(3)计算洞底空气中CO2的体积分数为;(4)为营造更好的旅游环境,降低洞内CO2的含量,你认为应采取的措施有。5.(2002年安徽卷)“南极的冰化了”,这是中央电视台2002年5月22日“东方时空”中的一个节目标题,说的是南极一块叫“拉伸B”的冰架发生坍塌,其撕裂的面积比上海市还大。这是大自然又一次发生的警告:地球正在变暖!温室效应的影响已经不容忽视。(1)造成温室效应的主要原因是 . (2)为了减缓温室效应,我们每个人都可以从自己身边做起,比如说使用双面纸张。双面使用纸张和减缓温室效应的关系是 .(3)请再举出一件你可以做到的有利于减缓温室效应的事情 知识点应用思考与分析识记要点识记完成练习完成练习
教后录
课 时 授 课 计 划 授课日期 年 月日星期
课题 第七单元 氢和碳
课时教学目标 1、掌握CO的性质、用途2、能对三种还原剂C、H2、CO进行比较3、掌握碳酸盐(CaCO3)的性质、鉴定4、了解碳的有机物
课时教学重 难 点 CO的性质,三种还原剂比较
教学媒体准 备 多媒体课件
时间 教 师 活 动 设计 学生活动
复习要点:2、一氧化碳(1)一氧化碳的性质物理性质:通常情况下无色、无味的气体,密度比空气略小,难溶于水。化学性质:可燃性 2CO + O2====2CO2 还原性 CO +CuO===Cu +CO2 yCO + FexOy ===xFe +yCO2毒 性 CO有剧毒 (2)一氧化碳对空气的污染 目前全世界人为排放出的CO总量每年约为几亿吨。其中,一半以上来自汽车排放的废气,其余主要来自煤等燃料的燃烧和石油炼制、钢铁冶炼等。森林火灾、生物的腐烂等过程也产生一氧化碳。三种还原剂——C、H2、CO比较1)、物质类别: C、H2 是非金属单质,CO是化合物 2)、物理性质木炭为黑色固体,不溶于水H2、CO都是无色、无味的气体,难溶于水,CO的密度比空气略小,H2是最轻的气体3)、化学性质: C、H2、CO都可燃性、还原性。CO有剧毒4)、H2还原氧化铜的实验比较: 仪器装置 实验操作注意事项 实验现象反应速度3、碳酸钙的性质、石灰石的用途及碳酸盐的鉴定(1)、碳酸钙的物理性质: 纯净的碳酸钙是白色粉末,难溶于水。碳酸钙在自然界中主要以大理石、石灰石和白垩的形式存在。大理石是自然界中比较纯净的碳酸钙;石灰石是自然界中含杂质较多的碳酸钙;白垩产于海洋中,是比较纯净的碳酸钙。
时间 教师活动设计 学生活动
(2)、碳酸钙的化学性质碳酸钙与盐酸反应:碳酸钙在高温下分解碳酸钙和碳酸氢钙之间可以互相转化(3)、石灰石、大理石的用途:它们都是重要的建筑材料。天安门的华表、人民大会堂的不少柱子都是用大理石做的。石灰石也是建筑上常用的石料。工业上用石灰石制生石灰,同时得到副产品二氧化碳。把粉碎的石灰石和粘土按适当比率混合,再加强热,就制得水泥4、碳酸盐的鉴定试剂:稀盐酸和澄清石灰水原理:碳酸盐中都含有碳酸根,碳酸根遇到酸中的氢离子,会生成二氧化碳气体。即: 2H+ + CO32- == CO2 +H2O例如:CaCO3+2HCl = CaCl2+H2O+CO2↑ Na2CO3+2HCl = 2NaCl+H2O+CO2↑ 方法:取少量待测液于试管中,向其中滴加稀盐酸或稀硝酸,将生成的气体通入澄清石灰水中。现象:有大量气泡产生,澄清石灰水变浑浊5、碳的有机物(1)甲烷 CH4 俗称 沼气 甲烷是无色、无味的气体,密度比空气小,极难溶于水,可以燃烧 CH4 + 2O2 ===CO2 + 2H2O (2)乙醇 C2H5OH 俗称 酒精乙醇是无色透明、具有特殊气味的液体。易挥发,能与水以任意比互溶,能溶解多种有机化合物。有可燃性 C2H5OH + 3O2===2CO2 + 3H2O (3)甲醇 有毒,饮后会使人眼睛失明,饮用大量时会使人 死亡。因此,绝对禁止饮用工业酒精,也绝不允许用工业酒 精来配酒出售(4)乙酸 CH3COOH 俗称 醋酸醋酸是无色透明、具有酸味的液体。易挥发,16 ℃时变为冰样固体也称冰醋酸醋酸具有酸的通性:
教后录
高温
高温
高温
高温
高温
高温
高温
高温
点燃
点燃
点燃
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
