第3节 化学反应与质量守恒
图片预览



文档简介
登陆21世纪教育 助您教考全无忧
第3节 化学反应与质量守恒
联想情景导入
在生产、生活科研中,人们接触和研究了许多化学反应。不同的化学反应中伴随的现象往往不同,需要的条件也不相同。如点燃木炭后木炭能够持续燃烧;而水只有在持续通电的情况下才能不断分解;过氧化氢需要在二氧化锰或其他物质作催化剂的时候才能不断放出氧气。你知道这是为什么吗 那么就让我们一起来了解一下不同的化学反应类型吧!
过氧化氢在二氧化锰的催化作用下可以发生反应生成水和氧气。对于这一化学反应,我们可用“过氧化氢======水+氧气”表示,也可以用“2H2O======2H2+O2↑表示。认真观察这两个化学反应的式子后,你有什么发现呢 你认为哪一个式子能更正确地表示化学反应的变化过程呢 哪一个式子能准确地表示物质在发生化学变化的过程中所遵循的质量关系呢 我想你一定会认为是第二个式子吧 因为它是一种通用的科学语言——化学方程式。
重点知识详解
一、化合反应与分解反应
由两种或两种以上的物质生成一种物质的反应叫做化合反应。由一种物质生成两种或两种以上物质的反应叫做分解反应。
二、利用分解反廊制氧气
1.买验原理:
(1)分解过氧化氢(双氧水)(H2O2)制取氧气。
2H2O2====== 2H2O + O2 ↑
(2)加热分解高锰酸钾制取氧气。
2KMnO4 ( http: / / www.21cnjy.com )K2MnO4+MnO2+O2↑
(3)加热分解氯酸钾制取氧气。
2KClO3======2KCl + 3O2↑
(4)催化剂:在氯酸钾和过氧化氢加热分解反应中,二氧化锰只起到改变反应速度的作用,本身的质量和化学性质在反应前后都没有改变。这种物质叫做催化剂。
2.实验装置:
加热氯酸钾制取氧气 分解过氧化氢制取氧气
说明:如果加热高锰酸钾制取氧气,要在试管口加入一团棉花,以免加热时产生的高锰酸钾粉末进入集气瓶。
3.实验步骤:
(1)连接装置仪器。
(2)检查装置的气密性。
(3)把药品平铺或斜铺在试管的底部,塞紧带导管的塞子,将试管固定在铁架台上。
(4)将集气瓶装满水倒立在水槽里。
(5)给试管加热。
(6)当导管的气泡连续并均匀地放出时,开始收集。
(7)当集气瓶的一侧有气泡放出时,将盖有玻璃片的集气瓶移出水槽,并正放在桌子上。
(8)将导管移出水槽,再熄灭酒精灯。
4.验满方法。
(1)排水法:当集气瓶的一侧有气泡放出时,证明已收集满。
(2)向上排空气法:将带火星的木条放在集气瓶口,若木条复燃,证明已收集满。
三、质莹守恒定律
1.质量守恒定律:在化学反应中,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。
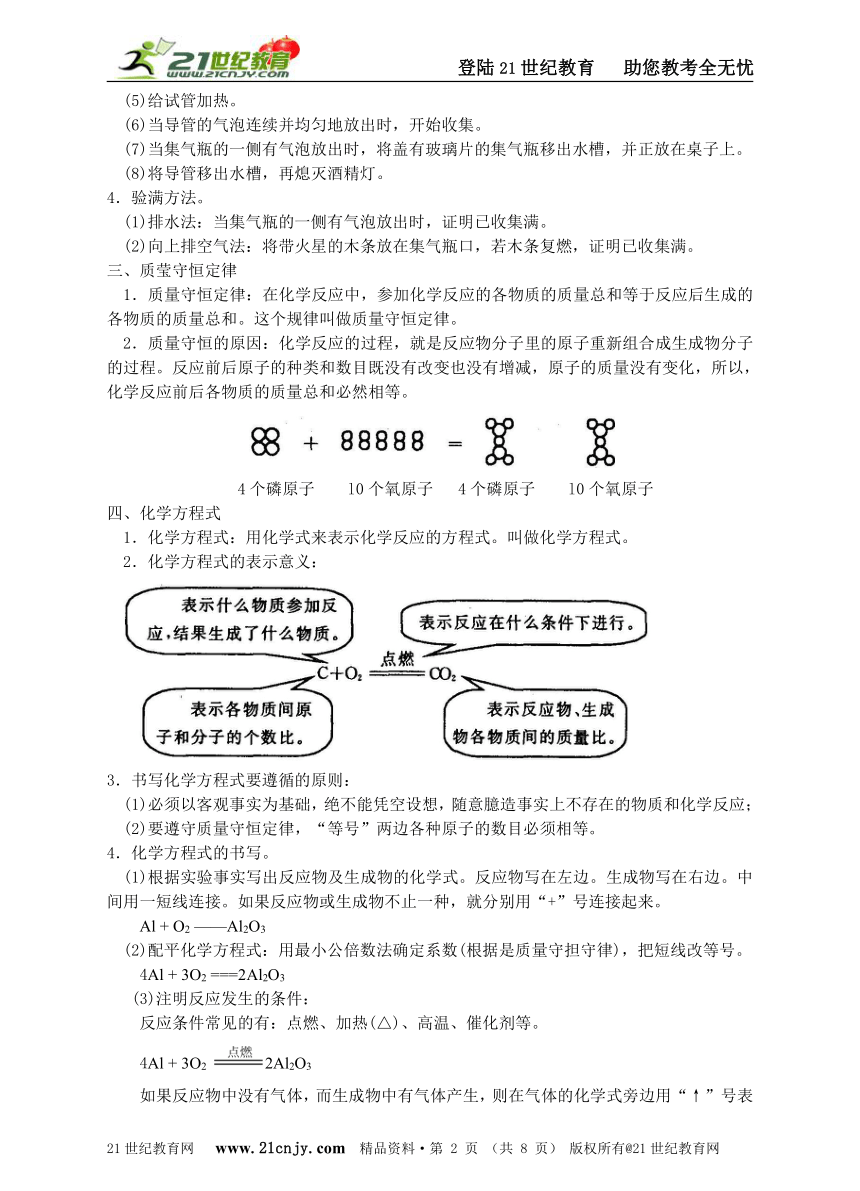
2.质量守恒的原因:化学反应的过程,就是反应物分子里的原子重新组合成生成物分子的过程。反应前后原子的种类和数目既没有改变也没有增减,原子的质量没有变化,所以,化学反应前后各物质的质量总和必然相等。
( http: / / www.21cnjy.com )
4个磷原子 l0个氧原子 4个磷原子 l0个氧原子
四、化学方程式
1.化学方程式:用化学式来表示化学反应的方程式。叫做化学方程式。
2.化学方程式的表示意义:
( http: / / www.21cnjy.com )
3.书写化学方程式要遵循的原则:
(1)必须以客观事实为基础,绝不能凭空设想,随意臆造事实上不存在的物质和化学反应;
(2)要遵守质量守恒定律,“等号”两边各种原子的数目必须相等。
4.化学方程式的书写。
(1)根据实验事实写出反应物及生成物的化学式。反应物写在左边。生成物写在右边。中间用一短线连接。如果反应物或生成物不止一种,就分别用“+”号连接起来。
Al + O2 ——Al2O3
(2)配平化学方程式:用最小公倍数法确定系数(根据是质量守担守律),把短线改等号。
4Al + 3O2 ===2Al2O3
(3)注明反应发生的条件:
反应条件常见的有:点燃、加热(△)、高温、催化剂等。
4Al + 3O2 ( http: / / www.21cnjy.com )2Al2O3
如果反应物中没有气体,而生成物中有气体产生,则在气体的化学式旁边用“↑”号表示;如果是溶液中发生的反应,反应物中无固体而生成物中有固体的,则在固体的化学式旁边用“↓”号表示。
2H2O ( http: / / www.21cnjy.com )2H2 ↑+ O2↑
CO2+Ca(OH)2===CaCO3↓+H2O
五、化学方程式与计算
根据化学方程式计算的一般步骤为:
1.设未知量;
2.写出化学方程式;
3.写出有关物质的相对分子质量和已知量;
4.列出比例式、求解;
s.写出简明答案。
例:实验室里用分解过氧化氢的方法制取氧气。现要制得2克氧气,需要多少克过氧化氢
解:设需要过氧化氢的质量为m。
2H2O2====== 2H2O + O2 ↑
68 32
m 2克
列比例式: HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 = HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 m = HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 =4.25克
答:需要过氧化氢4.25克。
精典例题解析
[例1]在一密闭的容器中有X、Y、Z、Q四种物质,在一定条件下充分反应,反应前后各物质的质量如下表:
物质 X Y Z Q
反应前质量(克) 10 10 10 10
反应后质量(克) 10 O 13 17
试判断该密闭容器中发生的反应属于 。
[解析]根据表中物质的数量变化可知,X质量不变,Y质量减少,Z、Q质量增加,而Y减少的质量刚好等于Z、Q增加的质量和,因此该密闭容器中的反应属于一种物质生成两种物质的反应,属于分解反应。
[答案]分解反应
[例2]一氧化氮是大气的主要污染物之一。近几年来又发现生物内存在少量一氧化氮,它有扩张血管、增强记忆的功能,成为当前生命科学研究的热点。工业上制取一氧化氮的化学方程式为:4X+5O2==4NO+6H2O,则X的化学式为 ( )
A.N2 B.NO2 C.NH3 D.N2O5
[解析]物质在发生化学变化前后,元素的种类不变,原子的个数不变,原子的质量也不变,根弱这一原则,不难判断出X物质的一个分子中应含有一个氮原子和三个氢原子。
[答案]C
[例3](1)在试管中加人5mL5%的过氧化氢溶液,把带火星的木条伸人试管,木条 复燃。
(2)在另一支试管中加入5mL5%的过氧化氢溶液,并加入少量二氧化锰,把带火星的木条伸入试管。现象是 。
(3)在上支试管不再产生气泡时,再加入过氧化氢溶液,现象是 。
[解析]二氧化锰在过氧化氢的分解反应过程中作为催化剂,能加快过氧化氢的分解反应速度而本身的质量和化学性质在化学反应前后不发生变化。在没有加入二氧化锰之前,过氧化氢分解反应速度较慢,产生微弱的氧气不足以使带火星的木条复燃。加入二氧化锰后,过氧化氢的分解反应速度加快,产生氧气使带火星的木条复燃。二氧化锰在化学反应前后质量和化学性质都不发生变化,因此,当过氧化氢完全反应后,剩余的二氧化锰仍然能对过氧化氢起催化作用。
[答案](1)不(2)迅速产生气泡,木条复燃 (3)又产生气泡,木条复燃
[例4]3克镁在氧气中充分燃烧,可以生成多少克氧化镁
[解答]设可生成氧化镁的质量为x
2Mg + O2 ( http: / / www.21cnjy.com )2MgO
48 80
3克 x
48 80
HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 = HYPERLINK " http://www.21cnjy.com" EMBED Equation.3
X= HYPERLINK " http://www.21cnjy.com" EMBED Equation.3
=5克
答:3克镁在氧气中充分燃烧可生成氧化镁5克。
考点应试必备
1.下列有关催化剂的叙述正确的是 ( )
A.在化学反应里能加快其他物质的化学反应速率,而本身的质量和性质在反应前后没有改变的物质
B.催化剂是二氧化锰
C.在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有改变的物质
D.要使过氧化氢溶液分解出氧气。必须要加入二氧化锰,否则就不能发生反应
2.实验室加热氯酸钾和二氧化锰的混合物制取氧气。下图中能正确表示出固体混合物中二氧化锰的质量分数随时问变化的是(二氧化锰的质量m,二氧化锰的质量分数R%。反应时间是t) ( )
( http: / / www.21cnjy.com )
3.证明集气瓶里的氧气是否已满的正确方法是 ( )
A.将带火星的木条伸到瓶底 B.将带火星的木条伸到瓶里
c.将带火星的木条插入瓶口 D.在瓶口点燃氧气
4.下列装置中(如图所示)不能用来收集氧气的是 ( )
( http: / / www.21cnjy.com )
5.对“质量守恒定律”的理解,正确的是 ( )
A.10克冰受热融化成10克水
B.参加反应的氢气和氧气的体积,等于生成的水的体积
C.反应物的质量等于生成物的质量
D.化学反应生成物的质量总和等于参加反应的各物质的质量总和
6.下列反应2AB+B2=2C中C的化学式是 ( )
A.AB2 B.A2B C.A2B4 D.A4B2
7.“神舟五号”的成功发射与回收,表明我国的载人航天技术已经有了突破性进展。在飞船的火箭推进器中常装有液态肼(用X表示)和液态双氧水(H2O2),它们混合时的反应方程式为:2H2O2+X==N2+4H2O,则肼(X)的化学式为 ( )
A.N2H6 B.N2H4 C.NH2 D.N2H4D2
8.在化学反应3H2+Fe2O3 ( http: / / www.21cnjy.com ) 2Fe+3H2O中,反应前后各物质的质量比为 ( )
A.1:1 B.3:1:2:3 C.3:80:56:27 D.1:80:28:9
9.在2A+B==C+D的反应中,7克A和8克B恰好反应生成9克D.那么同时生成C的质量是 ( )
A.6克 B.7克 C.8克 D.9克
10.实验室制取氧气大致可分为以下几个步骤:a将高锰酸钾装入试管,用带导管的橡皮塞塞紧试管口,并把它固定在铁架台上;b检查装置的气密性;c点燃酒精灯给试管加热;d用排水法收集氧气;e熄灭酒精灯;f将导气管从水中取出。正确的操作顺序是 ( )
A.bacdfe B.abcdef C.bacdef D.abcdfe
11.写出下列反应的化学方程式,指出反应类型(化合反应、分解反应、氧化反应)。
(1)水在通电情况下.产生氢气和氧气;
化学方程式: ;反应类型: 。
(2)铁丝与空气中的氧气反应生成红色的铁锈(Fe2O3);
化学方程式: ;反应类型: 。
(3)高锰酸钾(KMnO4)在加热条件下反应生成锰酸钾(K2MnO4、二氧化锰和氧气;
化学方程式: ;反应类型: 。
12.下图是某个化学反应前、后的微观模拟图。
请根据图示回答:
( http: / / www.21cnjy.com )
(1)该化学反应中 ( http: / / www.21cnjy.com )和 ( http: / / www.21cnjy.com )与参加反应的 ( http: / / www.21cnjy.com )各粒子间的个数比为 ;
(2)该反应的基本反应类型为 ;
(3)该反应中的生成物 (填“可能”或“不可能”)属于氧化物。
13.已知石蜡是蜡烛的主要成分,由于蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有 元素,可能含有 元素。
14.几种常见气体和空气的性质见下表,根据气体的性质回答:
气体 空 气 甲 烷 二氧化硫 二氧化碳 氢气 氨气
0℃,一标准大气压时的密度(克/升) 1.29 0.72 2.86 1.98 0.09 0.77
20℃,一标准 大气压时,在 1体积水中溶解气体的体积 / 0.038 40 0.83 0.018 680
( http: / / www.21cnjy.com )
(1)收集甲烷可使用的装置 。
(2)收集二氧化硫可使用的装置 。
(3)收集氢气可使用的装置 。
(4)只能用C装置收集的气体 。
、15.下列反应属于化合反应的是 属于分解反应是 。
(1)氢气+氧气 水
(2)蜡烛+氧气 二氧化碳+水
(3)水 氢气+氧气
(4)二氧化碳+水+氢氧化钙 碳酸氢钙
(5)碳酸氢铵 氨气+水蒸气+二氧化碳
(6)二氧化碳+氢氧化钙 碳酸钙+水
16.自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
(○表示氧原子;●表示氢原子; ( http: / / www.21cnjy.com )表示氯原子)
( http: / / www.21cnjy.com )
(1)图乙所示反应的基本反应类型为 反应;
(2)D物质中氯元素的化合价为 ;
(3)写出图甲所示反应的化学方程式 。
17.工业上用电解氯化镁方法生产金属镁:MgCl2 ( http: / / www.21cnjy.com )Mg+Cl2↑。现电解950千克氯化镁最多能生产多少千克单质镁 同时能得到多少千克氯气
参考答案:
第3节 化学反应与质量守恒
1.C 2.A 3.C 4.D 5.D 6.A 7.B 8.C 9.A 10.A
11.化学方程式略 分解反应 化学方程式略 氧化反应 化学方程式略 分解反应 12.(1)2:1:2 (2)化合反应 (3)可能
13.C、H O
14.(1)AC (2)B (3)AC (4)氨气
15.(1)(4) (3)(5)
16.(1)分解 (2)+1价 (3) H2O+Cl2==HCl + HClO
17. 240千克 710千克
二氧化锰
二氧化锰
二氧化锰
二氧化锰
加热
Mn02
点燃
点燃
通电
加热
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网 www.21cnjy.com 精品资料·第 1 页 (共 8 页) 版权所有@21世纪教育网
第3节 化学反应与质量守恒
联想情景导入
在生产、生活科研中,人们接触和研究了许多化学反应。不同的化学反应中伴随的现象往往不同,需要的条件也不相同。如点燃木炭后木炭能够持续燃烧;而水只有在持续通电的情况下才能不断分解;过氧化氢需要在二氧化锰或其他物质作催化剂的时候才能不断放出氧气。你知道这是为什么吗 那么就让我们一起来了解一下不同的化学反应类型吧!
过氧化氢在二氧化锰的催化作用下可以发生反应生成水和氧气。对于这一化学反应,我们可用“过氧化氢======水+氧气”表示,也可以用“2H2O======2H2+O2↑表示。认真观察这两个化学反应的式子后,你有什么发现呢 你认为哪一个式子能更正确地表示化学反应的变化过程呢 哪一个式子能准确地表示物质在发生化学变化的过程中所遵循的质量关系呢 我想你一定会认为是第二个式子吧 因为它是一种通用的科学语言——化学方程式。
重点知识详解
一、化合反应与分解反应
由两种或两种以上的物质生成一种物质的反应叫做化合反应。由一种物质生成两种或两种以上物质的反应叫做分解反应。
二、利用分解反廊制氧气
1.买验原理:
(1)分解过氧化氢(双氧水)(H2O2)制取氧气。
2H2O2====== 2H2O + O2 ↑
(2)加热分解高锰酸钾制取氧气。
2KMnO4 ( http: / / www.21cnjy.com )K2MnO4+MnO2+O2↑
(3)加热分解氯酸钾制取氧气。
2KClO3======2KCl + 3O2↑
(4)催化剂:在氯酸钾和过氧化氢加热分解反应中,二氧化锰只起到改变反应速度的作用,本身的质量和化学性质在反应前后都没有改变。这种物质叫做催化剂。
2.实验装置:
加热氯酸钾制取氧气 分解过氧化氢制取氧气
说明:如果加热高锰酸钾制取氧气,要在试管口加入一团棉花,以免加热时产生的高锰酸钾粉末进入集气瓶。
3.实验步骤:
(1)连接装置仪器。
(2)检查装置的气密性。
(3)把药品平铺或斜铺在试管的底部,塞紧带导管的塞子,将试管固定在铁架台上。
(4)将集气瓶装满水倒立在水槽里。
(5)给试管加热。
(6)当导管的气泡连续并均匀地放出时,开始收集。
(7)当集气瓶的一侧有气泡放出时,将盖有玻璃片的集气瓶移出水槽,并正放在桌子上。
(8)将导管移出水槽,再熄灭酒精灯。
4.验满方法。
(1)排水法:当集气瓶的一侧有气泡放出时,证明已收集满。
(2)向上排空气法:将带火星的木条放在集气瓶口,若木条复燃,证明已收集满。
三、质莹守恒定律
1.质量守恒定律:在化学反应中,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。
2.质量守恒的原因:化学反应的过程,就是反应物分子里的原子重新组合成生成物分子的过程。反应前后原子的种类和数目既没有改变也没有增减,原子的质量没有变化,所以,化学反应前后各物质的质量总和必然相等。
( http: / / www.21cnjy.com )
4个磷原子 l0个氧原子 4个磷原子 l0个氧原子
四、化学方程式
1.化学方程式:用化学式来表示化学反应的方程式。叫做化学方程式。
2.化学方程式的表示意义:
( http: / / www.21cnjy.com )
3.书写化学方程式要遵循的原则:
(1)必须以客观事实为基础,绝不能凭空设想,随意臆造事实上不存在的物质和化学反应;
(2)要遵守质量守恒定律,“等号”两边各种原子的数目必须相等。
4.化学方程式的书写。
(1)根据实验事实写出反应物及生成物的化学式。反应物写在左边。生成物写在右边。中间用一短线连接。如果反应物或生成物不止一种,就分别用“+”号连接起来。
Al + O2 ——Al2O3
(2)配平化学方程式:用最小公倍数法确定系数(根据是质量守担守律),把短线改等号。
4Al + 3O2 ===2Al2O3
(3)注明反应发生的条件:
反应条件常见的有:点燃、加热(△)、高温、催化剂等。
4Al + 3O2 ( http: / / www.21cnjy.com )2Al2O3
如果反应物中没有气体,而生成物中有气体产生,则在气体的化学式旁边用“↑”号表示;如果是溶液中发生的反应,反应物中无固体而生成物中有固体的,则在固体的化学式旁边用“↓”号表示。
2H2O ( http: / / www.21cnjy.com )2H2 ↑+ O2↑
CO2+Ca(OH)2===CaCO3↓+H2O
五、化学方程式与计算
根据化学方程式计算的一般步骤为:
1.设未知量;
2.写出化学方程式;
3.写出有关物质的相对分子质量和已知量;
4.列出比例式、求解;
s.写出简明答案。
例:实验室里用分解过氧化氢的方法制取氧气。现要制得2克氧气,需要多少克过氧化氢
解:设需要过氧化氢的质量为m。
2H2O2====== 2H2O + O2 ↑
68 32
m 2克
列比例式: HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 = HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 m = HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 =4.25克
答:需要过氧化氢4.25克。
精典例题解析
[例1]在一密闭的容器中有X、Y、Z、Q四种物质,在一定条件下充分反应,反应前后各物质的质量如下表:
物质 X Y Z Q
反应前质量(克) 10 10 10 10
反应后质量(克) 10 O 13 17
试判断该密闭容器中发生的反应属于 。
[解析]根据表中物质的数量变化可知,X质量不变,Y质量减少,Z、Q质量增加,而Y减少的质量刚好等于Z、Q增加的质量和,因此该密闭容器中的反应属于一种物质生成两种物质的反应,属于分解反应。
[答案]分解反应
[例2]一氧化氮是大气的主要污染物之一。近几年来又发现生物内存在少量一氧化氮,它有扩张血管、增强记忆的功能,成为当前生命科学研究的热点。工业上制取一氧化氮的化学方程式为:4X+5O2==4NO+6H2O,则X的化学式为 ( )
A.N2 B.NO2 C.NH3 D.N2O5
[解析]物质在发生化学变化前后,元素的种类不变,原子的个数不变,原子的质量也不变,根弱这一原则,不难判断出X物质的一个分子中应含有一个氮原子和三个氢原子。
[答案]C
[例3](1)在试管中加人5mL5%的过氧化氢溶液,把带火星的木条伸人试管,木条 复燃。
(2)在另一支试管中加入5mL5%的过氧化氢溶液,并加入少量二氧化锰,把带火星的木条伸入试管。现象是 。
(3)在上支试管不再产生气泡时,再加入过氧化氢溶液,现象是 。
[解析]二氧化锰在过氧化氢的分解反应过程中作为催化剂,能加快过氧化氢的分解反应速度而本身的质量和化学性质在化学反应前后不发生变化。在没有加入二氧化锰之前,过氧化氢分解反应速度较慢,产生微弱的氧气不足以使带火星的木条复燃。加入二氧化锰后,过氧化氢的分解反应速度加快,产生氧气使带火星的木条复燃。二氧化锰在化学反应前后质量和化学性质都不发生变化,因此,当过氧化氢完全反应后,剩余的二氧化锰仍然能对过氧化氢起催化作用。
[答案](1)不(2)迅速产生气泡,木条复燃 (3)又产生气泡,木条复燃
[例4]3克镁在氧气中充分燃烧,可以生成多少克氧化镁
[解答]设可生成氧化镁的质量为x
2Mg + O2 ( http: / / www.21cnjy.com )2MgO
48 80
3克 x
48 80
HYPERLINK " http://www.21cnjy.com" EMBED Equation.3 = HYPERLINK " http://www.21cnjy.com" EMBED Equation.3
X= HYPERLINK " http://www.21cnjy.com" EMBED Equation.3
=5克
答:3克镁在氧气中充分燃烧可生成氧化镁5克。
考点应试必备
1.下列有关催化剂的叙述正确的是 ( )
A.在化学反应里能加快其他物质的化学反应速率,而本身的质量和性质在反应前后没有改变的物质
B.催化剂是二氧化锰
C.在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有改变的物质
D.要使过氧化氢溶液分解出氧气。必须要加入二氧化锰,否则就不能发生反应
2.实验室加热氯酸钾和二氧化锰的混合物制取氧气。下图中能正确表示出固体混合物中二氧化锰的质量分数随时问变化的是(二氧化锰的质量m,二氧化锰的质量分数R%。反应时间是t) ( )
( http: / / www.21cnjy.com )
3.证明集气瓶里的氧气是否已满的正确方法是 ( )
A.将带火星的木条伸到瓶底 B.将带火星的木条伸到瓶里
c.将带火星的木条插入瓶口 D.在瓶口点燃氧气
4.下列装置中(如图所示)不能用来收集氧气的是 ( )
( http: / / www.21cnjy.com )
5.对“质量守恒定律”的理解,正确的是 ( )
A.10克冰受热融化成10克水
B.参加反应的氢气和氧气的体积,等于生成的水的体积
C.反应物的质量等于生成物的质量
D.化学反应生成物的质量总和等于参加反应的各物质的质量总和
6.下列反应2AB+B2=2C中C的化学式是 ( )
A.AB2 B.A2B C.A2B4 D.A4B2
7.“神舟五号”的成功发射与回收,表明我国的载人航天技术已经有了突破性进展。在飞船的火箭推进器中常装有液态肼(用X表示)和液态双氧水(H2O2),它们混合时的反应方程式为:2H2O2+X==N2+4H2O,则肼(X)的化学式为 ( )
A.N2H6 B.N2H4 C.NH2 D.N2H4D2
8.在化学反应3H2+Fe2O3 ( http: / / www.21cnjy.com ) 2Fe+3H2O中,反应前后各物质的质量比为 ( )
A.1:1 B.3:1:2:3 C.3:80:56:27 D.1:80:28:9
9.在2A+B==C+D的反应中,7克A和8克B恰好反应生成9克D.那么同时生成C的质量是 ( )
A.6克 B.7克 C.8克 D.9克
10.实验室制取氧气大致可分为以下几个步骤:a将高锰酸钾装入试管,用带导管的橡皮塞塞紧试管口,并把它固定在铁架台上;b检查装置的气密性;c点燃酒精灯给试管加热;d用排水法收集氧气;e熄灭酒精灯;f将导气管从水中取出。正确的操作顺序是 ( )
A.bacdfe B.abcdef C.bacdef D.abcdfe
11.写出下列反应的化学方程式,指出反应类型(化合反应、分解反应、氧化反应)。
(1)水在通电情况下.产生氢气和氧气;
化学方程式: ;反应类型: 。
(2)铁丝与空气中的氧气反应生成红色的铁锈(Fe2O3);
化学方程式: ;反应类型: 。
(3)高锰酸钾(KMnO4)在加热条件下反应生成锰酸钾(K2MnO4、二氧化锰和氧气;
化学方程式: ;反应类型: 。
12.下图是某个化学反应前、后的微观模拟图。
请根据图示回答:
( http: / / www.21cnjy.com )
(1)该化学反应中 ( http: / / www.21cnjy.com )和 ( http: / / www.21cnjy.com )与参加反应的 ( http: / / www.21cnjy.com )各粒子间的个数比为 ;
(2)该反应的基本反应类型为 ;
(3)该反应中的生成物 (填“可能”或“不可能”)属于氧化物。
13.已知石蜡是蜡烛的主要成分,由于蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有 元素,可能含有 元素。
14.几种常见气体和空气的性质见下表,根据气体的性质回答:
气体 空 气 甲 烷 二氧化硫 二氧化碳 氢气 氨气
0℃,一标准大气压时的密度(克/升) 1.29 0.72 2.86 1.98 0.09 0.77
20℃,一标准 大气压时,在 1体积水中溶解气体的体积 / 0.038 40 0.83 0.018 680
( http: / / www.21cnjy.com )
(1)收集甲烷可使用的装置 。
(2)收集二氧化硫可使用的装置 。
(3)收集氢气可使用的装置 。
(4)只能用C装置收集的气体 。
、15.下列反应属于化合反应的是 属于分解反应是 。
(1)氢气+氧气 水
(2)蜡烛+氧气 二氧化碳+水
(3)水 氢气+氧气
(4)二氧化碳+水+氢氧化钙 碳酸氢钙
(5)碳酸氢铵 氨气+水蒸气+二氧化碳
(6)二氧化碳+氢氧化钙 碳酸钙+水
16.自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
(○表示氧原子;●表示氢原子; ( http: / / www.21cnjy.com )表示氯原子)
( http: / / www.21cnjy.com )
(1)图乙所示反应的基本反应类型为 反应;
(2)D物质中氯元素的化合价为 ;
(3)写出图甲所示反应的化学方程式 。
17.工业上用电解氯化镁方法生产金属镁:MgCl2 ( http: / / www.21cnjy.com )Mg+Cl2↑。现电解950千克氯化镁最多能生产多少千克单质镁 同时能得到多少千克氯气
参考答案:
第3节 化学反应与质量守恒
1.C 2.A 3.C 4.D 5.D 6.A 7.B 8.C 9.A 10.A
11.化学方程式略 分解反应 化学方程式略 氧化反应 化学方程式略 分解反应 12.(1)2:1:2 (2)化合反应 (3)可能
13.C、H O
14.(1)AC (2)B (3)AC (4)氨气
15.(1)(4) (3)(5)
16.(1)分解 (2)+1价 (3) H2O+Cl2==HCl + HClO
17. 240千克 710千克
二氧化锰
二氧化锰
二氧化锰
二氧化锰
加热
Mn02
点燃
点燃
通电
加热
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网 www.21cnjy.com 精品资料·第 1 页 (共 8 页) 版权所有@21世纪教育网
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
