基础实验5 配制一定溶质质量分数的氯化钠溶液(15张PPT)
文档属性
| 名称 | 基础实验5 配制一定溶质质量分数的氯化钠溶液(15张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-28 00:00:00 | ||
图片预览






文档简介
课件15张PPT。 实验活动5
一定溶质质量分数的氯化钠溶液的配制
知道浓溶液和稀溶液间的转化。234掌握称量、量取、溶解等基本实验操作。1、溶质质量分数=
溶质质量=
溶液质量=
2、浓溶液加水稀释:
(1)浓溶液中溶质的质量 稀溶液中溶质的质量
(选择“< 、>或 =”)
(2)所用水的质量=
(3)溶液的体积=【课前检测】溶液质量×溶质质量分数溶质质量+溶剂质量=稀溶液质量-浓溶液质量溶液的质量×溶液的密度 【课前检测】3、药品的取用
取用粉末状固体药品时,应将瓶塞 放在桌面上,再用 取用。
4、天平的使用
称量一定质量的固体药品时,
应先在托盘两边各放一张 ,
再 ,砝码放在 ,药品放在 ,
为使药品不过量的技巧是
(5g以上用砝码)倒药匙干净的白纸调零右盘左盘,用手轻轻敲击拿药匙的手 【课前检测】5、量筒的使用
(1)量取液体时,量筒必须放平,视线必须与液体 保持平视。快接近刻度线时,改用 滴加液体。
(2)仰视或俯视读数时,读数与实际数值的关系:
仰视读数:实际量取的体积 读数体积(>、<、=)
俯视读数:实际量取的体积 读数体积(>、<、=)凹液面的最低处胶头滴管>< 【探究任务一】:固体加水配制溶液
计算34747称量托盘天平烧杯(3)_____:用______量取所需的水,倒入盛有氯化钠的烧杯中。
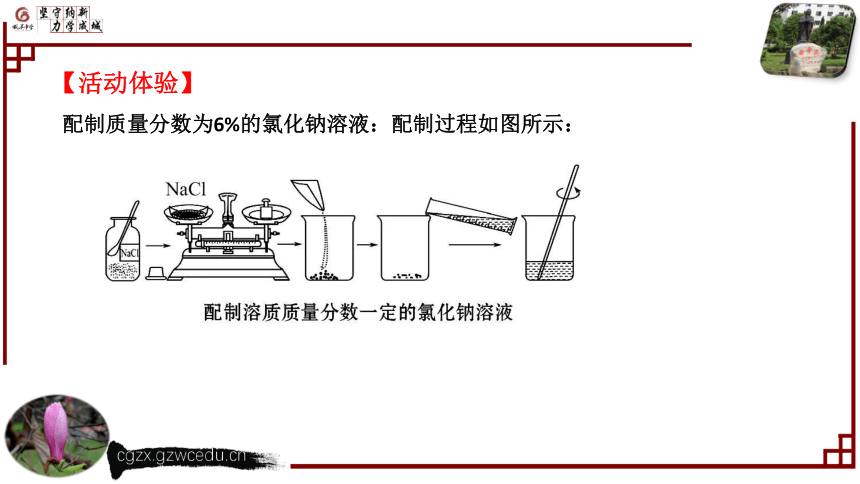
(4)_____:用________搅拌,使氯化钠溶解。 量取量筒溶解玻璃棒【活动体验】
配制质量分数为6%的氯化钠溶液:配制过程如图所示: 【探究任务二】:浓溶液加水配制稀溶液计算25242525量取量筒混匀 【探究任务三】:溶液的储存试剂瓶标签药品名称溶液中溶质的质量分数浓溶液加水稀释前后溶质质量不变。稀溶液的质量=浓溶液的质量+加水的质量(1)使用托盘天平时,要在桌上放平,游码拨到零处。
(2)左右两盘放等质量的纸。
(3)氯化钠放在左盘,砝码放在右盘。砝码用镊子夹,不能
用手拿,加砝码的顺序从大到小,最后移动游码。
(4)称量完毕,砝码放回砝码盒,将天平放回原处。答案答案【实验反思】视线要与凹液面最低处保持相平。实际生产中,许多时候必须使用溶质质量分数一定的溶液。如:农业上用16%的食盐溶液选种子。如太浓,优种会被选出,太稀劣质种子也将被选中。答案答案(1)天平未调零;(2)游码未归零;(3)称量前指针偏右;(4)称量时左盘垫有纸,右盘没垫纸;(5)称量时物质与砝码放反了,并使用了游码;(6)称量时天平指针略向左倾斜。(7)食盐中有杂质或食盐不干燥;(8)称量的食盐没完全转移到烧杯中;(9)用量筒量取水时,仰视水面刻度线来读取体积读数;(10)配制溶液的烧杯用蒸馏水润洗。答案(1)用食盐和水;
(2)用6%的食盐水加水稀释;
(3)用2%的食盐水加食盐;
(4)用6%和2%的食盐水;
(5)用2%的食盐水蒸发水分。答案 小结:
1.溶液配制的步骤:
计算. 称量. 溶解 . 转移
2.浓溶液与稀溶液的转化:
关键: 稀释前后溶质质量不变
即: m浓w浓=m稀w稀
溶质质量=
溶液质量=
2、浓溶液加水稀释:
(1)浓溶液中溶质的质量 稀溶液中溶质的质量
(选择“< 、>或 =”)
(2)所用水的质量=
(3)溶液的体积=【课前检测】溶液质量×溶质质量分数溶质质量+溶剂质量=稀溶液质量-浓溶液质量溶液的质量×溶液的密度 【课前检测】3、药品的取用
取用粉末状固体药品时,应将瓶塞 放在桌面上,再用 取用。
4、天平的使用
称量一定质量的固体药品时,
应先在托盘两边各放一张 ,
再 ,砝码放在 ,药品放在 ,
为使药品不过量的技巧是
(5g以上用砝码)倒药匙干净的白纸调零右盘左盘,用手轻轻敲击拿药匙的手 【课前检测】5、量筒的使用
(1)量取液体时,量筒必须放平,视线必须与液体 保持平视。快接近刻度线时,改用 滴加液体。
(2)仰视或俯视读数时,读数与实际数值的关系:
仰视读数:实际量取的体积 读数体积(>、<、=)
俯视读数:实际量取的体积 读数体积(>、<、=)凹液面的最低处胶头滴管>< 【探究任务一】:固体加水配制溶液
计算34747称量托盘天平烧杯(3)_____:用______量取所需的水,倒入盛有氯化钠的烧杯中。
(4)_____:用________搅拌,使氯化钠溶解。 量取量筒溶解玻璃棒【活动体验】
配制质量分数为6%的氯化钠溶液:配制过程如图所示: 【探究任务二】:浓溶液加水配制稀溶液计算25242525量取量筒混匀 【探究任务三】:溶液的储存试剂瓶标签药品名称溶液中溶质的质量分数浓溶液加水稀释前后溶质质量不变。稀溶液的质量=浓溶液的质量+加水的质量(1)使用托盘天平时,要在桌上放平,游码拨到零处。
(2)左右两盘放等质量的纸。
(3)氯化钠放在左盘,砝码放在右盘。砝码用镊子夹,不能
用手拿,加砝码的顺序从大到小,最后移动游码。
(4)称量完毕,砝码放回砝码盒,将天平放回原处。答案答案【实验反思】视线要与凹液面最低处保持相平。实际生产中,许多时候必须使用溶质质量分数一定的溶液。如:农业上用16%的食盐溶液选种子。如太浓,优种会被选出,太稀劣质种子也将被选中。答案答案(1)天平未调零;(2)游码未归零;(3)称量前指针偏右;(4)称量时左盘垫有纸,右盘没垫纸;(5)称量时物质与砝码放反了,并使用了游码;(6)称量时天平指针略向左倾斜。(7)食盐中有杂质或食盐不干燥;(8)称量的食盐没完全转移到烧杯中;(9)用量筒量取水时,仰视水面刻度线来读取体积读数;(10)配制溶液的烧杯用蒸馏水润洗。答案(1)用食盐和水;
(2)用6%的食盐水加水稀释;
(3)用2%的食盐水加食盐;
(4)用6%和2%的食盐水;
(5)用2%的食盐水蒸发水分。答案 小结:
1.溶液配制的步骤:
计算. 称量. 溶解 . 转移
2.浓溶液与稀溶液的转化:
关键: 稀释前后溶质质量不变
即: m浓w浓=m稀w稀
