物质反应后成分的探究——氢氧化钠溶液是否变质(20张PPT)
文档属性
| 名称 | 物质反应后成分的探究——氢氧化钠溶液是否变质(20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-31 00:00:00 | ||
图片预览






文档简介
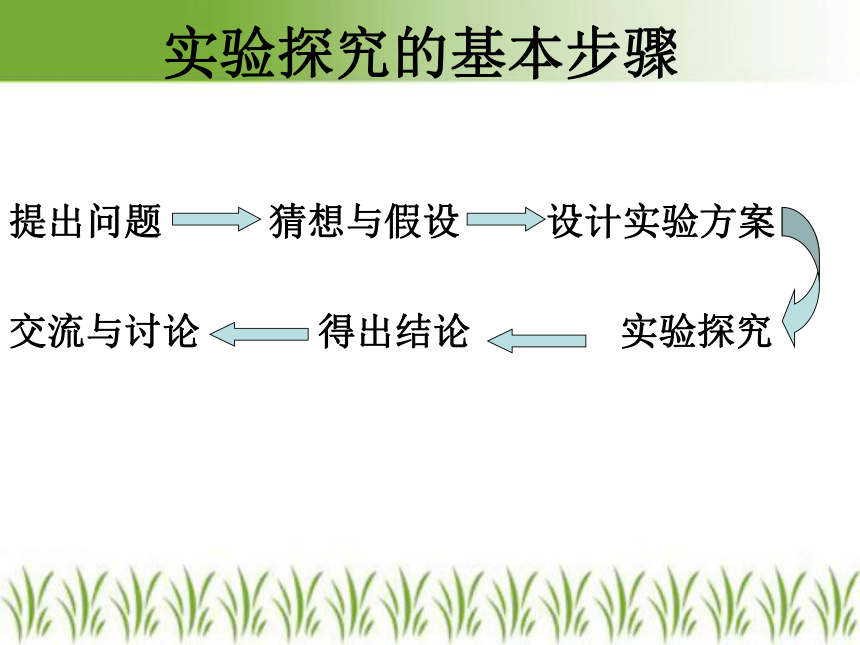
课件20张PPT。氢氧化钠溶液是否变质实验探究的基本步骤提出问题 猜想与假设 设计实验方案
交流与讨论 得出结论 实验探究 这些氢氧化钠变质了吗?猜想 :我想知道1.提出该假设的依据是什么?想一想:第一站②NaOH溶液没有变质①NaOH溶液已经变质2.如何证明氢氧化钠是否变质呢?思考与交流
检验NaOH溶液样品是否变质,可以检验NaOH
溶液样品中是否存在 。 Na2CO3思考与交流
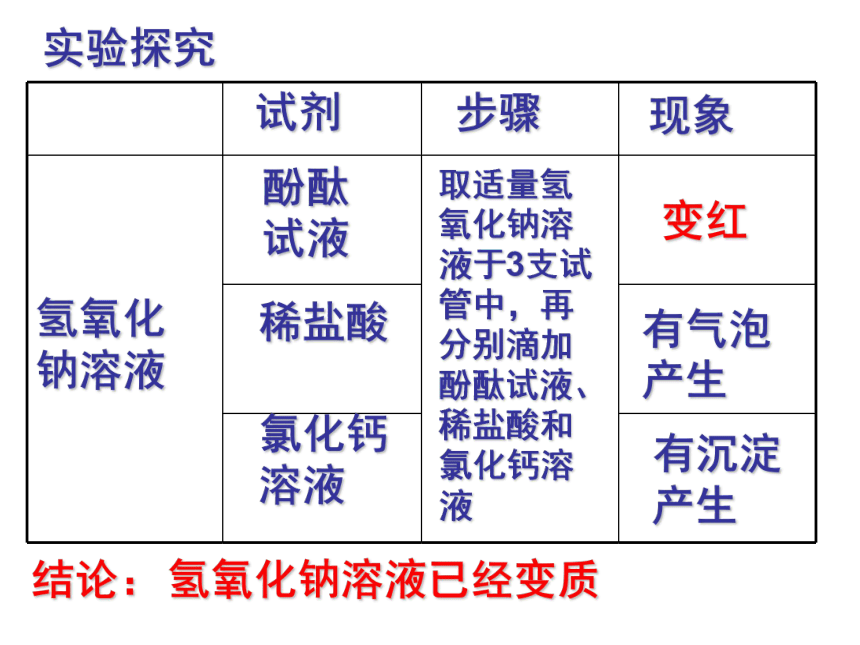
可选用哪些试剂来检验Na2CO3溶液?盐酸、氯化钙溶液、酚酞溶液等选用这些试剂的依据是什么?结论:氢氧化钠溶液已经变质氢氧化
钠溶液试剂步骤现象酚酞试液稀盐酸氯化钙溶液取适量氢氧化钠溶液于3支试管中,再分别滴加酚酞试液、稀盐酸和氯化钙溶液变红有气泡
产生有沉淀
产生实验探究氢氧化钠是全部变质还是部分变质呢?猜想 ②NaOH溶液部分变质①NaOH溶液全部变质全部变质:
部分变质:想一想:我想知道第二站如果NaOH溶液全部变质,存在的物质有哪些?部分变质呢?Na2CO3Na2CO3 和 NaOHNaOH交流与讨论
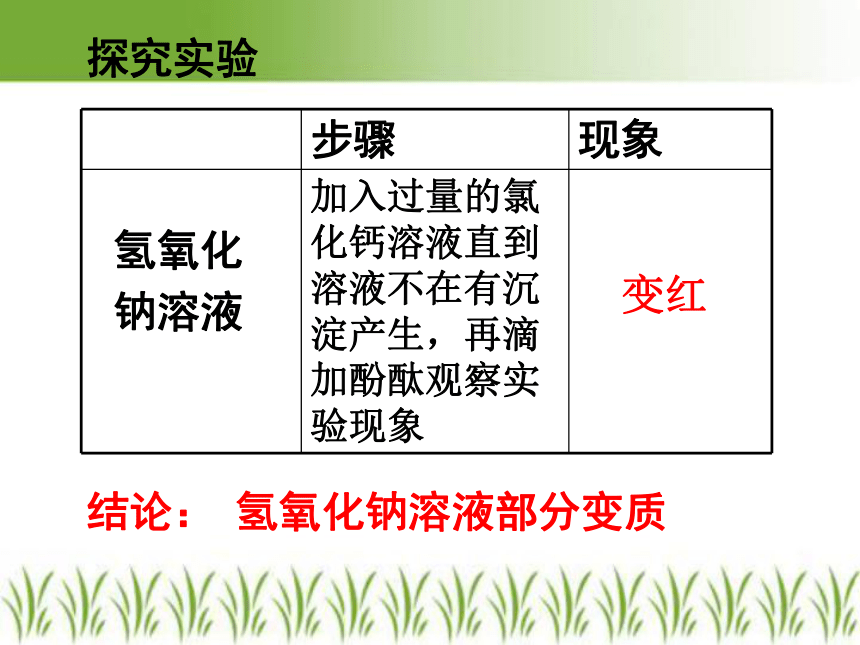
检验NaOH溶液样品是完全变质,还是部分变质,可以检验变质后的溶液中是否含 。全部变质:Na2CO3
部分变质:Na2CO3和NaOH可选用什么试剂来检验NaOH溶液? 无色酚酞试液变红探究实验氢氧化钠溶液部分变质结论:旅途拾趣问题1:久置的氢氧化钠变质了吗?
问题2:如果变质,变成了什么物质了呢?
问题3:这些氢氧化钠是否全部变质了呢?1.加入稀盐酸,一开始若没有气泡产生,能否说明NaOH溶液没有变质产生Na2CO3?2.若选用稀盐酸来检验产生了Na2CO3,对所加稀盐酸的量有什么要求? 习题:不能、因为盐酸优先与氢氧化钠反应,氢氧化钠被消耗完后再与碳酸钠反应。盐酸用量要足量3.写出NaOH固体变质的化学方程式
4.能否用酚酞试液检验NaOH是否变质,说明理由。不能。因为碳酸钠溶液呈碱性,也能使酚酞变红,用酚酞无法区分。5.为证明变质的固体中仍然存在NaOH,某同学按如下操作进行实验:
① 取少量固体溶于水,向其中加入足量CaCl2溶液,现象为______________。反应的化学方程式为___________________________________。
② 取①所得的溶液于试管中,向其中滴加少量的
______,现象为_____。其结论是_________
______________________。Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl 白色沉淀产生酚酞变红变质的固体中存在NaOH密封保存 【实验反思】谢谢OH–Na+CO32-过量CaCl2溶液CaCO3Na+Na+Cl-Ca2+Cl-Cl-Ca2+Cl-Na+CO32-CaCO3Na+Cl-Ca2+Cl-Cl-Ca2+Cl-碱性中性部分变质:Na2CO3和NaOH全部变质:Na2CO3红色无色OH–Na+CO32-过量Ca(OH)2溶液CaCO3Na+Na+OH-Ca2+OH-Ca2+OH-Na+CO32-CaCO3Na+OH-Ca2+OH-OH-Ca2+OH-碱性碱性部分变质:Na2CO3和NaOH全部变质:Na2CO3OH-红色红色补充实验:
取两支试管分别加入适量NaOH溶液和Na2CO3溶液,在分别滴加酚酞试液,观察现象探究实验结论:氢氧化钠溶液已经变质变红有气泡
产生有沉淀
产生变红没有沉
淀产生没有气
泡产生
交流与讨论 得出结论 实验探究 这些氢氧化钠变质了吗?猜想 :我想知道1.提出该假设的依据是什么?想一想:第一站②NaOH溶液没有变质①NaOH溶液已经变质2.如何证明氢氧化钠是否变质呢?思考与交流
检验NaOH溶液样品是否变质,可以检验NaOH
溶液样品中是否存在 。 Na2CO3思考与交流
可选用哪些试剂来检验Na2CO3溶液?盐酸、氯化钙溶液、酚酞溶液等选用这些试剂的依据是什么?结论:氢氧化钠溶液已经变质氢氧化
钠溶液试剂步骤现象酚酞试液稀盐酸氯化钙溶液取适量氢氧化钠溶液于3支试管中,再分别滴加酚酞试液、稀盐酸和氯化钙溶液变红有气泡
产生有沉淀
产生实验探究氢氧化钠是全部变质还是部分变质呢?猜想 ②NaOH溶液部分变质①NaOH溶液全部变质全部变质:
部分变质:想一想:我想知道第二站如果NaOH溶液全部变质,存在的物质有哪些?部分变质呢?Na2CO3Na2CO3 和 NaOHNaOH交流与讨论
检验NaOH溶液样品是完全变质,还是部分变质,可以检验变质后的溶液中是否含 。全部变质:Na2CO3
部分变质:Na2CO3和NaOH可选用什么试剂来检验NaOH溶液? 无色酚酞试液变红探究实验氢氧化钠溶液部分变质结论:旅途拾趣问题1:久置的氢氧化钠变质了吗?
问题2:如果变质,变成了什么物质了呢?
问题3:这些氢氧化钠是否全部变质了呢?1.加入稀盐酸,一开始若没有气泡产生,能否说明NaOH溶液没有变质产生Na2CO3?2.若选用稀盐酸来检验产生了Na2CO3,对所加稀盐酸的量有什么要求? 习题:不能、因为盐酸优先与氢氧化钠反应,氢氧化钠被消耗完后再与碳酸钠反应。盐酸用量要足量3.写出NaOH固体变质的化学方程式
4.能否用酚酞试液检验NaOH是否变质,说明理由。不能。因为碳酸钠溶液呈碱性,也能使酚酞变红,用酚酞无法区分。5.为证明变质的固体中仍然存在NaOH,某同学按如下操作进行实验:
① 取少量固体溶于水,向其中加入足量CaCl2溶液,现象为______________。反应的化学方程式为___________________________________。
② 取①所得的溶液于试管中,向其中滴加少量的
______,现象为_____。其结论是_________
______________________。Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl 白色沉淀产生酚酞变红变质的固体中存在NaOH密封保存 【实验反思】谢谢OH–Na+CO32-过量CaCl2溶液CaCO3Na+Na+Cl-Ca2+Cl-Cl-Ca2+Cl-Na+CO32-CaCO3Na+Cl-Ca2+Cl-Cl-Ca2+Cl-碱性中性部分变质:Na2CO3和NaOH全部变质:Na2CO3红色无色OH–Na+CO32-过量Ca(OH)2溶液CaCO3Na+Na+OH-Ca2+OH-Ca2+OH-Na+CO32-CaCO3Na+OH-Ca2+OH-OH-Ca2+OH-碱性碱性部分变质:Na2CO3和NaOH全部变质:Na2CO3OH-红色红色补充实验:
取两支试管分别加入适量NaOH溶液和Na2CO3溶液,在分别滴加酚酞试液,观察现象探究实验结论:氢氧化钠溶液已经变质变红有气泡
产生有沉淀
产生变红没有沉
淀产生没有气
泡产生
