人教版高中化学选修二第1单元课题1 化工生产过程中的基本问题 课件26张PPT
文档属性
| 名称 | 人教版高中化学选修二第1单元课题1 化工生产过程中的基本问题 课件26张PPT |
|
|
| 格式 | zip | ||
| 文件大小 | 668.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-11-17 00:00:00 | ||
图片预览








文档简介
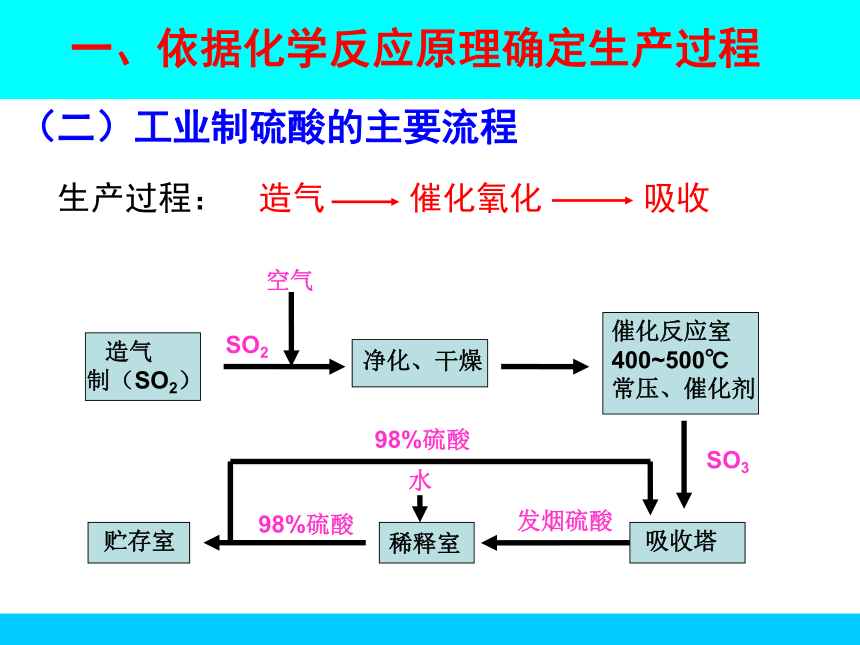
课件26张PPT。选修二——《化学与技术》课题1 化工生产过程中
的基本问题硫酸的性质(1)物理性质:
硫酸是一种无色,难挥发,易溶于水的油状液体。
浓硫酸溶于水时会放出大量的热。因此,稀释硫酸 时应该把 倒入 中,并 。浓硫酸水不断搅拌吸水脱水强氧化【复习回顾】(2)化学性质:
浓硫酸具有酸性, 性、 性和 性硫酸的消费水平是一个国家工业发达水平的重要标志一、依据化学反应原理确定生产过程(一)硫酸工业生产的原理1. 自然界中存在的含硫的物质有哪些?2. 这些物质能直接得到H2SO4吗?若不能,那么要经过哪些中间产物才能变成硫酸?硫磺、黄铁矿(FeS2)请写出有关的化学方程式!以硫磺为原料第一步:造气第二步:催化氧化第三步:吸收(一)硫酸工业生产的原理一、依据化学反应原理确定生产过程以黄铁矿(FeS2)为原料第一步:造气第二步:催化氧化第三步:吸收(一)硫酸工业生产的原理一、依据化学反应原理确定生产过程SO3空气SO2发烟硫酸98%硫酸98%硫酸水(二)工业制硫酸的主要流程一、依据化学反应原理确定生产过程二、生产中原料的选择1、硫酸生产中的三种原料:【思考】
(1)为什么早期我国是以黄铁矿为原料制硫酸?
(2)为什么不主张用黄铁矿(FeS2)作为原料生产硫酸?早期黄铁矿储存量比较大,而天然硫磺资源缺乏,又难以从国外购进,并且那时对环境保护不够重视。
硫磺制硫酸比黄铁矿制硫酸生产流程短,设备简单,三废治理量小,劳动生产率高,易于设备大型化,从而降低成本。硫磺或黄铁矿、空气、水【思考】从生产硫酸的原理看,硫酸厂中的生产设备最少应分几部分?2、工业生产硫酸的基本过程沸腾炉接触室吸收塔3、硫酸工业生产的三个主要设备SO2
O2 粉碎黄铁矿是增大矿石跟空气的接触面积,加快反应速率并使之充分燃烧;
通强大的空气流是为了使黄铁矿充分燃烧,同时增大廉价易得的反应物浓度,可以使较贵重的原料得以充分利用。不纯净,炉气中除SO2 还含有O2、N2、H2O和一些杂质。思考:接触室中热交换器的作用是什么?从接触室出来的气体成分是什么? 因为用水或稀H2SO4溶液做吸收剂容易形成酸雾且吸收速率慢;
液体由上向下流,气体由下向上升,两者在逆流过程中充分反应。三、生产中反应条件的控制注:这是一个气体总体积缩小的、放热的可逆反应(1)温度理论:温度越低,转化率越高——采用低温
实际:采用400~500℃温度太低催化剂活性不高,反应速率太小,耗时长,效率低【阅读 P6 思考与交流部分,回答相关问题】三、生产中反应条件的控制注:这是一个气体总体积缩小的、放热的可逆反应(2)压强理论:压强越大,转化率越高——采用高压
实际:常压① 常压下平衡转化率已较高
②采用高压设备增加设备成本,提供高压需要增加能耗(1)较高的温度(400~5000C)
(2)常压
(3)催化剂(V2O5) 三、生产中反应条件的控制接触氧化的适宜条件:四、硫酸工业生产过程中三废的处理1、三废:废气、废液、废渣2、三废的处理方法:(1)如何处理尾气中的SO2?方法一:石灰水吸收法方法二:氨水吸收法(2)、 如何处理废水中的酸性物质?(3)、如何利用废渣和生产过程中的产生的
大量热能?用石灰浆(Ca(OH)2或石灰石粉中和:废渣:回收炼铁、制水泥、制砖,铺路四、硫酸工业生产过程中三废的处理五、能量的充分利用 硫酸生产过程中的三个化学反应都是放热反应,可以充分利用这些反应放出的热能(工厂里把它们叫做“废热”)以降低生产成本。在沸腾炉旁设置“废热”锅炉,产生蒸汽来发电;
在接触室中设热交换装置。
据测算,生产1t硫酸约需消耗100kW·h的电能,而相应量反应物在生产过程中放出的反应热相当于200kW·h的电能。化工生产过程中应考虑的问题:(1)确定化学反应原理
(2)选择原料
(3)选择设备和工艺流程
(4)三废处理(环境保护)
(5)能源的利用(综合经济利益)
(6)其它问题(如厂址,成本,反应条件等问题)小结:小结:(本节课重点)1. 工业上接触法制硫酸概括为“五个三” :
三种原料:
三个反应:
三个生产过程:
三个主要设备:
硫酸工业生产的三个适宜条件:
2. 硫酸生产中的废气及废液的处理方法。硫磺(或黄铁矿)、空气和水造气、催化氧化、吸收沸 腾 炉、接 触 室、吸收塔(1) 400~5000C
(2)常压
(3)适当过量的空气1、在硫酸的工业制法中,下列生产操作与说明生产操作的原因二者都正确的是( )
A、硫铁矿燃烧前需将矿粒粉碎,这样易于向沸腾炉中投料
B、炉气进入接触室之前需要净化、干燥,因为炉气中的杂质易与SO2反应
C、SO2氧化为SO3时需要使用催化剂,这样可提高SO2的转化率
D、接触室的反应温度控制在400~500℃,因为在这个温度范围内,反应速率和SO2的转化率都比较理想,且催化剂的活性也较高练习D练习2、下列对硫酸生产中化学反应原理的分析正确的是( )
A、硫酸生产中涉及的三个化学反应因原料的不同可能全部是氧化还原反应
B、硫酸生产中涉及的三个化学反应都是放热反应
C、硫酸生产中涉及的三个化学反应都需要使用催化剂
D、硫酸生产中涉及的三个化学反应都需要在较高温度条件下进行B练习3、关于接触法制硫酸的叙述中,不正确的是( )
A、从沸腾炉出来的炉气必须净化,主要目的是防止催化剂中毒
B、之所以叫“接触法”是因为SO2被氧化成SO3时反应是在催化剂表面进行的
C、黄铁矿粉碎成细小矿粒,在沸腾炉中燃烧快、反应完全,提高了原料的利用率
D、SO3用稀硫酸吸收而不用水吸收,可防止形成酸雾并使SO3吸收完全D练习4、硫酸最古老的生产方法是把绿矾(FeSO4?7H2O)装入反应器中加强热,会流出油状液体,并放出有刺激性气味的气体(SO2),反应器中的固体变成了红色。写出这种方法中绿矾转化为硫酸的两个化学方程式:
(1)
(2)
的基本问题硫酸的性质(1)物理性质:
硫酸是一种无色,难挥发,易溶于水的油状液体。
浓硫酸溶于水时会放出大量的热。因此,稀释硫酸 时应该把 倒入 中,并 。浓硫酸水不断搅拌吸水脱水强氧化【复习回顾】(2)化学性质:
浓硫酸具有酸性, 性、 性和 性硫酸的消费水平是一个国家工业发达水平的重要标志一、依据化学反应原理确定生产过程(一)硫酸工业生产的原理1. 自然界中存在的含硫的物质有哪些?2. 这些物质能直接得到H2SO4吗?若不能,那么要经过哪些中间产物才能变成硫酸?硫磺、黄铁矿(FeS2)请写出有关的化学方程式!以硫磺为原料第一步:造气第二步:催化氧化第三步:吸收(一)硫酸工业生产的原理一、依据化学反应原理确定生产过程以黄铁矿(FeS2)为原料第一步:造气第二步:催化氧化第三步:吸收(一)硫酸工业生产的原理一、依据化学反应原理确定生产过程SO3空气SO2发烟硫酸98%硫酸98%硫酸水(二)工业制硫酸的主要流程一、依据化学反应原理确定生产过程二、生产中原料的选择1、硫酸生产中的三种原料:【思考】
(1)为什么早期我国是以黄铁矿为原料制硫酸?
(2)为什么不主张用黄铁矿(FeS2)作为原料生产硫酸?早期黄铁矿储存量比较大,而天然硫磺资源缺乏,又难以从国外购进,并且那时对环境保护不够重视。
硫磺制硫酸比黄铁矿制硫酸生产流程短,设备简单,三废治理量小,劳动生产率高,易于设备大型化,从而降低成本。硫磺或黄铁矿、空气、水【思考】从生产硫酸的原理看,硫酸厂中的生产设备最少应分几部分?2、工业生产硫酸的基本过程沸腾炉接触室吸收塔3、硫酸工业生产的三个主要设备SO2
O2 粉碎黄铁矿是增大矿石跟空气的接触面积,加快反应速率并使之充分燃烧;
通强大的空气流是为了使黄铁矿充分燃烧,同时增大廉价易得的反应物浓度,可以使较贵重的原料得以充分利用。不纯净,炉气中除SO2 还含有O2、N2、H2O和一些杂质。思考:接触室中热交换器的作用是什么?从接触室出来的气体成分是什么? 因为用水或稀H2SO4溶液做吸收剂容易形成酸雾且吸收速率慢;
液体由上向下流,气体由下向上升,两者在逆流过程中充分反应。三、生产中反应条件的控制注:这是一个气体总体积缩小的、放热的可逆反应(1)温度理论:温度越低,转化率越高——采用低温
实际:采用400~500℃温度太低催化剂活性不高,反应速率太小,耗时长,效率低【阅读 P6 思考与交流部分,回答相关问题】三、生产中反应条件的控制注:这是一个气体总体积缩小的、放热的可逆反应(2)压强理论:压强越大,转化率越高——采用高压
实际:常压① 常压下平衡转化率已较高
②采用高压设备增加设备成本,提供高压需要增加能耗(1)较高的温度(400~5000C)
(2)常压
(3)催化剂(V2O5) 三、生产中反应条件的控制接触氧化的适宜条件:四、硫酸工业生产过程中三废的处理1、三废:废气、废液、废渣2、三废的处理方法:(1)如何处理尾气中的SO2?方法一:石灰水吸收法方法二:氨水吸收法(2)、 如何处理废水中的酸性物质?(3)、如何利用废渣和生产过程中的产生的
大量热能?用石灰浆(Ca(OH)2或石灰石粉中和:废渣:回收炼铁、制水泥、制砖,铺路四、硫酸工业生产过程中三废的处理五、能量的充分利用 硫酸生产过程中的三个化学反应都是放热反应,可以充分利用这些反应放出的热能(工厂里把它们叫做“废热”)以降低生产成本。在沸腾炉旁设置“废热”锅炉,产生蒸汽来发电;
在接触室中设热交换装置。
据测算,生产1t硫酸约需消耗100kW·h的电能,而相应量反应物在生产过程中放出的反应热相当于200kW·h的电能。化工生产过程中应考虑的问题:(1)确定化学反应原理
(2)选择原料
(3)选择设备和工艺流程
(4)三废处理(环境保护)
(5)能源的利用(综合经济利益)
(6)其它问题(如厂址,成本,反应条件等问题)小结:小结:(本节课重点)1. 工业上接触法制硫酸概括为“五个三” :
三种原料:
三个反应:
三个生产过程:
三个主要设备:
硫酸工业生产的三个适宜条件:
2. 硫酸生产中的废气及废液的处理方法。硫磺(或黄铁矿)、空气和水造气、催化氧化、吸收沸 腾 炉、接 触 室、吸收塔(1) 400~5000C
(2)常压
(3)适当过量的空气1、在硫酸的工业制法中,下列生产操作与说明生产操作的原因二者都正确的是( )
A、硫铁矿燃烧前需将矿粒粉碎,这样易于向沸腾炉中投料
B、炉气进入接触室之前需要净化、干燥,因为炉气中的杂质易与SO2反应
C、SO2氧化为SO3时需要使用催化剂,这样可提高SO2的转化率
D、接触室的反应温度控制在400~500℃,因为在这个温度范围内,反应速率和SO2的转化率都比较理想,且催化剂的活性也较高练习D练习2、下列对硫酸生产中化学反应原理的分析正确的是( )
A、硫酸生产中涉及的三个化学反应因原料的不同可能全部是氧化还原反应
B、硫酸生产中涉及的三个化学反应都是放热反应
C、硫酸生产中涉及的三个化学反应都需要使用催化剂
D、硫酸生产中涉及的三个化学反应都需要在较高温度条件下进行B练习3、关于接触法制硫酸的叙述中,不正确的是( )
A、从沸腾炉出来的炉气必须净化,主要目的是防止催化剂中毒
B、之所以叫“接触法”是因为SO2被氧化成SO3时反应是在催化剂表面进行的
C、黄铁矿粉碎成细小矿粒,在沸腾炉中燃烧快、反应完全,提高了原料的利用率
D、SO3用稀硫酸吸收而不用水吸收,可防止形成酸雾并使SO3吸收完全D练习4、硫酸最古老的生产方法是把绿矾(FeSO4?7H2O)装入反应器中加强热,会流出油状液体,并放出有刺激性气味的气体(SO2),反应器中的固体变成了红色。写出这种方法中绿矾转化为硫酸的两个化学方程式:
(1)
(2)
