人教版高中化学选修二第2单元课题2 海水的综合利用 课件32张PPT
文档属性
| 名称 | 人教版高中化学选修二第2单元课题2 海水的综合利用 课件32张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-11-18 00:00:00 | ||
图片预览










文档简介
课件32张PPT。海水的综合利用 浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源 海水中储有大量的化学物质,储量可观的就有80多种化学元素,其中70多种可以被人类提取利用,海洋是地球上最大的矿产资源库。全世界每年都要从海洋中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。一、海水中盐的开发与利用结晶池蒸发池1.海水制盐大连复州湾盐场海南莺歌海盐场结晶池
盐是人类日常生活中的必需品,也是很多工业部门的原料之一,而海盐又是盐的主要来源之一。
海水制盐的方法主要有三种,即:盐田法、电渗析法和冷冻法。盐田法历史最悠久,而且也是最简便和经济有效的方法,现在还在广泛采用。
2、食盐资源的利用氯碱工业 以食盐为原料制取NaOH Cl2 H2 再进一步生产一系列的化工产品的工业 动手、动脑:分析图2-9所示实验,溶液中离子的运动,两极的电极反应式(1)电解饱和食盐水反应原理 阴极:
阳极:
总反应:2H+ + 2e- = H2↑2Cl- -2e- = Cl2↑思考?上述装置的弱点:1.H2和Cl2 混合不安全
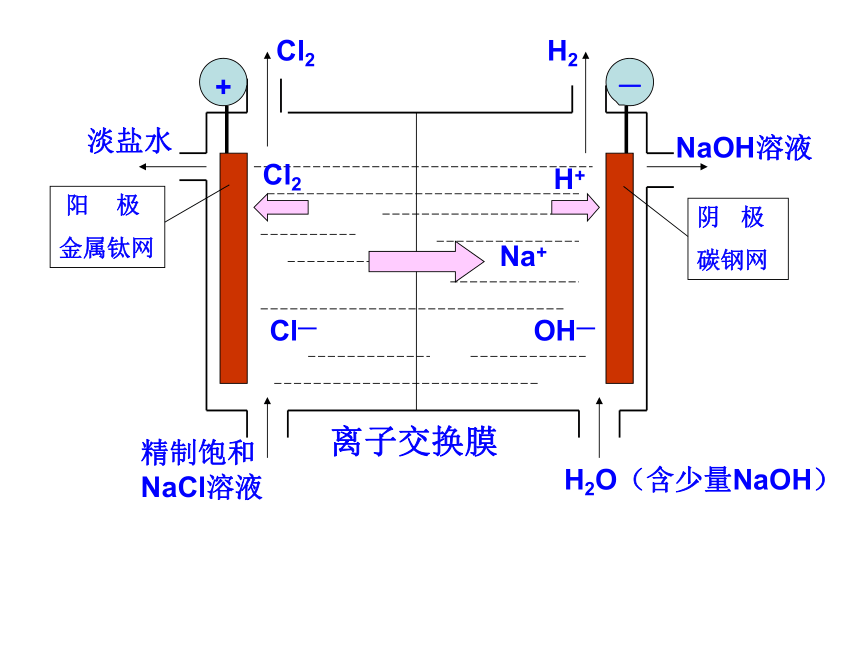
2.Cl2会和NaOH反应,会使得到的NaOH不纯(2)离子交换膜法制烧碱Cl2Cl2Cl—H2H+OH—淡盐水NaOH溶液精制饱和NaCl溶液H2O(含少量NaOH)离子交换膜1. 生产设备名称:离子交换膜电解槽
阳极:金属钛网(涂钛钌氧化物)
阴极:碳钢网(有镍涂层)
阳离子交换膜:只允许阳离子通过,把电解槽隔成阴极室和阳极室。
2. 离子交换膜的作用:
(1)防止氯气和氢气混合而引起爆炸
(2)避免氯气与氢氧化钠反应生成次氯酸钠
影响氢氧化钠的产量
(3)生产流程1.用什么方法除去泥沙?
2.用什么试剂除去Ca2+、Mg2+、Fe3+、SO42-?
3.所用试剂只有过量才能除净这些杂质,你能设计一个合理的顺序逐一除杂吗?
思考:粗盐水(Ca2+、Mg2+、Fe3+、SO42-)Ba2+ + SO42- =BaSO4Ca2+、Mg2+、Fe3+、Ba2+BaSO4Ca2+ + CO32- = CaCO3
Ba2+ + CO32- = BaCO3CaCO3
BaCO3Mg2+、Fe3+、CO32-Mg2+ + 2OH- = Mg(OH)2
Fe3+ + 3OH- = Fe(OH)3Fe(OH)3
Mg(OH)2OH-、CO32-精制食盐水氯碱工业(见P34)饱和食盐水氢气氯气氢氧化钠盐酸漂白剂冶炼金属等合成农药等造纸、玻璃、肥皂、纺织等海水的综合利用第二课时Cl2Cl2Cl—H2H+OH—淡盐水NaOH溶液精制饱和NaCl溶液H2O(含少量NaOH)离子交换膜复习: 1、氧化
工业上从海水中提取溴时,首先通氯气于pH为3.5左右晒盐后留下苦卤(富含Br-离子)中置换出Br2。二、海水提溴Cl2 +2Br - =Br2+ 2Cl - 2. 吹出
然后用空气把Br2吹出,再用Na2CO3溶液吸收,即得较浓的NaBr和NaBrO3溶液: 3CO32- + 3Br2 = 5Br- + BrO33- + 3CO2↑ 最后,用硫酸将溶液酸化,Br2即从溶液中游离出来:
5Br- + BrO33- + 6H+ = 3Br2 + 3H2O 3. 吸收
用还原剂二氧化硫使溴单质变为HBr,再用氯气将其氧化成溴产品。Cl2 +2Br - =Br2+ 2Cl - Br2 + SO2 +2H2O =2HBr+H2SO4思考:1.海水是一种混合溶液,其中主要含有哪 些离子?Cl- Na+ Mg2+ Ca2+ SO42- K+……2.结合海水资源的特点,我们从海水中提取镁到底有没有实际意义?在提取过程中又可能会面临怎样的困难?三、海水提镁思考:1、如何实现Mg2+ 的富集和分离?可以加入一种试剂使Mg2+ 沉淀2、是不是直接往海水中加沉淀剂?不是,因为海水中的Mg2+ 的浓度很小,直接加沉淀剂不利于Mg2+ 的沉淀,而且会增大沉淀剂的用量,我们可以先将海水浓缩,再加沉淀剂3、从综合角度考虑选用哪种试剂作沉淀剂好?Ca(OH)2思考:如何由贝壳制得氢氧化钙?贝壳(CaCO3)CaOCa(OH)21、从沉淀效果看,澄清石灰水比氢氧化钠效果差得多,如何解决这一矛盾?3、如何制得无水MgCl2 ?4、由MgCl2 到Mg究竟用还原法还是电解法好?思考:用石灰乳代替石灰水先加盐酸反应,再浓缩得MgCl2?6H2O晶体,然后再将MgCl2?6H2O晶体在HCl气氛中加热脱水即可得无水MgCl2 由于镁本身比较活泼,用还原法比较困难,工业上常使用电解熔融的氯化镁得到镁2、请设计由Mg(OH)2到Mg的可能途径。将石灰水改为石灰乳思考:电解产生的Cl2怎么处理?探究一:取一小段除去氧化膜的镁条投入盛有一定量稀盐酸的试管中;
现象:
结论或化学方程式: 镁条逐渐溶解,有大量气体产生 Mg+2HCl=MgCl2+H2↑探究二:取一小段除去氧化膜的镁条投入滴有酚酞的水中;
现象:
结论或化学方程式: 有气体产生,滴有酚酞的水溶液变红(但比钠与水反应缓和得多)探究三:取一根除去氧化膜的镁条,点燃后插入充满CO2的的集气瓶中。
现象:
结论或化学方程式: 燃着的镁条在CO2中继续燃烧,发出耀眼的白光,生成白色固体,在集气瓶的内壁有黑色固体附着四、Mg条与氮气的反应四、从海水中提取重水 海水中溶存着80多种元素,其中不少元素可以提取利用,具有重要的开发价值。据计算,每立方千米海水中含有3 750×104 t固体物质,其中除氯化钠约3 000×104 t外,镁约450×104 t,钾、溴、碘、钍、钼、铀等元素也不少。 中 国 海 域 镁在海水中含量很高,仅次于氯和钠,居第3位。 溴的浓度较高,平均为67×10-3 mL/L,地球上99%以上的溴都储存在海水里,故溴有“海洋元素”之称。 碘在海水中的浓度只有0.06× 10-6,属于微量元素。 钾在海水中的总量为500 ×1012 t以上。海水中所含钾的储量远远超过钾盐矿物储量。 铀海水中的总量非常可观,达45×108 t,相当于陆地储量的4500倍。 一吨海水中所含重水的核聚变反应,可释放出相当于256t石油燃烧所产生的能量。 重水核聚变反应可释放出相当能量,海水中约有200×108 t重水。 提取 氘是氢的同位素。氘的原子核除包含一个质子外,比氢多了一个中子。氘的化学性质与氢一样,但是一个氘原子比一个氢原子重一倍,所以叫做“重氢”。氢二氧一化合成水,重氢和氧化合成的水叫做“重水”。重水主要赋存于海水中,总量可达250亿吨。重水现在已是核反应堆运行不可缺少的辅助材料,也是制取氘的原料。
制备重水有两种方法:
蒸馏法:这种方法只能得到纯度为92%的重水;
电解法:可得99.7%的重水,但消耗电能特别大
化学法:
重水可以通过多种方法生产。然而只有两种方法已证明具有商业意义:
水-硫化氢交换法(和氨-氢交换法。 水-硫化氢交换法是基于在一系列塔内(通过顶部冷和底部热的方式操作)水和硫化氢之间氢与氘交换的一种方法。在此过程中,水向塔底流动,而硫化氢气体从塔底向塔顶循环。使用一系列多孔塔板促进硫化氢气体和水之间的混合。在低温下氘向水中迁移,而在高温下氘向硫化氢中迁移。氘被浓缩了的硫化氢气体或水从第一级塔的热段和冷段的接合处排出,并且在下一级塔中重复这一过程。最后一级的产品(氘浓缩至30%的水)送入一个蒸镏单元以制备反应堆级的重水(即99.75%的氧化氘)。
盐是人类日常生活中的必需品,也是很多工业部门的原料之一,而海盐又是盐的主要来源之一。
海水制盐的方法主要有三种,即:盐田法、电渗析法和冷冻法。盐田法历史最悠久,而且也是最简便和经济有效的方法,现在还在广泛采用。
2、食盐资源的利用氯碱工业 以食盐为原料制取NaOH Cl2 H2 再进一步生产一系列的化工产品的工业 动手、动脑:分析图2-9所示实验,溶液中离子的运动,两极的电极反应式(1)电解饱和食盐水反应原理 阴极:
阳极:
总反应:2H+ + 2e- = H2↑2Cl- -2e- = Cl2↑思考?上述装置的弱点:1.H2和Cl2 混合不安全
2.Cl2会和NaOH反应,会使得到的NaOH不纯(2)离子交换膜法制烧碱Cl2Cl2Cl—H2H+OH—淡盐水NaOH溶液精制饱和NaCl溶液H2O(含少量NaOH)离子交换膜1. 生产设备名称:离子交换膜电解槽
阳极:金属钛网(涂钛钌氧化物)
阴极:碳钢网(有镍涂层)
阳离子交换膜:只允许阳离子通过,把电解槽隔成阴极室和阳极室。
2. 离子交换膜的作用:
(1)防止氯气和氢气混合而引起爆炸
(2)避免氯气与氢氧化钠反应生成次氯酸钠
影响氢氧化钠的产量
(3)生产流程1.用什么方法除去泥沙?
2.用什么试剂除去Ca2+、Mg2+、Fe3+、SO42-?
3.所用试剂只有过量才能除净这些杂质,你能设计一个合理的顺序逐一除杂吗?
思考:粗盐水(Ca2+、Mg2+、Fe3+、SO42-)Ba2+ + SO42- =BaSO4Ca2+、Mg2+、Fe3+、Ba2+BaSO4Ca2+ + CO32- = CaCO3
Ba2+ + CO32- = BaCO3CaCO3
BaCO3Mg2+、Fe3+、CO32-Mg2+ + 2OH- = Mg(OH)2
Fe3+ + 3OH- = Fe(OH)3Fe(OH)3
Mg(OH)2OH-、CO32-精制食盐水氯碱工业(见P34)饱和食盐水氢气氯气氢氧化钠盐酸漂白剂冶炼金属等合成农药等造纸、玻璃、肥皂、纺织等海水的综合利用第二课时Cl2Cl2Cl—H2H+OH—淡盐水NaOH溶液精制饱和NaCl溶液H2O(含少量NaOH)离子交换膜复习: 1、氧化
工业上从海水中提取溴时,首先通氯气于pH为3.5左右晒盐后留下苦卤(富含Br-离子)中置换出Br2。二、海水提溴Cl2 +2Br - =Br2+ 2Cl - 2. 吹出
然后用空气把Br2吹出,再用Na2CO3溶液吸收,即得较浓的NaBr和NaBrO3溶液: 3CO32- + 3Br2 = 5Br- + BrO33- + 3CO2↑ 最后,用硫酸将溶液酸化,Br2即从溶液中游离出来:
5Br- + BrO33- + 6H+ = 3Br2 + 3H2O 3. 吸收
用还原剂二氧化硫使溴单质变为HBr,再用氯气将其氧化成溴产品。Cl2 +2Br - =Br2+ 2Cl - Br2 + SO2 +2H2O =2HBr+H2SO4思考:1.海水是一种混合溶液,其中主要含有哪 些离子?Cl- Na+ Mg2+ Ca2+ SO42- K+……2.结合海水资源的特点,我们从海水中提取镁到底有没有实际意义?在提取过程中又可能会面临怎样的困难?三、海水提镁思考:1、如何实现Mg2+ 的富集和分离?可以加入一种试剂使Mg2+ 沉淀2、是不是直接往海水中加沉淀剂?不是,因为海水中的Mg2+ 的浓度很小,直接加沉淀剂不利于Mg2+ 的沉淀,而且会增大沉淀剂的用量,我们可以先将海水浓缩,再加沉淀剂3、从综合角度考虑选用哪种试剂作沉淀剂好?Ca(OH)2思考:如何由贝壳制得氢氧化钙?贝壳(CaCO3)CaOCa(OH)21、从沉淀效果看,澄清石灰水比氢氧化钠效果差得多,如何解决这一矛盾?3、如何制得无水MgCl2 ?4、由MgCl2 到Mg究竟用还原法还是电解法好?思考:用石灰乳代替石灰水先加盐酸反应,再浓缩得MgCl2?6H2O晶体,然后再将MgCl2?6H2O晶体在HCl气氛中加热脱水即可得无水MgCl2 由于镁本身比较活泼,用还原法比较困难,工业上常使用电解熔融的氯化镁得到镁2、请设计由Mg(OH)2到Mg的可能途径。将石灰水改为石灰乳思考:电解产生的Cl2怎么处理?探究一:取一小段除去氧化膜的镁条投入盛有一定量稀盐酸的试管中;
现象:
结论或化学方程式: 镁条逐渐溶解,有大量气体产生 Mg+2HCl=MgCl2+H2↑探究二:取一小段除去氧化膜的镁条投入滴有酚酞的水中;
现象:
结论或化学方程式: 有气体产生,滴有酚酞的水溶液变红(但比钠与水反应缓和得多)探究三:取一根除去氧化膜的镁条,点燃后插入充满CO2的的集气瓶中。
现象:
结论或化学方程式: 燃着的镁条在CO2中继续燃烧,发出耀眼的白光,生成白色固体,在集气瓶的内壁有黑色固体附着四、Mg条与氮气的反应四、从海水中提取重水 海水中溶存着80多种元素,其中不少元素可以提取利用,具有重要的开发价值。据计算,每立方千米海水中含有3 750×104 t固体物质,其中除氯化钠约3 000×104 t外,镁约450×104 t,钾、溴、碘、钍、钼、铀等元素也不少。 中 国 海 域 镁在海水中含量很高,仅次于氯和钠,居第3位。 溴的浓度较高,平均为67×10-3 mL/L,地球上99%以上的溴都储存在海水里,故溴有“海洋元素”之称。 碘在海水中的浓度只有0.06× 10-6,属于微量元素。 钾在海水中的总量为500 ×1012 t以上。海水中所含钾的储量远远超过钾盐矿物储量。 铀海水中的总量非常可观,达45×108 t,相当于陆地储量的4500倍。 一吨海水中所含重水的核聚变反应,可释放出相当于256t石油燃烧所产生的能量。 重水核聚变反应可释放出相当能量,海水中约有200×108 t重水。 提取 氘是氢的同位素。氘的原子核除包含一个质子外,比氢多了一个中子。氘的化学性质与氢一样,但是一个氘原子比一个氢原子重一倍,所以叫做“重氢”。氢二氧一化合成水,重氢和氧化合成的水叫做“重水”。重水主要赋存于海水中,总量可达250亿吨。重水现在已是核反应堆运行不可缺少的辅助材料,也是制取氘的原料。
制备重水有两种方法:
蒸馏法:这种方法只能得到纯度为92%的重水;
电解法:可得99.7%的重水,但消耗电能特别大
化学法:
重水可以通过多种方法生产。然而只有两种方法已证明具有商业意义:
水-硫化氢交换法(和氨-氢交换法。 水-硫化氢交换法是基于在一系列塔内(通过顶部冷和底部热的方式操作)水和硫化氢之间氢与氘交换的一种方法。在此过程中,水向塔底流动,而硫化氢气体从塔底向塔顶循环。使用一系列多孔塔板促进硫化氢气体和水之间的混合。在低温下氘向水中迁移,而在高温下氘向硫化氢中迁移。氘被浓缩了的硫化氢气体或水从第一级塔的热段和冷段的接合处排出,并且在下一级塔中重复这一过程。最后一级的产品(氘浓缩至30%的水)送入一个蒸镏单元以制备反应堆级的重水(即99.75%的氧化氘)。
