海水资源的开发利用[下学期]
文档属性
| 名称 | 海水资源的开发利用[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 1022.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-06-14 00:00:00 | ||
图片预览








文档简介
课件25张PPT。海水资源的开发利用 地球有70.8%的面积为水所覆盖,但其中97.5%的水是咸水,无法饮用。在余下的2.5%的淡水中,有87%是人类难以利用的两极冰盖、高山冰川和永冻地带的冰雪。人类真正能够利用的是江河湖泊以及地下水中的一部分,仅约占地球总水量的0.26%。即使如此,总体而言,世界上是不缺水的。
但是,世界上淡水资源分布极不均匀,约65%的水资源集中在不到10个国家,而约占世界人口总数40%的80个国家和地区却严重缺水。人类使用水资源的方式以及污染更加剧了水资源的紧张形势。上个世纪90年代中期以来,全世界每年约有5000亿立方米污水排入江河湖海,造成35.5亿立方米以上的水体受到污染。 在地球为人类提供的“大水缸”里,可以饮用的水实际上只有一汤匙 淡水亮出“黄牌”联合国最新公布的数据触目惊心:全世界有十一亿人得不到干净的水。每天大约有6000名儿童死于不卫生的水和不合格的卫生和清洁条件所引起的疾病。正是认识到淡水在未来的极端重要性,全球100多个国家同意塔吉克斯坦总统拉赫莫诺夫的提议,将2003年定为“国际淡水年”。为此,2003年的世界水日、世界地球日等的主题都将是水资源。 全球水资源紧缺日益加剧,已经向人类亮出“黄牌”,如果再不解决水危机,21世纪人类可能被开除地球的“球籍”。 水的出路何在专家提出,解决淡水不足的办法有四条:寻找新水源、重新分配淡水资源、减少不必要的浪费以及循环利用。
从海洋里廉价地大量提取淡水是人们长期的梦想。
如果能够找到廉价运输淡水的方法,改善水资源不平均的状况,也可以缓解淡水不足。
节约用水是保护淡水资源的关键。
据联合国教科文组织估计,全球的水需求在上个世纪增加了5倍,比人口增速快两倍,因此循环利用是必由之路。
海水的利用水是生命之源,世界上缺水的地区越来越多,海水淡化已成为获得淡水资源重要的途径,海水利用包括海水直接利用、海水淡化和海水综合利用,以及海水农业等
海水直接利用是用海水代替淡水作为工业用水和生活用水。
海水淡化是海水利用的重点,到了21世纪中叶,我们会看到这样一个景象,每个岛屿或缺水的沿海城市都建有海水淡化工厂。 海水淡化 通过从海水中提取淡水或从海水中分离出盐分,都可以达到淡化海水的目的
海水淡化的方法已经有十几种,主要有蒸馏法、电渗析法离子交换法等,其中,蒸馏法的历史最久技术和工艺也比较完善,是目前海水淡化的主要手段。海水淡化技术? ①蒸馏法?
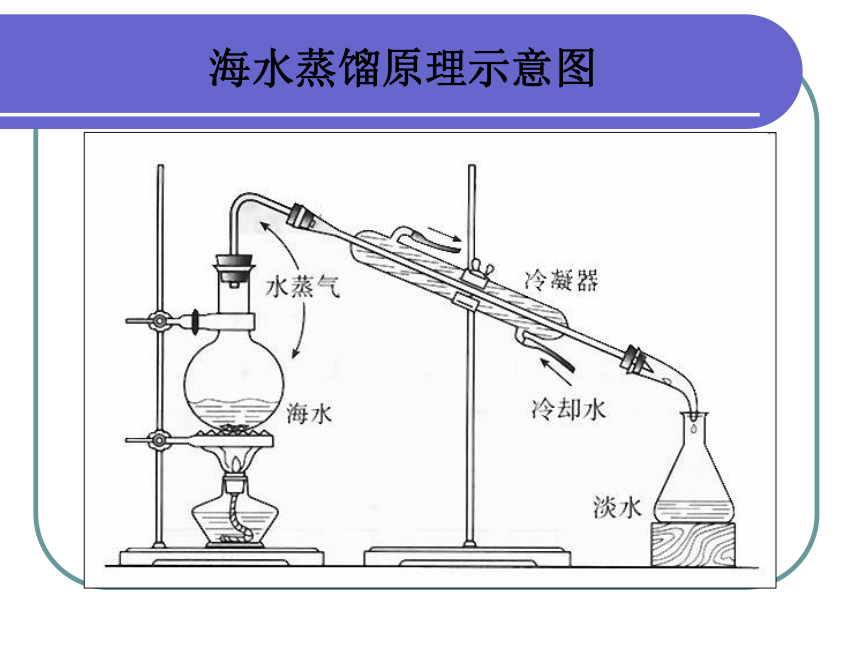
蒸馏法虽然是一种古老的方法,但由于技术不断地改进与发展,该法至今仍占统治地位。蒸馏淡化过程的实质就是水蒸气的形成过程,其原理如同海水受热蒸发形成云,云在一定条件下遇冷形成雨,而雨是不带咸味的。根据设备可分为蒸馏法、蒸汽压缩蒸馏法、多级闪急蒸馏法等。此外,以上方法的组合也日益受到重视。太阳能蒸发原理示意图海水蒸馏原理示意图 海水淡化技术?②离子交换法
离子交换法是液相中的离子和固相中离子间所进行的一种可逆性化学反应,当液相中的某些离子较为交换固体所喜好时,便会被离子交换固体吸附,为维持水溶液的电中性,离子交换固体必须释放出等价离子溶液中海水淡化技术?③电渗析法?
亦称换膜电渗析法该法的技术关键是新型离子交换膜的研制。离子交换膜是0.5 mm~1.0 mm厚度的功能性膜片,按其选择透过性区分为正离子交换膜(阳膜)与负离子交换膜(阴膜)。电渗析法是将具有选择透过性的阳膜与阴膜交替排列,组成多个相互独立的隔室海水被淡化,而相邻隔室海水浓缩,淡水与浓缩水得以分离。电渗析法不仅可以淡化海水,也可以作为水质处理的手段,为污水再利用作出贡献。此外,这种方法也越来越多地应用于化工、医药、食品等行业的浓缩、分离与提纯。电渗析淡化装置 海水淡化技术?④反渗透法?
通常又称超过滤法,是1953年才开始采用的一种膜分离淡化法。该法是利用半透膜只允许溶剂透过、不允许溶质透过的特点,将海水与淡水分隔开的。在通常情况下,淡水通过半透膜扩散到海水一侧,从而使海水一侧的液面逐渐升高,直至一定的高度才停止,这个过程为渗透。此时,海水一侧高出的水柱静压称为渗透压。如果对海水一侧施加一大于海水渗透压的外压,那么海水中的纯水将反渗透到淡水中。反渗透法的最大优点是节能。它的能耗仅为电渗析法的1/2,蒸馏法的1/40。因此,从1974年起,美、日等发达国家先后把发展重又转向反渗透法。反渗透海水淡化装置将海水冷冻到冰点以下,淡水结冰、分离、再融化为淡水的过程。
冷冻法有利用天然冰法和人工冷冻法两种。
冷冻法也是海水淡化的一种方法海水化学资源概况 海水的成分非常复杂,全球海洋的含盐量就达5亿亿吨,还含有大量非常稀有的元素,是地球上最大的矿产资源库。海洋资源的持续利用是人类生存发展的重要前提,目前,全世界每年从海洋中提取淡水20多亿吨、食盐5 000万吨、镁及氧化镁260多万吨、溴20万吨,总产值达6亿多美元。海水制盐历史悠久 目前,从海水中制得的氯化钠除用作工业食用外,还用作工业原料,如生产烧碱、纯碱、金属钠以及氯气、盐酸、漂白粉等含氯化工产品。从海水中制取镁、钾、溴及其化工产品,是在传统海水制盐工业上的发展海水提溴和海带中碘离子检验海水提溴的化学原理:将 Br – 转化成Br2海带中碘离子检验的原理:将I-转化成I2你会选择怎样的实验方法?请设计一个你认为可行的方案海水中提取溴单质NaBr+Cl2===Br2+2NaClBr2+SO2+2H2O===2HBr+H2SO42HBr+Cl2===Br2+2HCl 从海带中提取碘碘是人体生长发育不可缺少的微量元素,它在人体中仅有20—50毫克,人体用碘制造甲状腺素,调节新陈代谢。若摄入碘量不足,则人会得甲状腺肿大的粗脖子病即地甲病。为防止出现地甲病,我国颁布了《食盐加碘消除碘缺乏病管理条例》等法令,向食盐中加碘,碘盐就是在食盐中加入一定量的碘酸钾(碘酸钾由碘氧化制得)。那么,碘是从哪里来的呢?1.取食用干海带,用刷子刷去表面粘附物,不用水洗,称取3g,剪碎用酒精润湿,放入铁或瓷坩埚中,把坩埚置于泥三角上,高温灼烧,将海带烧成炭黑色后,自然冷却,
2.将坩埚内灼烧残余物放至小烧杯中,加入10mL蒸馏水,搅拌、煮沸2~3min,过滤。
3.在滤液中加入1mL饱和的新制氯水,振荡溶液,5分钟后,再滴入1%淀粉液1—2滴,溶液立刻由无色变成蓝色,由此证明溶液中含碘。 下面我们做一个从海带中提取碘的实验灼烧海带 ?????? 实验讨论1.实验前为什么要用刷子而不能用水洗食用干海带? 2.碘易升华,为什么还可以对干海带用酒精灯灼烧? 3.为什么要新制氯水与(2)的滤液反应?答案 1.因为在海带中碘主要以NaI形式存在,NaI易溶于水,如用水洗则由于NaI部分溶解而损失碘。
2.碘在海带中以NaI形式存在,NaI熔点很高,并且无水时O2不会氧化NaI,O2只能氧化溶液中的I- .
3.因为新制氯水中Cl2浓度较大,易发生 2I-+Cl2→I2+2Cl- 的反应,而久制氯水中Cl2少,实验效果不明显,且久制氯水中有HClO等高价氯氧化物会把I2继续氧化成高价碘化物,而不能使淀粉变蓝。
作业:课本85页第三题
但是,世界上淡水资源分布极不均匀,约65%的水资源集中在不到10个国家,而约占世界人口总数40%的80个国家和地区却严重缺水。人类使用水资源的方式以及污染更加剧了水资源的紧张形势。上个世纪90年代中期以来,全世界每年约有5000亿立方米污水排入江河湖海,造成35.5亿立方米以上的水体受到污染。 在地球为人类提供的“大水缸”里,可以饮用的水实际上只有一汤匙 淡水亮出“黄牌”联合国最新公布的数据触目惊心:全世界有十一亿人得不到干净的水。每天大约有6000名儿童死于不卫生的水和不合格的卫生和清洁条件所引起的疾病。正是认识到淡水在未来的极端重要性,全球100多个国家同意塔吉克斯坦总统拉赫莫诺夫的提议,将2003年定为“国际淡水年”。为此,2003年的世界水日、世界地球日等的主题都将是水资源。 全球水资源紧缺日益加剧,已经向人类亮出“黄牌”,如果再不解决水危机,21世纪人类可能被开除地球的“球籍”。 水的出路何在专家提出,解决淡水不足的办法有四条:寻找新水源、重新分配淡水资源、减少不必要的浪费以及循环利用。
从海洋里廉价地大量提取淡水是人们长期的梦想。
如果能够找到廉价运输淡水的方法,改善水资源不平均的状况,也可以缓解淡水不足。
节约用水是保护淡水资源的关键。
据联合国教科文组织估计,全球的水需求在上个世纪增加了5倍,比人口增速快两倍,因此循环利用是必由之路。
海水的利用水是生命之源,世界上缺水的地区越来越多,海水淡化已成为获得淡水资源重要的途径,海水利用包括海水直接利用、海水淡化和海水综合利用,以及海水农业等
海水直接利用是用海水代替淡水作为工业用水和生活用水。
海水淡化是海水利用的重点,到了21世纪中叶,我们会看到这样一个景象,每个岛屿或缺水的沿海城市都建有海水淡化工厂。 海水淡化 通过从海水中提取淡水或从海水中分离出盐分,都可以达到淡化海水的目的
海水淡化的方法已经有十几种,主要有蒸馏法、电渗析法离子交换法等,其中,蒸馏法的历史最久技术和工艺也比较完善,是目前海水淡化的主要手段。海水淡化技术? ①蒸馏法?
蒸馏法虽然是一种古老的方法,但由于技术不断地改进与发展,该法至今仍占统治地位。蒸馏淡化过程的实质就是水蒸气的形成过程,其原理如同海水受热蒸发形成云,云在一定条件下遇冷形成雨,而雨是不带咸味的。根据设备可分为蒸馏法、蒸汽压缩蒸馏法、多级闪急蒸馏法等。此外,以上方法的组合也日益受到重视。太阳能蒸发原理示意图海水蒸馏原理示意图 海水淡化技术?②离子交换法
离子交换法是液相中的离子和固相中离子间所进行的一种可逆性化学反应,当液相中的某些离子较为交换固体所喜好时,便会被离子交换固体吸附,为维持水溶液的电中性,离子交换固体必须释放出等价离子溶液中海水淡化技术?③电渗析法?
亦称换膜电渗析法该法的技术关键是新型离子交换膜的研制。离子交换膜是0.5 mm~1.0 mm厚度的功能性膜片,按其选择透过性区分为正离子交换膜(阳膜)与负离子交换膜(阴膜)。电渗析法是将具有选择透过性的阳膜与阴膜交替排列,组成多个相互独立的隔室海水被淡化,而相邻隔室海水浓缩,淡水与浓缩水得以分离。电渗析法不仅可以淡化海水,也可以作为水质处理的手段,为污水再利用作出贡献。此外,这种方法也越来越多地应用于化工、医药、食品等行业的浓缩、分离与提纯。电渗析淡化装置 海水淡化技术?④反渗透法?
通常又称超过滤法,是1953年才开始采用的一种膜分离淡化法。该法是利用半透膜只允许溶剂透过、不允许溶质透过的特点,将海水与淡水分隔开的。在通常情况下,淡水通过半透膜扩散到海水一侧,从而使海水一侧的液面逐渐升高,直至一定的高度才停止,这个过程为渗透。此时,海水一侧高出的水柱静压称为渗透压。如果对海水一侧施加一大于海水渗透压的外压,那么海水中的纯水将反渗透到淡水中。反渗透法的最大优点是节能。它的能耗仅为电渗析法的1/2,蒸馏法的1/40。因此,从1974年起,美、日等发达国家先后把发展重又转向反渗透法。反渗透海水淡化装置将海水冷冻到冰点以下,淡水结冰、分离、再融化为淡水的过程。
冷冻法有利用天然冰法和人工冷冻法两种。
冷冻法也是海水淡化的一种方法海水化学资源概况 海水的成分非常复杂,全球海洋的含盐量就达5亿亿吨,还含有大量非常稀有的元素,是地球上最大的矿产资源库。海洋资源的持续利用是人类生存发展的重要前提,目前,全世界每年从海洋中提取淡水20多亿吨、食盐5 000万吨、镁及氧化镁260多万吨、溴20万吨,总产值达6亿多美元。海水制盐历史悠久 目前,从海水中制得的氯化钠除用作工业食用外,还用作工业原料,如生产烧碱、纯碱、金属钠以及氯气、盐酸、漂白粉等含氯化工产品。从海水中制取镁、钾、溴及其化工产品,是在传统海水制盐工业上的发展海水提溴和海带中碘离子检验海水提溴的化学原理:将 Br – 转化成Br2海带中碘离子检验的原理:将I-转化成I2你会选择怎样的实验方法?请设计一个你认为可行的方案海水中提取溴单质NaBr+Cl2===Br2+2NaClBr2+SO2+2H2O===2HBr+H2SO42HBr+Cl2===Br2+2HCl 从海带中提取碘碘是人体生长发育不可缺少的微量元素,它在人体中仅有20—50毫克,人体用碘制造甲状腺素,调节新陈代谢。若摄入碘量不足,则人会得甲状腺肿大的粗脖子病即地甲病。为防止出现地甲病,我国颁布了《食盐加碘消除碘缺乏病管理条例》等法令,向食盐中加碘,碘盐就是在食盐中加入一定量的碘酸钾(碘酸钾由碘氧化制得)。那么,碘是从哪里来的呢?1.取食用干海带,用刷子刷去表面粘附物,不用水洗,称取3g,剪碎用酒精润湿,放入铁或瓷坩埚中,把坩埚置于泥三角上,高温灼烧,将海带烧成炭黑色后,自然冷却,
2.将坩埚内灼烧残余物放至小烧杯中,加入10mL蒸馏水,搅拌、煮沸2~3min,过滤。
3.在滤液中加入1mL饱和的新制氯水,振荡溶液,5分钟后,再滴入1%淀粉液1—2滴,溶液立刻由无色变成蓝色,由此证明溶液中含碘。 下面我们做一个从海带中提取碘的实验灼烧海带 ?????? 实验讨论1.实验前为什么要用刷子而不能用水洗食用干海带? 2.碘易升华,为什么还可以对干海带用酒精灯灼烧? 3.为什么要新制氯水与(2)的滤液反应?答案 1.因为在海带中碘主要以NaI形式存在,NaI易溶于水,如用水洗则由于NaI部分溶解而损失碘。
2.碘在海带中以NaI形式存在,NaI熔点很高,并且无水时O2不会氧化NaI,O2只能氧化溶液中的I- .
3.因为新制氯水中Cl2浓度较大,易发生 2I-+Cl2→I2+2Cl- 的反应,而久制氯水中Cl2少,实验效果不明显,且久制氯水中有HClO等高价氯氧化物会把I2继续氧化成高价碘化物,而不能使淀粉变蓝。
作业:课本85页第三题
