沪教版-九年级化学-杨艳-《溶解现象 溶液组成的表示》教案.doc
文档属性
| 名称 | 沪教版-九年级化学-杨艳-《溶解现象 溶液组成的表示》教案.doc |

|
|
| 格式 | rar | ||
| 文件大小 | 143.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-12-24 00:00:00 | ||
图片预览




文档简介
立德 践行 慎教 善导
【科目】化学 【班级】 【日期】2007-12-3 【教者】杨艳
【课题】第二节 溶液组成的表示 【课时】2-1 【类型】新授
第二节 溶液组成的表示
第一课时
教学目的:
1.了解溶液组成的含义。
2.掌握用溶质的质量分数表示溶液组成的方法和部分有关计算。
重点难点:
1.重点:溶质质量分数的表示方法及关系式的含义。
2.难点:溶液组成的含义。
教学过程:
上一节我们认识了溶液。生活中对溶液的利用很多。
你知道下面瓶中标签是什么意思吗?
下面我们就来学习溶液组成的表示方法。
复习:
你知道溶液由哪几部分组成的吗?它们之间的质量有什么关系?
溶液由溶质和溶剂组成。
溶液质量 = 溶质质量 + 溶剂质量
观察:
这三支试管所装的硫酸铜溶液有什么不同?
颜色的深浅不一样。说明里面含硫酸铜的浓度不一样。
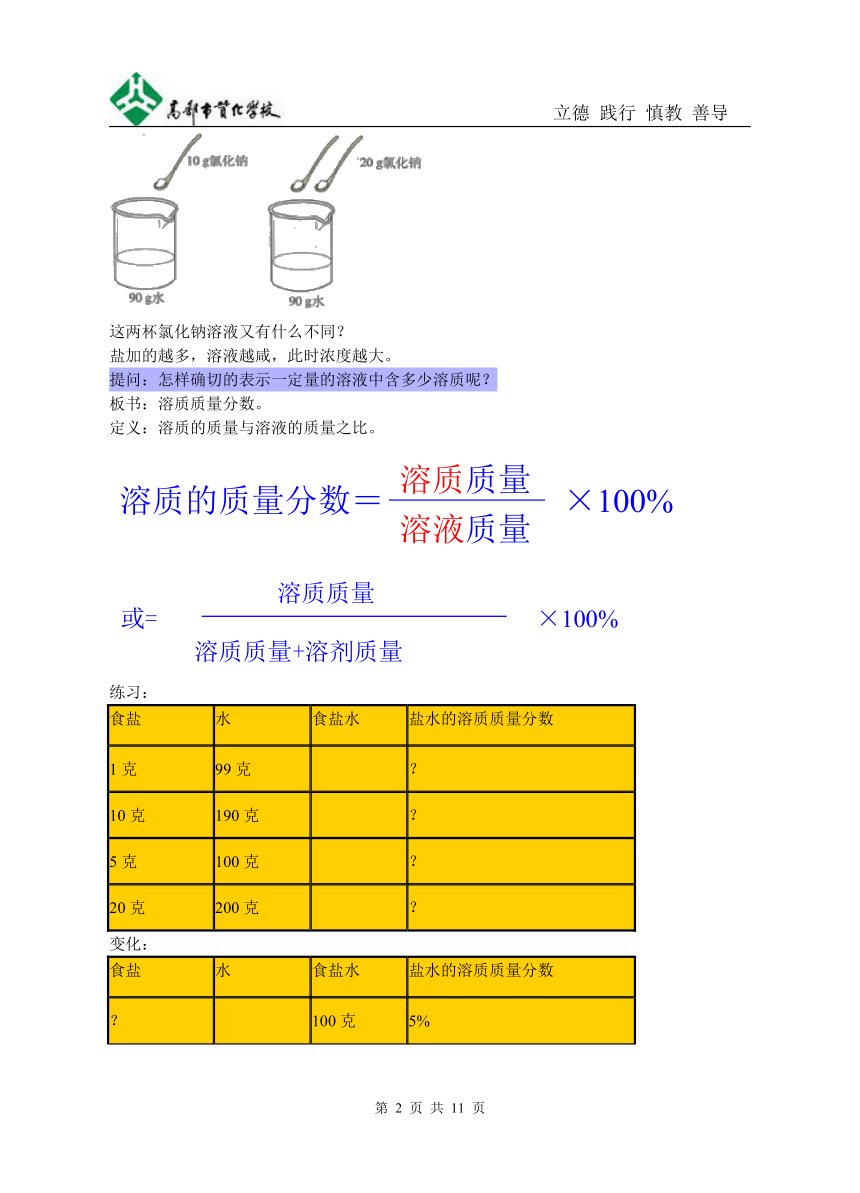
这两杯氯化钠溶液又有什么不同?
盐加的越多,溶液越咸,此时浓度越大。
提问:怎样确切的表示一定量的溶液中含多少溶质呢?
板书:溶质质量分数。
定义:溶质的质量与溶液的质量之比。
练习:
食盐 水 食盐水 盐水的溶质质量分数
1克 99克 ?
10克 190克 ?
5克 100克 ?
20克 200克 ?
变化:
食盐 水 食盐水 盐水的溶质质量分数
? 100克 5%
? 400克 15%
0.5克 10%
8克 ? ? 20%
下面我们来介绍一些有关溶液的计算。
1.有关溶液的基本计算
〖例1〗从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克氯化钾固体。试确定这瓶溶液中溶质的质量分数。
解:这瓶溶液中溶质的质量分数为:
答:这瓶溶液中氯化钾的质量分数为14%。
拓展:你有办法解决下列问题吗?
当堂巩固:
1、可以作为溶质的是
A.只有固体 B.只有液体
C.只有气体 D.气、液、固体均可
2、20%的蔗糖溶液中溶质、溶剂、溶液之间的质量比是
A. 1∶4∶5 B. 5∶4∶1
C. 4∶1∶5 D. 20∶80∶100
3、在常温下,向100g5%的氯化钠溶液中加入5g硝酸钾粉末完全溶解后,氯化钠的溶质质量分数将
A.增大 B.减小 C.不变 D.无法确定
4、溶质质量分数是表示 的一种方法,其数学意义是 之比。现有溶质质量分数为20%的氯化钠溶液,其20%表示的含义就是每 g氯化钠溶液中含有氯化钠 g。
5、医疗上的生理盐水是溶质质量分数约为0.9%的氯化钠溶液,现用1000g生理盐水给某病人输液,则有 克氯化钠和 克水进入病人体内。
请你来判断:
1、在100g水中溶解20g食盐,其溶质的质量分数为20 %
2、从质量分数为20%的100gNa2CO3 溶液中取出10g溶液,则取出的溶液中溶质的质量分数为2%
3、100gCuSO4溶液里含有17gCuSO4,若向其中加入3g无水CuSO4,使其完全溶解,则溶质的质量分数变为20 %
小结:当一瓶溶液中的溶质或溶剂的质量发生改变时,溶质的质量分数会发生改变;
当然若溶质和溶剂的质量成比例增加或减少时,质量分数不变。
2.有关溶液稀释的计算
〖例2〗把50g98%的硫酸稀释成20%的硫酸,需要水多少克
解:溶液稀释前后,溶质的质量不变。
稀释前、后溶质的质量为:
50g× 98%=49g
或
解:设需加水的质量为X
50g×98%=(50g+x)×20%
解之: x=195g
练习:在轧钢厂除锈工段里,要将1500千克质量分数为98%的浓硫酸稀释成10%的硫酸溶液,需用多少千克水?
课外作业:现有 80g 质量分数为 10% 的硝酸钠溶液,试通过计算回答下列问题:
1、上述硝酸钠溶液中含溶质质量和溶剂的质量各为多少克?
2、若向上述溶液中加入20 g 水,则所得溶液中溶质的质量分数为多少?
3、若向上述溶液中加入20 g 硝酸钠,则所得溶液中溶质的质量分数为多少?
4、若使上述溶液中溶质的质量分数变为 20%,则应加入硝酸钠多少克?
5、若使上述溶液中溶质的质量分数变为 20%,则应蒸发水多少克?
6、若使上述溶液中溶质的质量分数变为 5%,则应加水多少克?
课后思考:
日常生活中我们要科学地节约用水。现有一件刚用洗涤剂洗过的衣服,“拧干”后湿衣服上残留的溶液为100g,其中含洗涤剂的质量分数为1 %,则湿衣服上残留的洗涤剂质量为 g。现用5700g清水对这件衣服进行漂洗,有以下两种漂洗方法(假设每次“拧干”后湿衣服仍残留100g溶液)。
方法一:用5700g清水一次漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示) g;
方法二:将5700g清水均分成质量相等的三份(每份1900g),分三次漂洗。.第1次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示) g;第2次,再用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示)
g;第3次,再用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示) g。 由以上计算分析,用相同质量的水漂洗衣服,是一次漂洗效果好,还是将水等分成三份,分三次漂洗效果好?
教学后记:这部分的知识学生是有基础的,学习也不算费力,但是,要把质量分数的计算能学习的从实质上去理解,还要下功夫。最后一条题目,学生思考后认为能做,但是,大部分的学生都觉得会做而做不出来,教师点评后,大部分的学生都觉得真正的理解了,我的目的也达到了。
【科目】化学 【班级】九(7、17) 【日期】2007-12-3 【教者】郭从年
【课题】第二节 溶液组成的表示 【课时】2-2 【类型】新授
第二课时
教学目标:
1、练习涉及体积的溶液溶质质量分数的计算 。
2、练习反应后溶液的溶质质量分数的计算 。
3、积极主动与他人进行交流和讨论,形成良好的学习习惯和学习方法。
4、通过创设问题情景,提高分析问题与解决问题的能力,尝试编写计算应用题。
5、以计算为载体以生活实际为基础培养学生,理论联系实际的情感态度。
学习重难点:根据体积进行的溶液的配制的计算和稀释计算;反应后溶液中溶质质量分数的计算。
教学过程:
复习:
1.溶液组成的定量表示有许多种方法,其中最常使用的方法是溶质的质量分数。它的计算公式是 。溶质的质量分数越小,说明溶液中溶质的相对含量越 ,这时我们可以通过 、 等方法提高其质量分数;相反,溶质的质量分数越大,说明溶液中溶质的相对含量越 ,这时我们可以采取 、
等方法减小其质量分数。
2.从溶质的质量分数的计算公式,可以推断出溶质质量分数的大小只与 和
有关。
练习:
3.下列四种蔗糖溶液中,蔗糖的质量分数最大的是(A )
A.15g蔗糖溶于85g水中
B.150g水中溶解蔗糖30g
C.一定量蔗糖溶于80g水即制成100g硝酸钾溶液
D.85g蔗糖溶液中含有15g蔗糖
4.稀释某溶液时,溶液中保持不变的是(D )
A.溶液的质量 B.溶质的质量分数
C.溶剂的质量 D.溶质的质量
5.把100g质量分数为20%的食盐水分成两份,每一份溶液与原溶液相比,以下说法不正确的是(D )
A.溶液的质量为原来的一半 B.溶质的质量为原来的一半
C.溶剂的质量为原来的一半 D.溶质的质量分数为原来的一半
6.质量分数为25%的某溶液,其中溶质与溶剂的质量比为(A )
A.1:4 B.1:5
C.4:1 D.5:1
7.在100g10%的食盐水中加入100g水,则所得溶液(C )
A.溶剂质量不变 B.溶剂质量增加一倍
C.溶质质量分数变为原来的一半 D.溶液质量不变
8.把200g蔗糖溶液完全蒸干后,共得到固体50g,求原溶液中溶质的质量分数。
9.欲配制溶质质量分数为30%的糖水250g,需50%的糖水多少克?
新授:
3.涉及体积的溶液溶质质量分数的计算
〖例3〗配制500mL20%的硫酸需要98%的硫酸多少毫升
20%的硫酸的密度为1.14g/cm3,98%的硫酸的密度为1.84g/cm3。
设:需98%的硫酸的体积为x。
x × 1.84g/cm3 × 98% = 500 cm3 × 1.14g/cm3 × 20%
x = 63.2 cm3
答:配制500mL20%的硫酸需要63.2mL98%的硫酸。
练习:
练习:请看左图瓶上的标签,请计算要配制100g溶质质量分数14.6%的稀盐酸,需用这种浓盐酸多少毫升?
4.反应后溶液的溶质质量分数的计算
〖例4〗已知6.5g锌与100g稀硫酸,恰好完全反应,求所用稀硫酸溶质的质量分数是多少?
练习1:
32.5克锌与密度为 1.30g/cm3的硫酸溶液100毫升恰好完全反应,计算:(1)可制得氢气多少克?(2)硫酸溶液溶质质量分数为多少?(3)反应后溶液溶质的质量分数是多少?
答案:(1)可制得氢气1克(2)硫酸溶液溶质质量分数为37.7%(3)反应后溶液溶质的质量分数是49.8%
练习2:
金属钠与水反应的化学方程式为:2Na+2H2O==2NaOH+H2↑。将2.3g金属钠投入97.7g水中,充分反应后,所得溶液中溶质的质量分数为( )
A、等于2.3% B、等于4% C、小于4% D、大于4%
练习3:
(2005广东中考题)请根据右图要求,自编一道有关溶液的计算题,并进行解答。
小结:反应后所得溶液的质量=所有加入的物质-产生气体-沉淀-不溶性的物质。
课外作业:
第1题:2003年防非典期间,某医院要用含溶质质量分数为20%(密度为1.1g/cm3)的过氧乙酸溶液配制成溶质质量分数为0.4%(密度为1.0g/cm3)的消毒液15L,请问需要20%的过氧乙酸溶液体积是多少毫升?水多少毫升?
第2题:13 g锌可以跟100 g硫酸溶液恰好完全反应,计算:
(1)可制得氢气多少克?把溶液蒸干,得到多少克硫酸锌?
(2)这种硫酸溶液的溶质质量分数是多少?所得溶液的溶质质量分数是多少?
(3)100 g这种硫酸溶液稀释成10%的硫酸,需加水多少克?
教学后记:在解决课外第一题时,学生经过计算为现了这样一个问题,过氧已酸的体积与水的体积之和竞然小于所得混合液的体积,这是什么原因呢?其实液体间的混合,有可能总体积小于体积和,也可能大于它们的体积之和。
【科目】化学 【班级】九(7、17) 【日期】2007-12-3 【教者】郭从年
【课题】第二节 溶液组成的表示 【课时】2-2 【类型】新授
第三课时
教学目标:
1、复习涉及体积的溶液溶质质量分数的计算 。
2、复习根据体积进行的溶液的配制的计算和稀释计算。
3、让学生通过动手练习配制一定溶质质量分数的溶液,加深对溶质的质量分数的理解,熟练溶液配制和稀释的基本操作。
学习重难点:
熟练溶液配制和稀释的基本操作。
教学过程:
导入:前面我们学过了有关溶液中溶质质量分数的计算的题目,下面我们来看一条题目。
2003年防非典期间,某医院要用含溶质质量分数为20%(密度为1.1g/cm3)的过氧乙酸溶液配制成溶质质量分数为0.4%(密度为1.0g/cm3)的消毒液15L,请问需要20%的过氧乙酸溶液体积是多少毫升?水多少毫升?
做题前复习有关知识:
配制溶液时什么变了?什么没变?
质量、体积、密度之间的关系是什么?
学生做答。
展示部分学生的作业。
小结。
刚才我们学会了如何去计算所需的液体的体积,如果现在让我们去配制一定质量分数的溶液我们应该怎么做呢?
小组讨论:如何配制50克溶质质量分数为10%的氯化钠溶液?
小结。
小结:氯化钠溶液配制的主要步骤为三大步:1、计算;2、称量和量取;3、溶解;4、装瓶,贴上标签。
友情提醒:
托盘天平的使用的注意事项,量筒、胶头滴管使用的注意事项,搅拌时的注意事项。
学生实验。
小结刚才的学生实验。
练习1:下图是某同学配制一定质量的0.9%生理盐水的全过程:
(1)请找出上图中的错误:
① ;② 。
(2)如果配制的生理盐水中NaCl 的质量分数小于0.9%,则可能造成误差的原因有(至少举出三点)
① ② ③
提问:你能知道刚才配好的溶液的密度吗?
用质量除以体积。
生活中很多时候是用浓溶液来配制稀溶液。
如果用刚才配好的5%的氯化钠溶液来配制50g1%的氯化钠溶液。应该怎么做呢?
学生讨论。
小结:溶液稀释的主要步骤为三大步:1、计算;2、量取;3、溶解;4、装瓶,贴上标签。
还需要什么条件吗?
已知:通常状况下5%的氯化钠溶液的密度为1.03g/cm3。
学生实验。
求计算结果。V5%= VH2O=
小结刚才的学生实验。
练习2:现有24%的硝酸钾溶液、2%的硝酸钾溶液、硝酸钾固体和水。请选用上述不同的物质配制10%的硝酸钾溶液,将用量的最简整数比填入下表中相应的位置。
24%硝酸钾溶液 2%硝酸钾溶液 硝酸钾固体 水
示例 4 7
方案1
方案2
方案3
练习3:右图是病人输液时用的一瓶葡萄糖注射液 标签,请根据标签给出的数据计算该溶液中含水多少g,溶液的密度约为多少g/mL?葡萄糖注射液
练习4:配制质量分数为20%硫酸溶液460克,问需要98%的硫酸多少毫升?同时需要水多少毫升?(已知98%硫酸的密度为1.84克/厘米3)
练习5:生产上要用质量分数为10%的稀盐酸来清洗钢材,现需要用溶质质量分数为38%密度为1.19g/mL的浓盐酸来配制500克10%的盐酸溶液。请你和同学讨论,应如何配制,并将配制过程填入下面的空格中。
Ⅰ、请计算出所需浓盐酸的体积和水的体积:
。
Ⅱ、量取液体(并说明用什么规格的量筒):
。
Ⅲ、稀释:______________________________________。
Ⅳ、贴上标签。
教学后记:学生进行实验时,具体的操作并不到位,更对实验的目的不够明确,只是做一下,但是,学生在做完实验后,对固体溶质和液体溶质的溶液配制过程并不一样,目标达成。
×100%
溶质质量+溶剂质量
溶质质量
溶质的质量分数=
×100%
溶液质量
溶质质量
化学纯 500mL
浓盐酸(HCl)
含HCl 37 %
密度为1.18 g/cm3
或=
×100%= 14%
20g
2.8g
溶质的质量分数=
溶液质量
溶质质量
溶液质量=
溶质的质量分数
溶质质量
-50g = 195g
20%
49g
需要水的质量是:
Giucose in jection
规格:250mL内含葡糖12.5克
生产批号:0205203 2
有效期:至2006年3月
5%
姓名: 床号:
化学纯 500mL
浓盐酸(HCl)
含HCl 37 %
密度为1.18 g/cm3
稀释前后溶质质量在不变!
稀释后溶液中所含溶质
稀释前溶液中所含溶质
第 1 页 共 11 页
【科目】化学 【班级】 【日期】2007-12-3 【教者】杨艳
【课题】第二节 溶液组成的表示 【课时】2-1 【类型】新授
第二节 溶液组成的表示
第一课时
教学目的:
1.了解溶液组成的含义。
2.掌握用溶质的质量分数表示溶液组成的方法和部分有关计算。
重点难点:
1.重点:溶质质量分数的表示方法及关系式的含义。
2.难点:溶液组成的含义。
教学过程:
上一节我们认识了溶液。生活中对溶液的利用很多。
你知道下面瓶中标签是什么意思吗?
下面我们就来学习溶液组成的表示方法。
复习:
你知道溶液由哪几部分组成的吗?它们之间的质量有什么关系?
溶液由溶质和溶剂组成。
溶液质量 = 溶质质量 + 溶剂质量
观察:
这三支试管所装的硫酸铜溶液有什么不同?
颜色的深浅不一样。说明里面含硫酸铜的浓度不一样。
这两杯氯化钠溶液又有什么不同?
盐加的越多,溶液越咸,此时浓度越大。
提问:怎样确切的表示一定量的溶液中含多少溶质呢?
板书:溶质质量分数。
定义:溶质的质量与溶液的质量之比。
练习:
食盐 水 食盐水 盐水的溶质质量分数
1克 99克 ?
10克 190克 ?
5克 100克 ?
20克 200克 ?
变化:
食盐 水 食盐水 盐水的溶质质量分数
? 100克 5%
? 400克 15%
0.5克 10%
8克 ? ? 20%
下面我们来介绍一些有关溶液的计算。
1.有关溶液的基本计算
〖例1〗从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克氯化钾固体。试确定这瓶溶液中溶质的质量分数。
解:这瓶溶液中溶质的质量分数为:
答:这瓶溶液中氯化钾的质量分数为14%。
拓展:你有办法解决下列问题吗?
当堂巩固:
1、可以作为溶质的是
A.只有固体 B.只有液体
C.只有气体 D.气、液、固体均可
2、20%的蔗糖溶液中溶质、溶剂、溶液之间的质量比是
A. 1∶4∶5 B. 5∶4∶1
C. 4∶1∶5 D. 20∶80∶100
3、在常温下,向100g5%的氯化钠溶液中加入5g硝酸钾粉末完全溶解后,氯化钠的溶质质量分数将
A.增大 B.减小 C.不变 D.无法确定
4、溶质质量分数是表示 的一种方法,其数学意义是 之比。现有溶质质量分数为20%的氯化钠溶液,其20%表示的含义就是每 g氯化钠溶液中含有氯化钠 g。
5、医疗上的生理盐水是溶质质量分数约为0.9%的氯化钠溶液,现用1000g生理盐水给某病人输液,则有 克氯化钠和 克水进入病人体内。
请你来判断:
1、在100g水中溶解20g食盐,其溶质的质量分数为20 %
2、从质量分数为20%的100gNa2CO3 溶液中取出10g溶液,则取出的溶液中溶质的质量分数为2%
3、100gCuSO4溶液里含有17gCuSO4,若向其中加入3g无水CuSO4,使其完全溶解,则溶质的质量分数变为20 %
小结:当一瓶溶液中的溶质或溶剂的质量发生改变时,溶质的质量分数会发生改变;
当然若溶质和溶剂的质量成比例增加或减少时,质量分数不变。
2.有关溶液稀释的计算
〖例2〗把50g98%的硫酸稀释成20%的硫酸,需要水多少克
解:溶液稀释前后,溶质的质量不变。
稀释前、后溶质的质量为:
50g× 98%=49g
或
解:设需加水的质量为X
50g×98%=(50g+x)×20%
解之: x=195g
练习:在轧钢厂除锈工段里,要将1500千克质量分数为98%的浓硫酸稀释成10%的硫酸溶液,需用多少千克水?
课外作业:现有 80g 质量分数为 10% 的硝酸钠溶液,试通过计算回答下列问题:
1、上述硝酸钠溶液中含溶质质量和溶剂的质量各为多少克?
2、若向上述溶液中加入20 g 水,则所得溶液中溶质的质量分数为多少?
3、若向上述溶液中加入20 g 硝酸钠,则所得溶液中溶质的质量分数为多少?
4、若使上述溶液中溶质的质量分数变为 20%,则应加入硝酸钠多少克?
5、若使上述溶液中溶质的质量分数变为 20%,则应蒸发水多少克?
6、若使上述溶液中溶质的质量分数变为 5%,则应加水多少克?
课后思考:
日常生活中我们要科学地节约用水。现有一件刚用洗涤剂洗过的衣服,“拧干”后湿衣服上残留的溶液为100g,其中含洗涤剂的质量分数为1 %,则湿衣服上残留的洗涤剂质量为 g。现用5700g清水对这件衣服进行漂洗,有以下两种漂洗方法(假设每次“拧干”后湿衣服仍残留100g溶液)。
方法一:用5700g清水一次漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示) g;
方法二:将5700g清水均分成质量相等的三份(每份1900g),分三次漂洗。.第1次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示) g;第2次,再用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示)
g;第3次,再用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示) g。 由以上计算分析,用相同质量的水漂洗衣服,是一次漂洗效果好,还是将水等分成三份,分三次漂洗效果好?
教学后记:这部分的知识学生是有基础的,学习也不算费力,但是,要把质量分数的计算能学习的从实质上去理解,还要下功夫。最后一条题目,学生思考后认为能做,但是,大部分的学生都觉得会做而做不出来,教师点评后,大部分的学生都觉得真正的理解了,我的目的也达到了。
【科目】化学 【班级】九(7、17) 【日期】2007-12-3 【教者】郭从年
【课题】第二节 溶液组成的表示 【课时】2-2 【类型】新授
第二课时
教学目标:
1、练习涉及体积的溶液溶质质量分数的计算 。
2、练习反应后溶液的溶质质量分数的计算 。
3、积极主动与他人进行交流和讨论,形成良好的学习习惯和学习方法。
4、通过创设问题情景,提高分析问题与解决问题的能力,尝试编写计算应用题。
5、以计算为载体以生活实际为基础培养学生,理论联系实际的情感态度。
学习重难点:根据体积进行的溶液的配制的计算和稀释计算;反应后溶液中溶质质量分数的计算。
教学过程:
复习:
1.溶液组成的定量表示有许多种方法,其中最常使用的方法是溶质的质量分数。它的计算公式是 。溶质的质量分数越小,说明溶液中溶质的相对含量越 ,这时我们可以通过 、 等方法提高其质量分数;相反,溶质的质量分数越大,说明溶液中溶质的相对含量越 ,这时我们可以采取 、
等方法减小其质量分数。
2.从溶质的质量分数的计算公式,可以推断出溶质质量分数的大小只与 和
有关。
练习:
3.下列四种蔗糖溶液中,蔗糖的质量分数最大的是(A )
A.15g蔗糖溶于85g水中
B.150g水中溶解蔗糖30g
C.一定量蔗糖溶于80g水即制成100g硝酸钾溶液
D.85g蔗糖溶液中含有15g蔗糖
4.稀释某溶液时,溶液中保持不变的是(D )
A.溶液的质量 B.溶质的质量分数
C.溶剂的质量 D.溶质的质量
5.把100g质量分数为20%的食盐水分成两份,每一份溶液与原溶液相比,以下说法不正确的是(D )
A.溶液的质量为原来的一半 B.溶质的质量为原来的一半
C.溶剂的质量为原来的一半 D.溶质的质量分数为原来的一半
6.质量分数为25%的某溶液,其中溶质与溶剂的质量比为(A )
A.1:4 B.1:5
C.4:1 D.5:1
7.在100g10%的食盐水中加入100g水,则所得溶液(C )
A.溶剂质量不变 B.溶剂质量增加一倍
C.溶质质量分数变为原来的一半 D.溶液质量不变
8.把200g蔗糖溶液完全蒸干后,共得到固体50g,求原溶液中溶质的质量分数。
9.欲配制溶质质量分数为30%的糖水250g,需50%的糖水多少克?
新授:
3.涉及体积的溶液溶质质量分数的计算
〖例3〗配制500mL20%的硫酸需要98%的硫酸多少毫升
20%的硫酸的密度为1.14g/cm3,98%的硫酸的密度为1.84g/cm3。
设:需98%的硫酸的体积为x。
x × 1.84g/cm3 × 98% = 500 cm3 × 1.14g/cm3 × 20%
x = 63.2 cm3
答:配制500mL20%的硫酸需要63.2mL98%的硫酸。
练习:
练习:请看左图瓶上的标签,请计算要配制100g溶质质量分数14.6%的稀盐酸,需用这种浓盐酸多少毫升?
4.反应后溶液的溶质质量分数的计算
〖例4〗已知6.5g锌与100g稀硫酸,恰好完全反应,求所用稀硫酸溶质的质量分数是多少?
练习1:
32.5克锌与密度为 1.30g/cm3的硫酸溶液100毫升恰好完全反应,计算:(1)可制得氢气多少克?(2)硫酸溶液溶质质量分数为多少?(3)反应后溶液溶质的质量分数是多少?
答案:(1)可制得氢气1克(2)硫酸溶液溶质质量分数为37.7%(3)反应后溶液溶质的质量分数是49.8%
练习2:
金属钠与水反应的化学方程式为:2Na+2H2O==2NaOH+H2↑。将2.3g金属钠投入97.7g水中,充分反应后,所得溶液中溶质的质量分数为( )
A、等于2.3% B、等于4% C、小于4% D、大于4%
练习3:
(2005广东中考题)请根据右图要求,自编一道有关溶液的计算题,并进行解答。
小结:反应后所得溶液的质量=所有加入的物质-产生气体-沉淀-不溶性的物质。
课外作业:
第1题:2003年防非典期间,某医院要用含溶质质量分数为20%(密度为1.1g/cm3)的过氧乙酸溶液配制成溶质质量分数为0.4%(密度为1.0g/cm3)的消毒液15L,请问需要20%的过氧乙酸溶液体积是多少毫升?水多少毫升?
第2题:13 g锌可以跟100 g硫酸溶液恰好完全反应,计算:
(1)可制得氢气多少克?把溶液蒸干,得到多少克硫酸锌?
(2)这种硫酸溶液的溶质质量分数是多少?所得溶液的溶质质量分数是多少?
(3)100 g这种硫酸溶液稀释成10%的硫酸,需加水多少克?
教学后记:在解决课外第一题时,学生经过计算为现了这样一个问题,过氧已酸的体积与水的体积之和竞然小于所得混合液的体积,这是什么原因呢?其实液体间的混合,有可能总体积小于体积和,也可能大于它们的体积之和。
【科目】化学 【班级】九(7、17) 【日期】2007-12-3 【教者】郭从年
【课题】第二节 溶液组成的表示 【课时】2-2 【类型】新授
第三课时
教学目标:
1、复习涉及体积的溶液溶质质量分数的计算 。
2、复习根据体积进行的溶液的配制的计算和稀释计算。
3、让学生通过动手练习配制一定溶质质量分数的溶液,加深对溶质的质量分数的理解,熟练溶液配制和稀释的基本操作。
学习重难点:
熟练溶液配制和稀释的基本操作。
教学过程:
导入:前面我们学过了有关溶液中溶质质量分数的计算的题目,下面我们来看一条题目。
2003年防非典期间,某医院要用含溶质质量分数为20%(密度为1.1g/cm3)的过氧乙酸溶液配制成溶质质量分数为0.4%(密度为1.0g/cm3)的消毒液15L,请问需要20%的过氧乙酸溶液体积是多少毫升?水多少毫升?
做题前复习有关知识:
配制溶液时什么变了?什么没变?
质量、体积、密度之间的关系是什么?
学生做答。
展示部分学生的作业。
小结。
刚才我们学会了如何去计算所需的液体的体积,如果现在让我们去配制一定质量分数的溶液我们应该怎么做呢?
小组讨论:如何配制50克溶质质量分数为10%的氯化钠溶液?
小结。
小结:氯化钠溶液配制的主要步骤为三大步:1、计算;2、称量和量取;3、溶解;4、装瓶,贴上标签。
友情提醒:
托盘天平的使用的注意事项,量筒、胶头滴管使用的注意事项,搅拌时的注意事项。
学生实验。
小结刚才的学生实验。
练习1:下图是某同学配制一定质量的0.9%生理盐水的全过程:
(1)请找出上图中的错误:
① ;② 。
(2)如果配制的生理盐水中NaCl 的质量分数小于0.9%,则可能造成误差的原因有(至少举出三点)
① ② ③
提问:你能知道刚才配好的溶液的密度吗?
用质量除以体积。
生活中很多时候是用浓溶液来配制稀溶液。
如果用刚才配好的5%的氯化钠溶液来配制50g1%的氯化钠溶液。应该怎么做呢?
学生讨论。
小结:溶液稀释的主要步骤为三大步:1、计算;2、量取;3、溶解;4、装瓶,贴上标签。
还需要什么条件吗?
已知:通常状况下5%的氯化钠溶液的密度为1.03g/cm3。
学生实验。
求计算结果。V5%= VH2O=
小结刚才的学生实验。
练习2:现有24%的硝酸钾溶液、2%的硝酸钾溶液、硝酸钾固体和水。请选用上述不同的物质配制10%的硝酸钾溶液,将用量的最简整数比填入下表中相应的位置。
24%硝酸钾溶液 2%硝酸钾溶液 硝酸钾固体 水
示例 4 7
方案1
方案2
方案3
练习3:右图是病人输液时用的一瓶葡萄糖注射液 标签,请根据标签给出的数据计算该溶液中含水多少g,溶液的密度约为多少g/mL?葡萄糖注射液
练习4:配制质量分数为20%硫酸溶液460克,问需要98%的硫酸多少毫升?同时需要水多少毫升?(已知98%硫酸的密度为1.84克/厘米3)
练习5:生产上要用质量分数为10%的稀盐酸来清洗钢材,现需要用溶质质量分数为38%密度为1.19g/mL的浓盐酸来配制500克10%的盐酸溶液。请你和同学讨论,应如何配制,并将配制过程填入下面的空格中。
Ⅰ、请计算出所需浓盐酸的体积和水的体积:
。
Ⅱ、量取液体(并说明用什么规格的量筒):
。
Ⅲ、稀释:______________________________________。
Ⅳ、贴上标签。
教学后记:学生进行实验时,具体的操作并不到位,更对实验的目的不够明确,只是做一下,但是,学生在做完实验后,对固体溶质和液体溶质的溶液配制过程并不一样,目标达成。
×100%
溶质质量+溶剂质量
溶质质量
溶质的质量分数=
×100%
溶液质量
溶质质量
化学纯 500mL
浓盐酸(HCl)
含HCl 37 %
密度为1.18 g/cm3
或=
×100%= 14%
20g
2.8g
溶质的质量分数=
溶液质量
溶质质量
溶液质量=
溶质的质量分数
溶质质量
-50g = 195g
20%
49g
需要水的质量是:
Giucose in jection
规格:250mL内含葡糖12.5克
生产批号:0205203 2
有效期:至2006年3月
5%
姓名: 床号:
化学纯 500mL
浓盐酸(HCl)
含HCl 37 %
密度为1.18 g/cm3
稀释前后溶质质量在不变!
稀释后溶液中所含溶质
稀释前溶液中所含溶质
第 1 页 共 11 页
