6.2溶液组成的表示
图片预览







文档简介
课件20张PPT。第二节 溶液组成的表示教学目的:
1.了解溶液组成的含义。
2.掌握用溶质的质量分数表示溶液组成的方法和部分有关计算。
重点难点:
1.重点:溶质质量分数的表示方法及关系式的含义。
2.难点:溶液组成的含义。 你知道溶液由哪几部分组成的吗?它们之间
的质量有什么关系? 溶质:被溶解的物质
溶剂:溶解其它物质的物质溶质可以是固体、液体,也可以是气体。
水是最常用的溶剂
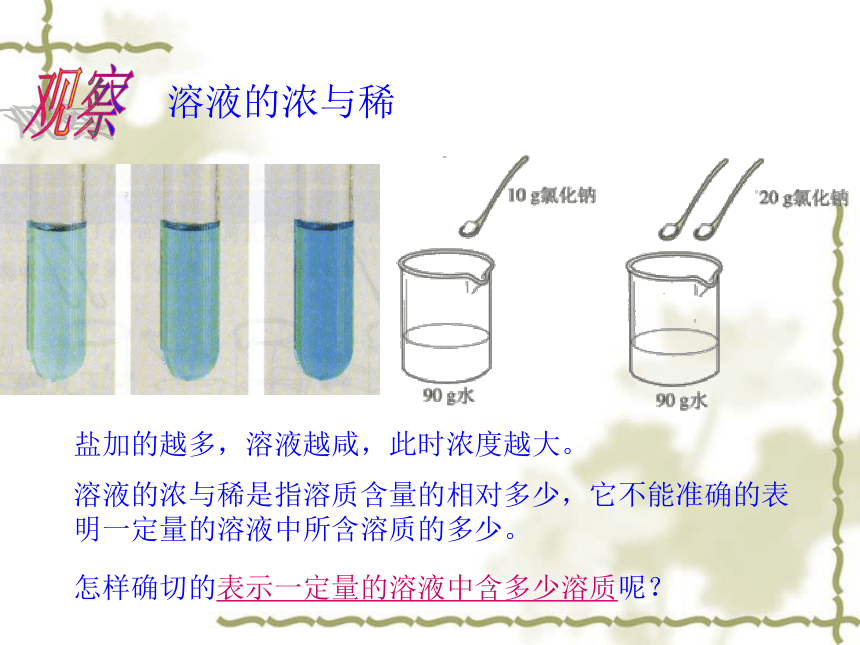
溶液质量 = 溶质质量 + 溶剂质量溶液盐加的越多,溶液越咸,此时浓度越大。溶液的浓与稀是指溶质含量的相对多少,它不能准确的表明一定量的溶液中所含溶质的多少。怎样确切的表示一定量的溶液中含多少溶质呢?观察溶液的浓与稀一、溶质的质量分数计算:定义:溶质的质量与溶液的质量之比。溶液组成的表示方法
溶质质量 —————溶液质量X 100%溶质的质量分数=
溶质的质量分数是表示溶液组成的方法之一。
仔细观察这个式子,你能得出哪些信息?交流与合作1.溶质的质量分数是由——和 ——共同决定的。
2. 关系式中——作分子,——作分母。
3. 结果用——表示,且小于1。
4 .与浓稀的关系是——。
5. 得出两个关系式:溶质的质量=溶液 的质量 X 溶质的质量分数
溶液 的质量=溶质的质量 / 溶质的质量分数
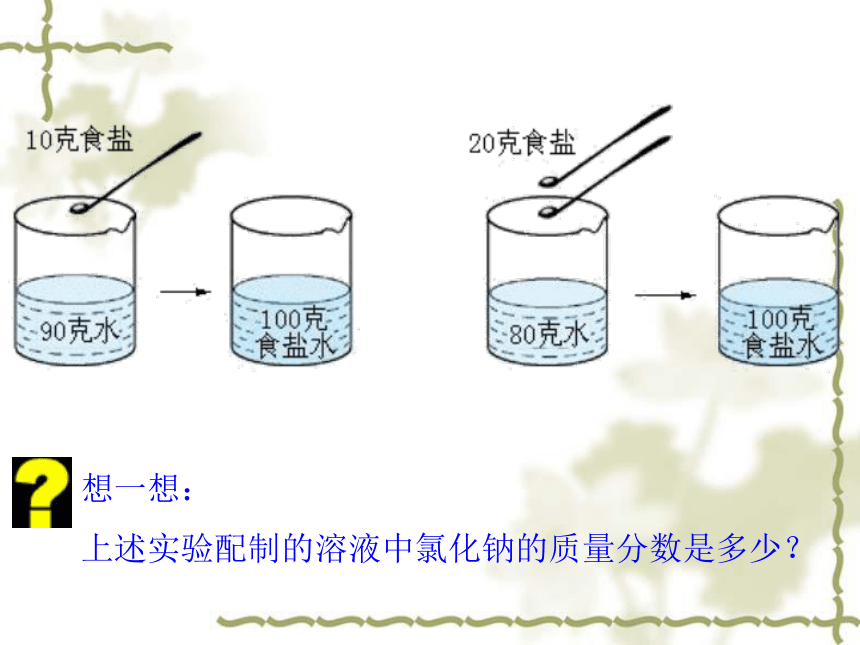
想一想:
上述实验配制的溶液中氯化钠的质量分数是多少?二、溶液中溶质的质量分数计算 〖例1〗从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克氯化钾固体。试确定这瓶溶液中溶质的质量分数。这瓶溶液中溶质的质量分数为:答:这瓶溶液中氯化钾的质量分数为14%。〖例2〗把50g98%的硫酸稀释成20%的硫酸,需要水多少克?解:溶液稀释前后,溶质的质量不变。稀释前、后溶质的质量为:
50g× 98%=49g综合列式求解解:设需加水的质量为X
50g×98%=(50g+x) ×20%
解之: x=195g〖例3〗配制500mL20%的硫酸需要98%的硫酸多少毫升?解:查硫酸密度和溶质质量分数对照表得出:20%的硫酸的密
度为1.14g/cm3,98%的硫酸的密度为1.84g/cm3。设:需98%的硫酸的体积为x。稀释前后溶质质量在不变!x × 1.84g/cm3 × 98% = 500 cm3 × 1.14g/cm3 × 20%稀释前溶液中所含溶质稀释后溶液中所含溶质x = 63.2 cm3答:配制500mL20%的硫酸需要63.2mL98%的硫酸。你真棒!1、10% 的蔗糖溶液表示什么意思?2、要配制50g10 % 的KNO3溶液,需要
g KNO3 固体和 g水?3、5 L 30 %的硫酸溶液(密度为1.22g/cm3)
中含有纯硫酸 g。快速抢答:请你来判断: 1、 在100g水中溶解20g食盐,其溶质的质量分数为20 % 2、从质量分数为20%的100gNa2CO3 溶液中取出10g溶液,则取出的溶液中溶质的质量分数为2% 3、100gCuSO4溶液里含有17gCuSO4,若向其中加入3g无水CuSO4,使其完全溶解,则溶质的质量分数变为20 %你已经知道了:
当一瓶溶液中的溶质或溶剂的质量发生改变时,溶质的质量分数会发生改变;
当然若溶质和溶剂的质量成比例增加或减少时,质量分数不变。
要使一瓶100g10%的NaOH溶液的溶质质量分数发生改变,看谁想的办法多??
放飞你想象的翅膀 配制某溶质的一定质量分数的溶液
步骤及所需仪器:1、计算:2、称量:3、溶解:天平、药匙、量筒、胶头滴管烧杯、玻璃棒基础训练: 一瓶溶液,若将其蒸发一部水或向其中加少量的水,溶质的质量、溶剂的质量、溶液的质量、溶质的质量分数将如何变化?关于稀释或浓缩问题的计算化学纯 500mL
浓盐酸(HCl)
含HCl 37 %
密度为1.18 g/cm3
这是从实验室取来的未开封的一瓶浓盐酸,请根据标签内容回答:
溶质的化学名称:
化学式 :
其中溶质的质量分数是:
溶质的质量是:
溶剂的质量是:
关于稀释或浓缩问题的计算
基础训练:1、计算:
2、量取浓盐酸和水:
3、稀释(配制溶液): 请你用我刚才实验室中提供的一瓶浓盐酸,来配制50g溶质质量分数为5%的盐酸溶液,将有关步骤简要地填在下面的空格中:
1.了解溶液组成的含义。
2.掌握用溶质的质量分数表示溶液组成的方法和部分有关计算。
重点难点:
1.重点:溶质质量分数的表示方法及关系式的含义。
2.难点:溶液组成的含义。 你知道溶液由哪几部分组成的吗?它们之间
的质量有什么关系? 溶质:被溶解的物质
溶剂:溶解其它物质的物质溶质可以是固体、液体,也可以是气体。
水是最常用的溶剂
溶液质量 = 溶质质量 + 溶剂质量溶液盐加的越多,溶液越咸,此时浓度越大。溶液的浓与稀是指溶质含量的相对多少,它不能准确的表明一定量的溶液中所含溶质的多少。怎样确切的表示一定量的溶液中含多少溶质呢?观察溶液的浓与稀一、溶质的质量分数计算:定义:溶质的质量与溶液的质量之比。溶液组成的表示方法
溶质质量 —————溶液质量X 100%溶质的质量分数=
溶质的质量分数是表示溶液组成的方法之一。
仔细观察这个式子,你能得出哪些信息?交流与合作1.溶质的质量分数是由——和 ——共同决定的。
2. 关系式中——作分子,——作分母。
3. 结果用——表示,且小于1。
4 .与浓稀的关系是——。
5. 得出两个关系式:溶质的质量=溶液 的质量 X 溶质的质量分数
溶液 的质量=溶质的质量 / 溶质的质量分数
想一想:
上述实验配制的溶液中氯化钠的质量分数是多少?二、溶液中溶质的质量分数计算 〖例1〗从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克氯化钾固体。试确定这瓶溶液中溶质的质量分数。这瓶溶液中溶质的质量分数为:答:这瓶溶液中氯化钾的质量分数为14%。〖例2〗把50g98%的硫酸稀释成20%的硫酸,需要水多少克?解:溶液稀释前后,溶质的质量不变。稀释前、后溶质的质量为:
50g× 98%=49g综合列式求解解:设需加水的质量为X
50g×98%=(50g+x) ×20%
解之: x=195g〖例3〗配制500mL20%的硫酸需要98%的硫酸多少毫升?解:查硫酸密度和溶质质量分数对照表得出:20%的硫酸的密
度为1.14g/cm3,98%的硫酸的密度为1.84g/cm3。设:需98%的硫酸的体积为x。稀释前后溶质质量在不变!x × 1.84g/cm3 × 98% = 500 cm3 × 1.14g/cm3 × 20%稀释前溶液中所含溶质稀释后溶液中所含溶质x = 63.2 cm3答:配制500mL20%的硫酸需要63.2mL98%的硫酸。你真棒!1、10% 的蔗糖溶液表示什么意思?2、要配制50g10 % 的KNO3溶液,需要
g KNO3 固体和 g水?3、5 L 30 %的硫酸溶液(密度为1.22g/cm3)
中含有纯硫酸 g。快速抢答:请你来判断: 1、 在100g水中溶解20g食盐,其溶质的质量分数为20 % 2、从质量分数为20%的100gNa2CO3 溶液中取出10g溶液,则取出的溶液中溶质的质量分数为2% 3、100gCuSO4溶液里含有17gCuSO4,若向其中加入3g无水CuSO4,使其完全溶解,则溶质的质量分数变为20 %你已经知道了:
当一瓶溶液中的溶质或溶剂的质量发生改变时,溶质的质量分数会发生改变;
当然若溶质和溶剂的质量成比例增加或减少时,质量分数不变。
要使一瓶100g10%的NaOH溶液的溶质质量分数发生改变,看谁想的办法多??
放飞你想象的翅膀 配制某溶质的一定质量分数的溶液
步骤及所需仪器:1、计算:2、称量:3、溶解:天平、药匙、量筒、胶头滴管烧杯、玻璃棒基础训练: 一瓶溶液,若将其蒸发一部水或向其中加少量的水,溶质的质量、溶剂的质量、溶液的质量、溶质的质量分数将如何变化?关于稀释或浓缩问题的计算化学纯 500mL
浓盐酸(HCl)
含HCl 37 %
密度为1.18 g/cm3
这是从实验室取来的未开封的一瓶浓盐酸,请根据标签内容回答:
溶质的化学名称:
化学式 :
其中溶质的质量分数是:
溶质的质量是:
溶剂的质量是:
关于稀释或浓缩问题的计算
基础训练:1、计算:
2、量取浓盐酸和水:
3、稀释(配制溶液): 请你用我刚才实验室中提供的一瓶浓盐酸,来配制50g溶质质量分数为5%的盐酸溶液,将有关步骤简要地填在下面的空格中:
