常见的酸和碱
图片预览







文档简介
课件22张PPT。常见的酸和碱1. 下列说法不正确的是 ( )
A.盐酸与碳酸钠反应,溶液中有气泡冒出
B.盐酸和铁粉反应后溶液呈黄色
C.盐酸使紫色石蕊试液变红色
D.盐酸可除去铁制品表面的锈
2.某一无色溶液具有如下性质:①使无色酚酞试液变红;②与硫酸铜溶液反应可产生蓝色沉淀;③与碳酸钠溶液反应产生白色沉淀,据以上推断,此溶液是( )
A.氢氧化钠溶液 B.澄清石灰水
C.氯化钙溶液 D.盐酸1、能和酸碱指示剂反应
2、能与活泼金属反应
3、能与金属氧化物反应
4、能与碱反应
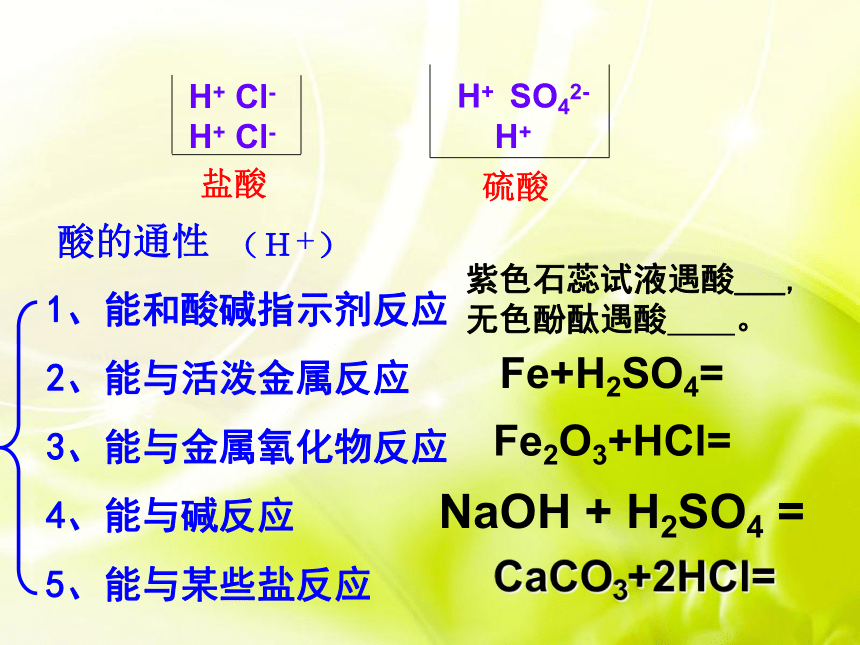
5、能与某些盐反应H+ Cl-
H+ Cl- H+ SO42-
H+盐酸硫酸酸的通性(H+)紫色石蕊试液遇酸___,无色酚酞遇酸 。Fe+H2SO4=CaCO3+2HCl=NaOH + H2SO4 =Fe2O3+HCl=1、能与指示剂作用
2、能与非金属氧化物反应
3、能与酸的反应
4、能与某些盐反应碱的通性(OH--) OH- Ca2+
OH- OH-
Na+氢氧化钠氢氧化钙紫色石蕊试液遇碱____,无色酚酞遇碱 。CO2+NaOH=NaOH + H2SO4=Ca(OH)2+Na2CO3=实验室里有两瓶失去标签的无色溶液,分别是稀硫酸和澄清石灰水,请你用两种方法,加以鉴别,完成下表。K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au金属活动性顺序表:金属活动性由强逐渐减弱初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请你认真填写下面的空白:
(1)金属活动性顺序表:
K Ca Na __ Al Zn Fe Sn Pb(H) Cu ___ Ag Pt Au
(2)金属与酸反应的规律是______________。
试举出实验应用的实例(可用化学方程式表示):____
__________________。
(3)金属与盐发生置换反应必须符合三点:
①K、Ca、Na三种金属非常活泼,不能把金属直接
从其盐溶液中置换出来;
②________________; ③_________________。
试举出实验应用的实例(可用化学方程式表示)____________________。 为验证Fe、Cu、Ag三种金属的活动性是依次减弱的,某化学兴趣小组设计了图2所示的四个实验。其中不必进行的是( )人体胃液中含有适量的盐酸,可以帮助消化。胃液的PH通常在0.9-1.5之间,超出这一范围,会引起胃部不适。以下是两位患者分别从医生处得到的药方的一部分。病人甲病人乙每日遵医嘱口服
胃舒平[主要成分Al(OH)3]每日遵医嘱口服
0.3﹪盐酸(主要成分HCl)(1)分别判断两位病人患胃病的情况。
(2)病人乙服用的药物,可用一种常见的调味品代替。这种调味品是什么?
(3)写出胃舒平治病时发生的化学方程式。当人被蚊虫叮咬(蚊虫叮咬时会向体内排放含有酸性物质的毒液)后,可在叮咬处涂抹 以减轻疼痛。肥皂水中和反应的应用:Why实验室中,小明发现准备桌上有一瓶试剂:用完的试剂这样放置会造成什么后果?氢氧化钠固体吸收水分氢氧化钠溶液吸收二氧化碳碳酸钠溶液水分蒸发碳酸钠固体吸水潮解与二氧化碳反应变质必须密封保存药品的保存:
浓盐酸
浓硫酸
生石灰
氢氧化钠固体
氢氧化钠溶液、氢氧化钙溶液引起变化的原因分别是什么?其中,会变质的有哪些?下列物质敞口放置在空气中,因发生化学变化而质量增加的是( )
A.浓硫酸 B.浓盐酸
C.氢氧化钠 D.氯化钠1.下列物质的俗名、学名、化学式三者表示同一物质的是 ( )
A、生石灰、氢氧化钙、CaO
B、纯碱、氢氧化钠、NaOH
C、小苏打、碳酸氢钠、NaHCO3
D、盐酸、氯化氢、HCl
2.混有水蒸气的下列气体中,既可以用浓硫酸干燥,又可以用苛性钠干燥的是( )
A.氧气 B.氨气
C.二氧化碳 D.氯化氢经典在线:3.下列物质能使酚酞试液变红色的是( )
A盐酸 B氢氧化钠溶液
C氯化钠溶液 D氢氧化铜
4.实验表明,用碱性溶液浸泡新鲜的蔬菜,能有效除去蔬菜上的残留农药,从而降低对人体的损害。根据上述原理,对刚买回来的蔬菜,你认为应浸泡在哪种溶液中( )
A.白酒 B.食醋
C.烧碱溶液 D.碳酸钠溶液5.下列物质能用稀酸和金属直接反应制取的是( )
A.CuSO4 B. FeCl3
C. MgSO4 D. AgCl
6. 氯化钙溶液中含少量盐酸,在没有指示剂的条件下为除去盐酸可选用( )
A、熟石灰 B、生石灰
C、石灰石 D、纯碱7. 右图所示的锥形瓶内充满气体X,胶头滴管内盛有液体Y,挤压胶头滴管,使液体Y进入瓶中,振荡,一会儿可见套在玻璃管下端的小气球a鼓起。气体X和液体Y可能是( )
A、X是CO2,Y是NaOH溶液
B、X是CO2,Y是稀硫酸
C、X是CaO,Y是水
D、X是CO,Y是石灰水8、人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛。小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图19所示。
为了验证该药物的主要成分是碳酸盐,他进行了如下实验:首先将药片放入试管中,向其中加入适量的稀盐酸,然后______
_____(写实验操作和实验现象)。 当小军看到药物说明书上的服用方法后,对此产生了探究的兴趣,请你和他一起完成探究活动。
【提出问题】抗酸药为什么嚼碎后服用?
【作出猜想】他的猜想是 。
【设计实验】实验一:将一片完整的药片放入试管中,向其中加入5mL5%的稀盐酸;
实验二:将 放入试管中,向其中加入5mL5%的稀盐酸。【现象与结论】实验二比实验一反应快。证明小军的猜想正确。
【拓展探究】(1)氢氧化镁、碳酸钙、碳酸氢钠等也常用于制作抗酸药。这些物质必须具备两个条件:一是能与胃酸作用;二是__________________。
(2)患有胃溃疡(胃黏膜溃烂)的病人胃酸过多时,不宜服用含碳酸盐的抗酸药,其原因是_________________________。
A.盐酸与碳酸钠反应,溶液中有气泡冒出
B.盐酸和铁粉反应后溶液呈黄色
C.盐酸使紫色石蕊试液变红色
D.盐酸可除去铁制品表面的锈
2.某一无色溶液具有如下性质:①使无色酚酞试液变红;②与硫酸铜溶液反应可产生蓝色沉淀;③与碳酸钠溶液反应产生白色沉淀,据以上推断,此溶液是( )
A.氢氧化钠溶液 B.澄清石灰水
C.氯化钙溶液 D.盐酸1、能和酸碱指示剂反应
2、能与活泼金属反应
3、能与金属氧化物反应
4、能与碱反应
5、能与某些盐反应H+ Cl-
H+ Cl- H+ SO42-
H+盐酸硫酸酸的通性(H+)紫色石蕊试液遇酸___,无色酚酞遇酸 。Fe+H2SO4=CaCO3+2HCl=NaOH + H2SO4 =Fe2O3+HCl=1、能与指示剂作用
2、能与非金属氧化物反应
3、能与酸的反应
4、能与某些盐反应碱的通性(OH--) OH- Ca2+
OH- OH-
Na+氢氧化钠氢氧化钙紫色石蕊试液遇碱____,无色酚酞遇碱 。CO2+NaOH=NaOH + H2SO4=Ca(OH)2+Na2CO3=实验室里有两瓶失去标签的无色溶液,分别是稀硫酸和澄清石灰水,请你用两种方法,加以鉴别,完成下表。K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au金属活动性顺序表:金属活动性由强逐渐减弱初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请你认真填写下面的空白:
(1)金属活动性顺序表:
K Ca Na __ Al Zn Fe Sn Pb(H) Cu ___ Ag Pt Au
(2)金属与酸反应的规律是______________。
试举出实验应用的实例(可用化学方程式表示):____
__________________。
(3)金属与盐发生置换反应必须符合三点:
①K、Ca、Na三种金属非常活泼,不能把金属直接
从其盐溶液中置换出来;
②________________; ③_________________。
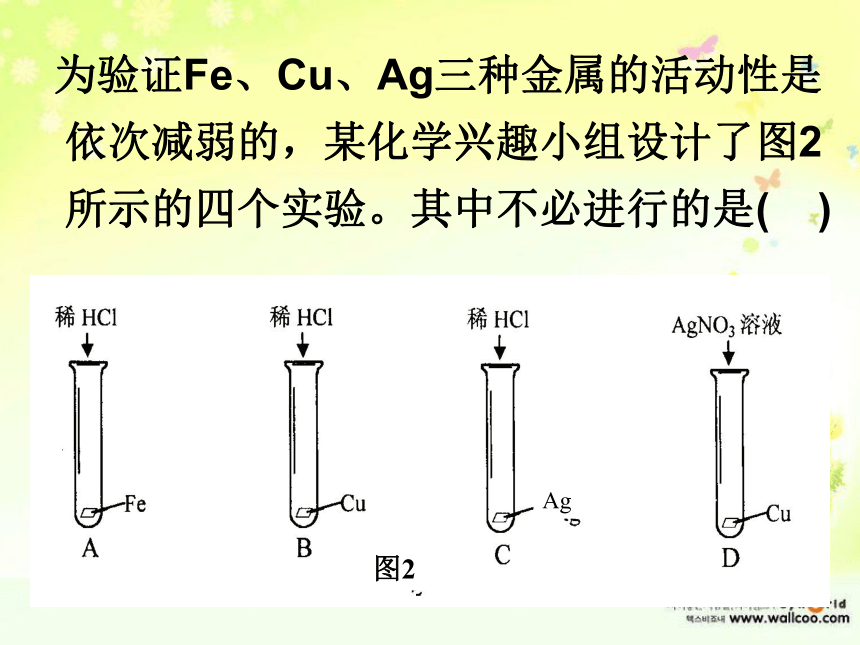
试举出实验应用的实例(可用化学方程式表示)____________________。 为验证Fe、Cu、Ag三种金属的活动性是依次减弱的,某化学兴趣小组设计了图2所示的四个实验。其中不必进行的是( )人体胃液中含有适量的盐酸,可以帮助消化。胃液的PH通常在0.9-1.5之间,超出这一范围,会引起胃部不适。以下是两位患者分别从医生处得到的药方的一部分。病人甲病人乙每日遵医嘱口服
胃舒平[主要成分Al(OH)3]每日遵医嘱口服
0.3﹪盐酸(主要成分HCl)(1)分别判断两位病人患胃病的情况。
(2)病人乙服用的药物,可用一种常见的调味品代替。这种调味品是什么?
(3)写出胃舒平治病时发生的化学方程式。当人被蚊虫叮咬(蚊虫叮咬时会向体内排放含有酸性物质的毒液)后,可在叮咬处涂抹 以减轻疼痛。肥皂水中和反应的应用:Why实验室中,小明发现准备桌上有一瓶试剂:用完的试剂这样放置会造成什么后果?氢氧化钠固体吸收水分氢氧化钠溶液吸收二氧化碳碳酸钠溶液水分蒸发碳酸钠固体吸水潮解与二氧化碳反应变质必须密封保存药品的保存:
浓盐酸
浓硫酸
生石灰
氢氧化钠固体
氢氧化钠溶液、氢氧化钙溶液引起变化的原因分别是什么?其中,会变质的有哪些?下列物质敞口放置在空气中,因发生化学变化而质量增加的是( )
A.浓硫酸 B.浓盐酸
C.氢氧化钠 D.氯化钠1.下列物质的俗名、学名、化学式三者表示同一物质的是 ( )
A、生石灰、氢氧化钙、CaO
B、纯碱、氢氧化钠、NaOH
C、小苏打、碳酸氢钠、NaHCO3
D、盐酸、氯化氢、HCl
2.混有水蒸气的下列气体中,既可以用浓硫酸干燥,又可以用苛性钠干燥的是( )
A.氧气 B.氨气
C.二氧化碳 D.氯化氢经典在线:3.下列物质能使酚酞试液变红色的是( )
A盐酸 B氢氧化钠溶液
C氯化钠溶液 D氢氧化铜
4.实验表明,用碱性溶液浸泡新鲜的蔬菜,能有效除去蔬菜上的残留农药,从而降低对人体的损害。根据上述原理,对刚买回来的蔬菜,你认为应浸泡在哪种溶液中( )
A.白酒 B.食醋
C.烧碱溶液 D.碳酸钠溶液5.下列物质能用稀酸和金属直接反应制取的是( )
A.CuSO4 B. FeCl3
C. MgSO4 D. AgCl
6. 氯化钙溶液中含少量盐酸,在没有指示剂的条件下为除去盐酸可选用( )
A、熟石灰 B、生石灰
C、石灰石 D、纯碱7. 右图所示的锥形瓶内充满气体X,胶头滴管内盛有液体Y,挤压胶头滴管,使液体Y进入瓶中,振荡,一会儿可见套在玻璃管下端的小气球a鼓起。气体X和液体Y可能是( )
A、X是CO2,Y是NaOH溶液
B、X是CO2,Y是稀硫酸
C、X是CaO,Y是水
D、X是CO,Y是石灰水8、人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛。小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图19所示。
为了验证该药物的主要成分是碳酸盐,他进行了如下实验:首先将药片放入试管中,向其中加入适量的稀盐酸,然后______
_____(写实验操作和实验现象)。 当小军看到药物说明书上的服用方法后,对此产生了探究的兴趣,请你和他一起完成探究活动。
【提出问题】抗酸药为什么嚼碎后服用?
【作出猜想】他的猜想是 。
【设计实验】实验一:将一片完整的药片放入试管中,向其中加入5mL5%的稀盐酸;
实验二:将 放入试管中,向其中加入5mL5%的稀盐酸。【现象与结论】实验二比实验一反应快。证明小军的猜想正确。
【拓展探究】(1)氢氧化镁、碳酸钙、碳酸氢钠等也常用于制作抗酸药。这些物质必须具备两个条件:一是能与胃酸作用;二是__________________。
(2)患有胃溃疡(胃黏膜溃烂)的病人胃酸过多时,不宜服用含碳酸盐的抗酸药,其原因是_________________________。
