同步精练精析鲁科版必修2:331乙醇
图片预览




文档简介
3.3.1 乙醇(鲁科版必修2)
【典例导悟】
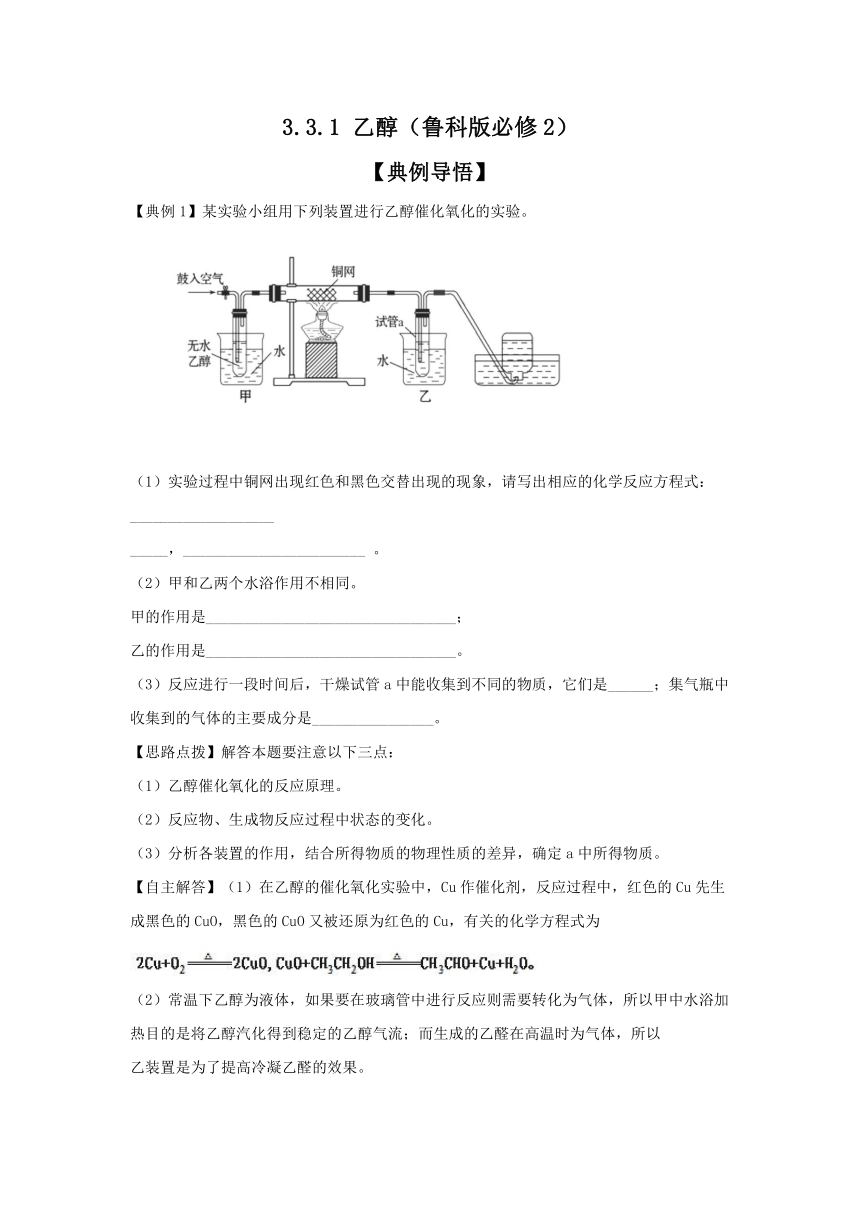
【典例1】某实验小组用下列装置进行乙醇催化氧化的实验。
(1)实验过程中铜网出现红色和黑色交替出现的现象,请写出相应的化学反应方程式:___________________
_____,________________________ 。
(2)甲和乙两个水浴作用不相同。
甲的作用是_________________________________;
乙的作用是_________________________________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是______;集气瓶中收集到的气体的主要成分是________________。
【思路点拨】解答本题要注意以下三点:
(1)乙醇催化氧化的反应原理。
(2)反应物、生成物反应过程中状态的变化。
(3)分析各装置的作用,结合所得物质的物理性质的差异,确定a中所得物质。
【自主解答】(1)在乙醇的催化氧化实验中,Cu作催化剂,反应过程中,红色的Cu先生成黑色的CuO,黑色的CuO又被还原为红色的Cu,有关的化学方程式为
(2)常温下乙醇为液体,如果要在玻璃管中进行反应则需要转化为气体,所以甲中水浴加热目的是将乙醇汽化得到稳定的乙醇气流;而生成的乙醛在高温时为气体,所以
乙装置是为了提高冷凝乙醛的效果。
(3)经过反应后并冷却,a中收集到的物质有易挥发的乙醇及反应生成的乙醛和水。集气瓶中收集到的气体主要为氮气。
=====
【变式训练】A、B、C三种醇同足量的金属钠完全反应,在相同条件下产生相同体积的氢气消耗这三种醇的物质的量之比为3∶6∶2,则A、B、C三种醇分子里羟基数之比是
( )
A.3∶2∶1 B.2∶6∶3
C.3∶1∶2 D.2∶1∶3
【解析】选D。三种醇与足量Na反应,产生相同体积的H2,说明这三种醇各自所提供的—OH数目相同,为方便计算,设所提供—OH的数目为a,由于三种醇物质的量之比为3∶6∶2,所以各醇分子中—OH数之比为
【典例2】乙烯和乙醇的混合气体V L,完全燃烧生成CO2和H2O,消耗相同状态下的O2 3V L,则混合气体中乙烯和乙醇的体积比为
A.1∶1 B.2∶1 C.1∶2 D.任意比
【规范解答】选D。解法一:化学方程式通式法:
则V L乙烯和V L乙醇蒸气都会消耗相同状态下的O2 3V L,所以两者以任意比混合时均满足题意要求,故选D项。
解法二:“分割法”:
将乙醇的分子式改写成C2H4·H2O,显然,等体积的乙烯和乙醇蒸气消耗相同状态下的O2相同,所以两者以任意比混合时均满足题意要求,故选D项。
【互动探究】若将上题中的“乙烯”改为“乙烷”、“乙醇”改为“乙酸(C2H4O2)”呢?
提示:由化学方程式知,1体积乙烷完全燃烧耗氧气3.5体积;1体积乙酸蒸气完全燃烧耗氧气2体积,由“十字交叉法”得:
【学业达标训练】
1.(2010·双鸭山高一检测)下列化学用语正确的是( )
A.NH3中氮元素的化合价是+3
B.乙醇的分子式:CH3CH2OH
C.乙烯的结构简式:CH2CH2
D.甲烷的结构式为:
【解析】选D。NH3中氮元素的化合价是-3价,故A项错误;乙醇的分子式为C2H6O,故B项错误;乙烯的结构简式为CH2CH2,故C项错误;甲烷的结构式为
故D项正确。
2.比较乙烷和乙醇的结构,下列说法错误的是( )
A.两个碳原子以单键相连
B.分子里都含6个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子
D.乙基与一个羟基相连就是乙醇分子
【解析】选B。乙烷和乙醇的结构简式分别为CH3CH3和CH3CH2OH,由于官能团—OH的存在,使乙醇的性质、结构与乙烷大不相同。
3.向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是( )
A.钠块开始反应时,浮在乙醇液面的上面
B.钠块熔化成小球
C.钠块在乙醇的液面上游动
D.钠块表面有气体放出
【解析】选D。由于钠的密度比乙醇的密度大,所以钠将沉在乙醇液面的底部,故A、C项均错误;钠与乙醇的反应虽然是放热反应,但由于放出的热量被周围的乙醇吸收,导致钠块不会熔化,故B项错误;由于钠与乙醇反应生成H2,所以在钠块表面产生气泡,故D项正确。
4.下列说法中,不正确的是( )
A.乙醇与金属钠反应时,是乙醇分子中羟基中的 O—H 键断裂
B.检验乙醇中是否含有水可加入少量无水硫酸铜,若变蓝则含水
C.禁止用工业酒精配制饮用酒和调味用的料酒
D.甲烷、乙烯、苯、乙醇都是无色不溶于水的有机化合物
【解析】选D。乙醇与金属钠反应生成乙醇钠,是乙醇分子中羟基中的O—H键发生断裂;检验乙醇中是否含有水可用无水硫酸铜作检验试剂,若变蓝表明其含水;工业酒精中含有对人体有害的甲醇,因此禁止用工业酒精配制饮用酒和调味用的料酒;甲烷、乙烯、苯都不溶于水,但乙醇却能与水以任意比例混溶。
5.16 g某一元醇与足量的金属钠完全反应,在标准状况下得到5.6 L氢气。该物质可能是( )
A.CH3OH B.C2H5OH
C.C3H7OH D.C4H9OH
6.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻后,使铜片质量增加的是( )
A.硝酸 B.无水乙醇
C.石灰水 D.盐酸
7.对同样的反应若使用不同的催化剂,可得到不同的产物。如:
又知C2H5OH在活性铜催化下,可生成CH3COOC2H5及其他产物,则其他产物可能为( )
A.H2 B.CO2 C.H2O D.H2和H2O
8.对化学反应进行分类是学习化学的重要方法之一。如我们学过的无机化学反应有两种主要的分类方法:①根据反应前后物质的变化分为化合反应、分解反应、置换反应和复分解反应;②根据化学反应中是否有电子转移,分为氧化还原反应和非氧化还原反应。请根据已经学过的化学反应类型,写出其反应的化学方程式,指出反应类型。
(1)乙烷与氯气生成一氯乙烷的反应:_____________
__________________________________________;
反应类型:_________________________________。
(2)乙烯与溴的反应:________________________;
反应类型:_____________________________。
(3)乙烯与水的反应:_________________________
______________________________________;
反应类型:________________________________。
(4)乙醇在铜的催化下被氧化生成乙醛的反应:______
_________________________________________;
反应类型:_________________________________。
(5)乙醇与钠的反应:_________________________
________________________________________;
反应类型:_________________________________。
【解析】由乙烷分子中只存在碳碳单键和碳氢键,所以乙烷的特征反应是取代反应;由于乙烯分子中存在碳碳双键,所以乙烯的特征反应是加成反应;由于乙醇分子中存在—OH。所以乙醇既能与活泼金属反应,又能发生催化氧化。
【素能综合检测】
一、选择题(本题包括5小题,每小题4分,共20分)
1.下列说法正确的是( )
A.日常生活中无水乙醇常用于杀菌消毒
B.用乙醇作萃取剂可以将碘从碘水中萃取出来
C.乙醇、乙烷和苯都可以与钠反应生成氢气
D.乙醇是一种再生能源
【解析】选D。日常生活中常用75%(体积分数)的乙醇水溶液杀菌消毒,故A项错误;由于乙醇与水互溶,不能发生分层,所以乙醇不能将碘从碘水中萃取出来,故B项错误;乙烷和苯都不与钠发生反应,故C项错误;由于乙醇燃烧生成CO2和H2O,CO2和H2O通过绿色植物的光合作用生长出粮食,而粮食是生产乙醇的重要原料,所以乙醇属于再生能源,故D项正确。
2.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A.1 mol乙醇燃烧生成3 mol水
B.1 mol乙醇可以生成1 mol乙醛
C.1 mol乙醇跟足量的金属Na作用得0.5 mol H2
D.乙醇可以制酒精饮料
【解析】选C。A项不能证明乙醇分子中的6个H原子是不同的;B项只能证明乙醇分子中的3个H原子与另外3个H原子不同;C项由于1 mol乙醇与足量钠反应生成0.5 mol H2,证明乙醇分子中的1个H原子与另外5个H原子不同;D项由于乙醇分子未发生化学变化,不能证明乙醇分子中的6个H原子是不同的,故选C项。
4.(2010·宣城同步检测)下列物质中,在一定条件下既能起加成反应,又能起取代反应,但不能使酸性KMnO4溶液褪色的是( )
A.乙烷 B.乙烯 C.苯 D.乙醇
【解析】选C。根据题意,A、B、C、D四种物质发生的反应分别为(“×”表示不反应,“√”表示反应)
5.(思维拓展题)一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量为( )
A.1.4 g B.2.2 g
C.4.4 g D.在2.2 g和4.4 g之间
二、非选择题(本题包括3小题,共30分)
6.(9分)(1)把表面附有CuO的铜丝在酒精灯焰心处加热,会发现铜丝由_________色变_________色,有关反应的化学方程式________________ ,由此可见铜丝在反应中起_________的作用。
(2)最近国外研究出一种高效的水果长期保鲜新技术:在3 ℃潮湿条件下的水果保鲜室中用一种特制的低压水银灯照射,引起光化学反应,使水果贮存过程中缓缓释放的催熟剂转化为没有催熟作用的有机物。试回答:
①可能较长期保鲜的主要原因是________________ 。
②写出主要反应的化学方程式__________________ 。
【解析】(1)铜丝表面附有CuO,插入焰心,焰心附近会有被汽化的酒精蒸气未来得及燃烧,乙醇蒸气和CuO在加热条件下会发生反应。
(2)熟水果能释放出乙烯,乙烯能催熟水果,要水果保鲜,应把乙烯转化为乙醇,主要的反应为CH2==CH2与水光照条件下反应生成乙醇。
(1)在空气中完全燃烧时,消耗氧气的质量由多到少的顺序__________,反应中生成CO2的体积(相同状况)由小到大的顺序__________ 。
(2)分别与足量的金属钠反应,放出H2的体积(相同状况)由少到多的顺序是__________ 。
【解析】(1)耗氧计算可先将四种物质改写成CxHy·nH2O的形式。
甲醇CH2·H2O 乙醇C2H4·H2O
乙二醇C2H2·2H2O 丙三醇C3H2·3H2O
可判断1 mol四种物质完全燃烧消耗氧气分别为1.5 mol、3 mol、2.5 mol、3.5 mol,故顺序为④②③①。生成CO2的体积只与碳原子数有关,与H、O原子个数无关,故顺序为①<②=③<④。
(2)与足量金属钠反应生成H2体积与原分子中羟基个数有关,羟基数目越多生成H2的体积越大,故由少到多的顺序为①=②<③<④。
答案:(1)④>②>③>① ①<②=③<④
(2)①=②<③<④
[实验·探究]
8.(12分)经测定乙醇的分子式是C2H6O,由于有机化合物普遍存在同分异构现象,推测乙醇分子的结构可能是下列两种之一:
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,甲、乙、丙三名学生利用如图所示装置进行实验确定乙醇分子的结构。
图中量气装置由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~200毫升),供量气用;乙管可上下移动,以调节液面高低。
(1)装置A的分液漏斗与蒸馏烧瓶间连接的导管所起的作用是________(填写编号)。
A.防止乙醇挥发 B.保证实验装置不漏气
C.使乙醇容易滴下
(2)学生甲得到一组实验数据
根据以上数据推断乙醇的结构应为________(用“Ⅰ”或“Ⅱ”表示),理由为______________________ 。
(3)学生乙认为:为了较准确地测量氢气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数、求其差值的过程中,应注意_________和_________(填写字母编号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(4)学生丙不想通过称取乙醇的质量来确定乙醇的物质的量,那么他还需要知道的数据是___________。
(5)实验后三名学生从乙醇的可能结构入手,对乙醇和钠的关系进行讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是____________。
【解析】(1)由于导管将分液漏斗与蒸馏烧瓶相连,导致两仪器内的压强相等,使乙醇容易滴下。
(2)Ⅰ式中有5个氢原子处于相同的位置,有1个氢原子明显处于与其他氢原子不同的位置上,Ⅱ式中6个氢原子处于完全相同的位置。与足量的钠反应,如果是Ⅰ式,可能性较大的有4种情况:①6个氢原子全反应;②只有5个氢原子反应;③只有1个氢原子反应;④都不反应。如果是Ⅱ式,则只有2种可能:①6个氢原子全反应;②都不反应。分析实验数据知,只有1个氢原子被置换出来,显然乙醇的结构应为Ⅰ式。
(3)在读数时,仰视和俯视都会对读数的准确性造成影响,因而一定要平视;另外,假设甲、乙两管液面不相平的话,就会造成仪器内部的压强与外部大气压不同,造成误差,因而读数时应上下移动乙管,使甲、乙两管液面相平。
(4)如果不直接称取乙醇的质量,可以用量筒或其他仪器量出乙醇的体积,然后,用其体积乘以密度,可求得其质量,进一步可确定其物质的量。
(5)C2H5OH ~ Na
1 1
n mol n mol
加入的钠有少量被空气中的氧气氧化且要求乙醇全部发生化学反应,故加入的金属钠应大于n mol。
答案:(1)C
(2)Ⅰ 乙醇和钠反应产生氢气,从量的关系看
0.010 mol乙醇产生0.005 mol氢气,说明1个乙醇分子中有1个氢原子与其他氢原子不同,因此可确定乙醇分子的结构为Ⅰ
(3)a c (4)乙醇样品的密度
(5)大于n mol
【典例导悟】
【典例1】某实验小组用下列装置进行乙醇催化氧化的实验。
(1)实验过程中铜网出现红色和黑色交替出现的现象,请写出相应的化学反应方程式:___________________
_____,________________________ 。
(2)甲和乙两个水浴作用不相同。
甲的作用是_________________________________;
乙的作用是_________________________________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是______;集气瓶中收集到的气体的主要成分是________________。
【思路点拨】解答本题要注意以下三点:
(1)乙醇催化氧化的反应原理。
(2)反应物、生成物反应过程中状态的变化。
(3)分析各装置的作用,结合所得物质的物理性质的差异,确定a中所得物质。
【自主解答】(1)在乙醇的催化氧化实验中,Cu作催化剂,反应过程中,红色的Cu先生成黑色的CuO,黑色的CuO又被还原为红色的Cu,有关的化学方程式为
(2)常温下乙醇为液体,如果要在玻璃管中进行反应则需要转化为气体,所以甲中水浴加热目的是将乙醇汽化得到稳定的乙醇气流;而生成的乙醛在高温时为气体,所以
乙装置是为了提高冷凝乙醛的效果。
(3)经过反应后并冷却,a中收集到的物质有易挥发的乙醇及反应生成的乙醛和水。集气瓶中收集到的气体主要为氮气。
=====
【变式训练】A、B、C三种醇同足量的金属钠完全反应,在相同条件下产生相同体积的氢气消耗这三种醇的物质的量之比为3∶6∶2,则A、B、C三种醇分子里羟基数之比是
( )
A.3∶2∶1 B.2∶6∶3
C.3∶1∶2 D.2∶1∶3
【解析】选D。三种醇与足量Na反应,产生相同体积的H2,说明这三种醇各自所提供的—OH数目相同,为方便计算,设所提供—OH的数目为a,由于三种醇物质的量之比为3∶6∶2,所以各醇分子中—OH数之比为
【典例2】乙烯和乙醇的混合气体V L,完全燃烧生成CO2和H2O,消耗相同状态下的O2 3V L,则混合气体中乙烯和乙醇的体积比为
A.1∶1 B.2∶1 C.1∶2 D.任意比
【规范解答】选D。解法一:化学方程式通式法:
则V L乙烯和V L乙醇蒸气都会消耗相同状态下的O2 3V L,所以两者以任意比混合时均满足题意要求,故选D项。
解法二:“分割法”:
将乙醇的分子式改写成C2H4·H2O,显然,等体积的乙烯和乙醇蒸气消耗相同状态下的O2相同,所以两者以任意比混合时均满足题意要求,故选D项。
【互动探究】若将上题中的“乙烯”改为“乙烷”、“乙醇”改为“乙酸(C2H4O2)”呢?
提示:由化学方程式知,1体积乙烷完全燃烧耗氧气3.5体积;1体积乙酸蒸气完全燃烧耗氧气2体积,由“十字交叉法”得:
【学业达标训练】
1.(2010·双鸭山高一检测)下列化学用语正确的是( )
A.NH3中氮元素的化合价是+3
B.乙醇的分子式:CH3CH2OH
C.乙烯的结构简式:CH2CH2
D.甲烷的结构式为:
【解析】选D。NH3中氮元素的化合价是-3价,故A项错误;乙醇的分子式为C2H6O,故B项错误;乙烯的结构简式为CH2CH2,故C项错误;甲烷的结构式为
故D项正确。
2.比较乙烷和乙醇的结构,下列说法错误的是( )
A.两个碳原子以单键相连
B.分子里都含6个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子
D.乙基与一个羟基相连就是乙醇分子
【解析】选B。乙烷和乙醇的结构简式分别为CH3CH3和CH3CH2OH,由于官能团—OH的存在,使乙醇的性质、结构与乙烷大不相同。
3.向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是( )
A.钠块开始反应时,浮在乙醇液面的上面
B.钠块熔化成小球
C.钠块在乙醇的液面上游动
D.钠块表面有气体放出
【解析】选D。由于钠的密度比乙醇的密度大,所以钠将沉在乙醇液面的底部,故A、C项均错误;钠与乙醇的反应虽然是放热反应,但由于放出的热量被周围的乙醇吸收,导致钠块不会熔化,故B项错误;由于钠与乙醇反应生成H2,所以在钠块表面产生气泡,故D项正确。
4.下列说法中,不正确的是( )
A.乙醇与金属钠反应时,是乙醇分子中羟基中的 O—H 键断裂
B.检验乙醇中是否含有水可加入少量无水硫酸铜,若变蓝则含水
C.禁止用工业酒精配制饮用酒和调味用的料酒
D.甲烷、乙烯、苯、乙醇都是无色不溶于水的有机化合物
【解析】选D。乙醇与金属钠反应生成乙醇钠,是乙醇分子中羟基中的O—H键发生断裂;检验乙醇中是否含有水可用无水硫酸铜作检验试剂,若变蓝表明其含水;工业酒精中含有对人体有害的甲醇,因此禁止用工业酒精配制饮用酒和调味用的料酒;甲烷、乙烯、苯都不溶于水,但乙醇却能与水以任意比例混溶。
5.16 g某一元醇与足量的金属钠完全反应,在标准状况下得到5.6 L氢气。该物质可能是( )
A.CH3OH B.C2H5OH
C.C3H7OH D.C4H9OH
6.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻后,使铜片质量增加的是( )
A.硝酸 B.无水乙醇
C.石灰水 D.盐酸
7.对同样的反应若使用不同的催化剂,可得到不同的产物。如:
又知C2H5OH在活性铜催化下,可生成CH3COOC2H5及其他产物,则其他产物可能为( )
A.H2 B.CO2 C.H2O D.H2和H2O
8.对化学反应进行分类是学习化学的重要方法之一。如我们学过的无机化学反应有两种主要的分类方法:①根据反应前后物质的变化分为化合反应、分解反应、置换反应和复分解反应;②根据化学反应中是否有电子转移,分为氧化还原反应和非氧化还原反应。请根据已经学过的化学反应类型,写出其反应的化学方程式,指出反应类型。
(1)乙烷与氯气生成一氯乙烷的反应:_____________
__________________________________________;
反应类型:_________________________________。
(2)乙烯与溴的反应:________________________;
反应类型:_____________________________。
(3)乙烯与水的反应:_________________________
______________________________________;
反应类型:________________________________。
(4)乙醇在铜的催化下被氧化生成乙醛的反应:______
_________________________________________;
反应类型:_________________________________。
(5)乙醇与钠的反应:_________________________
________________________________________;
反应类型:_________________________________。
【解析】由乙烷分子中只存在碳碳单键和碳氢键,所以乙烷的特征反应是取代反应;由于乙烯分子中存在碳碳双键,所以乙烯的特征反应是加成反应;由于乙醇分子中存在—OH。所以乙醇既能与活泼金属反应,又能发生催化氧化。
【素能综合检测】
一、选择题(本题包括5小题,每小题4分,共20分)
1.下列说法正确的是( )
A.日常生活中无水乙醇常用于杀菌消毒
B.用乙醇作萃取剂可以将碘从碘水中萃取出来
C.乙醇、乙烷和苯都可以与钠反应生成氢气
D.乙醇是一种再生能源
【解析】选D。日常生活中常用75%(体积分数)的乙醇水溶液杀菌消毒,故A项错误;由于乙醇与水互溶,不能发生分层,所以乙醇不能将碘从碘水中萃取出来,故B项错误;乙烷和苯都不与钠发生反应,故C项错误;由于乙醇燃烧生成CO2和H2O,CO2和H2O通过绿色植物的光合作用生长出粮食,而粮食是生产乙醇的重要原料,所以乙醇属于再生能源,故D项正确。
2.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A.1 mol乙醇燃烧生成3 mol水
B.1 mol乙醇可以生成1 mol乙醛
C.1 mol乙醇跟足量的金属Na作用得0.5 mol H2
D.乙醇可以制酒精饮料
【解析】选C。A项不能证明乙醇分子中的6个H原子是不同的;B项只能证明乙醇分子中的3个H原子与另外3个H原子不同;C项由于1 mol乙醇与足量钠反应生成0.5 mol H2,证明乙醇分子中的1个H原子与另外5个H原子不同;D项由于乙醇分子未发生化学变化,不能证明乙醇分子中的6个H原子是不同的,故选C项。
4.(2010·宣城同步检测)下列物质中,在一定条件下既能起加成反应,又能起取代反应,但不能使酸性KMnO4溶液褪色的是( )
A.乙烷 B.乙烯 C.苯 D.乙醇
【解析】选C。根据题意,A、B、C、D四种物质发生的反应分别为(“×”表示不反应,“√”表示反应)
5.(思维拓展题)一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量为( )
A.1.4 g B.2.2 g
C.4.4 g D.在2.2 g和4.4 g之间
二、非选择题(本题包括3小题,共30分)
6.(9分)(1)把表面附有CuO的铜丝在酒精灯焰心处加热,会发现铜丝由_________色变_________色,有关反应的化学方程式________________ ,由此可见铜丝在反应中起_________的作用。
(2)最近国外研究出一种高效的水果长期保鲜新技术:在3 ℃潮湿条件下的水果保鲜室中用一种特制的低压水银灯照射,引起光化学反应,使水果贮存过程中缓缓释放的催熟剂转化为没有催熟作用的有机物。试回答:
①可能较长期保鲜的主要原因是________________ 。
②写出主要反应的化学方程式__________________ 。
【解析】(1)铜丝表面附有CuO,插入焰心,焰心附近会有被汽化的酒精蒸气未来得及燃烧,乙醇蒸气和CuO在加热条件下会发生反应。
(2)熟水果能释放出乙烯,乙烯能催熟水果,要水果保鲜,应把乙烯转化为乙醇,主要的反应为CH2==CH2与水光照条件下反应生成乙醇。
(1)在空气中完全燃烧时,消耗氧气的质量由多到少的顺序__________,反应中生成CO2的体积(相同状况)由小到大的顺序__________ 。
(2)分别与足量的金属钠反应,放出H2的体积(相同状况)由少到多的顺序是__________ 。
【解析】(1)耗氧计算可先将四种物质改写成CxHy·nH2O的形式。
甲醇CH2·H2O 乙醇C2H4·H2O
乙二醇C2H2·2H2O 丙三醇C3H2·3H2O
可判断1 mol四种物质完全燃烧消耗氧气分别为1.5 mol、3 mol、2.5 mol、3.5 mol,故顺序为④②③①。生成CO2的体积只与碳原子数有关,与H、O原子个数无关,故顺序为①<②=③<④。
(2)与足量金属钠反应生成H2体积与原分子中羟基个数有关,羟基数目越多生成H2的体积越大,故由少到多的顺序为①=②<③<④。
答案:(1)④>②>③>① ①<②=③<④
(2)①=②<③<④
[实验·探究]
8.(12分)经测定乙醇的分子式是C2H6O,由于有机化合物普遍存在同分异构现象,推测乙醇分子的结构可能是下列两种之一:
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,甲、乙、丙三名学生利用如图所示装置进行实验确定乙醇分子的结构。
图中量气装置由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~200毫升),供量气用;乙管可上下移动,以调节液面高低。
(1)装置A的分液漏斗与蒸馏烧瓶间连接的导管所起的作用是________(填写编号)。
A.防止乙醇挥发 B.保证实验装置不漏气
C.使乙醇容易滴下
(2)学生甲得到一组实验数据
根据以上数据推断乙醇的结构应为________(用“Ⅰ”或“Ⅱ”表示),理由为______________________ 。
(3)学生乙认为:为了较准确地测量氢气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数、求其差值的过程中,应注意_________和_________(填写字母编号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(4)学生丙不想通过称取乙醇的质量来确定乙醇的物质的量,那么他还需要知道的数据是___________。
(5)实验后三名学生从乙醇的可能结构入手,对乙醇和钠的关系进行讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是____________。
【解析】(1)由于导管将分液漏斗与蒸馏烧瓶相连,导致两仪器内的压强相等,使乙醇容易滴下。
(2)Ⅰ式中有5个氢原子处于相同的位置,有1个氢原子明显处于与其他氢原子不同的位置上,Ⅱ式中6个氢原子处于完全相同的位置。与足量的钠反应,如果是Ⅰ式,可能性较大的有4种情况:①6个氢原子全反应;②只有5个氢原子反应;③只有1个氢原子反应;④都不反应。如果是Ⅱ式,则只有2种可能:①6个氢原子全反应;②都不反应。分析实验数据知,只有1个氢原子被置换出来,显然乙醇的结构应为Ⅰ式。
(3)在读数时,仰视和俯视都会对读数的准确性造成影响,因而一定要平视;另外,假设甲、乙两管液面不相平的话,就会造成仪器内部的压强与外部大气压不同,造成误差,因而读数时应上下移动乙管,使甲、乙两管液面相平。
(4)如果不直接称取乙醇的质量,可以用量筒或其他仪器量出乙醇的体积,然后,用其体积乘以密度,可求得其质量,进一步可确定其物质的量。
(5)C2H5OH ~ Na
1 1
n mol n mol
加入的钠有少量被空气中的氧气氧化且要求乙醇全部发生化学反应,故加入的金属钠应大于n mol。
答案:(1)C
(2)Ⅰ 乙醇和钠反应产生氢气,从量的关系看
0.010 mol乙醇产生0.005 mol氢气,说明1个乙醇分子中有1个氢原子与其他氢原子不同,因此可确定乙醇分子的结构为Ⅰ
(3)a c (4)乙醇样品的密度
(5)大于n mol
