高中化学鲁科版必修二第一节 化学键与化学反应课件 (30张)
文档属性
| 名称 | 高中化学鲁科版必修二第一节 化学键与化学反应课件 (30张) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-01 00:00:00 | ||
图片预览










文档简介
课件30张PPT。第二章化学键 化学反应与能量
第一节 化学键与化学反应
第一课时学习目标:
知识与技能 1、了解化学键的定义。
2、了解化学变化的实质。
3、了解离子键、共价键的定义以及判断。
过程与方法 通过对概念教学培 养学生的想象力和分析推理能力。
情感态度与价值观
通过对概念教学增进学生对物质构成的认识,培养探 究精神和团体合作精神。
学习重点:1. 化学键、离子键、共价键含义。
2. 对化学反应实质理解。
学习难点:对离子键、共价键本质理解。 木炭在空气中燃烧一、化学键与化学反应中的物质变化 思考1 .什么是化学变化?化学变化中的最小微粒是什么? 2.化学反应中为什么会发生
物质变化? 有新物质生成的反应 原子
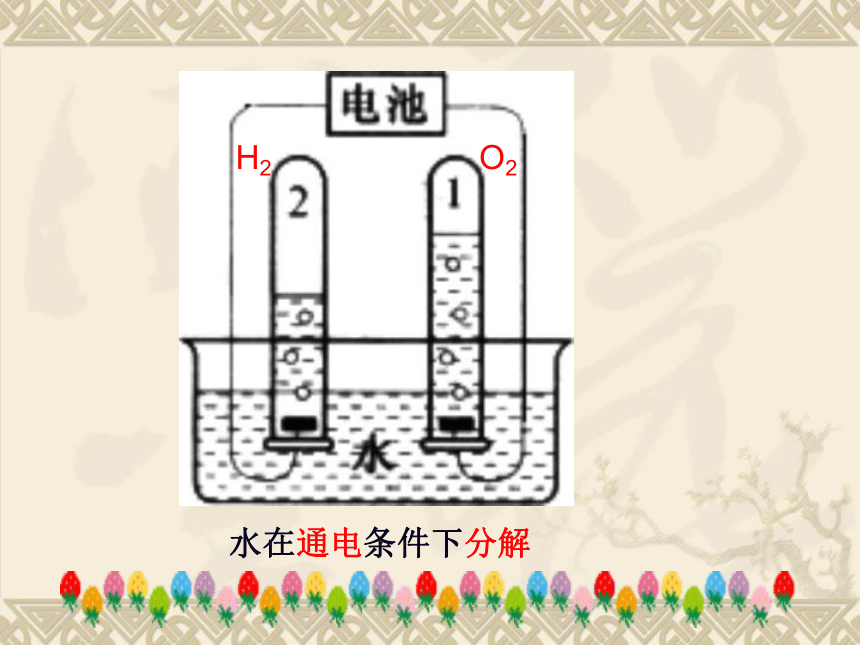
原子的重新组合水在通电条件下分解H2O2水分子是如何构成的?一个水分子是由两个氢原子和一个氧原子构成的。在水分子中氢原子和氧原子之间存在着很强的相互作用,要破坏这种相互作用就要消耗能量,通电正是为水的分解提供能量的。思考思考:什么是化学键?思考:1.下列哪种作用是化学键?
(1)一个水分子内氧原子和另一个水分子内氢原子间的作用
(2)一个水分子内两个氢原子间的作用
(3)一个水分子内氢氧原子间的作用2.水加热到100摄氏度可变成水蒸汽,而要使水分解需加热到
1000摄氏度以上,这说明了什么?
必须直接相邻(3)强烈相互作用(吸引力和排斥力)(一)化学键与物质变化
1.化学键
定义:
相邻原子间的强相互作用特别强调:这里原子包括中性原子和阴阳离子思考:
是不是所有的物质中都有化学键?结论:不是所有的物质中都有化学键,
如:稀有气体分子中不存在化学键。[示例]水在通电时发生分解反应生成氢气和氧气
2H2O === 2H2↑ + O2 ↑
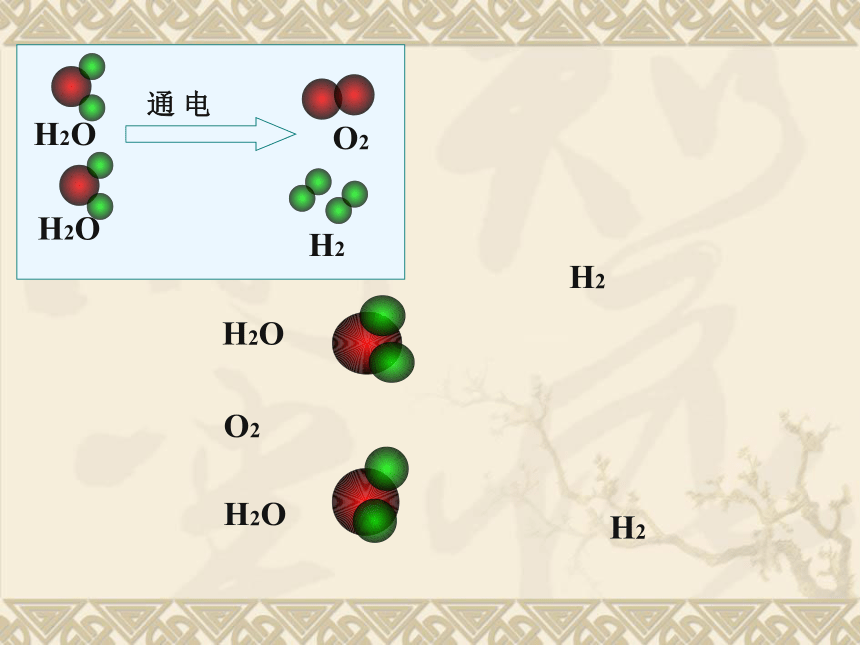
电解H2OH2OH2H2O2思考 水在通电发生分解反应时断裂了哪些化学键?形成了哪些化学键?
化学键断裂:氢氧键
化学键生成:氢氢键、氧氧键迁移应用氢氢键、氧氧键
氢氧键
氢氢键、氯氯键
氢氯键
氮氮键、氢氢键氮氢键你对化学反应中物质的变化有了什么新的认识?
讨论归纳总结化学反应中物质变化的实质:旧化学键断裂和新化学键形成思考:1氯化氢溶于水是化学变化吗?
2氯化钠溶液蒸干得氯化钠固体
是化学变化吗?
1、下列关于化学键的叙述正确的是( )
A. 化学键是指相邻原子间的相互作用
B. 化学键既存在于相邻原子之间,也存在于相邻分子之间
C. 化学键通常是指相邻的原子之间强烈的相互吸引作用
D. 化学键通常是指相邻的原子之间强烈的相互作用
2.物质间发生化学反应一定发生化学变化的是( )
A.颜色 B.状态 C.化学键 D.原子核针对性训练 CD1.画出氢原子和氯原子的结构示意图
2.氢原子和氯原子是否是稳定结构?
思考合作探究氢原子和氯原子之间为什么有形成分子
的趋势?(请结合知识支持中的电子式)氯化氢分子的形成过程: 通过共用电子对思考: 什么是共价键?2.共价键
强调:(1) 成键微粒:
(2)成键实质:
(3)成键元素:
原子之间通过共用电子对形成的化学键,叫共价键
原子共用电子对 一般是同种或不同种非金属元素原子间的相互作用。
注意:AlCl3中Al-Cl键为共价键定义:针对训练下列物质中是否有共价键?
1.H2 2.He 3.CO2 4.NH3 5.OH- 6.NH4+ 7金刚石8.NaCl钠在氯气中燃烧思考1.画出钠原子和氯原子结构示意图
2.它们是否是稳定结构?如何形成稳定结构?不稳定电子转移稳定阳离子阴离子静电作用思考:什么是离子键?卤素(VⅡA)及O、S等第ⅠA族、第ⅡA族的金属3.离子键定义:阴阳离子之间通过静电作用形成的化学键,叫离子键 强调: (1) 成键微粒:
(2)成键实质:
(3)成键元素:
阴阳离子静电作用 一般情况下,活泼金属元素原子与活泼非金属元素原子间易形成离子键。(包括静电引力和静电斥力)思考:
下列物质中含有离子键的是
1.KCI 2.CaO 3.Na2S 4.MgCl2
5.NaOH 6.KNO3 7.H2SO4 8. CH4 (1 2 3 4 5 6)归纳总结列表比较离子键和共价键:
阴阳离子之间通过静电作用形成的化学键 原子之间通过共用电子对形成的化学键阴阳离子
原子静电作用一般是活泼金属原子与活泼非金属原子间一般是非金属元素原子间共用电子对KCl CaO MgCl2Cl2 H2O CO2针对性训练1.下列化合物中含有离子键的是( )
A.Na2O B.CH4 C. NH3 D. CO2
2.下列物质中既含离子键又含共价键的是( )
A. H2O B.CaCl2 C.NaOH D.Cl2 E.Na2S
3.下列各组物质中,化学键类型相同的是( )
A.SO2 和 H2S B.CO2和H2O
C.NaCl和HCl D.CCl4 和 KClAA BC化学键离子键共价键化学反应中
物质变化实质 谈谈你对本节课的收获与困惑百家之言巩固练习1.下列各种原子序数表示两种元素,不能形成离子键的是( )
A. 6和8 B. 8和11 C. 12和9 D.11和17
2. 下列各种原子序数表示元素,其中能以共价键相互结合成稳定化合物的是( )
A.8与11 B.9与9 C.17与19 D.1与7
3.下列各组化合物中,化学键类型不同的是( )
A.NaCl和HNO3 B.H2O和NH3
C.CaCl2和KCl D.CCl4和Na2OADAD4.现有如下说法: ( )
①在水中氢氧原子间均以化学键相结合
②金属和非金属化合时一定形成离子键
③离子键是阴阳离子相互吸引作用
④根据电离方程式HCl=H++Cl-可判断HCl分子中存在离子键
⑤ H2分子和Cl2分子的反应过程是H2、Cl2分子里共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程。
A、①② ⑤正确 B、都不正确
C、只有④正确 D、仅①不正确
5.下列变化中,属于化学变化的是( )
A.干冰气化 B.水通电分解 C.氯化氢溶于水
D.氯气被木炭吸附 E.溴挥发 F.食盐熔化 G石灰石粉碎
BB6.下列物质:⑴HCl ⑵CO2 ⑶H2O ⑷N2 ⑸KOH ⑹Cl2 ⑺NaF ⑻CH4 ⑼CaO
⑽MgCl2 ⑾Na2SO4 (12) HNO3
只含共价键的是 ,只含离子键的是 ,既含共价键又含离子键的是 。
⑴ ⑵ ⑶ ⑷ ⑹⑻(12) ⑺⑼⑽ ⑸ ⑾
知识与技能 1、了解化学键的定义。
2、了解化学变化的实质。
3、了解离子键、共价键的定义以及判断。
过程与方法 通过对概念教学培 养学生的想象力和分析推理能力。
情感态度与价值观
通过对概念教学增进学生对物质构成的认识,培养探 究精神和团体合作精神。
学习重点:1. 化学键、离子键、共价键含义。
2. 对化学反应实质理解。
学习难点:对离子键、共价键本质理解。 木炭在空气中燃烧一、化学键与化学反应中的物质变化 思考1 .什么是化学变化?化学变化中的最小微粒是什么? 2.化学反应中为什么会发生
物质变化? 有新物质生成的反应 原子
原子的重新组合水在通电条件下分解H2O2水分子是如何构成的?一个水分子是由两个氢原子和一个氧原子构成的。在水分子中氢原子和氧原子之间存在着很强的相互作用,要破坏这种相互作用就要消耗能量,通电正是为水的分解提供能量的。思考思考:什么是化学键?思考:1.下列哪种作用是化学键?
(1)一个水分子内氧原子和另一个水分子内氢原子间的作用
(2)一个水分子内两个氢原子间的作用
(3)一个水分子内氢氧原子间的作用2.水加热到100摄氏度可变成水蒸汽,而要使水分解需加热到
1000摄氏度以上,这说明了什么?
必须直接相邻(3)强烈相互作用(吸引力和排斥力)(一)化学键与物质变化
1.化学键
定义:
相邻原子间的强相互作用特别强调:这里原子包括中性原子和阴阳离子思考:
是不是所有的物质中都有化学键?结论:不是所有的物质中都有化学键,
如:稀有气体分子中不存在化学键。[示例]水在通电时发生分解反应生成氢气和氧气
2H2O === 2H2↑ + O2 ↑
电解H2OH2OH2H2O2思考 水在通电发生分解反应时断裂了哪些化学键?形成了哪些化学键?
化学键断裂:氢氧键
化学键生成:氢氢键、氧氧键迁移应用氢氢键、氧氧键
氢氧键
氢氢键、氯氯键
氢氯键
氮氮键、氢氢键氮氢键你对化学反应中物质的变化有了什么新的认识?
讨论归纳总结化学反应中物质变化的实质:旧化学键断裂和新化学键形成思考:1氯化氢溶于水是化学变化吗?
2氯化钠溶液蒸干得氯化钠固体
是化学变化吗?
1、下列关于化学键的叙述正确的是( )
A. 化学键是指相邻原子间的相互作用
B. 化学键既存在于相邻原子之间,也存在于相邻分子之间
C. 化学键通常是指相邻的原子之间强烈的相互吸引作用
D. 化学键通常是指相邻的原子之间强烈的相互作用
2.物质间发生化学反应一定发生化学变化的是( )
A.颜色 B.状态 C.化学键 D.原子核针对性训练 CD1.画出氢原子和氯原子的结构示意图
2.氢原子和氯原子是否是稳定结构?
思考合作探究氢原子和氯原子之间为什么有形成分子
的趋势?(请结合知识支持中的电子式)氯化氢分子的形成过程: 通过共用电子对思考: 什么是共价键?2.共价键
强调:(1) 成键微粒:
(2)成键实质:
(3)成键元素:
原子之间通过共用电子对形成的化学键,叫共价键
原子共用电子对 一般是同种或不同种非金属元素原子间的相互作用。
注意:AlCl3中Al-Cl键为共价键定义:针对训练下列物质中是否有共价键?
1.H2 2.He 3.CO2 4.NH3 5.OH- 6.NH4+ 7金刚石8.NaCl钠在氯气中燃烧思考1.画出钠原子和氯原子结构示意图
2.它们是否是稳定结构?如何形成稳定结构?不稳定电子转移稳定阳离子阴离子静电作用思考:什么是离子键?卤素(VⅡA)及O、S等第ⅠA族、第ⅡA族的金属3.离子键定义:阴阳离子之间通过静电作用形成的化学键,叫离子键 强调: (1) 成键微粒:
(2)成键实质:
(3)成键元素:
阴阳离子静电作用 一般情况下,活泼金属元素原子与活泼非金属元素原子间易形成离子键。(包括静电引力和静电斥力)思考:
下列物质中含有离子键的是
1.KCI 2.CaO 3.Na2S 4.MgCl2
5.NaOH 6.KNO3 7.H2SO4 8. CH4 (1 2 3 4 5 6)归纳总结列表比较离子键和共价键:
阴阳离子之间通过静电作用形成的化学键 原子之间通过共用电子对形成的化学键阴阳离子
原子静电作用一般是活泼金属原子与活泼非金属原子间一般是非金属元素原子间共用电子对KCl CaO MgCl2Cl2 H2O CO2针对性训练1.下列化合物中含有离子键的是( )
A.Na2O B.CH4 C. NH3 D. CO2
2.下列物质中既含离子键又含共价键的是( )
A. H2O B.CaCl2 C.NaOH D.Cl2 E.Na2S
3.下列各组物质中,化学键类型相同的是( )
A.SO2 和 H2S B.CO2和H2O
C.NaCl和HCl D.CCl4 和 KClAA BC化学键离子键共价键化学反应中
物质变化实质 谈谈你对本节课的收获与困惑百家之言巩固练习1.下列各种原子序数表示两种元素,不能形成离子键的是( )
A. 6和8 B. 8和11 C. 12和9 D.11和17
2. 下列各种原子序数表示元素,其中能以共价键相互结合成稳定化合物的是( )
A.8与11 B.9与9 C.17与19 D.1与7
3.下列各组化合物中,化学键类型不同的是( )
A.NaCl和HNO3 B.H2O和NH3
C.CaCl2和KCl D.CCl4和Na2OADAD4.现有如下说法: ( )
①在水中氢氧原子间均以化学键相结合
②金属和非金属化合时一定形成离子键
③离子键是阴阳离子相互吸引作用
④根据电离方程式HCl=H++Cl-可判断HCl分子中存在离子键
⑤ H2分子和Cl2分子的反应过程是H2、Cl2分子里共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程。
A、①② ⑤正确 B、都不正确
C、只有④正确 D、仅①不正确
5.下列变化中,属于化学变化的是( )
A.干冰气化 B.水通电分解 C.氯化氢溶于水
D.氯气被木炭吸附 E.溴挥发 F.食盐熔化 G石灰石粉碎
BB6.下列物质:⑴HCl ⑵CO2 ⑶H2O ⑷N2 ⑸KOH ⑹Cl2 ⑺NaF ⑻CH4 ⑼CaO
⑽MgCl2 ⑾Na2SO4 (12) HNO3
只含共价键的是 ,只含离子键的是 ,既含共价键又含离子键的是 。
⑴ ⑵ ⑶ ⑷ ⑹⑻(12) ⑺⑼⑽ ⑸ ⑾
