鲁科版高中化学必修二第二章第一节 化学键与化学反应(25张ppt)
文档属性
| 名称 | 鲁科版高中化学必修二第二章第一节 化学键与化学反应(25张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-05 00:00:00 | ||
图片预览








文档简介
课件25张PPT。第2章 化学键 化学反应与能量第一节 化学键与化学反应第一课时制备新物质提供能源铜矿石汽油利用
物质
变化利用
能量
变化化学反应的应用第1课时:化学键与化学反应中的物质变化键的中文解释
基本字义 1.? 安装在车轴头上管住车轮或使轴与齿轮等连接固定的零件,一般是用钢制的长方条(亦称“辖”):关~。
2.? 插在门上关锁门户的金属棍子,将两扇门牢固连接:“掌授管~以启闭国门”。
3.? 琴或机器上使用时用手按动的部分:~盘。~子。琴~。
【学习目标】
1.初步学会从分子、原子的微观角度认识化学反应中物质变化的实质。
2.理解化学键的含义,能描述共价键、离子键的形成过程与形成条件。
3. 学会判断物质中存在的化学键。第1课时:化学键与化学反应中的物质变化一、化学键与物质变化 原子的重新组合。化学反应中的最小微粒是什么?
初中化学中曾经讨论过的化学反应的实质是什么?
3.
水在通电或高温(2000℃)时才能分解,请用模型演示这一过程,水分子是如何分解生成氢气与氧气的?并尝试解析消耗的高能量用在哪一环节?
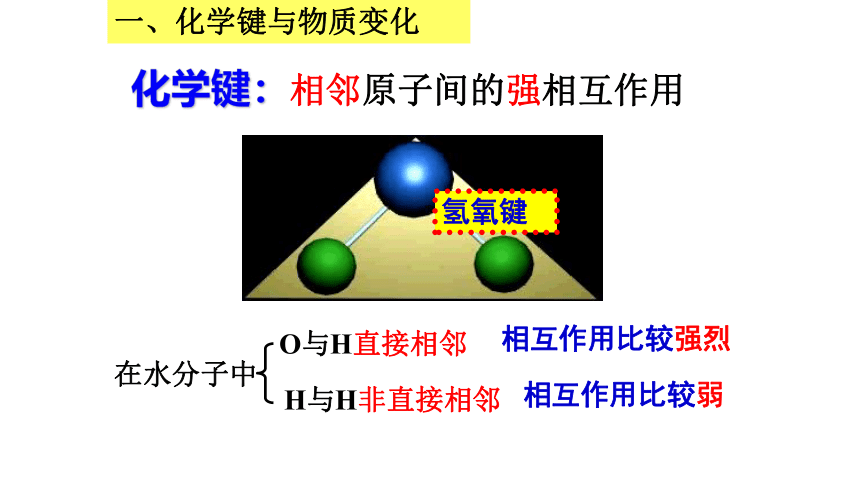
原子活动探究1:H2OH2OH2H2O2一、化学键与物质变化化学键:相邻原子间的强相互作用一、化学键与物质变化H与H非直接相邻O与H直接相邻相互作用比较强烈相互作用比较弱在水分子中氢氧键思考:一、化学键与物质变化下列说法是否正确,不正确的指出错误的原因。
①化学键是相邻的分子之间强烈的相互作用( )
②相邻原子之间的相互作用叫化学键( )
③相邻的原子之间强烈的相互吸引叫化学键( )
④任何物质中均存在化学键。 ( )××××一、化学键与物质变化二、化学反应中物质变化的实质: 旧化学键断裂和新化学键形成。 根据化学反应的实质是旧键断裂,新键生成这一事实,判断下列变化哪些是化学变化,并说出理由。1.石墨在高温下转化为金刚石;
2.碘升华;
3.氯气加压变成液氯;
4.HCl溶于水。
交流研讨1:? 1.试从化学键的角度分析水分解的最终产物是氢气和氧气,为何不是氢原子和氧原子?
2.稀有气体原子能够稳定存在,其它元素的原子不能稳定存在, 为什么?深度探究活动探究21.试画出H、Cl、Na原子结构示意图;
2.决定元素性质的主要因素是其最外层电子排布,用磁钉在黑板上摆出1个H、1个Na、2个Cl原子最外层电子排布情况。
3. 从元素原子得失电子能力的角度来分析,H与Cl、Na与Cl如何形成氯化氢与氯化钠?试用磁钉摆出它们最终的存在形式。
4.氯化氢中的化学键与氯化钠中的化学键是否一样?原子之间是如何形成化学键的?H原子间通过共用电子形成的化学键共价键1+17782共价键的形成三、化学键的类型—共价键(H2+ Cl2== 2HCl )点燃 请运用你所学的知识判断下列哪些物质中存在共价键?
NaF CH4 H2O CaO
H2 MgCl2 O2 CO 2 思考:2.化学键的类型1.共价键Na-+离子键阴、阳离子之间通过静电作用
形成的化学键
氯化钠的形成过程三、化学键的类型—离子键 请运用你所学的知识判断下列物质中分别存在哪些类型的化学键?
NaF CH4 H2O CaO KBr
HF BaCl2 O2 CO 2 MgCl2离子键: NaF CaO KBr BaCl2 MgCl2共价键: CH4 H2O HF O2 CO 2 三、化学键的类型归纳·比较原子有形成稳定结构的趋势
(最外层电子达到稳定结构)阴、阳离子
原子静电作用共用电子对一般为活泼金属和
活泼非金属一般为非金属和
非金属之间三、化学键的类型[交流研讨3]
①NaCl中Na +、Cl- 间是离子键,为何其固体不导电,熔融态和溶于水导电?
②实验表明AlCl3熔融态不导电,请大胆推想AlCl3中化学键的类型
③推导KNO3 这样的复杂盐中含有哪些类型的化学键?
④铵盐中的铵根是由氨气分子衍变来的,由于化学性质类似于金属,中国科学家将其命名为“铵” ,推断NH4Cl中可能有哪些类型的化学键? 熔融态或溶于水产生了自由移动的离子共价键离子键和共价键离子键和共价键小 结化学键化学反应中物质变化的实质旧键断裂,新键生成定义分类一百多种元素 千千万万种物质小 结化学键化学反应中物质变化的实质旧键断裂,新键生成阴阳离子通过静电作用通过共用电子对定义分类课堂练习·活动1.下列物质中含有离子键的是A.H2O B CaCl2 C. HCl D. Cl2课堂练习·活动2.下列各组化合物中化学键类型不同的是A. NaCl和KF B. H2O和NH3 C. CaF2和CsCl D. CCl4和Na2O3. 下列数值表示有关元素的原子序数,各原子能以离子键相互结合成稳定的化合物的是( )
A.10 与19 B. 6与 16
C. 11 与17 D. 14 与8
小 结化学键化学反应中物质变化的实质旧键断裂,新键生成阴阳离子通过静电作用通过共用电子对定义分类
物质
变化利用
能量
变化化学反应的应用第1课时:化学键与化学反应中的物质变化键的中文解释
基本字义 1.? 安装在车轴头上管住车轮或使轴与齿轮等连接固定的零件,一般是用钢制的长方条(亦称“辖”):关~。
2.? 插在门上关锁门户的金属棍子,将两扇门牢固连接:“掌授管~以启闭国门”。
3.? 琴或机器上使用时用手按动的部分:~盘。~子。琴~。
【学习目标】
1.初步学会从分子、原子的微观角度认识化学反应中物质变化的实质。
2.理解化学键的含义,能描述共价键、离子键的形成过程与形成条件。
3. 学会判断物质中存在的化学键。第1课时:化学键与化学反应中的物质变化一、化学键与物质变化 原子的重新组合。化学反应中的最小微粒是什么?
初中化学中曾经讨论过的化学反应的实质是什么?
3.
水在通电或高温(2000℃)时才能分解,请用模型演示这一过程,水分子是如何分解生成氢气与氧气的?并尝试解析消耗的高能量用在哪一环节?
原子活动探究1:H2OH2OH2H2O2一、化学键与物质变化化学键:相邻原子间的强相互作用一、化学键与物质变化H与H非直接相邻O与H直接相邻相互作用比较强烈相互作用比较弱在水分子中氢氧键思考:一、化学键与物质变化下列说法是否正确,不正确的指出错误的原因。
①化学键是相邻的分子之间强烈的相互作用( )
②相邻原子之间的相互作用叫化学键( )
③相邻的原子之间强烈的相互吸引叫化学键( )
④任何物质中均存在化学键。 ( )××××一、化学键与物质变化二、化学反应中物质变化的实质: 旧化学键断裂和新化学键形成。 根据化学反应的实质是旧键断裂,新键生成这一事实,判断下列变化哪些是化学变化,并说出理由。1.石墨在高温下转化为金刚石;
2.碘升华;
3.氯气加压变成液氯;
4.HCl溶于水。
交流研讨1:? 1.试从化学键的角度分析水分解的最终产物是氢气和氧气,为何不是氢原子和氧原子?
2.稀有气体原子能够稳定存在,其它元素的原子不能稳定存在, 为什么?深度探究活动探究21.试画出H、Cl、Na原子结构示意图;
2.决定元素性质的主要因素是其最外层电子排布,用磁钉在黑板上摆出1个H、1个Na、2个Cl原子最外层电子排布情况。
3. 从元素原子得失电子能力的角度来分析,H与Cl、Na与Cl如何形成氯化氢与氯化钠?试用磁钉摆出它们最终的存在形式。
4.氯化氢中的化学键与氯化钠中的化学键是否一样?原子之间是如何形成化学键的?H原子间通过共用电子形成的化学键共价键1+17782共价键的形成三、化学键的类型—共价键(H2+ Cl2== 2HCl )点燃 请运用你所学的知识判断下列哪些物质中存在共价键?
NaF CH4 H2O CaO
H2 MgCl2 O2 CO 2 思考:2.化学键的类型1.共价键Na-+离子键阴、阳离子之间通过静电作用
形成的化学键
氯化钠的形成过程三、化学键的类型—离子键 请运用你所学的知识判断下列物质中分别存在哪些类型的化学键?
NaF CH4 H2O CaO KBr
HF BaCl2 O2 CO 2 MgCl2离子键: NaF CaO KBr BaCl2 MgCl2共价键: CH4 H2O HF O2 CO 2 三、化学键的类型归纳·比较原子有形成稳定结构的趋势
(最外层电子达到稳定结构)阴、阳离子
原子静电作用共用电子对一般为活泼金属和
活泼非金属一般为非金属和
非金属之间三、化学键的类型[交流研讨3]
①NaCl中Na +、Cl- 间是离子键,为何其固体不导电,熔融态和溶于水导电?
②实验表明AlCl3熔融态不导电,请大胆推想AlCl3中化学键的类型
③推导KNO3 这样的复杂盐中含有哪些类型的化学键?
④铵盐中的铵根是由氨气分子衍变来的,由于化学性质类似于金属,中国科学家将其命名为“铵” ,推断NH4Cl中可能有哪些类型的化学键? 熔融态或溶于水产生了自由移动的离子共价键离子键和共价键离子键和共价键小 结化学键化学反应中物质变化的实质旧键断裂,新键生成定义分类一百多种元素 千千万万种物质小 结化学键化学反应中物质变化的实质旧键断裂,新键生成阴阳离子通过静电作用通过共用电子对定义分类课堂练习·活动1.下列物质中含有离子键的是A.H2O B CaCl2 C. HCl D. Cl2课堂练习·活动2.下列各组化合物中化学键类型不同的是A. NaCl和KF B. H2O和NH3 C. CaF2和CsCl D. CCl4和Na2O3. 下列数值表示有关元素的原子序数,各原子能以离子键相互结合成稳定的化合物的是( )
A.10 与19 B. 6与 16
C. 11 与17 D. 14 与8
小 结化学键化学反应中物质变化的实质旧键断裂,新键生成阴阳离子通过静电作用通过共用电子对定义分类
