浙教版科学八年级下册3.4 二氧化碳 教案
文档属性
| 名称 | 浙教版科学八年级下册3.4 二氧化碳 教案 |

|
|
| 格式 | zip | ||
| 文件大小 | 87.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-03-22 00:00:00 | ||
图片预览


文档简介
课题名称
二氧化碳
课程性质
新授课
教
学
目
标
知识与技能
1.认识二氧化碳,掌握其重要的化学性质,了解其物理性质和主要用途。
2.懂得设计实验来验证物质性质的方法。3.学会对实验中出现的现象进行分析并得出结论的方法。
过程与方法
1.通过观察演示实验的现象,培养学生分析和解决问题的能力。2.通过让学生自己设计实验去验证二氧化碳的性质,培养学生的实验设计能力。3.经过亲自动手实验,让学生懂得二氧化碳可以与水反应生成酸
性的碳酸。
情感态度
价值观
1.通过实验设计和小组活动,培养学生的问题意识以及思维的严密性,发展善于合作、勤于思考、用于创新的精神。2.通过各个验证实验,让学生亲自参与到知识的形成过程中,从而获得成功的喜悦,感受化学就在身边,激发对化学学习的持续兴趣。
教学重点
二氧化碳的化学性质,实验探究过程体验
教学难点
二氧化碳与水的反应的探究
教学方法
从学生已有的生活经验出发,用生活中的材料创设问题情景,整堂课围绕一瓶雪碧展开探究,充分调动学生学习的积极性,激发兴趣,调动思维。引导学生观察实验、分析现象、得出结论。培养学生的分析问题,解决问题和总结规律的能力,同时,把课堂的演示实验改为学生实验,让学生在亲自动手的过程中完成探究的过程,了解科学探究的一般方法。
课前准备
教师的准备:
装满二氧化碳气体的软塑料瓶若干、干冰、阶梯蜡烛、 火柴、烧杯、澄清石灰水、浸过石蕊的紫色小花、食醋、盐酸、酒精灯、试管架、试管夹、喷瓶。
学生分组实验的用品准备:汽水、软塑料瓶、石蕊试剂、气球、试管若干。
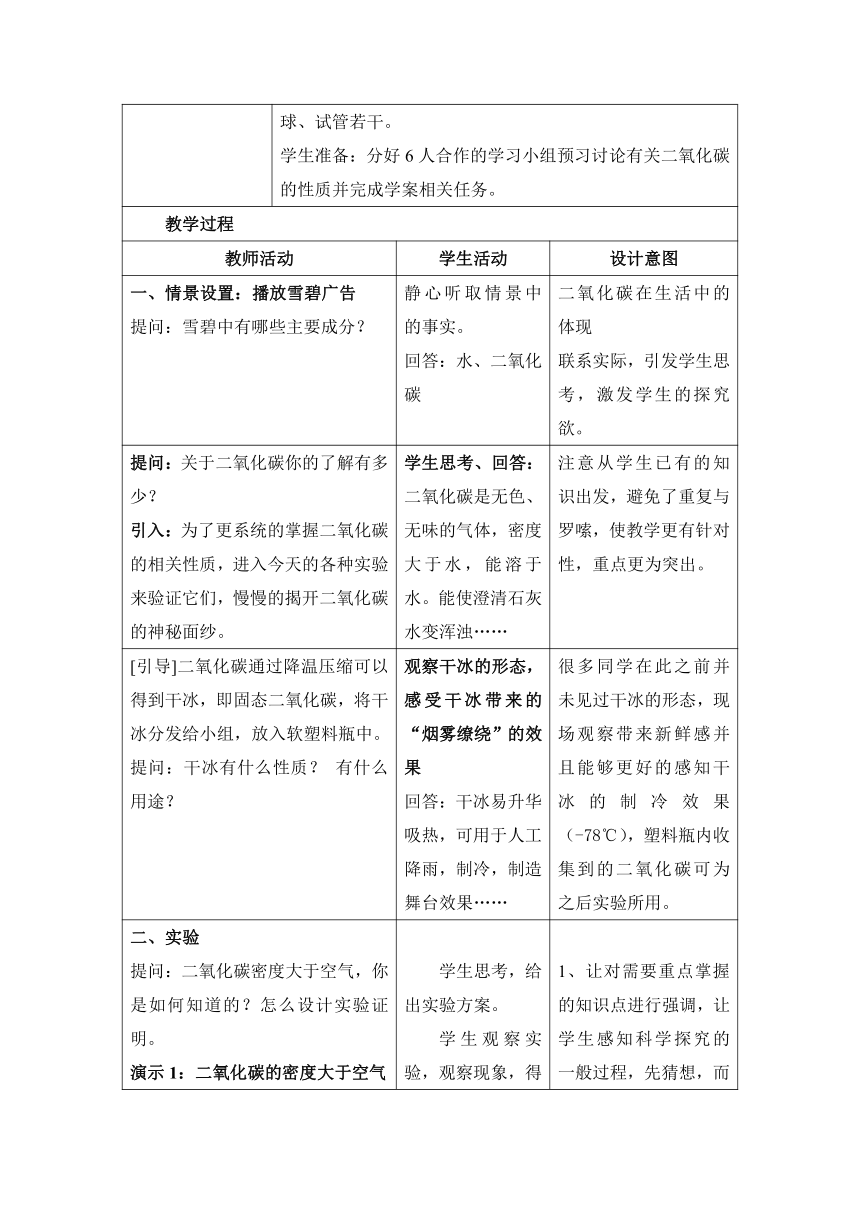
学生准备:分好6人合作的学习小组预习讨论有关二氧化碳的性质并完成学案相关任务。
教学过程
教师活动
学生活动
设计意图
一、情景设置:播放雪碧广告
提问:雪碧中有哪些主要成分?
静心听取情景中的事实。
回答:水、二氧化碳
二氧化碳在生活中的体现
联系实际,引发学生思考,激发学生的探究欲。
提问:关于二氧化碳你的了解有多少?
引入:为了更系统的掌握二氧化碳的相关性质,进入今天的各种实验来验证它们,慢慢的揭开二氧化碳的神秘面纱。
学生思考、回答:二氧化碳是无色、无味的气体,密度大于水,能溶于水。能使澄清石灰水变浑浊……
注意从学生已有的知识出发,避免了重复与罗嗦,使教学更有针对性,重点更为突出。
[引导]二氧化碳通过降温压缩可以得到干冰,即固态二氧化碳,将干冰分发给小组,放入软塑料瓶中。
提问:干冰有什么性质? 有什么用途?
观察干冰的形态,感受干冰带来的“烟雾缭绕”的效果
回答:干冰易升华吸热,可用于人工降雨,制冷,制造舞台效果……
很多同学在此之前并未见过干冰的形态,现场观察带来新鲜感并且能够更好的感知干冰的制冷效果(-78℃),塑料瓶内收集到的二氧化碳可为之后实验所用。
二、实验
提问:二氧化碳密度大于空气,你是如何知道的?怎么设计实验证明。
演示1:二氧化碳的密度大于空气
实验1.用二氧化碳倾倒阶梯上的蜡烛
[引导]同学们看到什么现象?这说明了二氧化碳具有什么性质?
[现象]下层蜡烛熄灭,上层蜡烛后熄灭。
[结论]二氧化的密度比空气大;其既不能燃烧也不能支持燃烧
学生活动1:验证二氧化碳溶于水
实验2.在装满二氧化碳的软塑料瓶内倒入少量水盖紧瓶盖。振荡。
[现象]瓶子变扁
[结论]二氧化碳能溶于水
[补充]1体积水能溶解1体积的二氧化碳,要使二氧化碳溶解度升高可通过加压的办法。
学生思考,给出实验方案。
学生观察实验,观察现象,得出结论。完成学习材料。
在快乐的氛围中快乐地学习知识,许多学生都能够分析出原因。
学生可能的猜想:蜡烛会熄灭,而且是下面的先熄灭上面的后熄灭学生观察实验现象并思考回答,解释原因。实验1说明二氧化碳的密度比空气大(物理性质),不能燃烧一般情况下也不能支持燃烧(化学性质)。
实验2说明二氧化碳能溶于水。
1、让对需要重点掌握的知识点进行强调,让学生感知科学探究的一般过程,先猜想,而后假设,近而实验,推出结论。培养学生对科学探究的情感。
2、培养学生的观察能力和表达能力。
培养学生的实验分析能力,通过小组的合作互相启迪互相补充并完善自己所学知识。
蜡烛燃烧具有一定的危险性并且会影响室内空气,因此该实验由教师完成;用之前收集到的二氧化碳完成第二个实验,现象直观明显,增加课堂趣味性。通过学生的亲身体会,对知识的掌握将更为深刻。
【过渡】前面我们刚做完倾倒二氧化碳熄灭蜡烛的实验,除了说明二氧化碳密度比空气大之外,又说明了二氧化碳既不燃烧又不支持燃烧,这是其化学性质之一那么二氧化碳的化学性质又有那些呢?
提问:进入菜窖、山洞之前要怎样验证二氧化碳浓度是否超标?
学生开始回忆总结
一般状况下,二氧化碳既不燃烧,也不支持燃烧
二氧化碳也不支持呼吸作用
灯火实验
培养学生对已有知识的归纳能力和思考能力。将化学与生活联系起来。加深学生对知识的影响,激发学生学习化学的热情。
设问:前面我们刚学到二氧化碳溶能于水,那么二氧化碳溶于水后的饮料为什么不叫做二氧化碳水溶液而叫做碳酸饮料?
介绍石蕊试剂-遇酸变红。
演示2:指示剂变色实验
向干燥的用紫色石蕊试液浸泡过的小花喷洒稀醋酸和盐酸
学生活动2:验证塑料瓶内的液体能使紫色石蕊试剂变红。
[结论]说明二氧化碳溶的水溶液中存在酸性物质。
提问:是什么让石蕊变色?设计实验支持你的观点。
【结合之前给出的实验材料,根据探究实验的一般步骤让学生在课下写出设计方案。写出设计每一步的目的,让学生讲述自己小组的实验设计。】
阅读学案中关于石蕊的介绍:石蕊是一种植物的色素,能在酸性、中性及碱性环境下显现出三种不同的颜色。
观察现象:紫色花变红色
得出结论:酸能使紫色石蕊变红
经过思考猜想:
1.让石蕊变色的可能是二氧化碳气体;
2.让石蕊变色的是二氧化碳与水反应的产物
讲述自己的设计和准备如何实施,并对实验现象进行猜想。
学生第一次接触酸碱指示剂,用直观现象让他们更好的感知指示剂的作用。亲自动手实验,通过变色反应自然的引导出碳酸。
通过让学生讲述自己的设计提高学生的表述能力,并使学生初步学会评价和改进实验设计;通过赞美学生的设计让学生感受成功的喜悦,激发学生的学习兴趣。
三、实验探究:
演示3:二氧化碳于水反应
1、把紫色花放入装有二氧化碳的集气瓶中
2、把喷水后的紫色花放入装有二氧化碳的瓶中
[讲述]和醋酸、盐酸一样,二氧化碳溶于水也产生了一种能使石蕊变红的酸性物质,名叫碳酸。
[引导]雪碧放久了,里面的二氧化碳跑掉了,味道就不如之前的好了,碳酸是否不稳定,溶解分解?
演示:4:将学生实验2中变红的紫色石蕊放在酒精灯上加热,再观察现象。
[提问]2.为什么变红的纸花又变回紫色?个人回答
观察现象:紫色花不变色
得出结论:干燥的二氧化碳不能使紫色石蕊变红
观察现象:紫色花变红色
得出结论:二氧化碳与水反应生成了一种酸,是这种酸使紫色石蕊变红色。
分析有关实验现象并获知:石蕊变回紫色,说明酸性物质不见了,则碳酸不稳定,受热很容易分解。
1、培养学生用发展的观点看问题。
2、对比实验是化学实验的重要方法,通过使石蕊变色的探究,初步让学生学习对比实验的理念和方法。
3、培养学生发现问题、解决问题、总结归纳的能力。
通过演示实验,让学生观察现象,学会根据实验现象分析、得出结论从而获得成功的喜悦和对化学学习的持续兴趣。
讲解:二氧化碳与水反应生成了碳酸的化学方程式。以及碳酸分解的化学方程式。
学生考虑、记忆、书写
提问:碳酸饮料中的气体是二氧化碳,如何设计实验检验?需教师引导收集碳酸饮料制取二氧化碳。
学生实验3:[引导学生设计]
1、用气球套紧可乐瓶口,晃动可乐瓶,使气球膨胀到拳头大小。
2、将气球套在装有澄清的石灰水的试管口,挤压气球同时振荡试管。
分组动手实验,记录实验现象。
加强实验设计的体验,再次体会实验探究的过程和方法,体会知识获得的过程。有趣的实验现象,增加课堂的趣味性。
归纳与整理:
师:本节课你学到了什么?根据二氧化碳的性质,它有哪些应用?
小组讨论总结。
归纳整理
二氧化碳的物理性质和化学性质
培养学生自我归纳总结的能力。留有疑问让学生有想象的空间。
练习巩固
投影:根据本课的有关知识点设计与生活密切相关的习题来进行知识的巩固和运用
思考,练习
使学生能把学到的知识与实际生活联系在一起,懂得运用有关的化学知识去解决生活中的一些简单的实际问题。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
