第2章 微粒的模型与符号-2.4-6元素、化学式与化合价-提高(学案)
文档属性
| 名称 | 第2章 微粒的模型与符号-2.4-6元素、化学式与化合价-提高(学案) |

|
|
| 格式 | zip | ||
| 文件大小 | 948.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-03-30 00:00:00 | ||
图片预览




文档简介
2019浙教版八年级下——2.4-6元素、化学式与化合价-提高
一、元素
内容一、元素是什么
1. 元素的定义
氧原子 氧分子 氧气
氧原子和氢原子 水分子 水
氧原子和碳原子 二氧化碳分子 二氧化碳
氧原子和磷原子 五氧化二磷分子 五氧化二磷
以上这些物质的分子的微粒中都含有氧原子,这些氧原子的核电荷数都是8,凡是核电荷数是8的原子都归为同一类,称氧元素。此外,把核电荷数为6的同一类原子称为碳元素;将核电荷数为15的同一类原子称为磷元素等等。
因此:元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
【注意】质子数决定元素的种类
2.元素与原子的区别和联系
元素 原子
区别 是宏观概念,只讲种类,不讲个数 是微观概念,既讲种类,也讲个数
使用范围 描述物质的宏观组成,如:水是由氢元素和氧元素组成的 用来描述由原子直接构成的物质或分子的构成。如铁是由铁原子构成的
联系 只要核电荷数相同的原子就属于同一种元素。原子是元素的最小单位,元素则是原子的一个归类“集体”。即元素和原子是总体和个体的关系。
3.用元素解释初中常见概念
单质:由同种元素组成的纯净物
化合物:由不同种元素组成的纯净物叫化合物。
氧化物:由两种元素组成,其中一种元素是氧元素的化合物。
【注意】氧化物不等同于含氧化合物,确切的说含氧化合物包括氧化物。如KMnO4为含氧化合物,不是氧化物。
【思考】现有下列物质,利用这些物质完成下面的物质分类网络,并将物质按照不同类别填入网络中:
石灰石、石墨、食盐水、空气、碘盐、医用酒精、冰水混合物、C60、CO、CH3OH 、O2、H2SO4、MgO、NaOH、SiO2、KClO3、CH3COOH、O3
(
混合物
纯净物
) (
A
)
(
B
) (
单质
化合物
)物质
其中属于氧化物的有
网络中A、B表示的是分类标准,请从以下提供的分类标准中找出正确的对应关系的序号填入空格中
A为 ;B为
①按由同种物质还是不同物质组成来分
②按由同种元素还是不同种元素组成来分
③按由同种原子还是不同种原子来分
④按物质的性质相同或不同来分
【答案】混合物:食盐水、空气、碘盐、医用酒精、石灰石
单质:石墨、C60、O2、O3
化合物:CO、CH3OH、H2SO4、MgO、NaOH、SiO2、KClO3、CH3COOH、冰水共存物
氧化物:CO、MgO、SiO2、冰水混合物
①②
内容二、元素周期表及元素符号
1.元素周期表
(
图5-1氧元素的信息
)(1)根据元素的原子结构和性质,将已知的100多种元素按原子序数(指按元素原子核电荷数递增的顺序给元素编的号,数值上等于核电荷数)科学有序地排列起来所得的表,叫做元素周期表。
(2)元素周期表的意义
① 为寻找新元素提供理论依据;
② 由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。
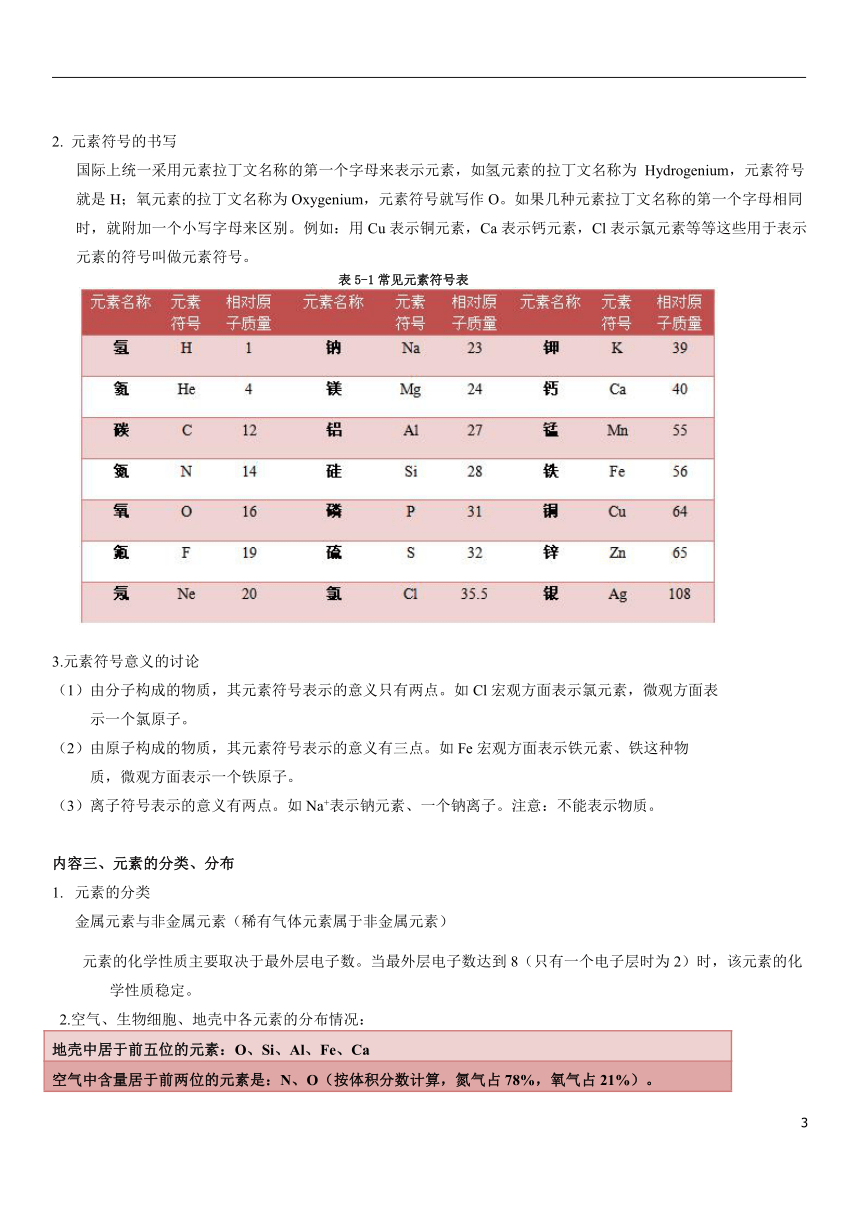
2. 元素符号的书写
国际上统一采用元素拉丁文名称的第一个字母来表示元素,如氢元素的拉丁文名称为 Hydrogenium,元素符号就是H;氧元素的拉丁文名称为Oxygenium,元素符号就写作O。如果几种元素拉丁文名称的第一个字母相同时,就附加一个小写字母来区别。例如:用Cu表示铜元素,Ca表示钙元素,Cl表示氯元素等等这些用于表示元素的符号叫做元素符号。
(
表5-1常见元素符号表
)
3.元素符号意义的讨论
(1)由分子构成的物质,其元素符号表示的意义只有两点。如Cl宏观方面表示氯元素,微观方面表
示一个氯原子。
(2)由原子构成的物质,其元素符号表示的意义有三点。如Fe宏观方面表示铁元素、铁这种物
质,微观方面表示一个铁原子。
(3)离子符号表示的意义有两点。如Na+表示钠元素、一个钠离子。注意:不能表示物质。
内容三、元素的分类、分布
元素的分类
金属元素与非金属元素(稀有气体元素属于非金属元素)
元素的化学性质主要取决于最外层电子数。当最外层电子数达到8(只有一个电子层时为2)时,该元素的化学性质稳定。
2.空气、生物细胞、地壳中各元素的分布情况:
地壳中居于前五位的元素:O、Si、Al、Fe、Ca
空气中含量居于前两位的元素是:N、O(按体积分数计算,氮气占78%,氧气占21%)。
人体中居于前四位的元素:O、C 、H、N。人体中含量最多的金属元素是Ca元素。
内容四、元素的性质—化合价
1.化合价的意义:化合价是元素的一种性质,它用来表示不同元素的原子之间相互化合的数目。
2.化合价的表示方法:通常在元素符号或原子团的正上方用“+n”“-n”表示,如、等。 (
表5-2常见元素的化合价表
)
元素 名称 元素 符号 常见的化合价 元素 名称 元素 符号 常见的化合价
钾 钠 银 钙 镁 钡 锌 铜 铁 铝 锰 K Na Ag Ca Mg Ba Zn Cu Fe Al Mn +1 +1 +1 +2 +2 +2 +2 +1,+2 +2,+3 +3 +2,+4,+6,+7 氢 氟 氯 氧 硫 碳 硅 氮 磷 H F Cl O S C Si N P +1 -1 -1,+1,+5,+7 -2 -2,+4,+6 +2,+4 +4 -3,+2,+4,+5 -3,+3,+5
常用元素化合价口诀:一价氯氢钾钠银,
二价氧镁钙钡锌,
三铝四硅五价磷,
二三铁、二四碳,
二四六硫都齐全,
铜汞二价最常见,
单质零价要记全。
(
-1
硝酸氢氧根,
-2
碳酸硫酸根,
+1
价的是铵根,
-3
价的磷酸根。
)记忆口诀:
计算化合价
(
例
如:
确定氯酸钾中氯元素的化合价。
解: ⑴写出氯酸钾的化学式:KClO
3
⑵查表得出钾元素为+1价,氧元素为-2价,但氯元素有-1价、+1价、+5价、+7价等。
⑶根据化合物中各元素正负化合价的代数和为零求出氯元素的化合价。
设氯元素的化合价为x。
1
+
x
+
(
-
2)
3=0
解得:x=
+
5
⑷ 标出各元素的化合价。
KClO
3
+1+5 -2
)
3.区别化合价的标示法和离子符号的标示法:
元素化合价的标示 离子符号的标示
区别 (1)标在元素符号上方 (2)正负号在数值之前 (3)其数值1要标出 (1)标在元素符号右上角 (2)正负号在数值后 (3)电荷数值为1时省略
联系 符号相同,数值相同
示例 (
Na
+
、
S
2-
)
【注意】有些物质的组成元素相同,但其中某元素的化合价不同,则表示不同的物质。(例:NH3、NO)
有些原子团表示方法相似,但其中某元素的化合价不同,则表示不同的原子团。(例:CO、CO2)
内容五、元素符号组成的式子化学式
1.化学式的含义:用元素符号和数字的组合表示物质组成的式子。
2.化学式的写法:
(1)单质化学式的写法:
① 稀有气体、金属和一些非金属是由原子直接构成的,它们的化学式可直接用元素符号来表示。如:氦气(He)、铜(Cu)、硫(S)等。
② 一些由分子构成的物质,其化学式要在元素符号的右下角标出原子个数。
如:氢气(H2)、氯气(Cl2)、臭氧(O3)等。
(2)化合物化学式的写法:
① 由两种元素组成的化合物中,如果是氧化物,习惯上把氧元素的符号写在右侧,另一种元素在左侧,然后在元素符号右下角标出每个分子中含该元素的原子个数,如:CO2、MgO、P2O5等。
② 如果是由金属元素和非金属元素组成的化合物,习惯上把金属元素的符号写在左侧,非金属元素的符号写在右侧,然后标出相应的原子个数,如:NaCl、Na2S、BaCl2等。
③两种非金属元素组成的化合物,正价元素在前、负价在后。
【小结】金左,非金右;正价左,负价右;氧化物,氧在右。
【思考】判断下列物质的化学式是否正确,如不正确请将正确的写在后面:
碳酸钠:NaCO3 Na2CO3
氢氧化钙:CaOH2 Ca(OH)2
四氧化三铁:Fe3O4 √
一氧化碳:Co CO
氧化镁:MgO2 MgO
硫酸铜:Cu2SO4 CuSO4
氧化铁:FeO Fe2O3
3.化学式的意义
物质的组成可以从宏观和微观两个方面进行描述,其中元素是从宏观上对物质的组成进行描述,而原子、分子是从微观上对物质的构成进行描述。
宏观方面:化学式表示一种物质,表示物质的元素组成。
微观方面:如果确知某种物质是由分子构成的,则化学式还表示该物质的一个分子及构成该分子中的原子。当在化学式前面加写了数字时,那就只能有微观意义,表示几个分子。
(
P
2
O
5
表示五氧化二磷这种物质
表示五氧化二磷是由磷氧两种元素组成
表示一个五氧化二磷分子
表示一个五氧化二磷分子是由两个磷原子和五个氧原子构成
宏观
微观
)例如:
(
2P
2
O
5
表示两个五氧化二磷分子
)
【思考】判断下列表示方法是否正确,如不正确请将正确的写在后面:
2个氢离子H2+ 2H+
2个碳酸根离子:2CO32- √
3个亚铁离子:3Fe3+ 3Fe2+
4个氢原子:2H2 4H
1个镁离子 Mg2+
2个氧分子O2 2O2
3个氮原子N3 3N
2H—2个氢元素 2个氢原子
(
例题精讲
)
【例1】右图为元素周期表第三周期的一部分。下列说法中正确的是( )
A.它们都属于金属元素
B.Al的相对原子质量是26.98g
C.Mg原子的核外电子排布是
D.Si元素的名称是硅,其核电荷数为14
【答案】D
【例2】
①由化学式推求化合价
工业明胶中含有毒的重铬酸钠(Na2CrO4),其中Cr元素的化合价为( )
A. +1价 B. +2价 C.+4价 D.+6价
白钨矿(主要成分为CaWO4)是一种重要的含钨矿物,CaWO4中钨元素(W)的化合价是( )
A.+6 B.+4 C.+2 D.-2
次氯酸钠(NaClO)是某种家用消毒液的主要成分,其中氯元素的化合价为( )
A.﹣1 B.﹢1 C.﹢3 D.﹢5
市场上有一种药品“亚硒酸钠片”能为人体补充必需的微量元素硒,“亚硒酸钠片”中主要成分为Na2SeO3,其中硒元素化合价是( )
A.﹣4 B.﹣6 C.﹢4 D.﹢6
“问题胶囊”已成为公众关注的热点,胶囊中铬含量超标对人体有害。请计算重铬酸
钾(K2Cr2O7)中铬元素的化合价( )
A. +3 B.+6 C.+7 D.+12
②用化合价推求化学式
磨牙器能有效帮助祛除牙齿表面的牙垢,磨牙器的磨头采用50%橡胶和50%的金刚砂(碳化硅)特制
而成。碳化硅中碳元素-4价、硅元素+4价,碳化硅的化学式
钛铁矿主要成分的化学式为FeTiOx,铁元素和钛元素的化合价均显+3价,则X为
【答案】①D;A;B; C;B ②SiC;3
【例3】①下列物质的主要成分属于氧化物的是( )
A.水晶(SiO2) B.钻石(C) C.食盐(NaCl) D.钟乳石(CaCO3)
【答案】A
②地壳中含量最多的元素是 ,最多的金属元素是
A.氧 B.硅 C.铝 D.铁
【答案】A;C
③日常生活中加碘食盐的“碘”是指( )
A.单质 B.分子 C.原子 D.元素
【答案】D
【例4】下列有关物质的分类中不正确的是( )
A. 二氧化碳、二氧化硫、水、氧化镁都属于氧化物
B. 氢气、氧气、氨气、碳、铁都属于单质
C. 水、二氧化碳、二氧化硫、磷都含有非金属元素
D. 高锰酸钾、过氧化氢、五氧化二磷都属于化合物
【答案】B
【例5】碳元素与氧元素的本质区别是 ( )
A.质子数不同 B.电子数不同
C.中子数不同 D.最外层电子数不同
【答案】A
【例6】稀土元素铕(Eu)是激光及原子能应用的重要材料。已知氯化铕的化
学式为EuCl3,则氧化铕的化学式为( )
A.EuO B.Eu2O3 C.Eu3O2? D.EuO3
【答案】B
【例7】下列符号表示正确的是( )
A. 2个氮分子:2N B. 2个碳酸根离子:2CO
C. 氧化铝元素的化合价: D.4个氢原子:2H2
【答案】B
【例8】下列有关叙述的七句话中,所选答案均正确的一组是( )
①表示二氧化碳这种物质 ②CO2是由碳和氧气两种单质组成的
③CO2是由一个碳原子和两个氧原子组成的 ④CO2是由碳原子和氧分子组成的
⑤CO2是由一个碳元素和两个氧元素组成的 ⑥CO2分子里含有一个碳元素和两个氧元素
⑦CO2是由碳和氧两种元素组成的
⑧CO2是由二氧化碳分子构成,每个二氧化碳分子是由两个氧原子和一个碳原子构成。
A.①③⑦ ⑧ B.①③⑥⑦⑧ C.①②③④⑦⑧ D.①⑦⑧
【答案】D
【例9】下列图示中,“●”和“○”分别表示不同的原子,请回答下列问题:
其中表示由分子构成的化合物是图 (填编号),图 中的分子构成的是混合物(填编号)。若黑球表示氢原子、白球表示氧原子则图中③的分子的化学式是 ,图中⑥的分子的化学式是 ,写出由氢氧两种元素组成的两种氧化物的化学式 、 。图①中的分子能否保持该物质的化学性质 (填“能”或“不能”)。
【答案】①④;②⑤⑦;H2,O2;H2O,H2O2;能
【例10】下表为元素周期表中某_周期元素的原子结构示意图。
请回答下列问题:
元素名称 钠 镁 铝 硅 磷 硫 氯 氩
元素符号 Na Mg Al Si P S Cl Ar
原子结构 示意图
(1)表中磷原子的核电荷数x=___________。
(2)表中具有相对稳定结构的元素是_____________。
(3)在化学反应中,每个铝原子失去_____________个电子形成铝离子。
(4)镁元素与氯元素形成的化合物化学式为_______________。
【答案】(1)15 (2)Ar (3)3 (4)MgCl2
二、化学式的计算
(1)计算相对分子质量
相对分子质量 =【(化学式中各原子的相对原子质量)×(其原子个数)】之和。
【注意】相对分子质量不带单位。
(2)计算物质组成元素的质量比
元素质量比 = 【(化学式中各原子的相对原子质量)×(其原子个数)】之比。
原子的个数比= 分子的个数比=
(3)计算物质中某元素的质量分数
某元素的质量分数 = (某元素的相对质量)÷(某物质的相对分子质量)×100%
(4)混合物中某元素的质量分数
混合物中某元素的质量分数 = 样品中某物质的质量分数某物质中某元素的质量分数
(
例题精讲
)
【例11】 甲型H1N1流感病毒正威胁着人类的健康和安全。“达菲”(C16H28O4N2)是目前世界上
治疗H1N1流感病毒的良药。生产“达菲”的主要原料是莽草酸,可从茴香中提取。回答下列问题:
(1)“达菲”分子的相对分子质量为_______________
(2)“达菲”分子中,氧、氮两种元素的质量比为______
(3)右图为莽草酸理化性质的描述,其中属于化学性质的是 (填序号)。 (
A
.熔点
185
℃
-191
℃
,气味辛酸。
B
.莽草酸为白色精细粉末。
C
.易溶于水,难溶于氯仿、苯和石油。
D
.能与活泼金属、酸性高锰酸钾溶液反应。
)
【答案】 (1)312 (2)16:7(3)D
【例12】①根据元素的质量比确定化学式:某氮的氧化物中,氮元素与氧元素的质量比为7:16,则该
氧化物的化学式为( )
A. NO B. NO2 C. N2O D. N2O5
【答案】B
②A、B两元素可组成多种化合物。已知在A2B化合物中,A和B的质量比为7:4,则符合
A、B质量比为7:12的化合物是( )
A. A2B B. A2B3 C. AB D. A2B5
【答案】B
【例13】1989年世界卫生组织把铝列为食品污染源之一,每人每日的摄入量控制在0.004g以下。若在
1kg米面食品中加入明矾2g(胆矾的化学式为KAl(SO4)2·12H2O,相对分子质量为474),回
答下列问题:
(1)人从食物中摄入的铝指的是 (填字母)。
A.铝元素 B.铝单质 C.铝合金 D.只有明矾
(2)明矾中各元素的质量比K∶Al∶S∶O∶H= ;铝元素的质量分数为
(计算结果精确到0.1%)。
(3)如果某人一天吃了100g上述面食品,通过计算说明其摄入的铝的量是否超过安全摄入量?
【答案】A;39∶27∶64∶320∶24;5.7%;超过。
(
拓展训练
)
1.某葡萄糖酸钙锌口服溶液使用说明书的部分内容如下:
本品为复方制剂,每瓶含葡萄糖酸钙【】、葡萄糖酸锌【】。 【规格】 【用法用量】婴幼儿每日。成人每日,分次饭后服或遵医嘱。
(1)葡萄糖酸钙【Ca(C6H11O7)2】中含有 种元素,其中钙元素和氧元素的
质量比为 。
(2)葡萄糖酸钙【Ca(C6H11O7)2】的相对分子质量为 。
(3)葡萄糖酸钙【Ca(C6H11O7)2】中钙元素的质量分数为 。
(4)某幼儿每日服用一定量该葡萄糖酸钙锌口服溶液,若他每日摄入的口服液含15 mg
葡萄糖酸锌,则同时摄入的钙元素的质量为 mg。
【答案】(1)4 5:28 (2)430
(3)9.3% (4)27.9
2. 在宏观、微观和符号之间建立联系是化学学科的特点。
(1)将“分子”、“原子”、“元素”填入如图1序号所对应的横线上。
① ;② ; ③ 。
(2)在铜、氯化钠、二氧化碳三种物质中,由离子构成的是 。
(3)请用化学符号填写:
(1)二氧化硫 (2)氧化钙中钙元素显+2价 (3)2个氢原子
(4)根据原子结构的相关知识和图2的信息填空:
图2
甲图中①代表的元素符号是 ,乙图中所示元素原子的核电荷数是 ,铝和氧两种元素形成化合物的化学式是 。
丙图所示粒子属于 (填“原子”、“阳离子”或“阴离子”),其微粒符号是 。
【答案】(1)①元素 ②原子 ③分子 (2)氯化钠
(3)SO2 2H
(4)Al 8 Al2O3 阳离子 Mg2+
(
复习巩固
)
【演练1】某反应的微观示意图如下,下列说法正确的是 ( )
A. 图中甲、乙、丙三种物质均是由分子构成的
B. 图中甲、乙、丙三种物质中,甲、丙属于氧化物
C. 该反应前后分子种类、原子种类均没有改变
D. 图中甲、乙、丙三种物质既有单质又有化合物
【答案】D
【演练2】在H2S、S、SO2、SO3、H2SO4、H2SO3、Na2SO4几种物质中,下列说法正确的是( )
A. 几种物质均含有硫原子
B. 几种物质均为含硫的化合物
C. 几种物质中有三种物质中硫元素的化合价为+6价
D. 几种物质中有一种物质中硫元素的化合价为+4价
【答案】C
【演练3】右图为某有机物()的分子模型,该有机物是一种高效食品防腐
剂。下列说法中,不正确的是( )
A.该有机物由3种元素组成
B.该有机物能减缓食品变质
C.该有机物分子中碳、氧原子的个数比为3:1
D.该有机物中含氧元素的质量分数最小
【答案】D
【演练4】 在质量相等的二氧化碳气体和一氧化碳气体中,含有氧原子个数比是( )
A. 1∶2 B. 2∶1 C. 11∶14 D. 14∶11
【答案】D
【演练5】在硝酸铵样品中氮元素的质量分数为33.6%,求样品中硝酸铵的质量分数(杂质中不含氮).
【答案】NH4NO3中氮元素的质量分数为:,
样品中硝酸铵的质量分数=.
(
1
)
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
