2.6 表示物质的符号(课件 47张PPT)(提高班)
文档属性
| 名称 | 2.6 表示物质的符号(课件 47张PPT)(提高班) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-04-01 00:00:00 | ||
图片预览








文档简介
表示物质的符号
第6节
用元素符号来表示物质分子组成的式子
化学式应由实验确定,一种物质只有一个化学式。不能随意写出!
一种元素能用符号表示,那么某一种物质能否用符号表示呢?
1. 单质化学式的写法:
(1)稀有气体是由原子直接构成的,就用元素符号来表示。
氦气____;氖气____;氩气______;
(2)金属单质和固态非金属单质也用元素符号来表示。
铝____;铜____;金刚石___;磷___.
硫____。
He
Ne
Ar
Al
Cu
C
P
S
化学式的书写规则:
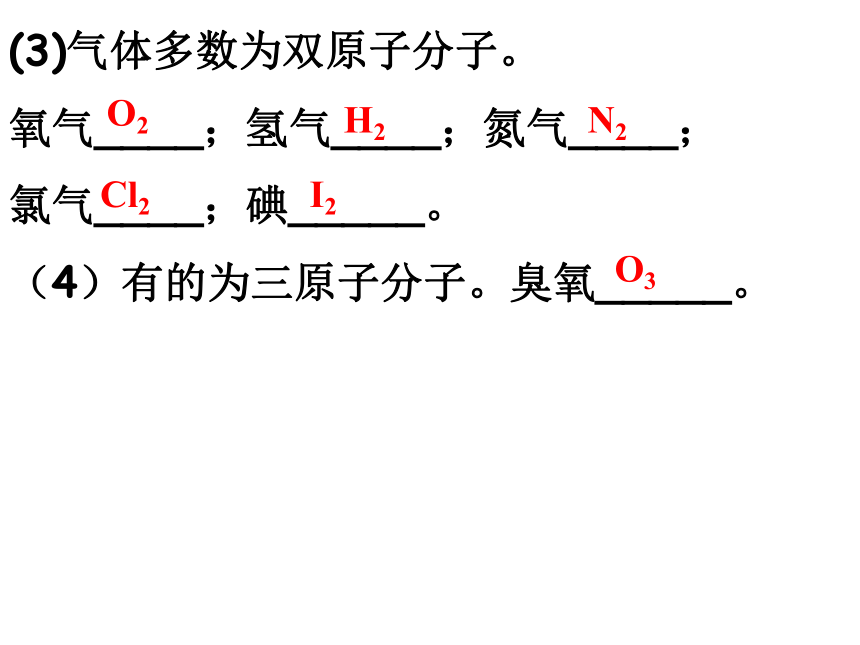
(3)气体多数为双原子分子。
氧气____;氢气____;氮气____;
氯气____;碘_____。
(4)有的为三原子分子。臭氧_____。
O2
H2
N2
Cl2
I2
O3
2.化合物化学式的写法:
(1)氧元素与另一元素组成的化合物,一般把氧元素符号写在右边。
一氧化碳____、二氧化碳_____.
一氧化氮____、二氧化氮_____.
二氧化硫____、三氧化硫_____.
四氧化三铁______.三氧化二铁_______
CO
NO
NO2
CO2
SO2
SO3
Fe3O4
Fe2O3
正左负右
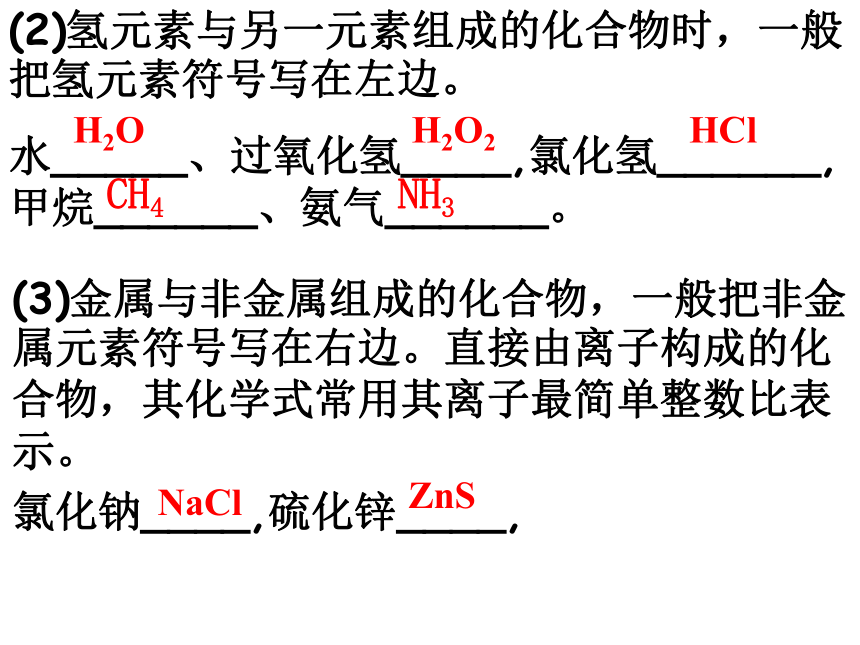
(2)氢元素与另一元素组成的化合物时,一般把氢元素符号写在左边。
NH3
CH4
HCl
H2O
H2O2
水_____、过氧化氢____,氯化氢______,
甲烷______、氨气______。
(3)金属与非金属组成的化合物,一般把非金属元素符号写在右边。直接由离子构成的化合物,其化学式常用其离子最简单整数比表示。
NaCl
ZnS
氯化钠____,硫化锌____,
读法:一般从右到左读“某化某”
或“几某化几某”
P2O5 ________SO3 _________
CuO_________MgO_________
CO __________N2O _________
五氧化二磷
三氧化硫
氧化铜
氧化镁
一氧化碳
一氧化二氮
化学式:
宏观:①一种物质;
②元素种类。
微观:①1个分子;
② 1个分子中各原子的个数。
例:化学式CO2 给你传递了什么信息?
化学式前面的系数:表示分子数。
例:2CO2 表示什么意思?
元素符号右上角;先数字后符号;1省略。
离子是带电的原子或原子团。
写法:
Cl- Na+
Ca2+ Mg2+等
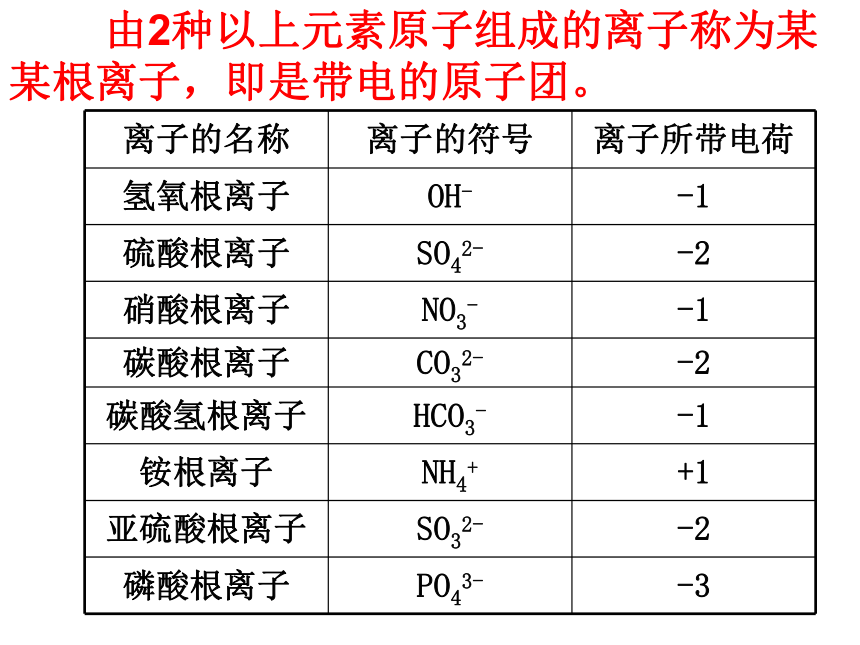
由2种以上元素原子组成的离子称为某某根离子,即是带电的原子团。
离子的名称 离子的符号 离子所带电荷
氢氧根离子 OH- -1
硫酸根离子 SO42- -2
硝酸根离子 NO3- -1
碳酸根离子 CO32- -2
碳酸氢根离子 HCO3- -1
铵根离子 NH4+ +1
亚硫酸根离子 SO32- -2
磷酸根离子 PO43- -3
1:2
2:1
2:2
1:4
1:1
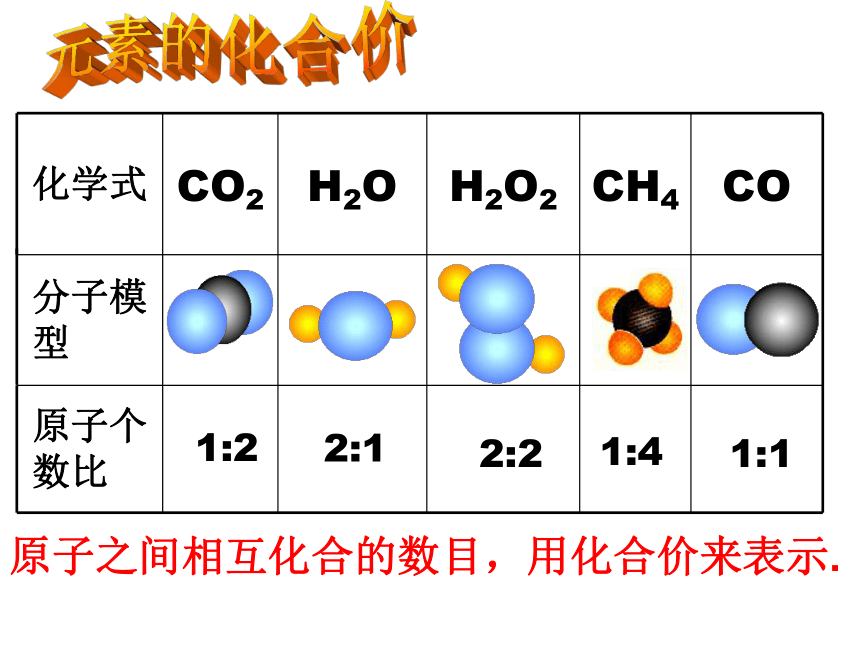
原子之间相互化合的数目,用化合价来表示.
化学式 CO2 H2O H2O2 CH4 CO
分子模型 ? ? ?
原子个数比 ? ?
氢元素的化合价为_____
+ 1
氧元素的化合价为______
- 2
化合物中所有元素化合价的代数和为____
零
标法: 元素符号的正上方;先符号后数字。 1不能省略。
+1 +2 +3 -2 -2 -1
Na Mg Al O S Cl
原因:
Na Mg Al O S Cl
+
2+
3+
2-
2-
-
-1
+4
-2
+6
-2
+2
+1
标出下列物质中带点元素的化合价:
HCl HClO HClO3
HClO4 HnRO2n+1
.
.
.
.
.
-1
+1
+5
+7
+(3n+2)
金属元素 元素
符号 常见的化合价 非金属
元素 元素符号 常见的
化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氧 O -2
钙 Ca +2 氯 Cl -1、+5、+7
镁 Mg +2 溴 Br -1、+5、+7
钡 Ba +2 碘 I -1、+5、+7
锌 Zn +2 氮 N -3、+5
铝 Al +3 磷 P -3、+5
铜 Cu +1、+2 硫 S -2、+4、+6
铁 Fe +2、+3 碳 C -4、+2、+4
锰 Mn +2、+4、+6、+7 硅 Si -4、+4
常见元素化合价记忆口诀
氢钾钠银+1价,钙镁钡锌+2价, 金属铝为+3价,氟氯溴碘-1价,
亚铜+1铜+2, 亚铁+2铁+3,
通常氧硫-2价,氮磷最低-3价,
还有其他可变价。单质全部为0价。
判断:微粒A是 微粒 B 是
微粒C是 。
Al3+
S2—
A B C
O
OH NH4 SO4 CO3
-2
-3
+1
+1
-2
+6
-2
+4
-1
+1
-2
-2
NO3 HCO3 SO3 PO4
+5
+4
+1
+4
+5
-2
-2
-2
-2
-1
-1
-2
-3
原子团化合价是怎样算出来的?
原子团中各元素化合价的代数和就是该原子团的化合价。
-1
-1
+1
-2
-2
-2
-3
思考:原子团是一种物质吗?
原子团 离子符号 电荷 化合价
氢氧根 OH- -1 -1
硝酸根 NO3- -1
碳酸氢根 HCO3- -1
铵根 NH4+ +1
硫酸根 SO42- -2
碳酸根 CO32- -2
亚硫酸根 SO32- -2
磷酸根 PO43- -3
化合价
化学式
交叉法
CaCl2
K2CO3
Ba (NO3)2
常见的化合物中氢总是____价,氧总是____价;金属元素常显_____价。 非金属元素跟氧化合时常显_____价,跟氢化合时常显_______价。 单质中元素的化合价为_____价。 在化合物里,元素正负化合价的代数和为____。有些元素在不同的化合物里常显_____的化合价,如____________;有些元素在不同的化合物里常显_______的化合价,如_______________。
+ 1
- 2
正
正
负
零
零
相同
不同
化合价的一般规则:
H2O CO2
CO CO2
1.单质化学式的写法; 化合物化学式的写法;
2.化学式的读法;
3.化学式传递的宏观与微观的信息;
4.离子符号的写法;
5.常见的带电原子团。
+1
+1
+1
+2
+2
+2
+2
+3
+1 +2
+2 +3
+2 +4 +6+7
+1
- 1
- 2
6. 常见元素的化合价
金属元素 元素
符号 常见的化合价 非金属
元素 元素符号 常见的
化合价
钾 K 氢 H
钠 Na 氟 F
银 Ag 氧 O
钙 Ca 氯 Cl -1、+5、+7
镁 Mg 溴 Br -1、+5、+7
钡 Ba 碘 I -1、+5、+7
锌 Zn 氮 N -3、+5
铝 Al 磷 P -3、+5
铜 Cu 硫 S -2、+4、+6
铁 Fe 碳 C -4、+2、+4
锰 Mn 硅 Si -4、+4
OH-
SO4 2 -
NO3-
CO3 2 -
HCO3-
NH4+
SO3 2 -
PO4 3 -
原子团的化合价
离子的名称 离子的符号
氢氧根离子
硫酸根离子
硝酸根离子
碳酸根离子
碳酸氢根离子
铵根离子
亚硫酸根离子
磷酸根离子
1、某矿泉水中含有的硒(Se)是一种非金属元素,它的化学性质与硫相似。在硒酸(H2SeO4)中Se元素的化合价为( )
A、+4 B、–2 C、+2 D、+6
D
2. A、B、C三种元素的化合价分别是+1、+4、-2,这三元素组成的化合物的化学式可能是 ( )
A.ABC4 B.A4BC3
C.A2BC3 D.A3BC2
C
6、交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机是否酒后开车,因为酒中的乙醇分子可以使橙红色的重铬酸钾)变成绿色的硫酸铬[Cr2(SO4)3],在重铬酸钾和硫酸铬中,铬的化合价依次是 ( )
A、+3、+5 B、+5、+3
C、+3、+6 D、+6、+3
D
12.地壳中含量最多的元素,最多的金属元素,空气中含量最多的元素组成的化合物的化学式是__________。
Al(NO3)3
11.地壳中含量最多的非金属元素跟含量最多的金属元素形成化合物的化学式为 。
Al2O3
13、化合价是元素的一种重要性质,只有在形成 ________ 时表现出来,
在①CuCl2、 ②KClO3、
③HClO4、④HClO四种物质中,按氯元素化合价由低到高顺序排列应是 ___ 。(填序号)
化合物
1 4 2 3
4、写出下列符号的含义:
2O2
H2O2
O
Al3+
-2
2个氧分子
1个过氧化氢分子
化合价为-2价的氧元素
带三个单位正电荷的铝离子
14、写出下列各式中数字“2”的意义:
①2H
②3H2
+2
③CaO
④4Ca2+
2个氢原子
一个氢分子中由2个氢原子构成
氧化钙中钙元素的化合价为+2
一个钙离子带2个单位正电荷
15、市售的“脑黄金”(DHA)是从深海鱼油中提取的,主要成分为一种不饱和脂肪酸,其化学式为C25H50COOH,它是由 种元素组成,每个分子中有 个原子。
3
79
17、下列含有不同原子团的一组物质是
( )
A、NaNO3和Mg(NO3)2
B、KMnO4和K2MnO4
C、Na2CO3和CaCO3
D、FeSO4和Fe2(SO4)3
B
18.标出带点元素的化合价:
NH3 CO2 H2SO4
CaCO3 KMnO4 K2MnO4
H3PO4 P2O5
-3
+4
+6
+4
+7
+6
+5
+5
19.用化学用语表示:
液态氢________水________
过氧化氢_______三氧化硫_________
二氧化硫 硫化氢______
干冰___________
氯化铁_______氯化亚铁______
四氧化三铁_________
氧化铁______氧化亚铁_________
H2
H2O
H2O2
SO3
SO2
H2S
CO2
FeCl3
FeCl2
Fe3O4
Fe2O3
FeO
氧化铝 氧化钠 _______
硫 酸 ___ 硝酸铵________
石灰石 ___ 熟石灰________
亚硫酸钠 _____ 碳酸氢铵________
Al2O3
Na2O
H2SO4
NH4NO3
NH4HCO3
Ca(OH)2
CaCO3
Na2SO3
2个钠离子________铝离子_______
亚铜离子______铜离子_________
亚铁离子____ 铁离子_______
氢离子_____ 氧离子_____
氯离子____ 硫离子_____
2Na+
Al 3+
Cu+
Cu 2 +
Fe 2 +
Fe 3+
H+
O2-
Cl-
S2-
2、下列化学式是否正确,若有错请更正。
氮气—N
氖气—Ne2
氧化镁—MgO
二氧化锰—MNO2
硫化钠—SNa2
√
N2
Ne
MnO2
Na2S
1.化合价为正二价的镁元素 ,
化合价为负二价的硫元素 ,
二氧化碳中的碳元素为正四价 。
Mg
+2
S
-2
CO2
+4
2. 读出下列化学式的名称。
NaCl NaF CaO ZnS MgO
ZnO HCl KCl
下列物质的化学式正确的是( )
(A )氯化钠Na Cl (B) 氧化铁FeO
(C )氧化钡OBa (D) 硫酸铝Al(SO )
2
4
3
2
D
1.已知M元素的化合价为+a价,N元素的化合价为-b价,请写出M N形成化合物的化学式。
MbNa
2.标出下列物质中N元素的化合价,请标在N元素的正上方:
①N2; ②NO;③NO2;④N2O5;
⑤HNO3;⑥NH4NO3
0
+2
+4
+5
+5
+5
-3
1.标出下列单质元素的化合价
Mg O2 Cl2 K
0 0 0 0
在发生化学反应前后,下列各项中
没有变化的是( )
①元素的种类;②分子的数目;
③原子的种类;④原子的数目;
⑤物质的种类
A①③④ B.①④⑤
C.②①③ D.①②④
A
1. 10 CO2分子中的氧原子个数与 个N2O5分子中氧原子的个数相同。
10. 3SO42-表示 _______ ,它共带______ 个单位负电荷。
11.比钠原子多一个质子少一个电子的微粒是( )
A.Ne B.Mg C.Na+ D.Mg2+
D
4
3个硫酸根离子
6
1. 下列化学符号既能表示一种元素、一个原子,还能表示一种单质的是( )
A、2O B、N C、 Fe D、Cl2
关于“2H3PO4”中数字,下列说法不正确的是( )
A、“3”表示氢元素的个数
B、“4”表示每个磷酸分子中含有氧原子的个数
C、“2”表示磷酸分子的个数
D、 “3”表示每个磷酸分子中含有氢原子的个数
C
A
1.下列粒子的结构示意图中,表示非金属元素的原子的是( )
C
2.某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,则该元素的核电荷数为 ( )
A.11 B.15
C.17 D.37
B
5.元素R在化合物中只有一种化合价,下列物质的化学式中错误的是( )
A.R(OH)2 B.RCl3
C.R2(SO4)3 D.R2O3
A
3、如图所示为元素周期表的一部分,已知A元素原子的化合价为+1价,D元素的原子核内有12个质子,回答下列问题:
①D元素属于 (金属、非金属、稀有气体)元素
②C元素的原子核内有 个质子 。
③请推测有关C元素的两点信息:
金属
11
原子序数为11;核外有11个电子 ;属于金属元素;C元素名称是钠; 最外层电子数为1; 电子层数为3层;在化合物中显+1价。
7.用化学用语填空:
(1)地壳中含最多的金属元素____
(2)水通电分解过程中的最小粒子____
(3)构成硫酸钠的阳离子的结构示意图____ (4)在氧化铝中铝显+3价____
(5)两个铵根离子____
(6)同种元素表现出两种化合价的物质____ (7)氩气____
Al
H O
第6节
用元素符号来表示物质分子组成的式子
化学式应由实验确定,一种物质只有一个化学式。不能随意写出!
一种元素能用符号表示,那么某一种物质能否用符号表示呢?
1. 单质化学式的写法:
(1)稀有气体是由原子直接构成的,就用元素符号来表示。
氦气____;氖气____;氩气______;
(2)金属单质和固态非金属单质也用元素符号来表示。
铝____;铜____;金刚石___;磷___.
硫____。
He
Ne
Ar
Al
Cu
C
P
S
化学式的书写规则:
(3)气体多数为双原子分子。
氧气____;氢气____;氮气____;
氯气____;碘_____。
(4)有的为三原子分子。臭氧_____。
O2
H2
N2
Cl2
I2
O3
2.化合物化学式的写法:
(1)氧元素与另一元素组成的化合物,一般把氧元素符号写在右边。
一氧化碳____、二氧化碳_____.
一氧化氮____、二氧化氮_____.
二氧化硫____、三氧化硫_____.
四氧化三铁______.三氧化二铁_______
CO
NO
NO2
CO2
SO2
SO3
Fe3O4
Fe2O3
正左负右
(2)氢元素与另一元素组成的化合物时,一般把氢元素符号写在左边。
NH3
CH4
HCl
H2O
H2O2
水_____、过氧化氢____,氯化氢______,
甲烷______、氨气______。
(3)金属与非金属组成的化合物,一般把非金属元素符号写在右边。直接由离子构成的化合物,其化学式常用其离子最简单整数比表示。
NaCl
ZnS
氯化钠____,硫化锌____,
读法:一般从右到左读“某化某”
或“几某化几某”
P2O5 ________SO3 _________
CuO_________MgO_________
CO __________N2O _________
五氧化二磷
三氧化硫
氧化铜
氧化镁
一氧化碳
一氧化二氮
化学式:
宏观:①一种物质;
②元素种类。
微观:①1个分子;
② 1个分子中各原子的个数。
例:化学式CO2 给你传递了什么信息?
化学式前面的系数:表示分子数。
例:2CO2 表示什么意思?
元素符号右上角;先数字后符号;1省略。
离子是带电的原子或原子团。
写法:
Cl- Na+
Ca2+ Mg2+等
由2种以上元素原子组成的离子称为某某根离子,即是带电的原子团。
离子的名称 离子的符号 离子所带电荷
氢氧根离子 OH- -1
硫酸根离子 SO42- -2
硝酸根离子 NO3- -1
碳酸根离子 CO32- -2
碳酸氢根离子 HCO3- -1
铵根离子 NH4+ +1
亚硫酸根离子 SO32- -2
磷酸根离子 PO43- -3
1:2
2:1
2:2
1:4
1:1
原子之间相互化合的数目,用化合价来表示.
化学式 CO2 H2O H2O2 CH4 CO
分子模型 ? ? ?
原子个数比 ? ?
氢元素的化合价为_____
+ 1
氧元素的化合价为______
- 2
化合物中所有元素化合价的代数和为____
零
标法: 元素符号的正上方;先符号后数字。 1不能省略。
+1 +2 +3 -2 -2 -1
Na Mg Al O S Cl
原因:
Na Mg Al O S Cl
+
2+
3+
2-
2-
-
-1
+4
-2
+6
-2
+2
+1
标出下列物质中带点元素的化合价:
HCl HClO HClO3
HClO4 HnRO2n+1
.
.
.
.
.
-1
+1
+5
+7
+(3n+2)
金属元素 元素
符号 常见的化合价 非金属
元素 元素符号 常见的
化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氧 O -2
钙 Ca +2 氯 Cl -1、+5、+7
镁 Mg +2 溴 Br -1、+5、+7
钡 Ba +2 碘 I -1、+5、+7
锌 Zn +2 氮 N -3、+5
铝 Al +3 磷 P -3、+5
铜 Cu +1、+2 硫 S -2、+4、+6
铁 Fe +2、+3 碳 C -4、+2、+4
锰 Mn +2、+4、+6、+7 硅 Si -4、+4
常见元素化合价记忆口诀
氢钾钠银+1价,钙镁钡锌+2价, 金属铝为+3价,氟氯溴碘-1价,
亚铜+1铜+2, 亚铁+2铁+3,
通常氧硫-2价,氮磷最低-3价,
还有其他可变价。单质全部为0价。
判断:微粒A是 微粒 B 是
微粒C是 。
Al3+
S2—
A B C
O
OH NH4 SO4 CO3
-2
-3
+1
+1
-2
+6
-2
+4
-1
+1
-2
-2
NO3 HCO3 SO3 PO4
+5
+4
+1
+4
+5
-2
-2
-2
-2
-1
-1
-2
-3
原子团化合价是怎样算出来的?
原子团中各元素化合价的代数和就是该原子团的化合价。
-1
-1
+1
-2
-2
-2
-3
思考:原子团是一种物质吗?
原子团 离子符号 电荷 化合价
氢氧根 OH- -1 -1
硝酸根 NO3- -1
碳酸氢根 HCO3- -1
铵根 NH4+ +1
硫酸根 SO42- -2
碳酸根 CO32- -2
亚硫酸根 SO32- -2
磷酸根 PO43- -3
化合价
化学式
交叉法
CaCl2
K2CO3
Ba (NO3)2
常见的化合物中氢总是____价,氧总是____价;金属元素常显_____价。 非金属元素跟氧化合时常显_____价,跟氢化合时常显_______价。 单质中元素的化合价为_____价。 在化合物里,元素正负化合价的代数和为____。有些元素在不同的化合物里常显_____的化合价,如____________;有些元素在不同的化合物里常显_______的化合价,如_______________。
+ 1
- 2
正
正
负
零
零
相同
不同
化合价的一般规则:
H2O CO2
CO CO2
1.单质化学式的写法; 化合物化学式的写法;
2.化学式的读法;
3.化学式传递的宏观与微观的信息;
4.离子符号的写法;
5.常见的带电原子团。
+1
+1
+1
+2
+2
+2
+2
+3
+1 +2
+2 +3
+2 +4 +6+7
+1
- 1
- 2
6. 常见元素的化合价
金属元素 元素
符号 常见的化合价 非金属
元素 元素符号 常见的
化合价
钾 K 氢 H
钠 Na 氟 F
银 Ag 氧 O
钙 Ca 氯 Cl -1、+5、+7
镁 Mg 溴 Br -1、+5、+7
钡 Ba 碘 I -1、+5、+7
锌 Zn 氮 N -3、+5
铝 Al 磷 P -3、+5
铜 Cu 硫 S -2、+4、+6
铁 Fe 碳 C -4、+2、+4
锰 Mn 硅 Si -4、+4
OH-
SO4 2 -
NO3-
CO3 2 -
HCO3-
NH4+
SO3 2 -
PO4 3 -
原子团的化合价
离子的名称 离子的符号
氢氧根离子
硫酸根离子
硝酸根离子
碳酸根离子
碳酸氢根离子
铵根离子
亚硫酸根离子
磷酸根离子
1、某矿泉水中含有的硒(Se)是一种非金属元素,它的化学性质与硫相似。在硒酸(H2SeO4)中Se元素的化合价为( )
A、+4 B、–2 C、+2 D、+6
D
2. A、B、C三种元素的化合价分别是+1、+4、-2,这三元素组成的化合物的化学式可能是 ( )
A.ABC4 B.A4BC3
C.A2BC3 D.A3BC2
C
6、交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机是否酒后开车,因为酒中的乙醇分子可以使橙红色的重铬酸钾)变成绿色的硫酸铬[Cr2(SO4)3],在重铬酸钾和硫酸铬中,铬的化合价依次是 ( )
A、+3、+5 B、+5、+3
C、+3、+6 D、+6、+3
D
12.地壳中含量最多的元素,最多的金属元素,空气中含量最多的元素组成的化合物的化学式是__________。
Al(NO3)3
11.地壳中含量最多的非金属元素跟含量最多的金属元素形成化合物的化学式为 。
Al2O3
13、化合价是元素的一种重要性质,只有在形成 ________ 时表现出来,
在①CuCl2、 ②KClO3、
③HClO4、④HClO四种物质中,按氯元素化合价由低到高顺序排列应是 ___ 。(填序号)
化合物
1 4 2 3
4、写出下列符号的含义:
2O2
H2O2
O
Al3+
-2
2个氧分子
1个过氧化氢分子
化合价为-2价的氧元素
带三个单位正电荷的铝离子
14、写出下列各式中数字“2”的意义:
①2H
②3H2
+2
③CaO
④4Ca2+
2个氢原子
一个氢分子中由2个氢原子构成
氧化钙中钙元素的化合价为+2
一个钙离子带2个单位正电荷
15、市售的“脑黄金”(DHA)是从深海鱼油中提取的,主要成分为一种不饱和脂肪酸,其化学式为C25H50COOH,它是由 种元素组成,每个分子中有 个原子。
3
79
17、下列含有不同原子团的一组物质是
( )
A、NaNO3和Mg(NO3)2
B、KMnO4和K2MnO4
C、Na2CO3和CaCO3
D、FeSO4和Fe2(SO4)3
B
18.标出带点元素的化合价:
NH3 CO2 H2SO4
CaCO3 KMnO4 K2MnO4
H3PO4 P2O5
-3
+4
+6
+4
+7
+6
+5
+5
19.用化学用语表示:
液态氢________水________
过氧化氢_______三氧化硫_________
二氧化硫 硫化氢______
干冰___________
氯化铁_______氯化亚铁______
四氧化三铁_________
氧化铁______氧化亚铁_________
H2
H2O
H2O2
SO3
SO2
H2S
CO2
FeCl3
FeCl2
Fe3O4
Fe2O3
FeO
氧化铝 氧化钠 _______
硫 酸 ___ 硝酸铵________
石灰石 ___ 熟石灰________
亚硫酸钠 _____ 碳酸氢铵________
Al2O3
Na2O
H2SO4
NH4NO3
NH4HCO3
Ca(OH)2
CaCO3
Na2SO3
2个钠离子________铝离子_______
亚铜离子______铜离子_________
亚铁离子____ 铁离子_______
氢离子_____ 氧离子_____
氯离子____ 硫离子_____
2Na+
Al 3+
Cu+
Cu 2 +
Fe 2 +
Fe 3+
H+
O2-
Cl-
S2-
2、下列化学式是否正确,若有错请更正。
氮气—N
氖气—Ne2
氧化镁—MgO
二氧化锰—MNO2
硫化钠—SNa2
√
N2
Ne
MnO2
Na2S
1.化合价为正二价的镁元素 ,
化合价为负二价的硫元素 ,
二氧化碳中的碳元素为正四价 。
Mg
+2
S
-2
CO2
+4
2. 读出下列化学式的名称。
NaCl NaF CaO ZnS MgO
ZnO HCl KCl
下列物质的化学式正确的是( )
(A )氯化钠Na Cl (B) 氧化铁FeO
(C )氧化钡OBa (D) 硫酸铝Al(SO )
2
4
3
2
D
1.已知M元素的化合价为+a价,N元素的化合价为-b价,请写出M N形成化合物的化学式。
MbNa
2.标出下列物质中N元素的化合价,请标在N元素的正上方:
①N2; ②NO;③NO2;④N2O5;
⑤HNO3;⑥NH4NO3
0
+2
+4
+5
+5
+5
-3
1.标出下列单质元素的化合价
Mg O2 Cl2 K
0 0 0 0
在发生化学反应前后,下列各项中
没有变化的是( )
①元素的种类;②分子的数目;
③原子的种类;④原子的数目;
⑤物质的种类
A①③④ B.①④⑤
C.②①③ D.①②④
A
1. 10 CO2分子中的氧原子个数与 个N2O5分子中氧原子的个数相同。
10. 3SO42-表示 _______ ,它共带______ 个单位负电荷。
11.比钠原子多一个质子少一个电子的微粒是( )
A.Ne B.Mg C.Na+ D.Mg2+
D
4
3个硫酸根离子
6
1. 下列化学符号既能表示一种元素、一个原子,还能表示一种单质的是( )
A、2O B、N C、 Fe D、Cl2
关于“2H3PO4”中数字,下列说法不正确的是( )
A、“3”表示氢元素的个数
B、“4”表示每个磷酸分子中含有氧原子的个数
C、“2”表示磷酸分子的个数
D、 “3”表示每个磷酸分子中含有氢原子的个数
C
A
1.下列粒子的结构示意图中,表示非金属元素的原子的是( )
C
2.某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,则该元素的核电荷数为 ( )
A.11 B.15
C.17 D.37
B
5.元素R在化合物中只有一种化合价,下列物质的化学式中错误的是( )
A.R(OH)2 B.RCl3
C.R2(SO4)3 D.R2O3
A
3、如图所示为元素周期表的一部分,已知A元素原子的化合价为+1价,D元素的原子核内有12个质子,回答下列问题:
①D元素属于 (金属、非金属、稀有气体)元素
②C元素的原子核内有 个质子 。
③请推测有关C元素的两点信息:
金属
11
原子序数为11;核外有11个电子 ;属于金属元素;C元素名称是钠; 最外层电子数为1; 电子层数为3层;在化合物中显+1价。
7.用化学用语填空:
(1)地壳中含最多的金属元素____
(2)水通电分解过程中的最小粒子____
(3)构成硫酸钠的阳离子的结构示意图____ (4)在氧化铝中铝显+3价____
(5)两个铵根离子____
(6)同种元素表现出两种化合价的物质____ (7)氩气____
Al
H O
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
