沪教版九年级下册化学 6.2溶液组成的表示(共22张PPT)
文档属性
| 名称 | 沪教版九年级下册化学 6.2溶液组成的表示(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-04-19 00:00:00 | ||
图片预览







文档简介
(第一课时)
假如你是一名护士,遵医嘱给病人静脉输液,对于你手里拿着的这瓶药液,你必须关注它的哪些方面?
学习目标
1.知道什么是溶质和溶剂,能区分溶液中的溶质和溶剂;
2. 理解溶液的组成 ,溶质、溶剂与溶液三者的关系;
3.理解溶质的质量分数的概念;
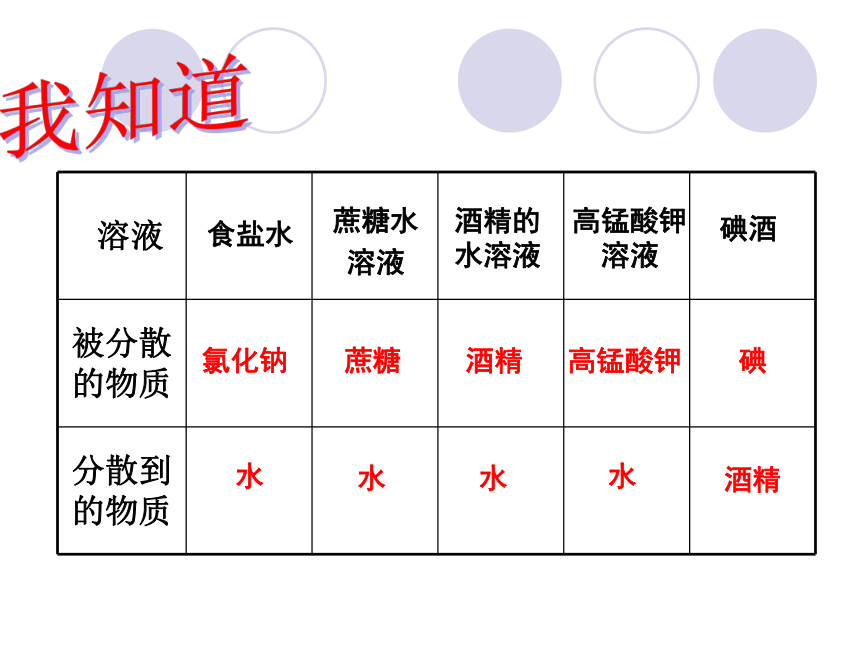
氯化钠
水
水
水
水
酒精
蔗糖
酒精
高锰酸钾
碘
食盐水
蔗糖水
溶液
酒精的
水溶液
高锰酸钾
溶液
碘酒
溶液
被分散的物质
分散到的物质
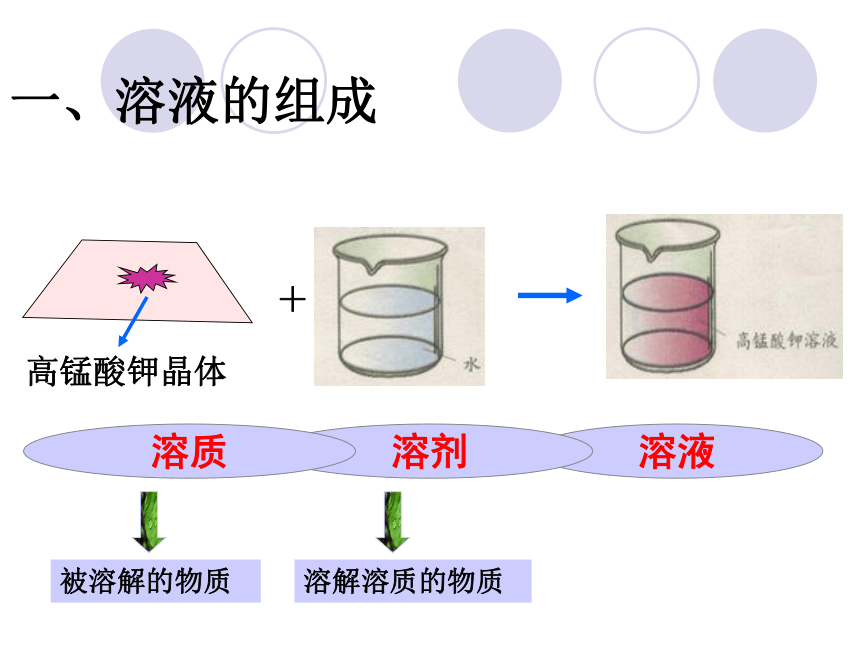
+
溶液
溶剂
溶质
被溶解的物质
溶解溶质的物质
一、溶液的组成
溶液的命名规律:
溶质的溶剂溶液
例如:氯化钠溶于水形成的
溶液叫做:氯化钠的水溶液,简称氯化钠溶液。
请将你知道的一些溶液的组成填入下表中,并与同学们交流。
表6-5 几种溶液的组成
酒精(液态)
水(液态)
氢氧化钠溶液
氢氧化钠(固态)
水(液态)
盐酸溶液
氯化氢(气态)
水(液态)
过氧化氢溶液
过氧化氢(液态)
水(液态)
氯化亚铁溶液
氯化亚铁(固态)
水(液态)
碘酒溶液
碘(固态)
酒精(液态)
溶 液 溶质(状态) 溶剂(状态)
酒精水溶液
1. 溶质的原状态可以是哪些?
2. 常见的溶剂是什么?
溶质的状态可以是固体、液体,也可以是气体。
水是最常用的溶剂。 除特别说明外,一般所说的溶液都是指水溶液。
1.固体、气体溶于液体时,固体、气体是溶质,液体是溶剂。
2.两种液体互相溶解时,通常把量多的一种叫做溶剂,量少的一种叫做溶质。
3.当物质与水混合形成溶液时,不论多少,水均为溶剂。
判断镁与稀盐酸恰好完全反应后所得溶液中溶质和溶剂及溶液的名称?
氯化镁溶液
溶质:氯化镁
溶剂:水
当溶质和溶剂混合后,下列有关量的关系?
1、10gNaCl完全溶解在100g水中所得溶液质量_____ 110g食盐水;
2、10mL酒精和10mL水混合后所得溶液体积______ 20mL的酒精溶液;
3、某食盐水的密度为1.04g/mL,现取100mL的该
食盐水,则该溶液的质量______104g。
=
<
=
溶液中存在的一些量的关系:
溶液的质量=溶质质量+溶剂质量
溶液的质量=溶液的密度×溶液的体积
溶液的体积不能是溶质和溶剂体积的简单相加
即:溶液的质量可以相加。
即:溶液的体积不可以相加。
1、溶液的溶质质量分数的概念
二、溶液浓度的表示
溶质质量与溶液质量之比叫做溶液的溶质质量分数。
溶质质量分数
溶质质量分数越大,说明溶液中溶质的相对含量越高。
2、计算式:
5%的氯化钠溶液,它的含义你知道吗?
表示每100份质量的氯化钠溶液中有5份质量的氯化钠和95份质量的水。
溶液质量
溶质质量
溶剂质量
100g
5g
95g
现有一杯常温下的10%的硝
酸钾溶液,经过一些变化后,
m溶质、m溶剂、m溶液和溶质的质量
分数分别有什么变化?
不变
增加
增加
减小
不变
减少
减少
增大
增加
不变
增加
增大
减少
不变
减少
减小
减少
减少
减少
不变
变化内容 溶质
质量 溶剂质量 溶液质量 溶质的质量分数
加水
蒸发少量水
加少量溶质
减少溶质
从100g10%的硝酸钾溶液中取出30g,剩余溶液
1、填空
1)、硫酸铜溶液中溶质是:_______,溶剂是______。澄清石灰水中溶质是_______,溶剂是_______。
2)、把少量的油脂溶于汽油中配成溶液,其中______是溶质,_______溶剂,这种溶液的名称是____________溶液。
3)、现有一瓶25%的氢氧化钠溶液,该溶液中溶质是_______,溶剂是_____,溶质质量:溶剂质量:溶液质量=________.
氢氧化钠
水
1:3:4
硫酸铜
水
氢氧化钙
水
油脂
汽油
油脂的汽油
2、下列说法是否正确:对的打√,错的打×。
1)、100g水中溶解了20g食盐,所得溶液的溶质质量分数为20%. ( )
2)、 从质量分数为20%的100g碳酸钠溶液中取出10g溶液,则取出的溶液的溶质质量分数变为2%. ( )
3)、100g硫酸铜溶液中含有17g硫酸铜,若再往其中加入1g无水硫酸铜,并使其完全溶解,则溶质质量分数为变18%. ( )
×
×
×
一、溶液的组成
二、溶液组成的定量表示
1、溶液的组成
2、溶液的命名
3、溶质、溶剂的判断
4、溶液中的一些量的关系
1、溶质质量分数的概念
2、计算式
3、注意点
假如你是一名护士,遵医嘱给病人静脉输液,对于你手里拿着的这瓶药液,你必须关注它的哪些方面?
学习目标
1.知道什么是溶质和溶剂,能区分溶液中的溶质和溶剂;
2. 理解溶液的组成 ,溶质、溶剂与溶液三者的关系;
3.理解溶质的质量分数的概念;
氯化钠
水
水
水
水
酒精
蔗糖
酒精
高锰酸钾
碘
食盐水
蔗糖水
溶液
酒精的
水溶液
高锰酸钾
溶液
碘酒
溶液
被分散的物质
分散到的物质
+
溶液
溶剂
溶质
被溶解的物质
溶解溶质的物质
一、溶液的组成
溶液的命名规律:
溶质的溶剂溶液
例如:氯化钠溶于水形成的
溶液叫做:氯化钠的水溶液,简称氯化钠溶液。
请将你知道的一些溶液的组成填入下表中,并与同学们交流。
表6-5 几种溶液的组成
酒精(液态)
水(液态)
氢氧化钠溶液
氢氧化钠(固态)
水(液态)
盐酸溶液
氯化氢(气态)
水(液态)
过氧化氢溶液
过氧化氢(液态)
水(液态)
氯化亚铁溶液
氯化亚铁(固态)
水(液态)
碘酒溶液
碘(固态)
酒精(液态)
溶 液 溶质(状态) 溶剂(状态)
酒精水溶液
1. 溶质的原状态可以是哪些?
2. 常见的溶剂是什么?
溶质的状态可以是固体、液体,也可以是气体。
水是最常用的溶剂。 除特别说明外,一般所说的溶液都是指水溶液。
1.固体、气体溶于液体时,固体、气体是溶质,液体是溶剂。
2.两种液体互相溶解时,通常把量多的一种叫做溶剂,量少的一种叫做溶质。
3.当物质与水混合形成溶液时,不论多少,水均为溶剂。
判断镁与稀盐酸恰好完全反应后所得溶液中溶质和溶剂及溶液的名称?
氯化镁溶液
溶质:氯化镁
溶剂:水
当溶质和溶剂混合后,下列有关量的关系?
1、10gNaCl完全溶解在100g水中所得溶液质量_____ 110g食盐水;
2、10mL酒精和10mL水混合后所得溶液体积______ 20mL的酒精溶液;
3、某食盐水的密度为1.04g/mL,现取100mL的该
食盐水,则该溶液的质量______104g。
=
<
=
溶液中存在的一些量的关系:
溶液的质量=溶质质量+溶剂质量
溶液的质量=溶液的密度×溶液的体积
溶液的体积不能是溶质和溶剂体积的简单相加
即:溶液的质量可以相加。
即:溶液的体积不可以相加。
1、溶液的溶质质量分数的概念
二、溶液浓度的表示
溶质质量与溶液质量之比叫做溶液的溶质质量分数。
溶质质量分数
溶质质量分数越大,说明溶液中溶质的相对含量越高。
2、计算式:
5%的氯化钠溶液,它的含义你知道吗?
表示每100份质量的氯化钠溶液中有5份质量的氯化钠和95份质量的水。
溶液质量
溶质质量
溶剂质量
100g
5g
95g
现有一杯常温下的10%的硝
酸钾溶液,经过一些变化后,
m溶质、m溶剂、m溶液和溶质的质量
分数分别有什么变化?
不变
增加
增加
减小
不变
减少
减少
增大
增加
不变
增加
增大
减少
不变
减少
减小
减少
减少
减少
不变
变化内容 溶质
质量 溶剂质量 溶液质量 溶质的质量分数
加水
蒸发少量水
加少量溶质
减少溶质
从100g10%的硝酸钾溶液中取出30g,剩余溶液
1、填空
1)、硫酸铜溶液中溶质是:_______,溶剂是______。澄清石灰水中溶质是_______,溶剂是_______。
2)、把少量的油脂溶于汽油中配成溶液,其中______是溶质,_______溶剂,这种溶液的名称是____________溶液。
3)、现有一瓶25%的氢氧化钠溶液,该溶液中溶质是_______,溶剂是_____,溶质质量:溶剂质量:溶液质量=________.
氢氧化钠
水
1:3:4
硫酸铜
水
氢氧化钙
水
油脂
汽油
油脂的汽油
2、下列说法是否正确:对的打√,错的打×。
1)、100g水中溶解了20g食盐,所得溶液的溶质质量分数为20%. ( )
2)、 从质量分数为20%的100g碳酸钠溶液中取出10g溶液,则取出的溶液的溶质质量分数变为2%. ( )
3)、100g硫酸铜溶液中含有17g硫酸铜,若再往其中加入1g无水硫酸铜,并使其完全溶解,则溶质质量分数为变18%. ( )
×
×
×
一、溶液的组成
二、溶液组成的定量表示
1、溶液的组成
2、溶液的命名
3、溶质、溶剂的判断
4、溶液中的一些量的关系
1、溶质质量分数的概念
2、计算式
3、注意点
