沪教版九年级化学全册(全国版)第七章第二节 中和反应(共31张PPT)
文档属性
| 名称 | 沪教版九年级化学全册(全国版)第七章第二节 中和反应(共31张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 322.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-12 00:00:00 | ||
图片预览











文档简介
第 七 章 第二节 常见的酸和碱
中和反应
[活动与探究]
[实验1] 在烧杯中加入10ml氢氧化钠溶液,滴入2~3滴无色酚酞溶液,插入一支温度计,测量溶液的温度。
再用胶头滴管吸取盐酸逐滴加入盛有氢氧化钠溶液的烧杯中。边滴边搅拌,当烧杯中溶液刚好变成无色时,停止加入盐酸。
[实验3] 取[实验1]所得的少量溶液于蒸发皿中,加热至蒸干,观察到什么现象?这说明了什么?
[实验2] 取[实验1]所得的少量溶液于一支试管中,另用一支胶头滴管,向试管中加入一滴氢氧化钠溶液,溶液又发生什么变化?这说明了什么?
[讨论]
1、在[实验1]中溶液的碱性发生了什么变化?这说明了什么?
2、在[实验1]中溶液的温度有什么变化?这说明了什么?
3、在[实验1]中,当滴入的盐酸较少时,溶液为什么颜色?这又说明了什么?溶液显什么(酸、碱、中)性?
4、在[实验1]中,当滴入的盐酸恰好使烧杯中溶液变成无色时,这又说明了什么?溶液显什么(酸、碱、中)性?
5、在[实验1]中,当滴入的盐酸恰好使烧杯中溶液变成无色时继续滴加一些盐酸,溶液为什么颜色?溶液显什么(酸、碱、中)性?
6、在[实验2]中,当滴入的盐酸恰好使烧杯中溶液变成无色时,然后向试管中加入一滴氢氧化钠溶液,溶液又发生什么变化?这说明了什么?溶液显什么(酸、碱、中)性?
7、蒸发皿中的物质是氢氧化钠吗?为什么?写出反应的化学方程式。
NaOH + HCl =
NaCl + H2O
实验步骤 实验现象 实验结论
实验一 烧杯中液体呈红色;
反应前溶液的温度为 10℃ 左右。
烧杯内溶液的颜色由红色突然变成无色
反应后溶液的温度为 16℃ 左右。 氢氧化钠溶液呈碱性,能使无色酚酞变成红色。pH>7
发生化学反应,生成物NaCl
为中性,pH=7:
NaOH + HCl== NaCl + H2O
该反应为放热反应。
实验二 滴加NaOH溶液后,溶液变为红色 滴加NaOH后,溶液中氢氧化钠过量,溶液呈碱性,使无色酚酞变为红色,pH>7。
实验三 蒸发皿中出现白色固体 该固体为NaCl晶体。
[练习]
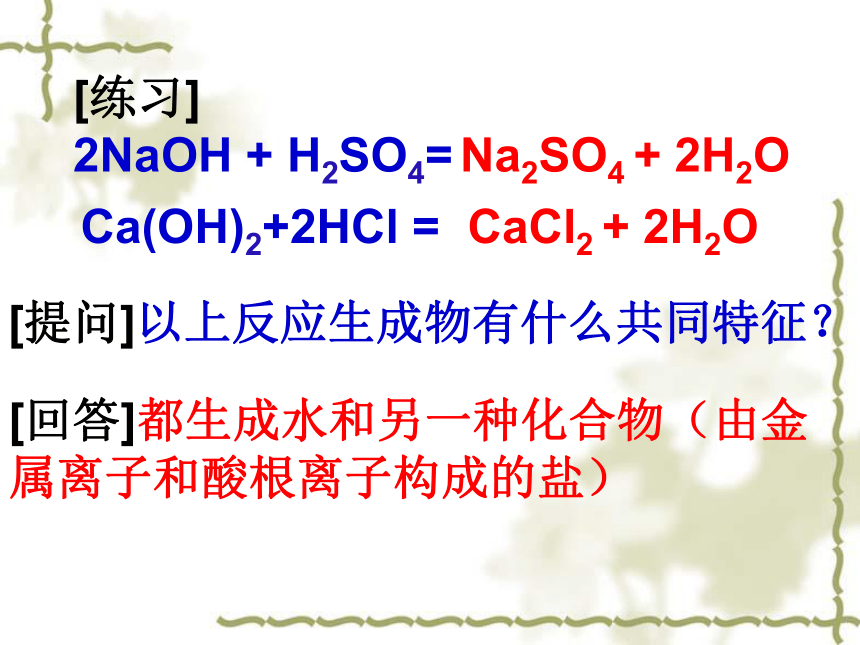
2NaOH + H2SO4=
Na2SO4 + 2H2O
Ca(OH)2+2HCl =
CaCl2 + 2H2O
[提问]以上反应生成物有什么共同特征?
[回答]都生成水和另一种化合物(由金
属离子和酸根离子构成的盐)
[板书]
一、中和反应
1、酸和碱作用使各自的特性都消失,生成盐和水的反应叫做中和反应。
酸+碱→盐+水(放热)
NaOH + HCl = NaCl + H2O
[提问] NaOH + HCl = NaCl + H2O属于什么基本反应类型?
[板书]
2、中和反应属于复分解反应。
3、中和反应的实质是 H++OH-==H2O
二、中和反应的应用
[交流与讨论]
1、参照氢氧化钠与盐酸反应的化学方程式,写出氢氧化钙与稀硫酸反应的化学方程式。
2、有些化工厂排放的废水中含有硫酸,如果用氨水(NH3·H2O)中和它,能得到一种氮肥——硫酸铵[(NH4)2SO4]。写出该反应的化学方程式。
3、施用熟石灰可以改良酸性土壤;被蚂蚁、蚊子咬了,昆虫分泌的酸性物质进入肌肉,使肌肉酸痛,涂上稀氨水或肥皂水可以止痛、消肿。你知道其中的道理吗?
[板书]
二、中和反应的应用
1、用熟石灰来改良酸性土壤。
2、处理工厂废水中的酸。
3、用于医药——中和胃酸及昆虫分泌的酸性物质等。
三[拓展视野]
复分解反应包括:
酸+碱——盐+水
酸+盐——新酸+新盐
碱+盐——新碱+新盐
盐+盐——新盐+新盐
酸+金属氧化物---盐+水
酸碱盐之间是否一定能发生复分解反应呢?
观察下列实验药品,能否按照酸、碱、盐进行分类
比一比,你分的对吗?
酸 碱 盐
H2SO4
NaOH
KNO3
CuSO4
Na2CO3
分析
H2SO4 + Na2CO3——
Na2SO4+ + H2O
H+、SO42-
Na+、CO3 2 -
Na+、SO42-
反应前
反应后
溶液中离子种类发生改变
√
H2SO4 + KNO3 ——
K2SO4 + HNO3
H+、SO42-
K+、NO3-
K+、SO42-
H+、NO3-
反应前
反应后
溶液中离子种类没有改变
×
复分解反应发生的条件之一
生成物中
有沉淀(↓)
或有气体(↑)
或有水(H2O)
复分解反应才能发生
分组讨论二:
判断下列反应能否发生?为什么?
A.①NaOH+H2SO4— B.① FeCl3+NaOH—
② CaCO3+HCl— ② Cu(OH)2+FeCl3—
C. ① AgNO3+NaCl— D.①H2SO4+BaCl2—
②AgCl+Na2CO3— ②H2SO4+NaCl—
A.①2NaOH+H2SO4 = Na2SO4+2H2O
② CaCO3+2HCl = CaCl 2 + H2O +CO2↑
B. ① 2FeCl3+3Ca(OH)2 = 2Fe (OH) 3 ↓+ 3CaCl 2
② Cu(OH)2+FeCl3
C. ① AgNO3+ NaCl = AgCl↓+ NaNO3
②AgCl+ Na2CO3
D.①H2SO4+ BaCl2 = BaSO4 ↓ + 2HCl
② H2SO4+ NaCl
小 结:
复分解反应发生的条件是什么?
能溶于水或酸;
有水、气体、沉淀三者之一产生。
1、下列反应,属于化合反应的是( ),属于分解反应的是( ),属于置换反应的是( ),属于复分解反应的是( )属于中和反应的是( )
A、Fe + H2SO4 = FeSO4 + H2↑
B、H2CO3 = H2O + CO2↑
C、2NaOH + H2SO4 = Na2SO4 +2 H2O
点燃
D、S + O2 ==== SO2
E、2NaOH + CuSO4 = Na2SO4 +Cu(OH)2↓
目标检测:
2、一张洁白干燥的滤纸上,依次喷洒A、B、C三种无色液体。当喷洒A时,滤纸无明显变化;再喷洒B时,滤纸上出现一只红猫;最后喷洒C时,小猫渐渐消失。
回答下列问题:
无色液体:A是____,B是____,C是____;
或A是____,B是____,C是____。
(从 氢氧化钾溶液、稀硫酸、酚酞溶液中选择填写)
3、某地有间大型火力发电厂(燃烧煤发电),排放出大量的有害气体,,其方程式为_________,这种气体会形成酸雨,造成土壤酸化,不利于作物的生长,为了减小土壤的酸性,可在土壤中加入适量________,以中和酸性。
这种药物能中和过多的胃酸。
Al(OH)3+3HCl=AlCl 3 +3H2O
发酵产生的酸和加入的纯碱(Na2CO3)反应,生成CO2气体,使馒头内生成许多小洞,因此馒头疏松多孔。
中和反应
[活动与探究]
[实验1] 在烧杯中加入10ml氢氧化钠溶液,滴入2~3滴无色酚酞溶液,插入一支温度计,测量溶液的温度。
再用胶头滴管吸取盐酸逐滴加入盛有氢氧化钠溶液的烧杯中。边滴边搅拌,当烧杯中溶液刚好变成无色时,停止加入盐酸。
[实验3] 取[实验1]所得的少量溶液于蒸发皿中,加热至蒸干,观察到什么现象?这说明了什么?
[实验2] 取[实验1]所得的少量溶液于一支试管中,另用一支胶头滴管,向试管中加入一滴氢氧化钠溶液,溶液又发生什么变化?这说明了什么?
[讨论]
1、在[实验1]中溶液的碱性发生了什么变化?这说明了什么?
2、在[实验1]中溶液的温度有什么变化?这说明了什么?
3、在[实验1]中,当滴入的盐酸较少时,溶液为什么颜色?这又说明了什么?溶液显什么(酸、碱、中)性?
4、在[实验1]中,当滴入的盐酸恰好使烧杯中溶液变成无色时,这又说明了什么?溶液显什么(酸、碱、中)性?
5、在[实验1]中,当滴入的盐酸恰好使烧杯中溶液变成无色时继续滴加一些盐酸,溶液为什么颜色?溶液显什么(酸、碱、中)性?
6、在[实验2]中,当滴入的盐酸恰好使烧杯中溶液变成无色时,然后向试管中加入一滴氢氧化钠溶液,溶液又发生什么变化?这说明了什么?溶液显什么(酸、碱、中)性?
7、蒸发皿中的物质是氢氧化钠吗?为什么?写出反应的化学方程式。
NaOH + HCl =
NaCl + H2O
实验步骤 实验现象 实验结论
实验一 烧杯中液体呈红色;
反应前溶液的温度为 10℃ 左右。
烧杯内溶液的颜色由红色突然变成无色
反应后溶液的温度为 16℃ 左右。 氢氧化钠溶液呈碱性,能使无色酚酞变成红色。pH>7
发生化学反应,生成物NaCl
为中性,pH=7:
NaOH + HCl== NaCl + H2O
该反应为放热反应。
实验二 滴加NaOH溶液后,溶液变为红色 滴加NaOH后,溶液中氢氧化钠过量,溶液呈碱性,使无色酚酞变为红色,pH>7。
实验三 蒸发皿中出现白色固体 该固体为NaCl晶体。
[练习]
2NaOH + H2SO4=
Na2SO4 + 2H2O
Ca(OH)2+2HCl =
CaCl2 + 2H2O
[提问]以上反应生成物有什么共同特征?
[回答]都生成水和另一种化合物(由金
属离子和酸根离子构成的盐)
[板书]
一、中和反应
1、酸和碱作用使各自的特性都消失,生成盐和水的反应叫做中和反应。
酸+碱→盐+水(放热)
NaOH + HCl = NaCl + H2O
[提问] NaOH + HCl = NaCl + H2O属于什么基本反应类型?
[板书]
2、中和反应属于复分解反应。
3、中和反应的实质是 H++OH-==H2O
二、中和反应的应用
[交流与讨论]
1、参照氢氧化钠与盐酸反应的化学方程式,写出氢氧化钙与稀硫酸反应的化学方程式。
2、有些化工厂排放的废水中含有硫酸,如果用氨水(NH3·H2O)中和它,能得到一种氮肥——硫酸铵[(NH4)2SO4]。写出该反应的化学方程式。
3、施用熟石灰可以改良酸性土壤;被蚂蚁、蚊子咬了,昆虫分泌的酸性物质进入肌肉,使肌肉酸痛,涂上稀氨水或肥皂水可以止痛、消肿。你知道其中的道理吗?
[板书]
二、中和反应的应用
1、用熟石灰来改良酸性土壤。
2、处理工厂废水中的酸。
3、用于医药——中和胃酸及昆虫分泌的酸性物质等。
三[拓展视野]
复分解反应包括:
酸+碱——盐+水
酸+盐——新酸+新盐
碱+盐——新碱+新盐
盐+盐——新盐+新盐
酸+金属氧化物---盐+水
酸碱盐之间是否一定能发生复分解反应呢?
观察下列实验药品,能否按照酸、碱、盐进行分类
比一比,你分的对吗?
酸 碱 盐
H2SO4
NaOH
KNO3
CuSO4
Na2CO3
分析
H2SO4 + Na2CO3——
Na2SO4+ + H2O
H+、SO42-
Na+、CO3 2 -
Na+、SO42-
反应前
反应后
溶液中离子种类发生改变
√
H2SO4 + KNO3 ——
K2SO4 + HNO3
H+、SO42-
K+、NO3-
K+、SO42-
H+、NO3-
反应前
反应后
溶液中离子种类没有改变
×
复分解反应发生的条件之一
生成物中
有沉淀(↓)
或有气体(↑)
或有水(H2O)
复分解反应才能发生
分组讨论二:
判断下列反应能否发生?为什么?
A.①NaOH+H2SO4— B.① FeCl3+NaOH—
② CaCO3+HCl— ② Cu(OH)2+FeCl3—
C. ① AgNO3+NaCl— D.①H2SO4+BaCl2—
②AgCl+Na2CO3— ②H2SO4+NaCl—
A.①2NaOH+H2SO4 = Na2SO4+2H2O
② CaCO3+2HCl = CaCl 2 + H2O +CO2↑
B. ① 2FeCl3+3Ca(OH)2 = 2Fe (OH) 3 ↓+ 3CaCl 2
② Cu(OH)2+FeCl3
C. ① AgNO3+ NaCl = AgCl↓+ NaNO3
②AgCl+ Na2CO3
D.①H2SO4+ BaCl2 = BaSO4 ↓ + 2HCl
② H2SO4+ NaCl
小 结:
复分解反应发生的条件是什么?
能溶于水或酸;
有水、气体、沉淀三者之一产生。
1、下列反应,属于化合反应的是( ),属于分解反应的是( ),属于置换反应的是( ),属于复分解反应的是( )属于中和反应的是( )
A、Fe + H2SO4 = FeSO4 + H2↑
B、H2CO3 = H2O + CO2↑
C、2NaOH + H2SO4 = Na2SO4 +2 H2O
点燃
D、S + O2 ==== SO2
E、2NaOH + CuSO4 = Na2SO4 +Cu(OH)2↓
目标检测:
2、一张洁白干燥的滤纸上,依次喷洒A、B、C三种无色液体。当喷洒A时,滤纸无明显变化;再喷洒B时,滤纸上出现一只红猫;最后喷洒C时,小猫渐渐消失。
回答下列问题:
无色液体:A是____,B是____,C是____;
或A是____,B是____,C是____。
(从 氢氧化钾溶液、稀硫酸、酚酞溶液中选择填写)
3、某地有间大型火力发电厂(燃烧煤发电),排放出大量的有害气体,,其方程式为_________,这种气体会形成酸雨,造成土壤酸化,不利于作物的生长,为了减小土壤的酸性,可在土壤中加入适量________,以中和酸性。
这种药物能中和过多的胃酸。
Al(OH)3+3HCl=AlCl 3 +3H2O
发酵产生的酸和加入的纯碱(Na2CO3)反应,生成CO2气体,使馒头内生成许多小洞,因此馒头疏松多孔。
