沪教化学下册第7章基础实验8 酸、碱的化学性质(共27张PPT)
文档属性
| 名称 | 沪教化学下册第7章基础实验8 酸、碱的化学性质(共27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 614.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-01 00:00:00 | ||
图片预览







文档简介
课件27张PPT。 酸和碱的性质研究
——氢氧化钠 氢氧化钙碱的物理性质一、氢氧化钠白色固体吸收水蒸气
而逐渐溶解,
NaOH固体
可作干燥剂易溶
于水,
放热腐蚀性
俗称火碱、
烧碱、
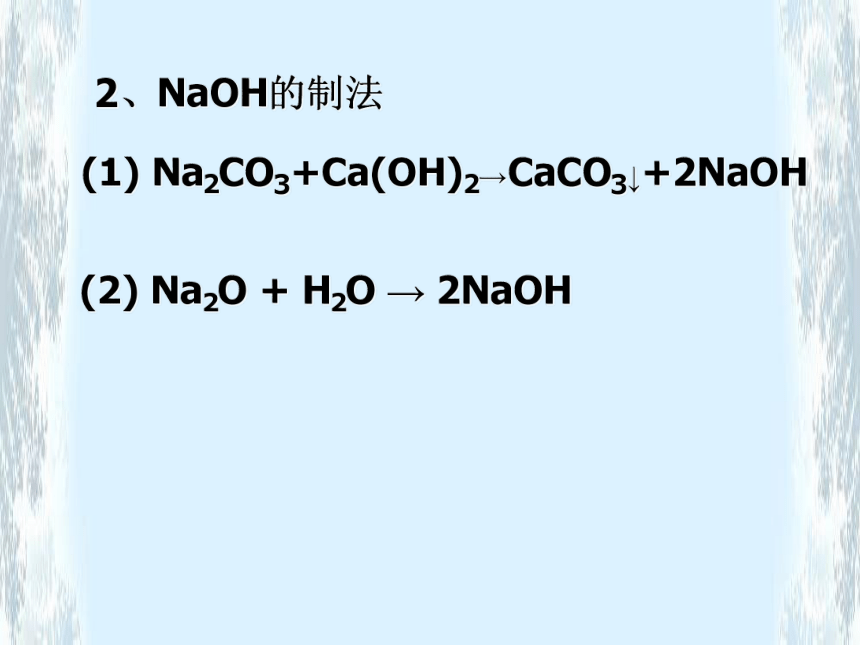
苛性钠NaOH干燥管粗进细出易潮解的物质:1、氢氧化钠 2、氯化钙 3、氯化镁溶于水放出大量热的物质1、浓硫酸 2、生石灰 3、氢氧化钠氢氧化钠具有强烈的腐蚀性,切不可用嘴尝和用手拿,万一手上或衣服上碰到,要立即用水冲洗。氢氧化钙也有腐蚀性,也不能用嘴尝和用手拿。潮解——暴露在空气里的固体吸收空气里的水分表面潮湿而逐步溶解2、NaOH的制法(1) Na2CO3+Ca(OH)2→CaCO3↓+2NaOH(2) Na2O + H2O → 2NaOH1、_____色固体,____于水,溶解时大量 热。
固体具有吸水性,其可做_______ 。可干燥H2、O2
等,不可干燥CO2等气体。快速回答:氢氧化钠的物理性质白易放干燥剂2、具有腐蚀性,俗称______、______、______。
3、若不慎沾到皮肤上,应_________________
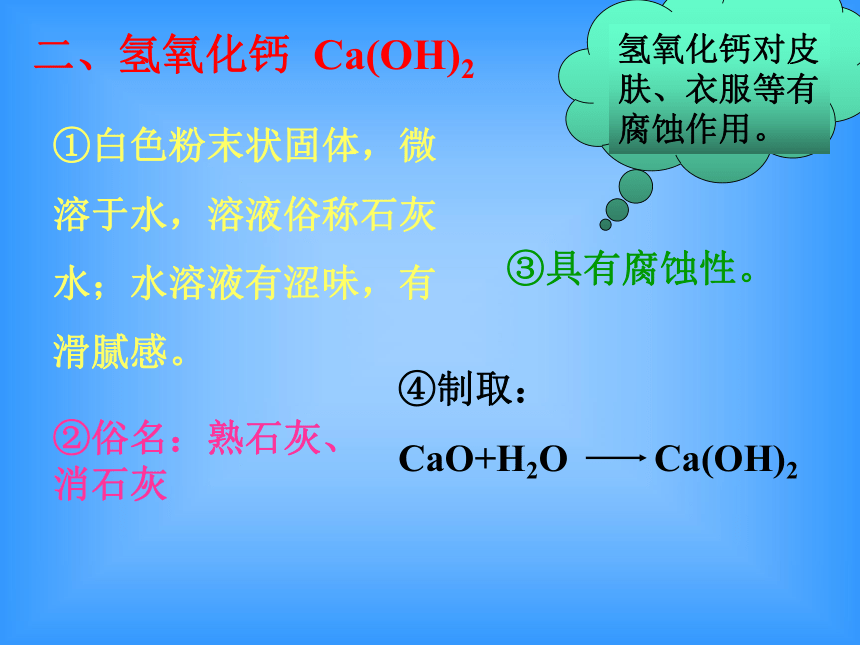
烧碱火碱苛性钠先用大量水冲洗,再涂上硼酸溶液二、氢氧化钙 Ca(OH)2④制取: CaO+H2O Ca(OH)2①白色粉末状固体,微溶于水,溶液俗称石灰水;水溶液有涩味,有滑腻感。②俗名:熟石灰、消石灰快速回答:白色固体微溶于水,水溶液
俗称石灰水熟石灰、消石灰与石灰有关的说法
纯净物:生石灰________ 熟石灰_________
混合物(主要成分):
石灰石________
石灰水、石灰浆、石灰乳________
碱石灰_______________CaOCa(OH)2CaCO3Ca(OH)2NaOH和CaO的混合物三、用途:氢氧化钠:造纸、洗涤剂、纺织、炼铝、
精炼石油等氢氧化钙:建筑材料、中和酸性土壤、
制农药波尔多液、制造漂白剂等制农药波尔多液Ca(OH)2 + CuSO4 →CaSO4↓+ Cu(OH)2↓制漂粉精2Cl2 + 2Ca(OH)2 → Ca(ClO)2 + CaCl2 + 2H2O 熟石灰的用途农业上:改良酸性土壤、配制农药波尔多液建筑业:建筑材料工业上:
工业原料2、碱的化学性质与酸碱指示剂反应与非金属氧化物反应与酸反应与盐发生复分解反应石蕊石灰水实验一 结论
氢氧化钙溶液能使石蕊试液变蓝色,使无色酚酞试液变红色氢氧化钙的化学性质酚酞石灰水与酸碱指示剂作用2、与非金属氧化物反应氢氧化钙的化学性质问题与思考(此反应可用于用于检验CO2) 长期盛石灰水的试剂瓶内壁上常常生成一层白色固体,它是什么?应怎样洗去?为什么澄清石灰水用新配制的效果好?Ca(OH)2+CO2 CaCO3↓+H2O 稀盐酸 CaCO3+2HCl CaCl2+H2O+CO2↑ 碳酸钙 Ca(OH)2+CO2 CaCO3↓+H2O 3、与酸发生中和反应Xiaody 制作氢氧化钙的化学性质稀盐酸 酚酞
石灰水稀硝酸酚酞
石灰水Ca(OH)2+2HCl CaCl2+2H2OCa(OH)2+2HNO3 Ca(NO3)2+2H2O4、与盐发生反应氢氧化钙的化学性质实验:在石灰水里注入浓碳酸钠溶液Ca(OH)2+Na2CO3 CaCO3↓+2NaOH
可以用来制造氢氧化钠非金属氧化物非金属氧化物 凡能与碱反应生成盐和水的氧化物.酸性氧化物例如:CO2P2O5SO2 酸 性氧化物多数是多数是除NO、CO、H2O等SiO2酸性氧化物多数能溶于
水,跟水化合生成酸。碱的化学性质与酸碱指示剂反应与酸性氧化物反应与酸反应与盐发生复分解反应紫色石蕊变蓝酚酞红盐+水盐+水新盐+新碱小结四、碱的通性 能跟酸碱指示剂起反应,使石蕊变蓝,
酚酞变红
能跟多数酸性氧化物起反应,生成
盐和水
能跟酸起中和反应,生成盐和水
能跟某些盐起反应,生成另一种盐和
另一种碱请你来设计用实验证明二氧化碳确已跟氢氧化钠溶液反应了1、根据瓶中压强减小来证明2、根据反应后的生成物(Na2CO3)来证明在反应后的溶液中加入盐酸……
在反应后的溶液中加入澄清石灰水……
在反应后的溶液中加入氯化钙或氯化钡……你能用几种方法鉴别二瓶白色固体,一瓶是氢氧化钠,一瓶是氢氧化钙?1、各取少量白色固体加适量的水,……2、各取少量白色固体放在表面皿中,一段时间后……4、各取少量白色固体加水后滴加碳酸钠溶液……3、各取少量白色固体加水后通二氧化碳气体……1、只用一种试剂鉴别下列各组物质:
(1)溶液:稀硫酸、NaCl、BaCl2
(2)溶液:石灰水、氢氧化钠、稀盐酸
(3)溶液:AgNO3、碳酸钠、氯化钠
(4)溶液: KOH 、稀硝酸 、水
(5)白色粉末:CaCO3、CuSO4、KNO3、NaOH课堂练习碳酸钠溶液碳酸钠溶液稀盐酸紫色石蕊液KOH稀硝酸水不溶溶溶溶且放热 (1)NaCl(Na2SO4)
(2)NaOH [ Ca(OH)2 ]
(3)HNO3 ( HCl )
(4)Cu ( Fe )课堂练习BaCl2+Na2SO4 BaSO4↓+2NaClFe+H2SO4 FeSO4+H2↑Fe+CuSO4 Cu+FeSO4Ca(OH)2+Na2CO3 CaCO3↓+2NaOHHCl+AgNO3 AgCl↓+HNO3或2、除杂质(括号中为杂质),写出化学方程式3、以纯碱、碳酸钙、水为原料制取烧碱课堂练习CaO+H2O Ca(OH)2Ca(OH)2+Na2CO3 CaCO3↓+2NaOH三、碱的分类、命名金属离子氢氧根离子Mg(OH)2+命名氢氧化某氢氧化镁那么,Fe(OH)2和Fe(OH)3又该怎样区分命名呢?把具有高价金属离子的碱叫做“氢氧化某”Fe(OH)3 氢氧化铁把具有次高价金属离子的碱叫做“氢氧化亚某”Fe(OH)2 氢氧化亚铁三、碱的分类、命名碱按水溶性分按氢氧根的个数分按碱性强弱分可溶性碱只有五种:氨水、氢氧化钠、氢氧化钾、氢氧化钡和氢氧化钙。其余的碱都不溶于水回家作业:1、将下列物质 放入水中,然后 滴加酚酞能变红色 的是( )
A、NaCl B 、 HCl C、 Cu(OH)2 D、Na2O2、在溶液导电性实验装置中盛有硫酸铜溶液,通电时灯泡发亮,若不断加入某物质,发现灯泡逐渐变暗,直至熄灭,再继续加入该物质灯泡又亮,则加入的物质是( )
A、氢氧化钠溶液 B、硝酸钠溶液
C、氢氧化钡溶液 D、铁粉C、DC3、滴入酚酞的氢氧化钡溶液与下列各物质恰好完全反应,溶液仍显红色的是( )
A 、 H2SO4 B、 HCl C 、CO2 D、 K2CO34、用下列试剂中的一种试剂就能鉴别氢氧化钠、氢氧化钙和硫酸 三种无色液体,这种试剂是( )
A、酚酞试液 B、氯化钡
C 硫酸钠溶液 D、碳酸钠溶液5、若完全中和某一盐酸溶液需用氢氧化钠溶液m克,现改用相同质量相同质量分数的氢氧化钾溶液去中和,反应完毕后,滴入石蕊试液显示的颜色为( )
A、红色 B、 紫色 C、 蓝色 D 、无色DDA
而逐渐溶解,
NaOH固体
可作干燥剂易溶
于水,
放热腐蚀性
俗称火碱、
烧碱、
苛性钠NaOH干燥管粗进细出易潮解的物质:1、氢氧化钠 2、氯化钙 3、氯化镁溶于水放出大量热的物质1、浓硫酸 2、生石灰 3、氢氧化钠氢氧化钠具有强烈的腐蚀性,切不可用嘴尝和用手拿,万一手上或衣服上碰到,要立即用水冲洗。氢氧化钙也有腐蚀性,也不能用嘴尝和用手拿。潮解——暴露在空气里的固体吸收空气里的水分表面潮湿而逐步溶解2、NaOH的制法(1) Na2CO3+Ca(OH)2→CaCO3↓+2NaOH(2) Na2O + H2O → 2NaOH1、_____色固体,____于水,溶解时大量 热。
固体具有吸水性,其可做_______ 。可干燥H2、O2
等,不可干燥CO2等气体。快速回答:氢氧化钠的物理性质白易放干燥剂2、具有腐蚀性,俗称______、______、______。
3、若不慎沾到皮肤上,应_________________
烧碱火碱苛性钠先用大量水冲洗,再涂上硼酸溶液二、氢氧化钙 Ca(OH)2④制取: CaO+H2O Ca(OH)2①白色粉末状固体,微溶于水,溶液俗称石灰水;水溶液有涩味,有滑腻感。②俗名:熟石灰、消石灰快速回答:白色固体微溶于水,水溶液
俗称石灰水熟石灰、消石灰与石灰有关的说法
纯净物:生石灰________ 熟石灰_________
混合物(主要成分):
石灰石________
石灰水、石灰浆、石灰乳________
碱石灰_______________CaOCa(OH)2CaCO3Ca(OH)2NaOH和CaO的混合物三、用途:氢氧化钠:造纸、洗涤剂、纺织、炼铝、
精炼石油等氢氧化钙:建筑材料、中和酸性土壤、
制农药波尔多液、制造漂白剂等制农药波尔多液Ca(OH)2 + CuSO4 →CaSO4↓+ Cu(OH)2↓制漂粉精2Cl2 + 2Ca(OH)2 → Ca(ClO)2 + CaCl2 + 2H2O 熟石灰的用途农业上:改良酸性土壤、配制农药波尔多液建筑业:建筑材料工业上:
工业原料2、碱的化学性质与酸碱指示剂反应与非金属氧化物反应与酸反应与盐发生复分解反应石蕊石灰水实验一 结论
氢氧化钙溶液能使石蕊试液变蓝色,使无色酚酞试液变红色氢氧化钙的化学性质酚酞石灰水与酸碱指示剂作用2、与非金属氧化物反应氢氧化钙的化学性质问题与思考(此反应可用于用于检验CO2) 长期盛石灰水的试剂瓶内壁上常常生成一层白色固体,它是什么?应怎样洗去?为什么澄清石灰水用新配制的效果好?Ca(OH)2+CO2 CaCO3↓+H2O 稀盐酸 CaCO3+2HCl CaCl2+H2O+CO2↑ 碳酸钙 Ca(OH)2+CO2 CaCO3↓+H2O 3、与酸发生中和反应Xiaody 制作氢氧化钙的化学性质稀盐酸 酚酞
石灰水稀硝酸酚酞
石灰水Ca(OH)2+2HCl CaCl2+2H2OCa(OH)2+2HNO3 Ca(NO3)2+2H2O4、与盐发生反应氢氧化钙的化学性质实验:在石灰水里注入浓碳酸钠溶液Ca(OH)2+Na2CO3 CaCO3↓+2NaOH
可以用来制造氢氧化钠非金属氧化物非金属氧化物 凡能与碱反应生成盐和水的氧化物.酸性氧化物例如:CO2P2O5SO2 酸 性氧化物多数是多数是除NO、CO、H2O等SiO2酸性氧化物多数能溶于
水,跟水化合生成酸。碱的化学性质与酸碱指示剂反应与酸性氧化物反应与酸反应与盐发生复分解反应紫色石蕊变蓝酚酞红盐+水盐+水新盐+新碱小结四、碱的通性 能跟酸碱指示剂起反应,使石蕊变蓝,
酚酞变红
能跟多数酸性氧化物起反应,生成
盐和水
能跟酸起中和反应,生成盐和水
能跟某些盐起反应,生成另一种盐和
另一种碱请你来设计用实验证明二氧化碳确已跟氢氧化钠溶液反应了1、根据瓶中压强减小来证明2、根据反应后的生成物(Na2CO3)来证明在反应后的溶液中加入盐酸……
在反应后的溶液中加入澄清石灰水……
在反应后的溶液中加入氯化钙或氯化钡……你能用几种方法鉴别二瓶白色固体,一瓶是氢氧化钠,一瓶是氢氧化钙?1、各取少量白色固体加适量的水,……2、各取少量白色固体放在表面皿中,一段时间后……4、各取少量白色固体加水后滴加碳酸钠溶液……3、各取少量白色固体加水后通二氧化碳气体……1、只用一种试剂鉴别下列各组物质:
(1)溶液:稀硫酸、NaCl、BaCl2
(2)溶液:石灰水、氢氧化钠、稀盐酸
(3)溶液:AgNO3、碳酸钠、氯化钠
(4)溶液: KOH 、稀硝酸 、水
(5)白色粉末:CaCO3、CuSO4、KNO3、NaOH课堂练习碳酸钠溶液碳酸钠溶液稀盐酸紫色石蕊液KOH稀硝酸水不溶溶溶溶且放热 (1)NaCl(Na2SO4)
(2)NaOH [ Ca(OH)2 ]
(3)HNO3 ( HCl )
(4)Cu ( Fe )课堂练习BaCl2+Na2SO4 BaSO4↓+2NaClFe+H2SO4 FeSO4+H2↑Fe+CuSO4 Cu+FeSO4Ca(OH)2+Na2CO3 CaCO3↓+2NaOHHCl+AgNO3 AgCl↓+HNO3或2、除杂质(括号中为杂质),写出化学方程式3、以纯碱、碳酸钙、水为原料制取烧碱课堂练习CaO+H2O Ca(OH)2Ca(OH)2+Na2CO3 CaCO3↓+2NaOH三、碱的分类、命名金属离子氢氧根离子Mg(OH)2+命名氢氧化某氢氧化镁那么,Fe(OH)2和Fe(OH)3又该怎样区分命名呢?把具有高价金属离子的碱叫做“氢氧化某”Fe(OH)3 氢氧化铁把具有次高价金属离子的碱叫做“氢氧化亚某”Fe(OH)2 氢氧化亚铁三、碱的分类、命名碱按水溶性分按氢氧根的个数分按碱性强弱分可溶性碱只有五种:氨水、氢氧化钠、氢氧化钾、氢氧化钡和氢氧化钙。其余的碱都不溶于水回家作业:1、将下列物质 放入水中,然后 滴加酚酞能变红色 的是( )
A、NaCl B 、 HCl C、 Cu(OH)2 D、Na2O2、在溶液导电性实验装置中盛有硫酸铜溶液,通电时灯泡发亮,若不断加入某物质,发现灯泡逐渐变暗,直至熄灭,再继续加入该物质灯泡又亮,则加入的物质是( )
A、氢氧化钠溶液 B、硝酸钠溶液
C、氢氧化钡溶液 D、铁粉C、DC3、滴入酚酞的氢氧化钡溶液与下列各物质恰好完全反应,溶液仍显红色的是( )
A 、 H2SO4 B、 HCl C 、CO2 D、 K2CO34、用下列试剂中的一种试剂就能鉴别氢氧化钠、氢氧化钙和硫酸 三种无色液体,这种试剂是( )
A、酚酞试液 B、氯化钡
C 硫酸钠溶液 D、碳酸钠溶液5、若完全中和某一盐酸溶液需用氢氧化钠溶液m克,现改用相同质量相同质量分数的氢氧化钾溶液去中和,反应完毕后,滴入石蕊试液显示的颜色为( )
A、红色 B、 紫色 C、 蓝色 D 、无色DDA
