高中化学鲁科版必修二第二章第一节3.9化学键与化学反应习题评讲课件(共23张ppt)
文档属性
| 名称 | 高中化学鲁科版必修二第二章第一节3.9化学键与化学反应习题评讲课件(共23张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-10 00:00:00 | ||
图片预览





文档简介
(共30张PPT)
化学键与化学反应习题评讲
1.化学键的巩固
2.电子式的书写
3.化学键能量高低与物质稳定性的关系
化学键>氢键>分子间作用力
*
研修班
*
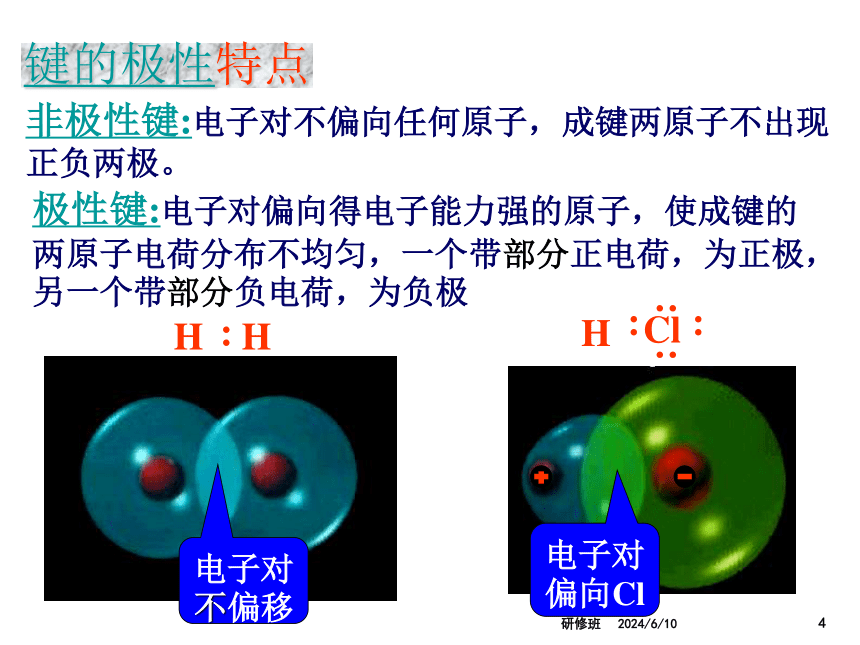
键的极性特点
非极性键:电子对不偏向任何原子,成键两原子不出现正负两极。
电子对不偏移
极性键:电子对偏向得电子能力强的原子,使成键的两原子电荷分布不均匀,一个带部分正电荷,为正极,另一个带部分负电荷,为负极
电子对偏向Cl
1.下列叙述中,正确的是( )。
A.离子化合物中可能同时含有极性共价键
B.非金属原子之间不可能形成离子化合物
C.两个非金属原子之间可以形成离子键
D.氢键是一种特殊共价键
2、下列有关物质性质的比较,结论正确的是(?? )
A.溶解度:Na2CO3
B.热稳定性:HClC.沸点:C2H5SH
D.碱性:LiOH2、下列物质:
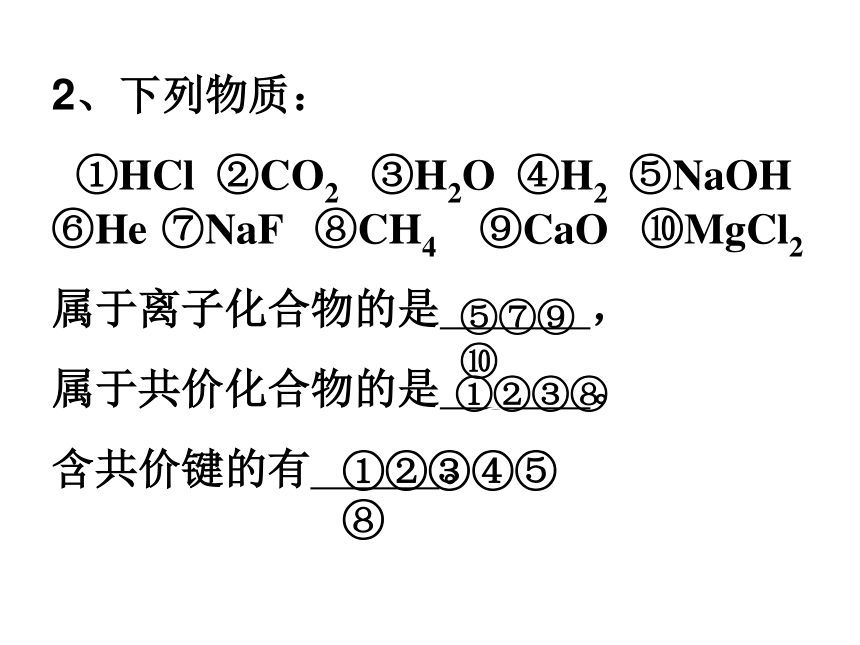
①HCl ②CO2 ③H2O ④H2 ⑤NaOH ⑥He ⑦NaF ⑧CH4 ⑨CaO ⑩MgCl2
属于离子化合物的是 ,
属于共价化合物的是 。
含共价键的有 。
⑤⑦⑨⑩
①②③⑧
⑤⑦⑨⑩
①②③⑧
①②③④⑤⑧
2、根据化学反应的实质是旧键断裂,新键生成这一事实,判断下列变化哪些是化学变化,并说出理由。
1、石墨在高温下转化为金刚石;
2、碘升华;
3、氯气加压变成液氯;
4、氯化钠的融化
结论:只有旧键断裂,无有新键生成,也就是说没有新物质生成,就不是化学变化。
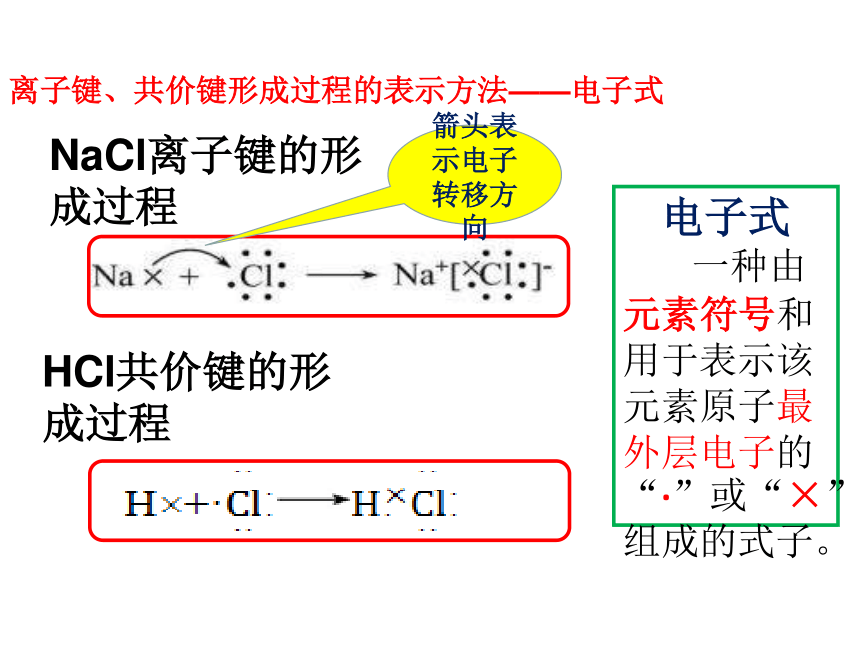
离子键、共价键形成过程的表示方法——电子式
NaCl离子键的形成过程
HCl共价键的形成过程
电子式
一种由元素符号和用于表示该元素原子最外层电子的“·”或“×”组成的式子。
箭头表示电子转移方向
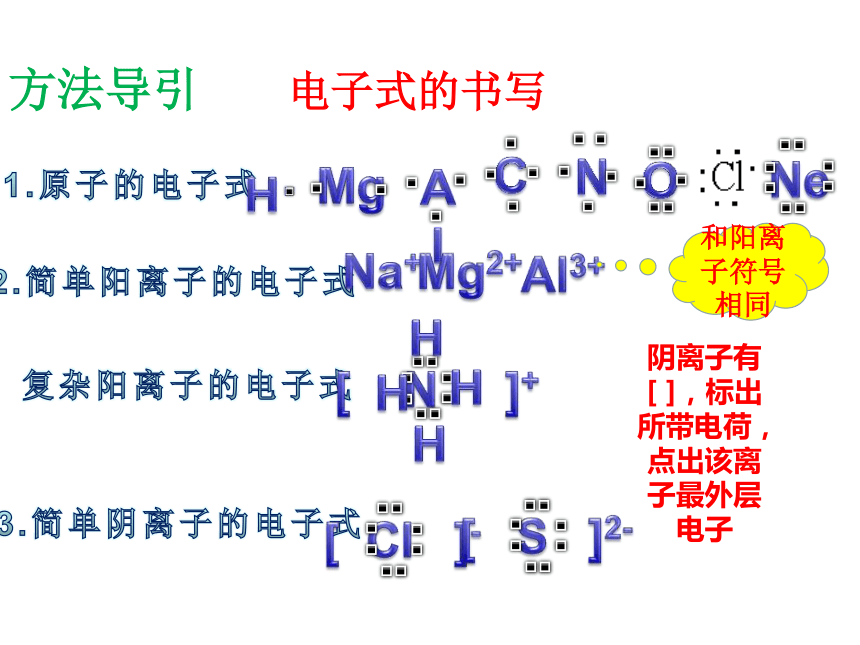
方法导引
和阳离子符号相同
电子式的书写
阴离子有[ ],标出所带电荷,点出该离子最外层电子
方法导引
电子式的书写
CO2
将阴阳离子的电子式写在一起,相同离子不合并,尽量对称
电子式的书写
1.下列电子式,正确的是( )
2.下列表示物质形成过程的电子式正确的是( )
反应物总能量 > 生成物总能量
是放热反应
反应物总能量 < 生成物总能量
是吸热反应
[结论]
常见的吸热反应
1、所有的燃烧反应
2、酸碱中和反应
3、金属与水或酸发生的置换反应
5、铝热反应
2、大多数分解反应
1、铵盐与碱的反应
3、以C、H2、CO为还原剂的氧化还原反应
4、大多数化合反应(C与CO2 反应等除外)
下列化学反应是释放能量还是吸收能量?
1、2Mg+O2=2MgO
2、 C+CO2=2CO
3、 H2SO4+2KOH=K2SO4+2H2O
4、 Mg+2HCl=MgCl2+H2 ↑
5、Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
6、2Al+Fe2O3=Al2O3+2Fe
7、C+H2O=CO+H2
点燃
高温
高温
高温
10.氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。
请回答下列问题:
(1)Na3N是由_______键形成的,它的电子式 ______,该化合物属于_____
(2)Na3N与盐酸反应生成 ____________种盐,化学反应方程式_________
(3)Na3N与水的反应属于___________反应,化学反应方程式___________
(4)Na3N中两种微粒的半径:r(Na+) ____________r(N3-)。 (填“>”“=”或“<”)
14.(15分)下列中的数据是破坏1mol物质中的化学键所消耗的能量(单位:kJ):
根据上述数据回答:
(1)下列物质本身具有的能量最低的是( )。
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中最稳定的是( )。
A.HCl B.HBr C.HI
(3)X2+H2=2HX(X代表Cl、Br、I)的反应是吸热反应还是放热反应?_____。
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是___________________。
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答:_________;你的根据是________________________________。
14.(1)A (2)A (3)放热 (4) Cl2
(5)能 非金属性越强,生成HX越稳定,放热越多
物质 Cl2 Br2 I2 HCl HBr HI H2
能量(kJ) 243 193 151 432 366 298 436
化学键与化学反应习题评讲
1.化学键的巩固
2.电子式的书写
3.化学键能量高低与物质稳定性的关系
化学键>氢键>分子间作用力
*
研修班
*
键的极性特点
非极性键:电子对不偏向任何原子,成键两原子不出现正负两极。
电子对不偏移
极性键:电子对偏向得电子能力强的原子,使成键的两原子电荷分布不均匀,一个带部分正电荷,为正极,另一个带部分负电荷,为负极
电子对偏向Cl
1.下列叙述中,正确的是( )。
A.离子化合物中可能同时含有极性共价键
B.非金属原子之间不可能形成离子化合物
C.两个非金属原子之间可以形成离子键
D.氢键是一种特殊共价键
2、下列有关物质性质的比较,结论正确的是(?? )
A.溶解度:Na2CO3
B.热稳定性:HCl
D.碱性:LiOH
①HCl ②CO2 ③H2O ④H2 ⑤NaOH ⑥He ⑦NaF ⑧CH4 ⑨CaO ⑩MgCl2
属于离子化合物的是 ,
属于共价化合物的是 。
含共价键的有 。
⑤⑦⑨⑩
①②③⑧
⑤⑦⑨⑩
①②③⑧
①②③④⑤⑧
2、根据化学反应的实质是旧键断裂,新键生成这一事实,判断下列变化哪些是化学变化,并说出理由。
1、石墨在高温下转化为金刚石;
2、碘升华;
3、氯气加压变成液氯;
4、氯化钠的融化
结论:只有旧键断裂,无有新键生成,也就是说没有新物质生成,就不是化学变化。
离子键、共价键形成过程的表示方法——电子式
NaCl离子键的形成过程
HCl共价键的形成过程
电子式
一种由元素符号和用于表示该元素原子最外层电子的“·”或“×”组成的式子。
箭头表示电子转移方向
方法导引
和阳离子符号相同
电子式的书写
阴离子有[ ],标出所带电荷,点出该离子最外层电子
方法导引
电子式的书写
CO2
将阴阳离子的电子式写在一起,相同离子不合并,尽量对称
电子式的书写
1.下列电子式,正确的是( )
2.下列表示物质形成过程的电子式正确的是( )
反应物总能量 > 生成物总能量
是放热反应
反应物总能量 < 生成物总能量
是吸热反应
[结论]
常见的吸热反应
1、所有的燃烧反应
2、酸碱中和反应
3、金属与水或酸发生的置换反应
5、铝热反应
2、大多数分解反应
1、铵盐与碱的反应
3、以C、H2、CO为还原剂的氧化还原反应
4、大多数化合反应(C与CO2 反应等除外)
下列化学反应是释放能量还是吸收能量?
1、2Mg+O2=2MgO
2、 C+CO2=2CO
3、 H2SO4+2KOH=K2SO4+2H2O
4、 Mg+2HCl=MgCl2+H2 ↑
5、Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
6、2Al+Fe2O3=Al2O3+2Fe
7、C+H2O=CO+H2
点燃
高温
高温
高温
10.氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。
请回答下列问题:
(1)Na3N是由_______键形成的,它的电子式 ______,该化合物属于_____
(2)Na3N与盐酸反应生成 ____________种盐,化学反应方程式_________
(3)Na3N与水的反应属于___________反应,化学反应方程式___________
(4)Na3N中两种微粒的半径:r(Na+) ____________r(N3-)。 (填“>”“=”或“<”)
14.(15分)下列中的数据是破坏1mol物质中的化学键所消耗的能量(单位:kJ):
根据上述数据回答:
(1)下列物质本身具有的能量最低的是( )。
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中最稳定的是( )。
A.HCl B.HBr C.HI
(3)X2+H2=2HX(X代表Cl、Br、I)的反应是吸热反应还是放热反应?_____。
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是___________________。
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答:_________;你的根据是________________________________。
14.(1)A (2)A (3)放热 (4) Cl2
(5)能 非金属性越强,生成HX越稳定,放热越多
物质 Cl2 Br2 I2 HCl HBr HI H2
能量(kJ) 243 193 151 432 366 298 436
