3.4 二氧化碳 导学案(含答案)
图片预览


文档简介
二氧化碳
课前一练
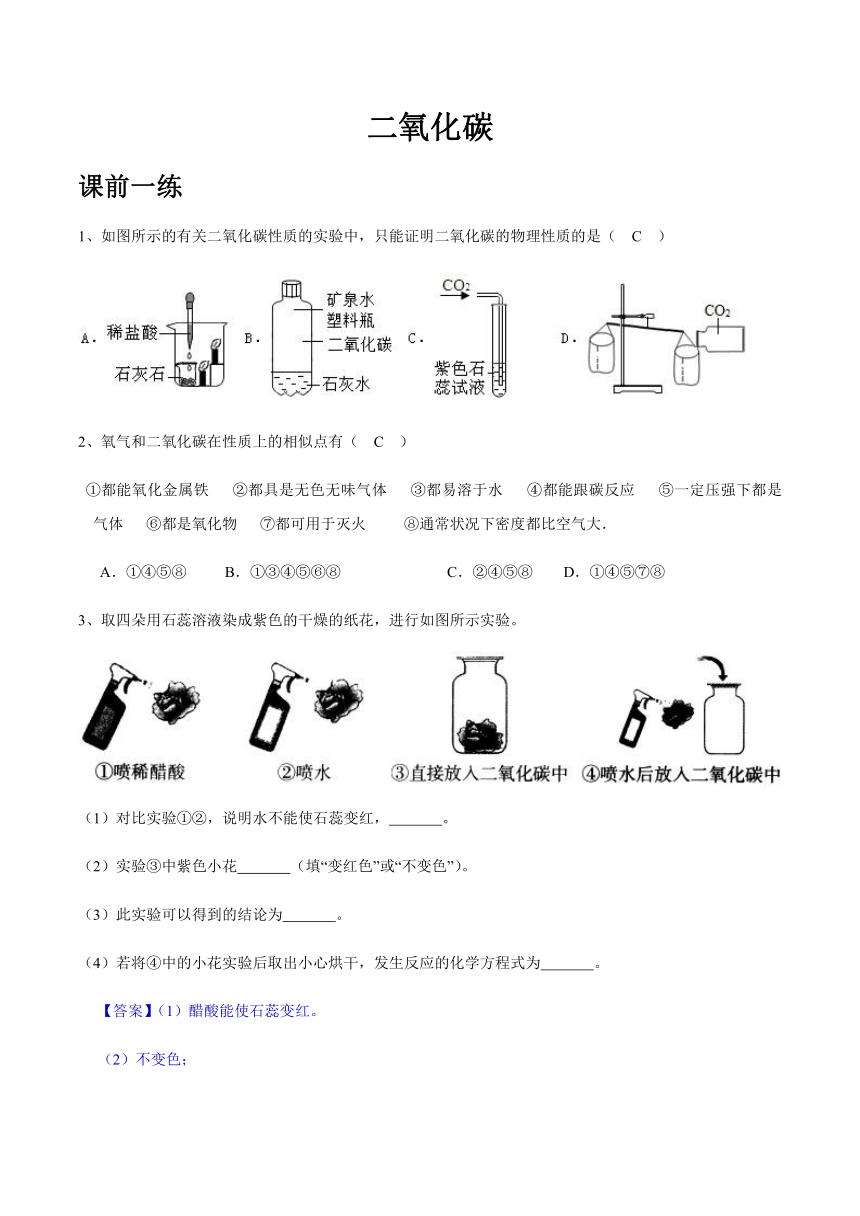
1、如图所示的有关二氧化碳性质的实验中,只能证明二氧化碳的物理性质的是( C )
2、氧气和二氧化碳在性质上的相似点有( C )
①都能氧化金属铁 ②都具是无色无味气体 ③都易溶于水 ④都能跟碳反应 ⑤一定压强下都是气体 ⑥都是氧化物 ⑦都可用于灭火 ⑧通常状况下密度都比空气大.
A.①④⑤⑧ B.①③④⑤⑥⑧ C.②④⑤⑧ D.①④⑤⑦⑧
3、取四朵用石蕊溶液染成紫色的干燥的纸花,进行如图所示实验。
(1)对比实验①②,说明水不能使石蕊变红, 。
(2)实验③中紫色小花 (填“变红色”或“不变色”)。
(3)此实验可以得到的结论为 。
(4)若将④中的小花实验后取出小心烘干,发生反应的化学方程式为 。
【答案】(1)醋酸能使石蕊变红。
(2)不变色;
(3)二氧化碳和水反应,生成酸性物质。
(4)H2CO3=CO2↑+H2O。
要点导航
一、自然界中的二氧化碳
1、二氧化碳在空气中含量不多,约占 0.03%。
2、二氧化碳是由大量二氧化碳分子 (CO2) 聚集而成,每个二氧化碳分子由一个碳原子和两个氧原子构成,其分子结构模型如图所示:
3、CO2本身没有毒性,但当空气中的 CO2超过正常含量时,会对人体产生有害的影响。
二、二氧化碳的性质
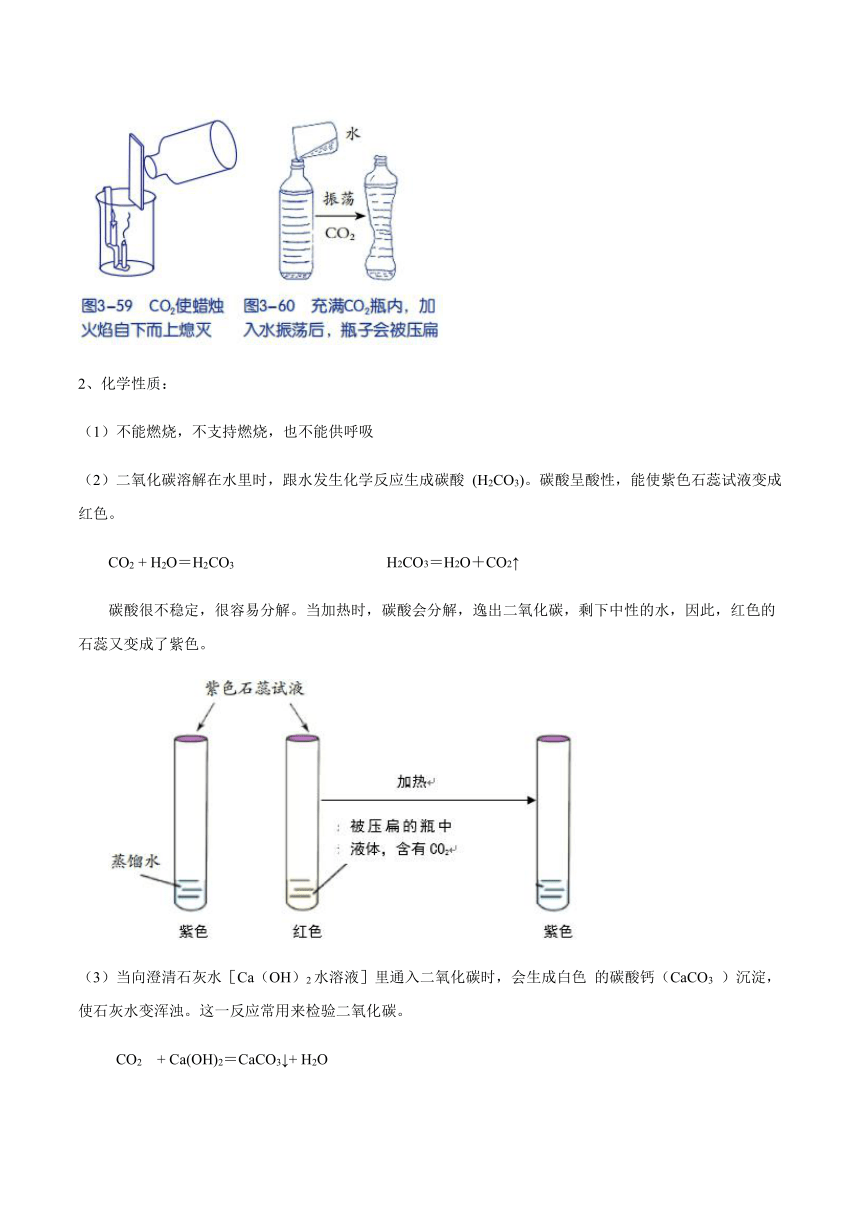
1、物理性质:二氧化碳在通常状态下,无色无味,能溶于水,密度比空气大;固体(干冰)
2、化学性质:
(1)不能燃烧,不支持燃烧,也不能供呼吸
(2)二氧化碳溶解在水里时,跟水发生化学反应生成碳酸 (H2CO3)。碳酸呈酸性,能使紫色石蕊试液变成红色。
CO2 + H2O=H2CO3 H2CO3=H2O+CO2↑
碳酸很不稳定,很容易分解。当加热时,碳酸会分解,逸出二氧化碳,剩下中性的水,因此,红色的石蕊又变成了紫色。
(3)当向澄清石灰水[Ca(OH)2水溶液]里通入二氧化碳时,会生成白色 的碳酸钙(CaCO3 )沉淀,使石灰水变浑浊。这一反应常用来检验二氧化碳。
CO2 + Ca(OH)2=CaCO3↓+ H2O
(4)与Mg反应:2Mg+CO22MgO+C
现象:Mg条在CO2中剧烈燃烧,放出白光和大量热,生成黑色固体和白色固体。
(5)与C反应:CO2 + C2CO
CO2 与C 在高温条件下,生成无色、无臭、无味的气体CO ,密度比空气小,具有毒性,一氧化碳进入人体之后会和血液中的血红蛋白结合,产生碳氧血红蛋白,进而使血红蛋白不能与氧气结合,从而引起机体组织出现缺氧,导致人体窒息死亡。
二氧化碳的制备
1、实验室制备
(1)制备原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
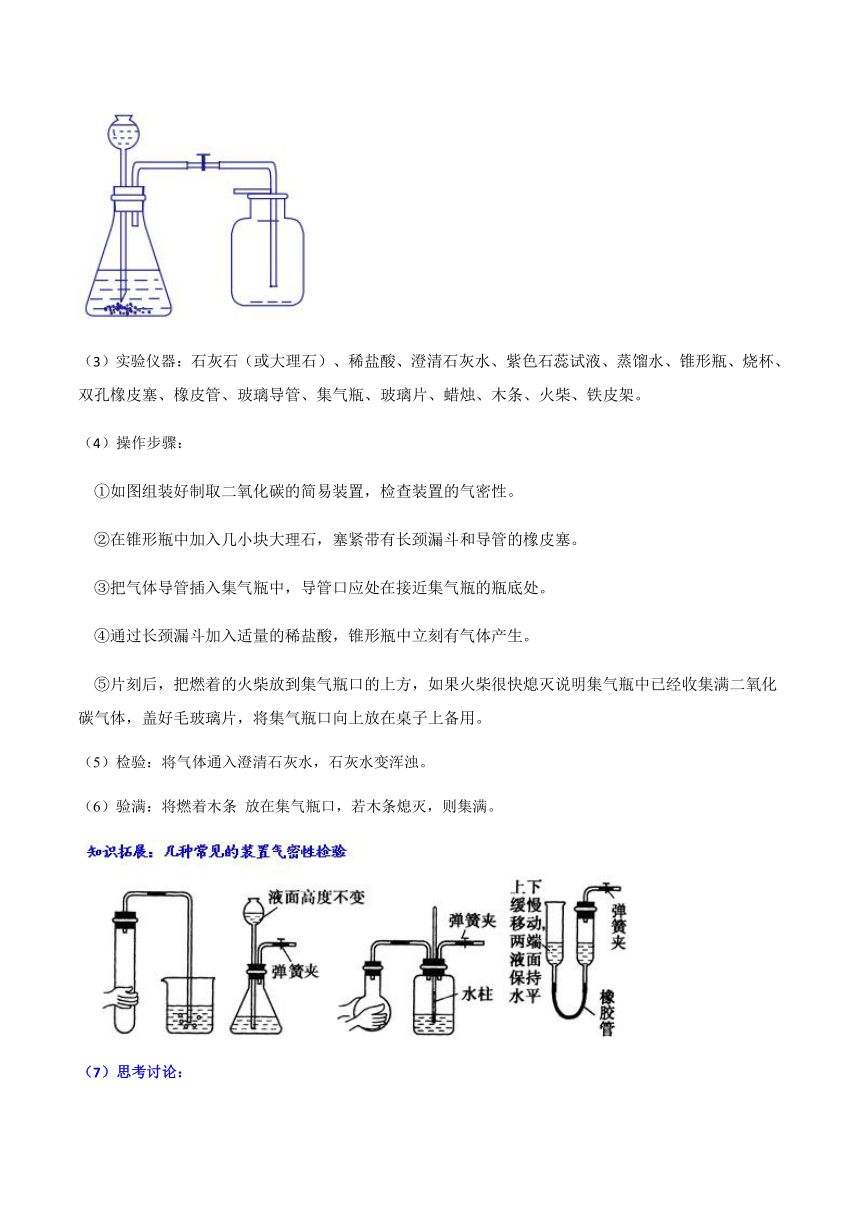
(2)制取装置:
(3)实验仪器:石灰石(或大理石)、稀盐酸、澄清石灰水、紫色石蕊试液、蒸馏水、锥形瓶、烧杯、双孔橡皮塞、橡皮管、玻璃导管、集气瓶、玻璃片、蜡烛、木条、火柴、铁皮架。
(4)操作步骤:
①如图组装好制取二氧化碳的简易装置,检查装置的气密性。
②在锥形瓶中加入几小块大理石,塞紧带有长颈漏斗和导管的橡皮塞。
③把气体导管插入集气瓶中,导管口应处在接近集气瓶的瓶底处。
④通过长颈漏斗加入适量的稀盐酸,锥形瓶中立刻有气体产生。
⑤片刻后,把燃着的火柴放到集气瓶口的上方,如果火柴很快熄灭说明集气瓶中已经收集满二氧化碳气体,盖好毛玻璃片,将集气瓶口向上放在桌子上备用。
(5)检验:将气体通入澄清石灰水,石灰水变浑浊。
(6)验满:将燃着木条 放在集气瓶口,若木条熄灭,则集满。
(7)思考讨论:
①装置缺陷—盐酸易挥发,污染环境;反应不能控制,不能随用随停。
②改进装置:
(8)注意事项:
①制备二氧化碳的盐酸不宜太浓,否则从盐酸里会挥发出氯化氢气体,使制得的二氧化碳不纯,有时还会影响实验的结果。
②不宜使用硫酸和石灰石来制取二氧化碳,因为硫酸与碳酸钙反应后生成溶解性较小的硫酸钙,会覆盖在石灰石表面从而阻止反应的继续进行。
③如果使用长颈漏斗,最好不要使用纯净的碳酸钙或碳酸钠。因为使用纯度高的碳酸钙或碳酸钠会造成反应过快,不宜控制。但是将长颈漏斗改成分液漏斗,就可以使用纯度高的碳酸钙或碳酸钠来制取二氧化碳了。
(9)误点评析:
①长颈漏斗下口没有伸入液面下,会导致二氧化碳从长颈漏斗逸出。
②出气导管管口不应伸入液面下,这样二氧化碳会把酸液沿导管压出,无法收集气体,该出气导管管口应在锥形瓶上方,略伸出橡皮塞。
2、工业制备
(1)制备原理:高温煅烧碳酸钙制得二氧化碳
(2)反应方程式:CaCO3 CaO + CO2↑
四、二氧化碳的应用
用途:
(1)作为灭火剂。
(2)固态的二氧化碳即“干冰”,主要用作致冷剂,用飞机在高空喷撒“干冰”,可以使空气中水蒸气冷凝,形成人工降雨。
(3)农业上,温室里直接施用二氧化碳作肥料,可以增进植物的光合作用。
2、影响:温室效应,二氧化碳具有保温的作用,会逐渐使地球表面温度升高。
[同步练习
1. 身边处处有科学,科学与我们的生产、生活密切相关。请根据你的生活经验和所学的科学知识判断,下列做法合理的是 ( B )
A.用电器短路着火,立即用水扑灭
B.在冰箱里放入活性炭,除去冰箱里的异味
C.室内烤火取暖放一盆水,防止CO中毒
D.在食品袋里充入氧气,延长食品的保质期
2. “两型”社会,提倡“低碳”生活,下列有关碳及其化合物的 说法正确的是 ( C )
A.二氧化碳是导致酸雨的主要气体
B.室内放一盆水能防止一氧化碳中毒
C.大气中二氧化碳消耗的途径主要是绿色植物的光合作用
D.金刚石、石墨是碳的单质,而C60则是碳的化合物
3. 用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是(??D )
A.隔绝空气 B.降低可燃物的着火点
C.清除可燃物 D.使可燃物温度降到着火点以下
4. 温室效应有功有过,产生温室效应的主要气体是CO2,下列有关认识错误的是 ( A )
A.CO2能使干燥石蕊纸花变红
B.CO2能使澄清石灰水变浑浊
C.“低碳”是指较少的CO2排放
D.温室效应为人类提供了适宜的生存温度
5. 下列有关二氧化碳的说法正确的是 ( B )
A.二氧化碳是引发酸雨的“罪魁祸首”
B.二氧化碳固体可用于人工降雨
C.二氧化碳可使紫色石蕊试液变蓝
D.二氧化碳有毒不能制作碳酸饮料
6. 通过实验探究可获得较多的化学知识,对下图所示的实验分析错误的是(??D )
两支蜡烛自下而上依次熄灭 B. 二氧化碳不能燃烧
C. 二氧化碳的密度比空气大 D. 二氧化碳支持燃烧
7. 如图所示,向盛有某种液体的烧杯中通人二氧化碳气体,可观察到烧杯中的液体发生了明显变化.烧杯中盛放的液体是什么呢?甲同学认为:可能是澄清的石灰水,乙同学认为:可能是蒸馏水;丙同学认为可能是紫色的石蕊试液.你认为三位同学提出的看法中正确的是( B )
A. 甲和乙 B. 甲和丙 C. 乙和丙 D. 甲、乙和丙
8. 可生成二氧化碳的反应很多,例如:①酒精的燃烧 ②木炭在空气中燃烧 ③碳与氧化铜反应 ④高温煅烧石灰石 ⑤石灰石与稀硫酸反应 ⑥石灰石与稀盐酸反应 ⑦碳酸钙粉末与浓盐酸 ⑧人和动物的呼吸作用。其中可用于实验室制取二氧化碳的是( C )
A.①②③ B.③④⑤ C.⑥ D.全部
9. 二氧化碳气体既是温室效应的元凶,又是一种潜在的碳资源。实验室里,科学家已成功利用二氧化碳与环氧丙烷(一种简单有机物)在催化剂的作用下合成“二氧化碳塑料”。该新型塑料在投入工业生产前,以下不是科学家重点考虑的问题是( D )
A. 如何提高催化剂的催化效率 B. 新型塑料是否可降解
C. 新型塑料的化学性质是否稳定 D. 新型塑料生产是否影响碳循环
10. 利用四氧化三钴纳米棒作催化剂,可将汽车尾气中的CO在低温下转化为CO2。下列关于该反应的说法中,正确的是 ( C )
A.反应物和生成物都是化合物,该反应属于化合反应
B.反应前后四氧化三钴纳米棒的化学性质发生了变化
C.可有效降低汽车尾气对大气的污染
D.反应前后氧原子数目发生了变化
11. 超临界流体是物质介于气态和液态之间的新状态,目前应用最广泛的是超临界二氧化碳,它在化学工业上可取代氟利昂作溶剂等。下列有关超临界二氧化碳的说法中不正确的是( A )
A.超临界二氧化碳是合成的一种新物质
B.超临界二氧化碳是由CO2分子构成的
C.超临界二氧化碳溶解某些物质后,二氧化碳可在常温常压下完全挥发
D.用超临界二氧化碳代替氟利昂,可减轻大量使用氟利昂对大气臭氧层造成的破坏
12. 某化学小组Ⅰ探究用大理石和稀盐酸反应制取二氧化碳气体,并进行性质实验.如图是有关实验的部分装置,请根据要求回答问题: (1)a仪器的名称为_____________;甲同学用A和C组合制取二氧化碳,乙同学用B和C组合制取二氧化碳,你认为哪个组合更便于控制反应___________(填写甲或乙). (2)甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,用化学方程式表示可能的原因________________________________________; (3)装置G的胶头滴管内的NaOH滴入锥形瓶后,小气球的形状将会________(填“变大”或“变小”); (4)装置B中若放入10g不纯的锌,组装仪器后,称得药品和仪器的总质量为120g,反应完全后,称得装置的总质量为119.8g,粗锌的质量分数为__________________.
答案: (1)长颈漏斗;乙;(2)H2CO3=H2O+CO2↑;(3)变大;(4)65%。
13. 实验室按如图所示装置制取CO2,并检验CO2的性质。试回答以下问题:
(1)实验开始前,先应检查装置A的_______________;
(2)用装置A来制取CO2,所用的药品是___________和____________(写化学式);
(3)若要用装置B鉴定CO2,在B中应盛放的试剂名称是_____________,当将标①和②的导管口连接时,B中看到的实验现象是___________________;
(4)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是___________,当将标①和③的导管口连接时,C中看到的实验现象是______________;
(5)烧杯D中放有燃着的蜡烛如图所示,当将标①和④的导管口连接时,D中看到的实验现象是__________________________________________;
(6)继续设计并进行有关CO2性质的探究实验,如装置E、F。先在装置E中放一个用空气充胀的气球,制取一瓶二氧化碳倒入E装置后,出现如F装置实验现象。请回答:该实验的目的是探究_________________________________________。
【答案】 (1)气密性(2)CaCO3;HCl(3)澄清的石灰水;澄清的石灰水变浑浊(4)紫色石蕊溶液;紫色变成红色(5)下面的蜡烛先熄灭,上面的蜡烛后熄灭(6)CO2的密度是否比空气大.
课前一练
1、如图所示的有关二氧化碳性质的实验中,只能证明二氧化碳的物理性质的是( C )
2、氧气和二氧化碳在性质上的相似点有( C )
①都能氧化金属铁 ②都具是无色无味气体 ③都易溶于水 ④都能跟碳反应 ⑤一定压强下都是气体 ⑥都是氧化物 ⑦都可用于灭火 ⑧通常状况下密度都比空气大.
A.①④⑤⑧ B.①③④⑤⑥⑧ C.②④⑤⑧ D.①④⑤⑦⑧
3、取四朵用石蕊溶液染成紫色的干燥的纸花,进行如图所示实验。
(1)对比实验①②,说明水不能使石蕊变红, 。
(2)实验③中紫色小花 (填“变红色”或“不变色”)。
(3)此实验可以得到的结论为 。
(4)若将④中的小花实验后取出小心烘干,发生反应的化学方程式为 。
【答案】(1)醋酸能使石蕊变红。
(2)不变色;
(3)二氧化碳和水反应,生成酸性物质。
(4)H2CO3=CO2↑+H2O。
要点导航
一、自然界中的二氧化碳
1、二氧化碳在空气中含量不多,约占 0.03%。
2、二氧化碳是由大量二氧化碳分子 (CO2) 聚集而成,每个二氧化碳分子由一个碳原子和两个氧原子构成,其分子结构模型如图所示:
3、CO2本身没有毒性,但当空气中的 CO2超过正常含量时,会对人体产生有害的影响。
二、二氧化碳的性质
1、物理性质:二氧化碳在通常状态下,无色无味,能溶于水,密度比空气大;固体(干冰)
2、化学性质:
(1)不能燃烧,不支持燃烧,也不能供呼吸
(2)二氧化碳溶解在水里时,跟水发生化学反应生成碳酸 (H2CO3)。碳酸呈酸性,能使紫色石蕊试液变成红色。
CO2 + H2O=H2CO3 H2CO3=H2O+CO2↑
碳酸很不稳定,很容易分解。当加热时,碳酸会分解,逸出二氧化碳,剩下中性的水,因此,红色的石蕊又变成了紫色。
(3)当向澄清石灰水[Ca(OH)2水溶液]里通入二氧化碳时,会生成白色 的碳酸钙(CaCO3 )沉淀,使石灰水变浑浊。这一反应常用来检验二氧化碳。
CO2 + Ca(OH)2=CaCO3↓+ H2O
(4)与Mg反应:2Mg+CO22MgO+C
现象:Mg条在CO2中剧烈燃烧,放出白光和大量热,生成黑色固体和白色固体。
(5)与C反应:CO2 + C2CO
CO2 与C 在高温条件下,生成无色、无臭、无味的气体CO ,密度比空气小,具有毒性,一氧化碳进入人体之后会和血液中的血红蛋白结合,产生碳氧血红蛋白,进而使血红蛋白不能与氧气结合,从而引起机体组织出现缺氧,导致人体窒息死亡。
二氧化碳的制备
1、实验室制备
(1)制备原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
(2)制取装置:
(3)实验仪器:石灰石(或大理石)、稀盐酸、澄清石灰水、紫色石蕊试液、蒸馏水、锥形瓶、烧杯、双孔橡皮塞、橡皮管、玻璃导管、集气瓶、玻璃片、蜡烛、木条、火柴、铁皮架。
(4)操作步骤:
①如图组装好制取二氧化碳的简易装置,检查装置的气密性。
②在锥形瓶中加入几小块大理石,塞紧带有长颈漏斗和导管的橡皮塞。
③把气体导管插入集气瓶中,导管口应处在接近集气瓶的瓶底处。
④通过长颈漏斗加入适量的稀盐酸,锥形瓶中立刻有气体产生。
⑤片刻后,把燃着的火柴放到集气瓶口的上方,如果火柴很快熄灭说明集气瓶中已经收集满二氧化碳气体,盖好毛玻璃片,将集气瓶口向上放在桌子上备用。
(5)检验:将气体通入澄清石灰水,石灰水变浑浊。
(6)验满:将燃着木条 放在集气瓶口,若木条熄灭,则集满。
(7)思考讨论:
①装置缺陷—盐酸易挥发,污染环境;反应不能控制,不能随用随停。
②改进装置:
(8)注意事项:
①制备二氧化碳的盐酸不宜太浓,否则从盐酸里会挥发出氯化氢气体,使制得的二氧化碳不纯,有时还会影响实验的结果。
②不宜使用硫酸和石灰石来制取二氧化碳,因为硫酸与碳酸钙反应后生成溶解性较小的硫酸钙,会覆盖在石灰石表面从而阻止反应的继续进行。
③如果使用长颈漏斗,最好不要使用纯净的碳酸钙或碳酸钠。因为使用纯度高的碳酸钙或碳酸钠会造成反应过快,不宜控制。但是将长颈漏斗改成分液漏斗,就可以使用纯度高的碳酸钙或碳酸钠来制取二氧化碳了。
(9)误点评析:
①长颈漏斗下口没有伸入液面下,会导致二氧化碳从长颈漏斗逸出。
②出气导管管口不应伸入液面下,这样二氧化碳会把酸液沿导管压出,无法收集气体,该出气导管管口应在锥形瓶上方,略伸出橡皮塞。
2、工业制备
(1)制备原理:高温煅烧碳酸钙制得二氧化碳
(2)反应方程式:CaCO3 CaO + CO2↑
四、二氧化碳的应用
用途:
(1)作为灭火剂。
(2)固态的二氧化碳即“干冰”,主要用作致冷剂,用飞机在高空喷撒“干冰”,可以使空气中水蒸气冷凝,形成人工降雨。
(3)农业上,温室里直接施用二氧化碳作肥料,可以增进植物的光合作用。
2、影响:温室效应,二氧化碳具有保温的作用,会逐渐使地球表面温度升高。
[同步练习
1. 身边处处有科学,科学与我们的生产、生活密切相关。请根据你的生活经验和所学的科学知识判断,下列做法合理的是 ( B )
A.用电器短路着火,立即用水扑灭
B.在冰箱里放入活性炭,除去冰箱里的异味
C.室内烤火取暖放一盆水,防止CO中毒
D.在食品袋里充入氧气,延长食品的保质期
2. “两型”社会,提倡“低碳”生活,下列有关碳及其化合物的 说法正确的是 ( C )
A.二氧化碳是导致酸雨的主要气体
B.室内放一盆水能防止一氧化碳中毒
C.大气中二氧化碳消耗的途径主要是绿色植物的光合作用
D.金刚石、石墨是碳的单质,而C60则是碳的化合物
3. 用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是(??D )
A.隔绝空气 B.降低可燃物的着火点
C.清除可燃物 D.使可燃物温度降到着火点以下
4. 温室效应有功有过,产生温室效应的主要气体是CO2,下列有关认识错误的是 ( A )
A.CO2能使干燥石蕊纸花变红
B.CO2能使澄清石灰水变浑浊
C.“低碳”是指较少的CO2排放
D.温室效应为人类提供了适宜的生存温度
5. 下列有关二氧化碳的说法正确的是 ( B )
A.二氧化碳是引发酸雨的“罪魁祸首”
B.二氧化碳固体可用于人工降雨
C.二氧化碳可使紫色石蕊试液变蓝
D.二氧化碳有毒不能制作碳酸饮料
6. 通过实验探究可获得较多的化学知识,对下图所示的实验分析错误的是(??D )
两支蜡烛自下而上依次熄灭 B. 二氧化碳不能燃烧
C. 二氧化碳的密度比空气大 D. 二氧化碳支持燃烧
7. 如图所示,向盛有某种液体的烧杯中通人二氧化碳气体,可观察到烧杯中的液体发生了明显变化.烧杯中盛放的液体是什么呢?甲同学认为:可能是澄清的石灰水,乙同学认为:可能是蒸馏水;丙同学认为可能是紫色的石蕊试液.你认为三位同学提出的看法中正确的是( B )
A. 甲和乙 B. 甲和丙 C. 乙和丙 D. 甲、乙和丙
8. 可生成二氧化碳的反应很多,例如:①酒精的燃烧 ②木炭在空气中燃烧 ③碳与氧化铜反应 ④高温煅烧石灰石 ⑤石灰石与稀硫酸反应 ⑥石灰石与稀盐酸反应 ⑦碳酸钙粉末与浓盐酸 ⑧人和动物的呼吸作用。其中可用于实验室制取二氧化碳的是( C )
A.①②③ B.③④⑤ C.⑥ D.全部
9. 二氧化碳气体既是温室效应的元凶,又是一种潜在的碳资源。实验室里,科学家已成功利用二氧化碳与环氧丙烷(一种简单有机物)在催化剂的作用下合成“二氧化碳塑料”。该新型塑料在投入工业生产前,以下不是科学家重点考虑的问题是( D )
A. 如何提高催化剂的催化效率 B. 新型塑料是否可降解
C. 新型塑料的化学性质是否稳定 D. 新型塑料生产是否影响碳循环
10. 利用四氧化三钴纳米棒作催化剂,可将汽车尾气中的CO在低温下转化为CO2。下列关于该反应的说法中,正确的是 ( C )
A.反应物和生成物都是化合物,该反应属于化合反应
B.反应前后四氧化三钴纳米棒的化学性质发生了变化
C.可有效降低汽车尾气对大气的污染
D.反应前后氧原子数目发生了变化
11. 超临界流体是物质介于气态和液态之间的新状态,目前应用最广泛的是超临界二氧化碳,它在化学工业上可取代氟利昂作溶剂等。下列有关超临界二氧化碳的说法中不正确的是( A )
A.超临界二氧化碳是合成的一种新物质
B.超临界二氧化碳是由CO2分子构成的
C.超临界二氧化碳溶解某些物质后,二氧化碳可在常温常压下完全挥发
D.用超临界二氧化碳代替氟利昂,可减轻大量使用氟利昂对大气臭氧层造成的破坏
12. 某化学小组Ⅰ探究用大理石和稀盐酸反应制取二氧化碳气体,并进行性质实验.如图是有关实验的部分装置,请根据要求回答问题: (1)a仪器的名称为_____________;甲同学用A和C组合制取二氧化碳,乙同学用B和C组合制取二氧化碳,你认为哪个组合更便于控制反应___________(填写甲或乙). (2)甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,用化学方程式表示可能的原因________________________________________; (3)装置G的胶头滴管内的NaOH滴入锥形瓶后,小气球的形状将会________(填“变大”或“变小”); (4)装置B中若放入10g不纯的锌,组装仪器后,称得药品和仪器的总质量为120g,反应完全后,称得装置的总质量为119.8g,粗锌的质量分数为__________________.
答案: (1)长颈漏斗;乙;(2)H2CO3=H2O+CO2↑;(3)变大;(4)65%。
13. 实验室按如图所示装置制取CO2,并检验CO2的性质。试回答以下问题:
(1)实验开始前,先应检查装置A的_______________;
(2)用装置A来制取CO2,所用的药品是___________和____________(写化学式);
(3)若要用装置B鉴定CO2,在B中应盛放的试剂名称是_____________,当将标①和②的导管口连接时,B中看到的实验现象是___________________;
(4)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是___________,当将标①和③的导管口连接时,C中看到的实验现象是______________;
(5)烧杯D中放有燃着的蜡烛如图所示,当将标①和④的导管口连接时,D中看到的实验现象是__________________________________________;
(6)继续设计并进行有关CO2性质的探究实验,如装置E、F。先在装置E中放一个用空气充胀的气球,制取一瓶二氧化碳倒入E装置后,出现如F装置实验现象。请回答:该实验的目的是探究_________________________________________。
【答案】 (1)气密性(2)CaCO3;HCl(3)澄清的石灰水;澄清的石灰水变浑浊(4)紫色石蕊溶液;紫色变成红色(5)下面的蜡烛先熄灭,上面的蜡烛后熄灭(6)CO2的密度是否比空气大.
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
