鲁科化学必修2第二章1化学键与化学反应(共18张PPT)
文档属性
| 名称 | 鲁科化学必修2第二章1化学键与化学反应(共18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 6.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-11 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
第一节
化学键与化学反应
学
探
探究活动
1、老师给每个小组准备了若干个氢原子和氧原子的模型,
请相互讨论,试着用氧原子和氢原子的模型不借
助任何工具拼接出水分子。
拼接不成,原子之间没有能使它们结合在一起的作用力。
2、老师给每个小组发放几个链接原子的细铁棍,再试一次。
每个小组都拼接出水分子的模型。
[结论]:原子要构成物质,必须有一种能使它们彼此结合在一起的作用。
一、化学键:
1、定义:相邻原子间强相互作用
化学键与物质变化
注意:化学键存在在分子内
思
化学键是一种较强的相互作用
(包括吸引和排斥达到平衡)
探
探究活动
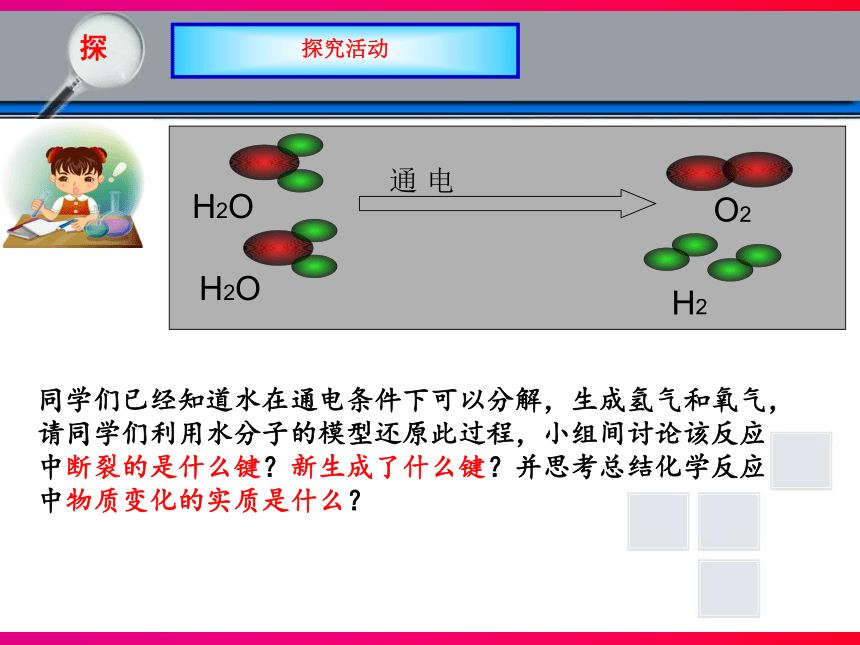
同学们已经知道水在通电条件下可以分解,生成氢气和氧气,
请同学们利用水分子的模型还原此过程,小组间讨论该反应
中断裂的是什么键?新生成了什么键?并思考总结化学反应
中物质变化的实质是什么?
H2O
H2O
H2
H2
O2
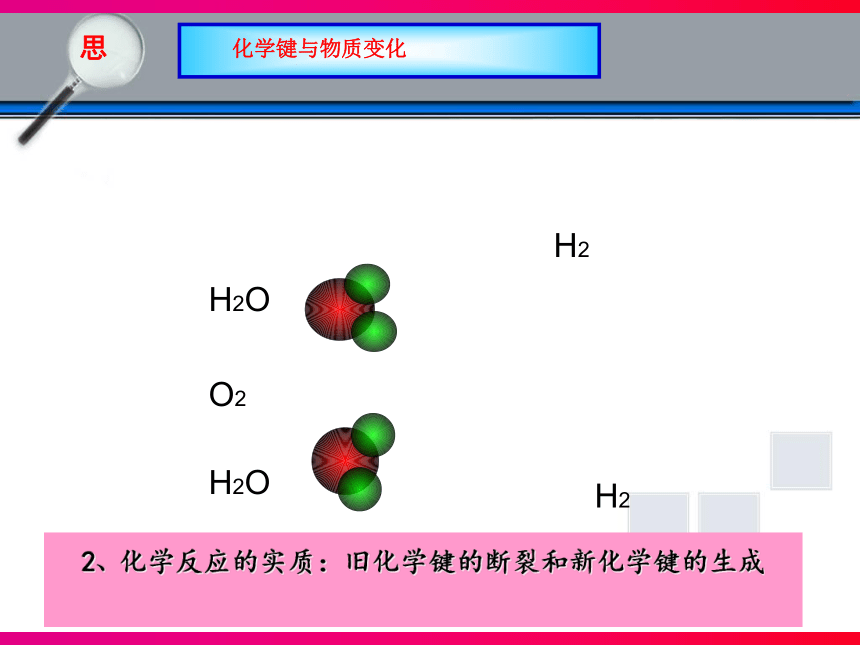
2、化学反应的实质:旧化学键的断裂和新化学键的生成
思
化学键与物质变化
讨
化学键与物质变化
[小组思考交流讨论]
1、构成单质分子的粒子一定含有化学键吗?
2、氯化钠的熔化、氯化氢的溶解是否是化学变化?
3、石墨在一定条件下转化为金刚石是否是化学变化?
惰性气体单质中不存在化学键
同素异形体的转化属于化学变化
物质的溶解及熔化都属于物理变化
钠可以在氯气中燃烧生成氯化钠,氢气在氯气中燃烧生成氯化氢,氯化
氢分子存在着氢原子和氯原子形成的化学键,氯化钠固体中也存在化
学键,但是两者中的化学键是否相同?
思
化学键的分类
讨
化学键的分类
阅读教材p33-34的内容,结合化学反应的实质,根
据核外电子排布规律,小组讨论以下问题,并从成
键原因、成键元素、成键作用力三个方面比较NaCl和
HCl的形成过程,思考什么是离子键?什么是共价键?
1、画出Na、Cl和H的原子结构示意图
2、Na、Cl和H的原子结构是否稳定?
3、NaCl是怎样形成的?
4、HCl分子是怎样形成的?
失 e-
得 e-
静电作用
Na+
Cl-
讨
氯化钠的形成过程
通过共用电子对
讨
氯化氢的形成过程
结
想形成稳定结构
Na+和Cl-
H和Cl
静电作用
共用电子对相互作用
离子键:阴、阳离子间通过静电作用形成的化学键
共价键:原子间通过共用电子对形成的化学键
化学键的分类
NaCl HCl
成键原因
成键微粒
成键作用力
结
离子键、共价键比较
离子键、共价键的比较
想形成稳定结构
静电作用
共用电子对相互作用
阴阳离子
原子
活泼金属元素(IA、IIA)和活泼非金属元素(VIA、VIIA)
非金属元素
离子键 共价键
成键原因
成键方式
成键微粒
成键元素
讨
共价键的分类
1、通过什么判断化学键的类型?
2、是不是非金属元素间形成的化学键都是共价键?
3、是不是只有不同非金属间才能形成共价键?
交流研讨
下表给出的都是你熟悉的物质,请利用化学键的知识
分析它们的构成情况,并思考下面的问题
形成化化学键的微粒
否,铵盐间的化学键为离子键
否,相同非金属间也可以形成共价键
氢原子和氧原子
氢原子和氢原子
钾离子和氯离子
铵根离子和氯离子
共价键
共价键
离子键
离子键
4、氢气和氯化氢间的化学键有什么区别?
物质 形成化学键的微粒 化学键类型
水
氢气
氯化钾
氯化铵
共价键的分类
结
极性共价键(极性键):由不同种非金属元素形成的化学键
例如:氮气中的氮氮键,氢气中的氢氢键都属于非极性键
例如:氯化氢中的氢氯键,水分子中的氢氧键都属于极性键
非极性共价键(非极性键):由同种非金属元素形成的化学键
电子对不偏移
电子对偏向Cl
练
学以致用
练习1、下列各数值表示有关元素的原子序数,其所表示的各原子组中能以
离子键相互结合成稳定化合物的是( )
A.10与12 B.8与17 C. 11与17 D.6与14
练习2、下列说法正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属原子之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.钠离子与氯离子通过离子键结合形成氯化钠
D
C
练
学以致用
练习3、下列物质中,只含有非极性共价键的是( )
A、 NaBr B、NaCl C、 Br2 D、 H2S
练习4、下列物质中,含有极性共价键的是( )
A、I2 B、MgCl2 C、 NaOH D、 H2O
C
CD
化学键
离子键
阴阳离子通过静电作用
共价键
通过共用电子对
化学变化的实质
旧键断裂,新键生成
极性共价键
非极性共价键
结
课堂小结
课标新卷:P19页
练
第一节
化学键与化学反应
学
探
探究活动
1、老师给每个小组准备了若干个氢原子和氧原子的模型,
请相互讨论,试着用氧原子和氢原子的模型不借
助任何工具拼接出水分子。
拼接不成,原子之间没有能使它们结合在一起的作用力。
2、老师给每个小组发放几个链接原子的细铁棍,再试一次。
每个小组都拼接出水分子的模型。
[结论]:原子要构成物质,必须有一种能使它们彼此结合在一起的作用。
一、化学键:
1、定义:相邻原子间强相互作用
化学键与物质变化
注意:化学键存在在分子内
思
化学键是一种较强的相互作用
(包括吸引和排斥达到平衡)
探
探究活动
同学们已经知道水在通电条件下可以分解,生成氢气和氧气,
请同学们利用水分子的模型还原此过程,小组间讨论该反应
中断裂的是什么键?新生成了什么键?并思考总结化学反应
中物质变化的实质是什么?
H2O
H2O
H2
H2
O2
2、化学反应的实质:旧化学键的断裂和新化学键的生成
思
化学键与物质变化
讨
化学键与物质变化
[小组思考交流讨论]
1、构成单质分子的粒子一定含有化学键吗?
2、氯化钠的熔化、氯化氢的溶解是否是化学变化?
3、石墨在一定条件下转化为金刚石是否是化学变化?
惰性气体单质中不存在化学键
同素异形体的转化属于化学变化
物质的溶解及熔化都属于物理变化
钠可以在氯气中燃烧生成氯化钠,氢气在氯气中燃烧生成氯化氢,氯化
氢分子存在着氢原子和氯原子形成的化学键,氯化钠固体中也存在化
学键,但是两者中的化学键是否相同?
思
化学键的分类
讨
化学键的分类
阅读教材p33-34的内容,结合化学反应的实质,根
据核外电子排布规律,小组讨论以下问题,并从成
键原因、成键元素、成键作用力三个方面比较NaCl和
HCl的形成过程,思考什么是离子键?什么是共价键?
1、画出Na、Cl和H的原子结构示意图
2、Na、Cl和H的原子结构是否稳定?
3、NaCl是怎样形成的?
4、HCl分子是怎样形成的?
失 e-
得 e-
静电作用
Na+
Cl-
讨
氯化钠的形成过程
通过共用电子对
讨
氯化氢的形成过程
结
想形成稳定结构
Na+和Cl-
H和Cl
静电作用
共用电子对相互作用
离子键:阴、阳离子间通过静电作用形成的化学键
共价键:原子间通过共用电子对形成的化学键
化学键的分类
NaCl HCl
成键原因
成键微粒
成键作用力
结
离子键、共价键比较
离子键、共价键的比较
想形成稳定结构
静电作用
共用电子对相互作用
阴阳离子
原子
活泼金属元素(IA、IIA)和活泼非金属元素(VIA、VIIA)
非金属元素
离子键 共价键
成键原因
成键方式
成键微粒
成键元素
讨
共价键的分类
1、通过什么判断化学键的类型?
2、是不是非金属元素间形成的化学键都是共价键?
3、是不是只有不同非金属间才能形成共价键?
交流研讨
下表给出的都是你熟悉的物质,请利用化学键的知识
分析它们的构成情况,并思考下面的问题
形成化化学键的微粒
否,铵盐间的化学键为离子键
否,相同非金属间也可以形成共价键
氢原子和氧原子
氢原子和氢原子
钾离子和氯离子
铵根离子和氯离子
共价键
共价键
离子键
离子键
4、氢气和氯化氢间的化学键有什么区别?
物质 形成化学键的微粒 化学键类型
水
氢气
氯化钾
氯化铵
共价键的分类
结
极性共价键(极性键):由不同种非金属元素形成的化学键
例如:氮气中的氮氮键,氢气中的氢氢键都属于非极性键
例如:氯化氢中的氢氯键,水分子中的氢氧键都属于极性键
非极性共价键(非极性键):由同种非金属元素形成的化学键
电子对不偏移
电子对偏向Cl
练
学以致用
练习1、下列各数值表示有关元素的原子序数,其所表示的各原子组中能以
离子键相互结合成稳定化合物的是( )
A.10与12 B.8与17 C. 11与17 D.6与14
练习2、下列说法正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属原子之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.钠离子与氯离子通过离子键结合形成氯化钠
D
C
练
学以致用
练习3、下列物质中,只含有非极性共价键的是( )
A、 NaBr B、NaCl C、 Br2 D、 H2S
练习4、下列物质中,含有极性共价键的是( )
A、I2 B、MgCl2 C、 NaOH D、 H2O
C
CD
化学键
离子键
阴阳离子通过静电作用
共价键
通过共用电子对
化学变化的实质
旧键断裂,新键生成
极性共价键
非极性共价键
结
课堂小结
课标新卷:P19页
练
