鲁科版高一化学必修2第3章第1节认识有机化合物(共26张PPT)
文档属性
| 名称 | 鲁科版高一化学必修2第3章第1节认识有机化合物(共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-11 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
轮胎橡胶
家用电器的外壳
煤油、汽油
生活中常见的有机物
纤维素
燃料: 汽油、煤油、柴油
建材: 木材、黏结剂、涂料、油漆
日用品: 塑料、橡胶、纤维、清洁剂
食物: 糖类、油脂、蛋白质
有机化合物种类繁多(超过2000万种),分布广泛,在人类的生活及生产中发挥重要作用。
丰富多彩的有机化合物
第3章 重要的有机化合物
第1节 认识有机化合物
学习目标
1. 认识什么是有机物
有机物与有机化学
1、定义:
2、组成元素:
大多数含有碳元素的化合物为有机物。
碳、氢、氧、氮、硫、磷、卤素等
除CO、CO2、H2CO3及其盐、氢氰酸(HCN)及其盐、硫氰酸(HSCN) 、氰酸(HCNO)及其盐、金属碳化物等以外的其它含碳化合物。
主要元素
其他元素
3、研究有机物的组成、结构、性质、制备方法与应用的科学叫。
有机化学
Organic compound
1、有机物
里程碑
1828年,德国化学家维勒(F.Wohler)用无机化合物氰酸铵(NH4CNO)合成出有机化合物——尿素[CO(NH2)2],由此突破了无机化合物与有机化合物之间的界限,第一次实现了通过无机物人工合成有机物,成为有机合成史上的里程碑。
典例1、下列说法正确的是
A 有机物只能从有机体中获取而不能利用无机物来合成
B 有机物是在动植物体内提取的有生命的化合物
C 大多数有机物是共价化合物,它们不具备无机物的性质
D 有机物有的不溶于水,有的可溶于水
一、 最简单的有机化合物-甲烷
走进有机化学,探索有机世界的奥秘,从学习甲烷开始!
甲烷的分子构成和空间结构
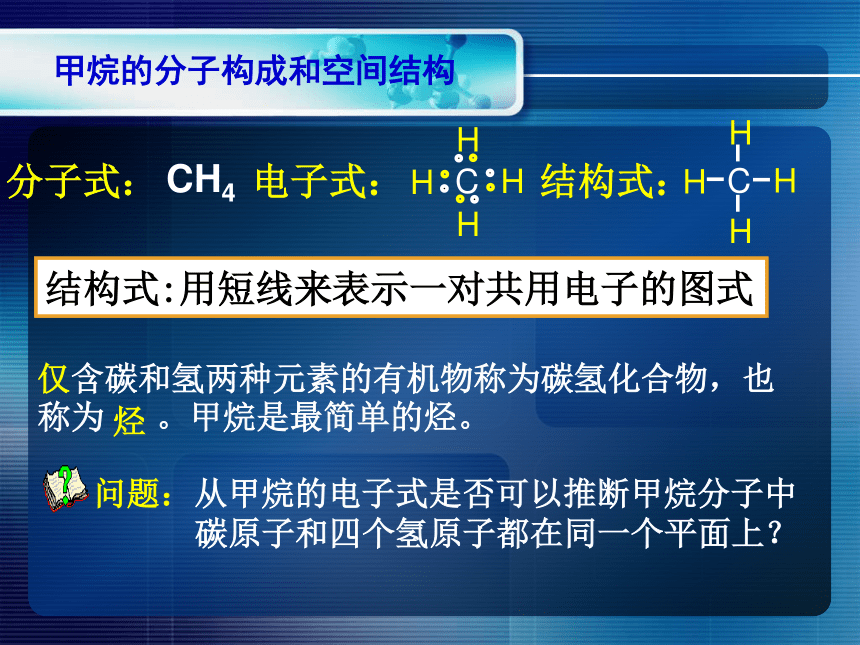
分子式:
电子式:
结构式:
CH4
结构式:用短线来表示一对共用电子的图式
仅含碳和氢两种元素的有机物称为碳氢化合物,也称为 。甲烷是最简单的烃。
烃
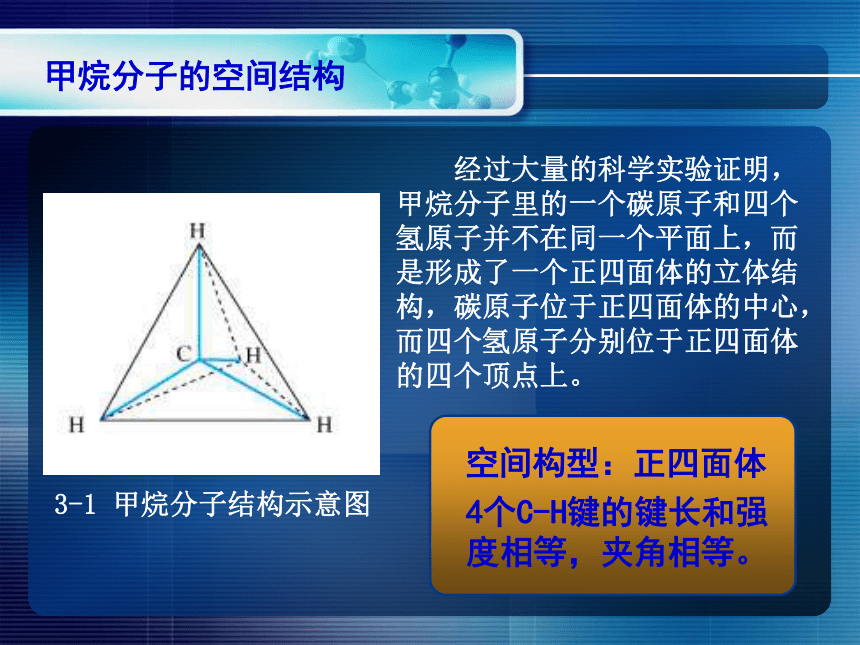
甲烷分子的空间结构
经过大量的科学实验证明,甲烷分子里的一个碳原子和四个氢原子并不在同一个平面上,而是形成了一个正四面体的立体结构,碳原子位于正四面体的中心,而四个氢原子分别位于正四面体的四个顶点上。
空间构型:正四面体
4个C-H键的键长和强度相等,夹角相等。
甲烷的分子模型
紫球表示碳原子,蓝球表
示氢原子,短棍表示价键
用紫球和蓝球的体积比来大体
上表示碳原子和氢原子的体积比
甲烷是池沼底部产生的沼气和煤矿的坑道所产生的气体的主要成分。这些甲烷都是在隔绝空气的情况下,由植物残体经过微生物发酵的作用而生成的。
甲烷在自然界的存在
甲烷的物理性质
1、在通常状况下,甲烷是一种无色、无气味的气体。
根据上述甲烷的物理性质,你知道如何收集甲烷吗?
甲烷的收集方法:
1、由于甲烷密度比空气小,所以能用瓶口向下排空气法收集。
2、由于甲烷难溶于水,所以能用排水法收集。
3、极难溶解于水。
2、密度比空气小,在标准状况下,是0.717g/L。
课堂练习
下列物质属于有机物的是____________,属于烃的是_________________
H2S (B) C2H2 (C) CH3Cl
(D) C2H5OH (E) CH4 (F) HCN
(G) 金刚石 (H)CH3COOH (I) CO2
(J) C2H4
(B)
(E)
(J)
(B)
(C)
(D)
(E)
(H)
(J)
甲烷的化学性质——稳定性
在通常情况下,甲烷性质比较 ,与 、 、 一般不发生化学反应。
问题:
能不能与酸性高锰酸钾溶液反应?
结论:
甲烷不能使酸性高锰酸钾溶液褪色
稳定
强酸
强碱
强氧化剂
甲烷的化学性质——可燃性
1.甲烷的氧化反应
实验:把甲烷经导管通出点燃, 观察火焰颜色,然后用一个冷而干燥的烧杯罩在火焰上方,取下烧杯正放,向烧杯内滴入澄清的石灰水?。?
实验视频
甲烷中
含氢元素
甲烷中
含碳元素
甲烷易燃
现象与结论
安静燃烧,火焰明亮呈淡蓝色
烧杯内壁有水珠
澄清石灰水变浑浊
实验步骤 实验现象 实验结论
1. 点燃
纯净的甲烷
2.在火焰的上方罩干燥洁净的烧杯
3、向反应后的烧杯中注入澄清的石灰水
想一想:
怎么用最简单的方法把
甲烷和氢气区分开?
能不能用该法推出甲烷就是由C,H 两种元素组成的.
煤矿安全措施:
1、建立良好的通风系统和监测系统,保证甲烷含量不在爆炸极限内
2、严禁明火、电火花等
点燃甲烷和空气的混合气体会有什么后果呢?
科学探究
取一支大试管,用排饱和食盐水的方法收集体积比为1:4的甲烷和氯气,用橡皮塞塞好管口,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸)。一定时间后,将试管倒立于水槽中并取下试管口的橡皮塞,观察实验现象。
1.你从实验中得到哪些信息?
2.从所得的实验信息中你能得到哪些启示?
甲烷的取代反应
实验视频
V(甲烷)∶V(氯气)
=1∶4的试管
漫射日光照射
①黄绿色变浅 ②试管内壁有少量油状物生成
氯气参加反应,有新液体有机物生成
把试管倒立在盛满水的水槽中,取下橡皮塞
取试管中的水少许,滴入蓝色石蕊试液
③试管中液面不断上升
反应使气体量减少或者有溶于水的气体生成导致试管中压强减小
石蕊试液变红
反应中有HCl生成
现象与结论
实验步骤 实验现象 实验结论
甲烷的取代反应的历程
1.一氯甲烷的形成
动画演示
光照下甲烷与氯气发生取代反应
1、下列反应属于取代反应的是
A. 2KI + Cl2 == 2KCl + I2
B.(NH4)2SO4+BaCl2==BaSO4↓+2NH4Cl
C.CH2Cl2+Cl2 CHCl3+HCl
D.CH4 C+2H2
2、在光照条件下,将等物质的量的CH4和Cl2充分反应,得到产物的物质的量最多的是
A. CH3Cl B. CH2Cl2 C. CCl4 D. HCl
小试身手
三、甲烷的化学性质
①稳定性
②氧化反应
③取代反应
二、甲烷的物理性质
一、甲烷分子的构成和空间结构
整理小结
高考链接
轮胎橡胶
家用电器的外壳
煤油、汽油
生活中常见的有机物
纤维素
燃料: 汽油、煤油、柴油
建材: 木材、黏结剂、涂料、油漆
日用品: 塑料、橡胶、纤维、清洁剂
食物: 糖类、油脂、蛋白质
有机化合物种类繁多(超过2000万种),分布广泛,在人类的生活及生产中发挥重要作用。
丰富多彩的有机化合物
第3章 重要的有机化合物
第1节 认识有机化合物
学习目标
1. 认识什么是有机物
有机物与有机化学
1、定义:
2、组成元素:
大多数含有碳元素的化合物为有机物。
碳、氢、氧、氮、硫、磷、卤素等
除CO、CO2、H2CO3及其盐、氢氰酸(HCN)及其盐、硫氰酸(HSCN) 、氰酸(HCNO)及其盐、金属碳化物等以外的其它含碳化合物。
主要元素
其他元素
3、研究有机物的组成、结构、性质、制备方法与应用的科学叫。
有机化学
Organic compound
1、有机物
里程碑
1828年,德国化学家维勒(F.Wohler)用无机化合物氰酸铵(NH4CNO)合成出有机化合物——尿素[CO(NH2)2],由此突破了无机化合物与有机化合物之间的界限,第一次实现了通过无机物人工合成有机物,成为有机合成史上的里程碑。
典例1、下列说法正确的是
A 有机物只能从有机体中获取而不能利用无机物来合成
B 有机物是在动植物体内提取的有生命的化合物
C 大多数有机物是共价化合物,它们不具备无机物的性质
D 有机物有的不溶于水,有的可溶于水
一、 最简单的有机化合物-甲烷
走进有机化学,探索有机世界的奥秘,从学习甲烷开始!
甲烷的分子构成和空间结构
分子式:
电子式:
结构式:
CH4
结构式:用短线来表示一对共用电子的图式
仅含碳和氢两种元素的有机物称为碳氢化合物,也称为 。甲烷是最简单的烃。
烃
甲烷分子的空间结构
经过大量的科学实验证明,甲烷分子里的一个碳原子和四个氢原子并不在同一个平面上,而是形成了一个正四面体的立体结构,碳原子位于正四面体的中心,而四个氢原子分别位于正四面体的四个顶点上。
空间构型:正四面体
4个C-H键的键长和强度相等,夹角相等。
甲烷的分子模型
紫球表示碳原子,蓝球表
示氢原子,短棍表示价键
用紫球和蓝球的体积比来大体
上表示碳原子和氢原子的体积比
甲烷是池沼底部产生的沼气和煤矿的坑道所产生的气体的主要成分。这些甲烷都是在隔绝空气的情况下,由植物残体经过微生物发酵的作用而生成的。
甲烷在自然界的存在
甲烷的物理性质
1、在通常状况下,甲烷是一种无色、无气味的气体。
根据上述甲烷的物理性质,你知道如何收集甲烷吗?
甲烷的收集方法:
1、由于甲烷密度比空气小,所以能用瓶口向下排空气法收集。
2、由于甲烷难溶于水,所以能用排水法收集。
3、极难溶解于水。
2、密度比空气小,在标准状况下,是0.717g/L。
课堂练习
下列物质属于有机物的是____________,属于烃的是_________________
H2S (B) C2H2 (C) CH3Cl
(D) C2H5OH (E) CH4 (F) HCN
(G) 金刚石 (H)CH3COOH (I) CO2
(J) C2H4
(B)
(E)
(J)
(B)
(C)
(D)
(E)
(H)
(J)
甲烷的化学性质——稳定性
在通常情况下,甲烷性质比较 ,与 、 、 一般不发生化学反应。
问题:
能不能与酸性高锰酸钾溶液反应?
结论:
甲烷不能使酸性高锰酸钾溶液褪色
稳定
强酸
强碱
强氧化剂
甲烷的化学性质——可燃性
1.甲烷的氧化反应
实验:把甲烷经导管通出点燃, 观察火焰颜色,然后用一个冷而干燥的烧杯罩在火焰上方,取下烧杯正放,向烧杯内滴入澄清的石灰水?。?
实验视频
甲烷中
含氢元素
甲烷中
含碳元素
甲烷易燃
现象与结论
安静燃烧,火焰明亮呈淡蓝色
烧杯内壁有水珠
澄清石灰水变浑浊
实验步骤 实验现象 实验结论
1. 点燃
纯净的甲烷
2.在火焰的上方罩干燥洁净的烧杯
3、向反应后的烧杯中注入澄清的石灰水
想一想:
怎么用最简单的方法把
甲烷和氢气区分开?
能不能用该法推出甲烷就是由C,H 两种元素组成的.
煤矿安全措施:
1、建立良好的通风系统和监测系统,保证甲烷含量不在爆炸极限内
2、严禁明火、电火花等
点燃甲烷和空气的混合气体会有什么后果呢?
科学探究
取一支大试管,用排饱和食盐水的方法收集体积比为1:4的甲烷和氯气,用橡皮塞塞好管口,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸)。一定时间后,将试管倒立于水槽中并取下试管口的橡皮塞,观察实验现象。
1.你从实验中得到哪些信息?
2.从所得的实验信息中你能得到哪些启示?
甲烷的取代反应
实验视频
V(甲烷)∶V(氯气)
=1∶4的试管
漫射日光照射
①黄绿色变浅 ②试管内壁有少量油状物生成
氯气参加反应,有新液体有机物生成
把试管倒立在盛满水的水槽中,取下橡皮塞
取试管中的水少许,滴入蓝色石蕊试液
③试管中液面不断上升
反应使气体量减少或者有溶于水的气体生成导致试管中压强减小
石蕊试液变红
反应中有HCl生成
现象与结论
实验步骤 实验现象 实验结论
甲烷的取代反应的历程
1.一氯甲烷的形成
动画演示
光照下甲烷与氯气发生取代反应
1、下列反应属于取代反应的是
A. 2KI + Cl2 == 2KCl + I2
B.(NH4)2SO4+BaCl2==BaSO4↓+2NH4Cl
C.CH2Cl2+Cl2 CHCl3+HCl
D.CH4 C+2H2
2、在光照条件下,将等物质的量的CH4和Cl2充分反应,得到产物的物质的量最多的是
A. CH3Cl B. CH2Cl2 C. CCl4 D. HCl
小试身手
三、甲烷的化学性质
①稳定性
②氧化反应
③取代反应
二、甲烷的物理性质
一、甲烷分子的构成和空间结构
整理小结
高考链接
