第6章 溶解现象 复习课件(34张PPT)
文档属性
| 名称 | 第6章 溶解现象 复习课件(34张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 10.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-07 00:00:00 | ||
图片预览









文档简介
(共34张PPT)
溶解现象
复习
一、溶液的特征
均一性
稳定性
二、水溶液的某些性质
少量的固体物质溶于水,使稀溶液的
升高
(高于100℃),
降低(低于0℃)。
沸腾温度
凝固温度
溶液具有
导电性
混合物
部分
三、溶液的组成
溶液由溶质和溶剂组成。
溶液质量
=
溶质质量
+
溶剂质量
四、溶解现象
物质溶解于水的过程中通常伴随热量的变化
氢氧化钠固体溶于水放热,使溶液温度升高;
硝酸铵固体溶于水吸热,使溶液温度降低。
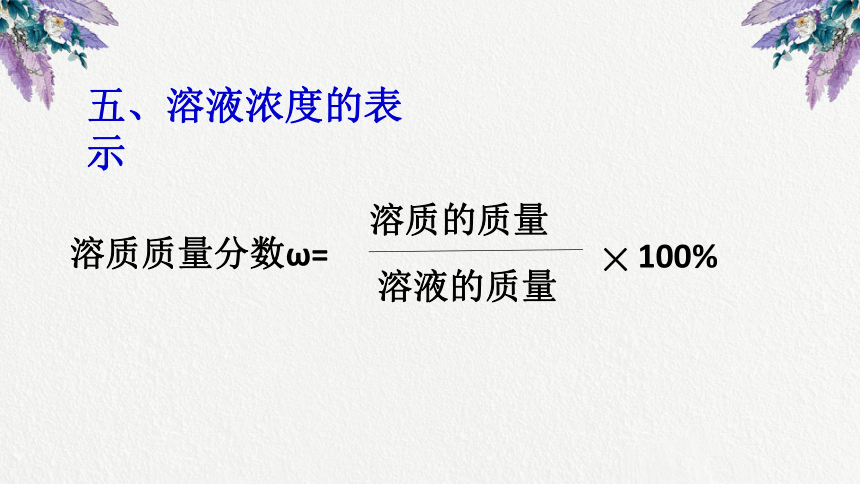
五、溶液浓度的表示
不饱和溶液
饱和溶液
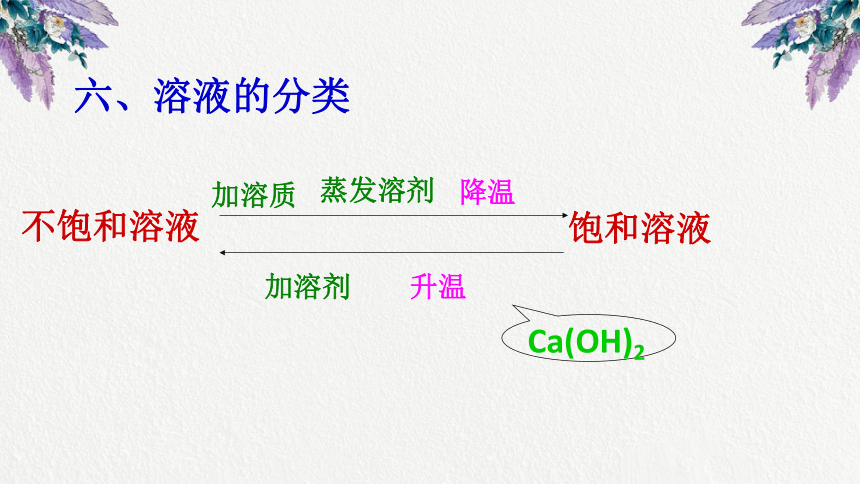
六、溶液的分类
加溶质
蒸发溶剂
降温
加溶剂
升温
情境一
稀溶液的沸腾温度升高
稀溶液的凝固温度降低
情境二
物质溶解于水的过程中通常伴随热量的变化
硝酸铵NH4NO3
氢氧化钠NaOH
食盐NaCl
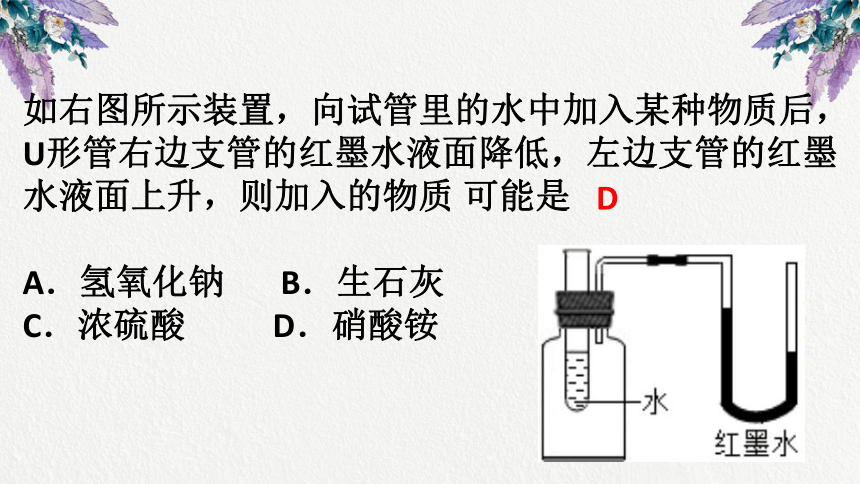
如右图所示装置,向试管里的水中加入某种物质后,
U形管右边支管的红墨水液面降低,左边支管的红墨
水液面上升,则加入的物质
可能是
A.氢氧化钠
B.生石灰
C.浓硫酸
D.硝酸铵
D
情境三
油难溶于水,但如果在油与水的混合物中加入一些洗洁精,震荡后,油能以很小的液滴的形式悬浮在水中形成乳浊液,这种现象称为
。
乳化
人们把能促使两种互不相溶的液体形成稳定乳浊液的物质叫
。
乳化剂
汽油
情境四
海带提碘是中国工业碘的主要来源之一,而提碘工艺中有一个重要步骤就是加某种有机溶剂,将碘富集起来。
为什么加有机溶剂,而不用水呢?
中考链接
【2017苏州中考】
为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所用汽油与KMnO4、碘均不发生化学反应)
【实验l】KMnO4晶体在不同溶剂中的溶解实验
根据实验步骤、实验操作图示填写相关实验现象。
紫红
实验步骤
实验操作图示
实验操作及现象
步骤1
振荡后静置:
(1)A试管中晶体全部溶解,溶液呈________色;B试管中晶体不溶解,汽油不变色。
液体分层,上层为无色,下层为紫红色,试管底部无固体残留
步骤2
将步骤1中A试管内溶液倒人B试管中,振荡后静置:(2)B试管中观察到的现象为__________。
【实验2】碘在不同溶剂中的溶解实验
微
碘的汽油溶液
强
实验操作图示
实验结论或解释
(3)由图2所示现象可知:碘_____(选填“不”、“微”或“易”)溶于水
(4)图3所示试管中液体分层。上层紫红色溶液的名称是________。说明碘在汽油中的溶解性比在水中_____(选填“强”或“弱”)
【反思与应用】
(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体______(选填“分层”或“不分层”)。
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2】中第二步操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是________。
不分层
碘在这种液体中的溶解度远大于在水中的溶解度
与水不互溶
情境五
配制一定溶质质量分数的溶液
中考链接
【2016苏州中考】
“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500g溶质质量分数为0.9%的生理盐水,需要氯化钠固体___________g。
下列实验操作与目的分析均正确的一组_________(填序号).
4.5
√
×
×
×
项目
实验操作
目的分析
A
称量时,将取出的过量氯化钠放回原瓶
节约药品
B
溶解氯化钠时用玻璃棒搅拌
增大氯化钠的溶解度
C
称取氯化钠时,在天平两边托盘上放一张质量相等的纸
整洁美观
D
量取所需水时,视线与量筒液体凹液面的最低处保持水平
准确读数
(2)实验室若用15%的氯化钠溶液加水稀释成500g6%的氯化钠溶液,需要15%的氯化钠溶液________g。加入水的质量
胶头滴管
200
溶质质量不变
m(浓)ω(浓)
=
m(稀)ω(稀)
m(加水)
=
m(稀)
-
m(浓)
此时需要用到的玻璃仪器有:烧杯、玻璃棒,量筒和___
300g
(3)实验室若用恒温蒸发的方法将l5%的氯化钠溶液变成饱和溶液.其过程如下图所示。
与丙烧杯中溶液溶质量分数一定相同的是_______烧杯中的溶液(填序号)。
丁
【2015苏州中考】
若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足生产的需要,可采用的最简便的方法是?
已知:20℃时氯化钠的溶解度为36g。
我国青海湖地区有一种说法,冬天捞碱,夏天晒盐。这里碱是指碳酸钠,盐是指氯化钠
情境六
结晶
在一定条件下,从溶液中析出晶体的过程称为结晶。
情境七
结晶的方法:
冷却结晶
(适用于“缓升型”)如食盐
(适用于“陡升型”)如硝酸钾
蒸发结晶
【2015苏州中考】
若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足生产的需要,可采用的最简便的方法是?
已知:20℃时氯化钠的溶解度为36g。
【2014苏州中考】
某温度下饱和氯化钠溶液的溶质质量分数为26%,试列式计算该温度下氯化钠的溶解度S(计算结果保留小数点后一位).
溶解度
定义
在一定温度下,物质(固体)在100g溶剂中达到饱和状态时所溶解的质量。
溶解度曲线
用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要15%的氯化钠溶液 _________ g.
200
【2014苏州中考】
影响物质溶解性的因素
溶质性质
溶剂性质
温度
溶解现象
复习
一、溶液的特征
均一性
稳定性
二、水溶液的某些性质
少量的固体物质溶于水,使稀溶液的
升高
(高于100℃),
降低(低于0℃)。
沸腾温度
凝固温度
溶液具有
导电性
混合物
部分
三、溶液的组成
溶液由溶质和溶剂组成。
溶液质量
=
溶质质量
+
溶剂质量
四、溶解现象
物质溶解于水的过程中通常伴随热量的变化
氢氧化钠固体溶于水放热,使溶液温度升高;
硝酸铵固体溶于水吸热,使溶液温度降低。
五、溶液浓度的表示
不饱和溶液
饱和溶液
六、溶液的分类
加溶质
蒸发溶剂
降温
加溶剂
升温
情境一
稀溶液的沸腾温度升高
稀溶液的凝固温度降低
情境二
物质溶解于水的过程中通常伴随热量的变化
硝酸铵NH4NO3
氢氧化钠NaOH
食盐NaCl
如右图所示装置,向试管里的水中加入某种物质后,
U形管右边支管的红墨水液面降低,左边支管的红墨
水液面上升,则加入的物质
可能是
A.氢氧化钠
B.生石灰
C.浓硫酸
D.硝酸铵
D
情境三
油难溶于水,但如果在油与水的混合物中加入一些洗洁精,震荡后,油能以很小的液滴的形式悬浮在水中形成乳浊液,这种现象称为
。
乳化
人们把能促使两种互不相溶的液体形成稳定乳浊液的物质叫
。
乳化剂
汽油
情境四
海带提碘是中国工业碘的主要来源之一,而提碘工艺中有一个重要步骤就是加某种有机溶剂,将碘富集起来。
为什么加有机溶剂,而不用水呢?
中考链接
【2017苏州中考】
为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所用汽油与KMnO4、碘均不发生化学反应)
【实验l】KMnO4晶体在不同溶剂中的溶解实验
根据实验步骤、实验操作图示填写相关实验现象。
紫红
实验步骤
实验操作图示
实验操作及现象
步骤1
振荡后静置:
(1)A试管中晶体全部溶解,溶液呈________色;B试管中晶体不溶解,汽油不变色。
液体分层,上层为无色,下层为紫红色,试管底部无固体残留
步骤2
将步骤1中A试管内溶液倒人B试管中,振荡后静置:(2)B试管中观察到的现象为__________。
【实验2】碘在不同溶剂中的溶解实验
微
碘的汽油溶液
强
实验操作图示
实验结论或解释
(3)由图2所示现象可知:碘_____(选填“不”、“微”或“易”)溶于水
(4)图3所示试管中液体分层。上层紫红色溶液的名称是________。说明碘在汽油中的溶解性比在水中_____(选填“强”或“弱”)
【反思与应用】
(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体______(选填“分层”或“不分层”)。
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2】中第二步操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是________。
不分层
碘在这种液体中的溶解度远大于在水中的溶解度
与水不互溶
情境五
配制一定溶质质量分数的溶液
中考链接
【2016苏州中考】
“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500g溶质质量分数为0.9%的生理盐水,需要氯化钠固体___________g。
下列实验操作与目的分析均正确的一组_________(填序号).
4.5
√
×
×
×
项目
实验操作
目的分析
A
称量时,将取出的过量氯化钠放回原瓶
节约药品
B
溶解氯化钠时用玻璃棒搅拌
增大氯化钠的溶解度
C
称取氯化钠时,在天平两边托盘上放一张质量相等的纸
整洁美观
D
量取所需水时,视线与量筒液体凹液面的最低处保持水平
准确读数
(2)实验室若用15%的氯化钠溶液加水稀释成500g6%的氯化钠溶液,需要15%的氯化钠溶液________g。加入水的质量
胶头滴管
200
溶质质量不变
m(浓)ω(浓)
=
m(稀)ω(稀)
m(加水)
=
m(稀)
-
m(浓)
此时需要用到的玻璃仪器有:烧杯、玻璃棒,量筒和___
300g
(3)实验室若用恒温蒸发的方法将l5%的氯化钠溶液变成饱和溶液.其过程如下图所示。
与丙烧杯中溶液溶质量分数一定相同的是_______烧杯中的溶液(填序号)。
丁
【2015苏州中考】
若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足生产的需要,可采用的最简便的方法是?
已知:20℃时氯化钠的溶解度为36g。
我国青海湖地区有一种说法,冬天捞碱,夏天晒盐。这里碱是指碳酸钠,盐是指氯化钠
情境六
结晶
在一定条件下,从溶液中析出晶体的过程称为结晶。
情境七
结晶的方法:
冷却结晶
(适用于“缓升型”)如食盐
(适用于“陡升型”)如硝酸钾
蒸发结晶
【2015苏州中考】
若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足生产的需要,可采用的最简便的方法是?
已知:20℃时氯化钠的溶解度为36g。
【2014苏州中考】
某温度下饱和氯化钠溶液的溶质质量分数为26%,试列式计算该温度下氯化钠的溶解度S(计算结果保留小数点后一位).
溶解度
定义
在一定温度下,物质(固体)在100g溶剂中达到饱和状态时所溶解的质量。
溶解度曲线
用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要15%的氯化钠溶液 _________ g.
200
【2014苏州中考】
影响物质溶解性的因素
溶质性质
溶剂性质
温度
