第3节 原子结构的模型 第2课时(课件 22张ppt)
文档属性
| 名称 | 第3节 原子结构的模型 第2课时(课件 22张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-02-13 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
原子结构的模型
第二课时
第三节
原子种类
核电荷数
质子数
中子数
核外电子数
氢原子
1
1
0
1
氦原子
2
2
2
2
碳原子
6
6
8
6
氮原子
7
7
7
7
铝原子
13
13
14
13
硫原子
16
16
17
16
氯原子
17
17
20
17
铁原子
26
26
30
26
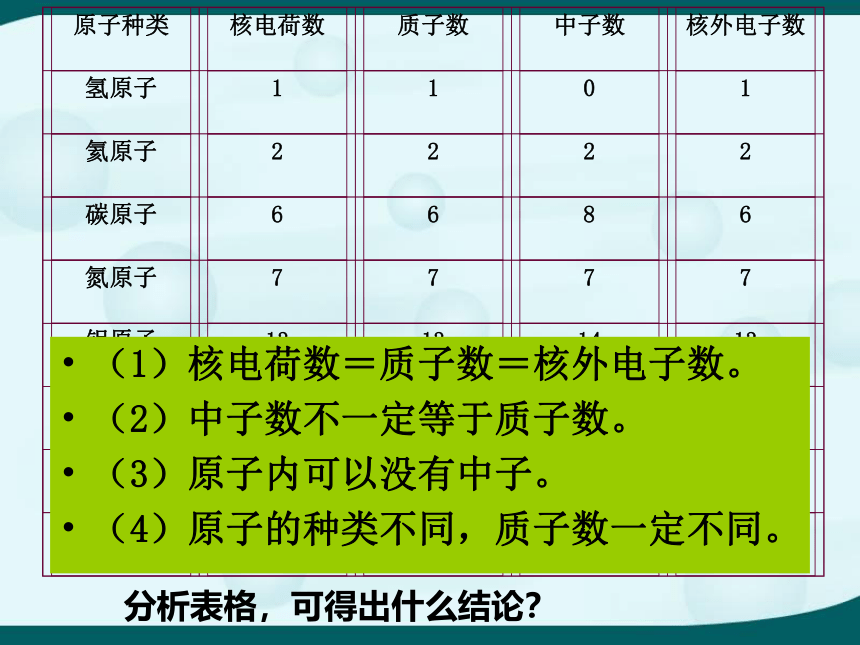
分析表格,可得出什么结论?
(1)核电荷数=质子数=核外电子数。
(2)中子数不一定等于质子数。
(3)原子内可以没有中子。
(4)原子的种类不同,质子数一定不同。
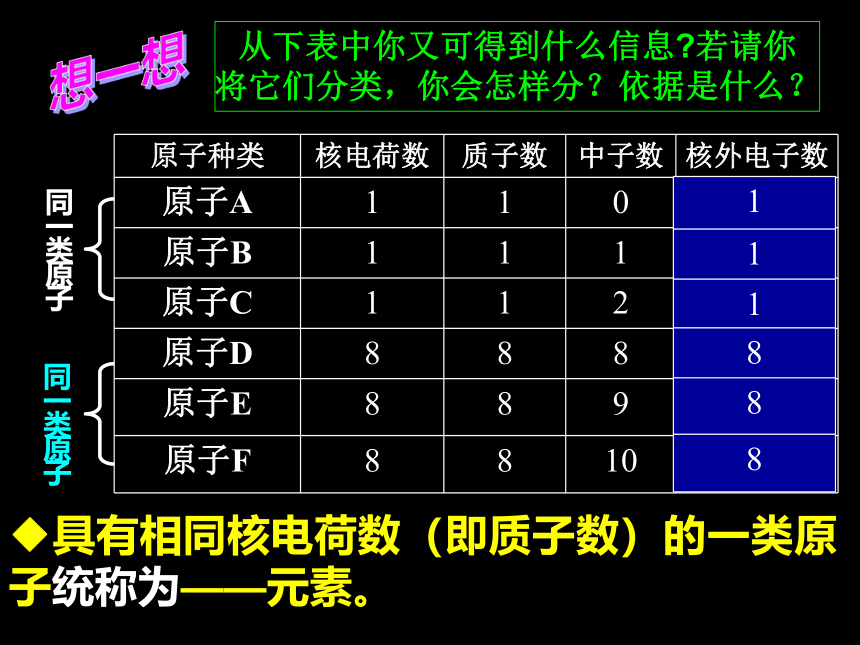
从下表中你又可得到什么信息?若请你将它们分类,你会怎样分?依据是什么?
原子种类
核电荷数
质子数
中子数
核外电子数
原子A
1
1
0
?
原子B
1
1
1
?
原子C
1
1
2
?
原子D
8
8
8
?
原子E
8
8
9
?
原子F
8
8
10
?
◆具有相同核电荷数(即质子数)的一类原子统称为——元素。
1
1
1
8
8
8
同一类原子
同一类原子
例如:我们把质子数为8的氧原子总称为氧元素。氧分子、二氧化碳分子、水分子中都有氧原子,且氧原子原子核内都有8个质子,属于同种
元素---氧元素。
元素的种类由原子中的核电荷数(质子数)决定。
2、元素的特征:
读图:
(1)A原子核中有___个质子,
___个中子。
(2)B原子核中有
___个质子,___个中子。
(3)C原子核中有___个质子,____个中子。·
8
8
8
9
8
10
他们是同一种元素吗?这三个原子完全一样?
是同一元素,因为质子数相同,都是氧元素
他们不一样,因为中子数不同
3、原子中原子核内质子数相同、中子数不相同的同类原子互为同位素(原子)。
如原子核内质子数是8个的所有原子(不管中子数是多少)都是氧原子,都是氧元素的同位素原子。
元素与同位素的区别:
元素是同位素的总称,
同位素是一种元素的不同种原子。
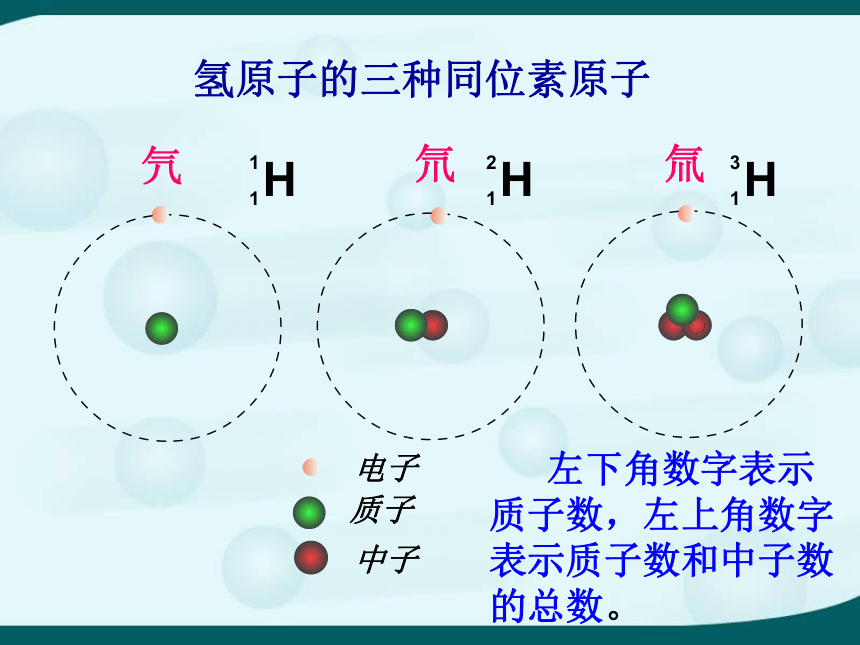
H
1
1
H
2
1
H
3
1
左下角数字表示质子数,左上角数字表示质子数和中子数的总数。
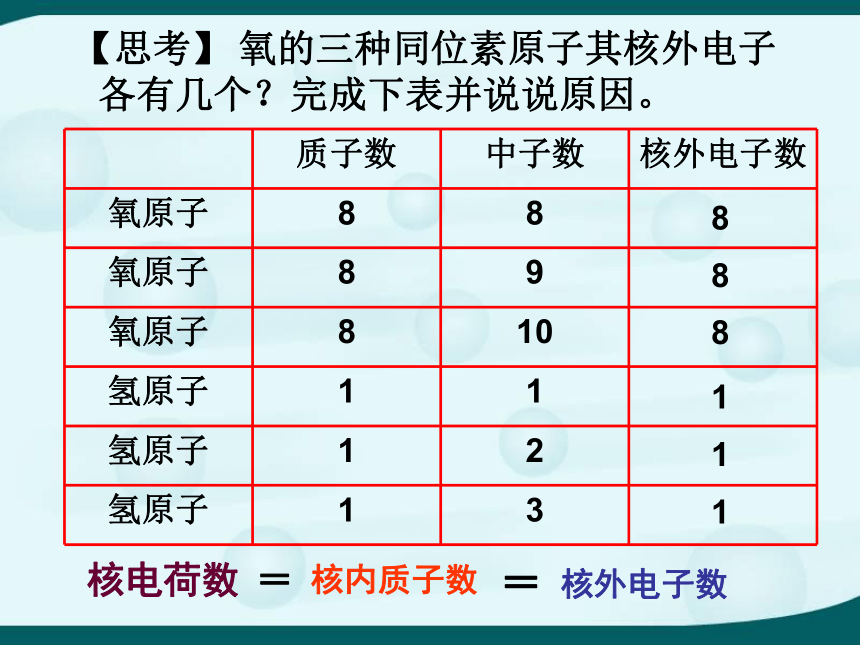
【思考】
氧的三种同位素原子其核外电子各有几个?完成下表并说说原因。
质子数
中子数
核外电子数
氧原子
8
8
氧原子
8
9
氧原子
8
10
氢原子
1
1
氢原子
1
2
氢原子
1
3
8
8
8
1
1
1
核内质子数
核外电子数
核电荷数
=
=
常见元素的同位素及其符号和用途
元素
同位素(符号)
用途
氢(H)
H、D、T
D、T制造氢弹的原料,D2O可作核反应堆中的中子减速剂
碳(C)
C
12
、C13、
C14
C12—原子量的标准
C14—考古学中测定年代
氧(O)
O
16
、O17、
O18
?
?
铀(U)
U234、U235、
U238
U235—制造原子弹和核反应堆的燃料
示踪
有些同位素具有放射性,叫做放射性同位素.用人工方法得到的放射性同位素已经在工农业、医疗卫生和和科学研究等许多方面得到了广泛的应用.
①.利用它的射线
医学诊断、检查金属内部有没有沙眼或裂纹等。α射线的电离作用很强,可以用来消除机器在运转中因摩擦而产生的有害静电.
②.利用它核反应放出巨大能量。例核潜艇、原子弹、氢弹。
③.利用它的示踪性。免疫研究、古董鉴定、测定年代、化学分析。
4、原子的同位素的应用
四、带电的原子——离子
取一瓶氯气,用镊子夹一小块钠放入燃烧匙中,点燃钠,将燃烧匙伸入氯气瓶中,反应结束后观察瓶内的物质。
【现象】
钠剧烈燃烧,产生白烟,反应结束后瓶内有白色固体。
钠原子失去一个电子成为一个带正电的微粒叫钠离子
氯原子得到一个电子成为一个带负电的微粒
叫氯离子
1.我们把带电的原子(或原子团)叫离子
2.离子也是构成物质的一种微粒。
3.构成物质微粒共有分子、原子、离子。
四、离子
阳离子:
带正电的原子或原子团。
阴离子:
带负电的原子或原子团。
1、氕、氘、氚三种原子具有相同的(
)
A、原子质量
B、原子核结构
C、核电荷数
D、中子数
C
2、
我国计划在2007年发射一颗绕月探测卫星,其任务之一是寻找一种新能源——氦3。氦3的原子核是由一个中子和两个质子构成的,其原子核外电子数为(
)
A、1
B、2
C、3
D、6
B
3.有两种原子,所含的质子数相同,下列说法正确的是
(
)
A.它们属于同种元素
B.它们属于不同种元素
C.它们属于同种原子
D.以上叙述都不对
4.氕、氘、氚三种原子的______相同,互为_________。
A
质子数
同位素原子
5.具有相同_________的同类原子总称为元素,铁钉、铁锈中都含有________。
6.元素的种类决定于原子的
(
)
A.中子数
B.质子数
C.相对原子质量
D.电子数
7.下列有关氯化钠的叙述正确的是
(
)
A.氯化钠由氯化钠分子构成
B.氯化钠由钠原子和氯原子构成
C.氯化钠由钠离子和氯离子构成
D.以上叙述都不对
核电荷数
铁元素
B
C
9.科学家制造出原子核内质子数为112的新原子,关于该新原子的下列叙述正确的是
(
)
A.其核内中子数为112
B.其核外电子数为112
C.原子带正电荷112个
D.以上都不对
10.下列叙述正确的是
(
)
A.二氧化碳是由碳和氧气组成的
B.1个二氧化碳分子是由2个氧原子和1个碳原子构成的
C.二氧化碳是由碳原子和氧原子组成的
D.二氧化碳分子是由2个氧原子和1个碳原子构成的
B
B
11.下列有关原子的说法正确的是
(
)
A.原子是不可再分的最小微粒
B.原子都是由质子、中子和电子构成的
C.原子的类别是由原子核内的质子数决定的
D.以上说法都不确切
12.下列叙述正确的是(
)
A、
属于同位素不同原子即其核电荷数相同但核外电子数不同。
B、
属于同位素不同原子即其核电荷数相同但中子数不同。
C、
属于同位素不同原子即其核外电子数相同但核电荷数不同。
D、属于同位素不同原子即其中子数相同但核外电子数不同。
C
B
原子结构的模型
第二课时
第三节
原子种类
核电荷数
质子数
中子数
核外电子数
氢原子
1
1
0
1
氦原子
2
2
2
2
碳原子
6
6
8
6
氮原子
7
7
7
7
铝原子
13
13
14
13
硫原子
16
16
17
16
氯原子
17
17
20
17
铁原子
26
26
30
26
分析表格,可得出什么结论?
(1)核电荷数=质子数=核外电子数。
(2)中子数不一定等于质子数。
(3)原子内可以没有中子。
(4)原子的种类不同,质子数一定不同。
从下表中你又可得到什么信息?若请你将它们分类,你会怎样分?依据是什么?
原子种类
核电荷数
质子数
中子数
核外电子数
原子A
1
1
0
?
原子B
1
1
1
?
原子C
1
1
2
?
原子D
8
8
8
?
原子E
8
8
9
?
原子F
8
8
10
?
◆具有相同核电荷数(即质子数)的一类原子统称为——元素。
1
1
1
8
8
8
同一类原子
同一类原子
例如:我们把质子数为8的氧原子总称为氧元素。氧分子、二氧化碳分子、水分子中都有氧原子,且氧原子原子核内都有8个质子,属于同种
元素---氧元素。
元素的种类由原子中的核电荷数(质子数)决定。
2、元素的特征:
读图:
(1)A原子核中有___个质子,
___个中子。
(2)B原子核中有
___个质子,___个中子。
(3)C原子核中有___个质子,____个中子。·
8
8
8
9
8
10
他们是同一种元素吗?这三个原子完全一样?
是同一元素,因为质子数相同,都是氧元素
他们不一样,因为中子数不同
3、原子中原子核内质子数相同、中子数不相同的同类原子互为同位素(原子)。
如原子核内质子数是8个的所有原子(不管中子数是多少)都是氧原子,都是氧元素的同位素原子。
元素与同位素的区别:
元素是同位素的总称,
同位素是一种元素的不同种原子。
H
1
1
H
2
1
H
3
1
左下角数字表示质子数,左上角数字表示质子数和中子数的总数。
【思考】
氧的三种同位素原子其核外电子各有几个?完成下表并说说原因。
质子数
中子数
核外电子数
氧原子
8
8
氧原子
8
9
氧原子
8
10
氢原子
1
1
氢原子
1
2
氢原子
1
3
8
8
8
1
1
1
核内质子数
核外电子数
核电荷数
=
=
常见元素的同位素及其符号和用途
元素
同位素(符号)
用途
氢(H)
H、D、T
D、T制造氢弹的原料,D2O可作核反应堆中的中子减速剂
碳(C)
C
12
、C13、
C14
C12—原子量的标准
C14—考古学中测定年代
氧(O)
O
16
、O17、
O18
?
?
铀(U)
U234、U235、
U238
U235—制造原子弹和核反应堆的燃料
示踪
有些同位素具有放射性,叫做放射性同位素.用人工方法得到的放射性同位素已经在工农业、医疗卫生和和科学研究等许多方面得到了广泛的应用.
①.利用它的射线
医学诊断、检查金属内部有没有沙眼或裂纹等。α射线的电离作用很强,可以用来消除机器在运转中因摩擦而产生的有害静电.
②.利用它核反应放出巨大能量。例核潜艇、原子弹、氢弹。
③.利用它的示踪性。免疫研究、古董鉴定、测定年代、化学分析。
4、原子的同位素的应用
四、带电的原子——离子
取一瓶氯气,用镊子夹一小块钠放入燃烧匙中,点燃钠,将燃烧匙伸入氯气瓶中,反应结束后观察瓶内的物质。
【现象】
钠剧烈燃烧,产生白烟,反应结束后瓶内有白色固体。
钠原子失去一个电子成为一个带正电的微粒叫钠离子
氯原子得到一个电子成为一个带负电的微粒
叫氯离子
1.我们把带电的原子(或原子团)叫离子
2.离子也是构成物质的一种微粒。
3.构成物质微粒共有分子、原子、离子。
四、离子
阳离子:
带正电的原子或原子团。
阴离子:
带负电的原子或原子团。
1、氕、氘、氚三种原子具有相同的(
)
A、原子质量
B、原子核结构
C、核电荷数
D、中子数
C
2、
我国计划在2007年发射一颗绕月探测卫星,其任务之一是寻找一种新能源——氦3。氦3的原子核是由一个中子和两个质子构成的,其原子核外电子数为(
)
A、1
B、2
C、3
D、6
B
3.有两种原子,所含的质子数相同,下列说法正确的是
(
)
A.它们属于同种元素
B.它们属于不同种元素
C.它们属于同种原子
D.以上叙述都不对
4.氕、氘、氚三种原子的______相同,互为_________。
A
质子数
同位素原子
5.具有相同_________的同类原子总称为元素,铁钉、铁锈中都含有________。
6.元素的种类决定于原子的
(
)
A.中子数
B.质子数
C.相对原子质量
D.电子数
7.下列有关氯化钠的叙述正确的是
(
)
A.氯化钠由氯化钠分子构成
B.氯化钠由钠原子和氯原子构成
C.氯化钠由钠离子和氯离子构成
D.以上叙述都不对
核电荷数
铁元素
B
C
9.科学家制造出原子核内质子数为112的新原子,关于该新原子的下列叙述正确的是
(
)
A.其核内中子数为112
B.其核外电子数为112
C.原子带正电荷112个
D.以上都不对
10.下列叙述正确的是
(
)
A.二氧化碳是由碳和氧气组成的
B.1个二氧化碳分子是由2个氧原子和1个碳原子构成的
C.二氧化碳是由碳原子和氧原子组成的
D.二氧化碳分子是由2个氧原子和1个碳原子构成的
B
B
11.下列有关原子的说法正确的是
(
)
A.原子是不可再分的最小微粒
B.原子都是由质子、中子和电子构成的
C.原子的类别是由原子核内的质子数决定的
D.以上说法都不确切
12.下列叙述正确的是(
)
A、
属于同位素不同原子即其核电荷数相同但核外电子数不同。
B、
属于同位素不同原子即其核电荷数相同但中子数不同。
C、
属于同位素不同原子即其核外电子数相同但核电荷数不同。
D、属于同位素不同原子即其中子数相同但核外电子数不同。
C
B
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
