2020-2021学年九年级沪教版化学7.3《几种重要的盐》课时练习(有答案)
文档属性
| 名称 | 2020-2021学年九年级沪教版化学7.3《几种重要的盐》课时练习(有答案) | 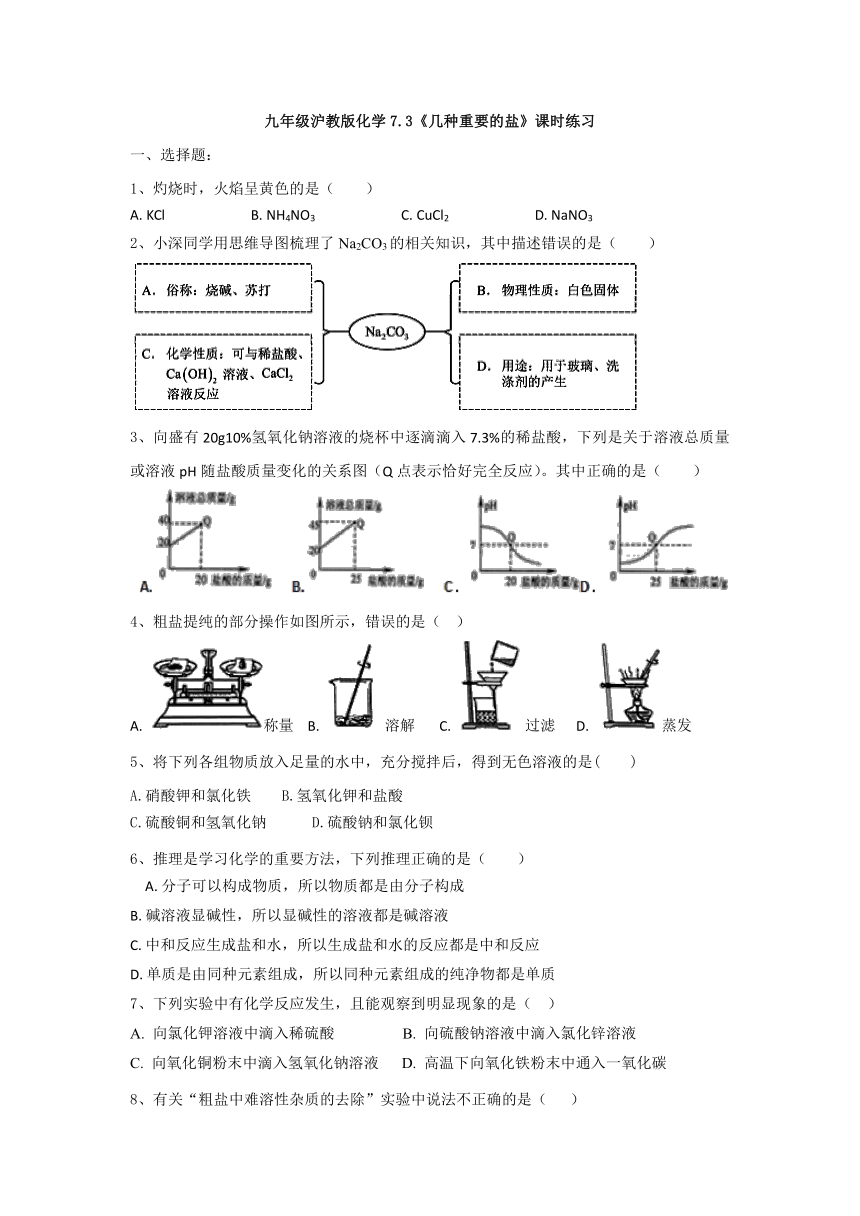 | |
| 格式 | zip | ||
| 文件大小 | 251.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-17 21:03:51 | ||
图片预览


文档简介
九年级沪教版化学7.3《几种重要的盐》课时练习
一、选择题:
1、灼烧时,火焰呈黄色的是( )
A.?KCl?????????????????????????B.?NH4NO3?????????????????????????C.?CuCl2?????????????????????????D.?NaNO3
2、小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是( )
3、向盛有20g10%氢氧化钠溶液的烧杯中逐滴滴入7.3%的稀盐酸,下列是关于溶液总质量或溶液pH随盐酸质量变化的关系图(Q点表示恰好完全反应)。其中正确的是( )
4、粗盐提纯的部分操作如图所示,错误的是(??
)
A.?称量????B.?溶解???????C.?过滤??????D.?蒸发
5、将下列各组物质放入足量的水中,充分搅拌后,得到无色溶液的是(
)
A.硝酸钾和氯化铁 B.氢氧化钾和盐酸
C.硫酸铜和氢氧化钠 D.硫酸钠和氯化钡
6、推理是学习化学的重要方法,下列推理正确的是( )
?A.?分子可以构成物质,所以物质都是由分子构成
B.?碱溶液显碱性,所以显碱性的溶液都是碱溶液
C.?中和反应生成盐和水,所以生成盐和水的反应都是中和反应
D.?单质是由同种元素组成,所以同种元素组成的纯净物都是单质
7、下列实验中有化学反应发生,且能观察到明显现象的是(
)
A.
向氯化钾溶液中滴入稀硫酸
B.
向硫酸钠溶液中滴入氯化锌溶液
C.
向氧化铜粉末中滴入氢氧化钠溶液
D.
高温下向氧化铁粉末中通入一氧化碳
8、有关“粗盐中难溶性杂质的去除”实验中说法不正确的是(
)
A.多加水,让粗盐加速溶解
B.玻璃棒用了4次,但作用各不相同
C.粗盐经过溶解、过滤、蒸发、结晶可以得到初步提纯
D.当蒸发皿中出现较多量固体时,停止加热,利用余热使滤液蒸干
9、学习了物质分类与转化规律后,某同学绘制了部分物质间相互反应的关系图。图中阴影部分表示相邻两类物质的反应,其中不能用于制取ZnCl2的是( )
A.①
B.②
C.③
D.④
10、把HCl、Na2CO3、H2SO4、NaOH、NaNO3五种无色溶液鉴别开来,实验方案中所加试剂和先后顺序最合理的是( )
A.?石蕊试液、稀HNO3、AgNO3溶液???????????????????????????B.?BaCl2溶液、稀HNO3、石蕊试液????
C.?稀HNO3、石蕊试液、AgNO3溶液????????????????????????????D.?稀HNO3、酚酞试液、BaCl2溶液
11、去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是
(
)
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用题35图装置加热蒸发,至水分完全蒸干时停止加热
12、下列各组物质的溶液,不用其他试剂,仅通过观察和用组内溶液相互混合的方法,不能将其逐一鉴别出来的是( )
A.?NaOH??Ca(OH)2??HCl???Na2CO3
B.?KCl??Ba(NO3)2????CuSO4??NaOH
C.?AgNO3???HCl???Na2CO3???CaCl2
D.?Ba(OH)2???KCl???Na2SO4???Na2CO3
13、如图,将胶头滴管中的物质X滴入装有物质Y的试管中,两物质充分反应。下列说法错误的是( )
A.X为稀硫酸,若反应有气泡产生,则生成的气体一定是H2
B.X为AgNO3溶液,Y为Cu片,根据现象可判断金属活动性:Cu>Ag
C.X为BaCl2溶液,Y为Na2SO4溶液,反应产生白色沉淀
D.X为稀盐酸,Y为Al(OH)3,该反应可应用于治疗胃酸过多症
14、某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
A.图中b点所示溶液中,溶质是NaCl
B.向图中c点所示溶液中滴加无色酚酞,溶液不变色
C.该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
15、(多选)某同学从网上获悉:高温灼烤下,沙粒中含有的少量碳酸钙会发生反应:CaCO3=CaO+CO2↑,含有这类沙粒的“沙尘暴”可中和酸雨。该“沙尘暴”中能中和酸雨的物质是(??
)
A.?氧化钙????????????????????????????B.?二氧化碳????????????????????????????C.?氢氧化钙????????????????????????????D.?热的沙粒
二、解答题:
16、“了解漳州,爱我家乡”.请结合所学化学知识回答问题:
(1)花果之乡﹣﹣漳州水仙、云霄枇杷、平和蜜柚、长泰芦柑、龙海荔枝、天宝香蕉闻名遐迩.甜美的水果中富含的果糖(C6H12O6)是由________?种元素组成,其中碳、氢原子的个数比是________? ;硝酸钾(KNO3)是花卉、果树的重要肥料,它属于________肥(填“氮”、“钾”或“复合”).
(2)旅游圣地﹣﹣东山风动石、龙文云洞岩、漳浦天福园是游览观光、品尝美食的好去处.海鲜﹣﹣鱼、虾主要富含________(填“维生素”或“蛋白质”);云洞岩盐鸡的制作需要用到食盐,食盐的主要成分是________?.
(3)文明之城﹣﹣诏安书画之乡、南靖云水谣、田螺坑土楼、华安二宜楼等享誉国内外.用墨写的字可以长时间保存,是因为碳在常温下化学性质________(填“活泼”或“不活泼”);碳点燃能与氧气反应,其完全燃烧的化学方程式是________?;土楼里常设有水井,便于取水灭火,用水灭火的原理是________?,石灰浆是修建土楼的主要材料之一,它与二氧化碳反应的化学方程式是 ________? .
17、下图是某实验中各物质间的变化关系:
请回答:
①写出氧化铜与稀硫酸反应的化学方程式:______.
②气体C的化学式是______,溶液D中一定含有的溶质是______.
③固体B和固体E中都含有的物质是______,固体B中该物质的质量______(填“<”或“>”或“=”)固体E中该物质的质量.
18、2020
年
6
月
8
日是第
12
个“世界海洋日”,海洋是巨大的资源宝库。某课题小组模拟工业海水提镁的流程,在实验室制取生产镁的原料——氯化镁,设计方案如下:
【信息】①海水和苦卤中都含有
NaCl、Na2SO4、MgCl2、CaCl2、KCl
等。
②苦卤是海水晒盐后剩余的溶液。
③右表是某品牌不同碱的价格。
试剂
NaOH
Ca(OH)2
Ba(OH)2
KOH
价格(元/吨)
2400
850
5300
5500
请分析与计算。
(1)海水和苦卤都可以作为制取氯化镁的原料,甲同学提出选择苦卤更好,小组同学一致同意他的观点,理由是
。
(2)在工业生产中为了降低成本,试剂
X
最好选择表格中的_____________。
(3)该方案制取氯化镁时,要经历步骤
I
和步骤
II
两步转化,其主要目的是
。
(4)小组同学按上述方案进行了实验,并制得
19.0g
干燥纯净的氯化镁固体。若步骤Ⅱ中溶质质量分数为
10%的稀盐酸与氢氧化镁恰好完全反应,且步骤
III
中氯化镁没有损失,求步骤
II
中消耗稀盐酸的质量。(写出计算步骤)
参考答案
一、选择题:
1、D
2、A
3、
B
4、C
5、B
6、
D
7、D
8、A
9、
C
10、B
11、C
12、D
13、A
14、
B
15、AC
二、解答题:
16、3;1:2;复合;蛋白质;氯化钠;不活泼;C+O2CO2;降低温度至可燃物的着火点以下;
Ca(OH)2+CO2═CaCO3↓+H2O
17、CuO+H2SO4=CuSO4+H2O;H2、CO2;FeSO4;Cu(或铜);<?????
18、(1)镁离子富集浓度高,成本低
(2)Ca
(OH)2
(3)富集镁
(4)
消耗盐酸的质量为146g。
一、选择题:
1、灼烧时,火焰呈黄色的是( )
A.?KCl?????????????????????????B.?NH4NO3?????????????????????????C.?CuCl2?????????????????????????D.?NaNO3
2、小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是( )
3、向盛有20g10%氢氧化钠溶液的烧杯中逐滴滴入7.3%的稀盐酸,下列是关于溶液总质量或溶液pH随盐酸质量变化的关系图(Q点表示恰好完全反应)。其中正确的是( )
4、粗盐提纯的部分操作如图所示,错误的是(??
)
A.?称量????B.?溶解???????C.?过滤??????D.?蒸发
5、将下列各组物质放入足量的水中,充分搅拌后,得到无色溶液的是(
)
A.硝酸钾和氯化铁 B.氢氧化钾和盐酸
C.硫酸铜和氢氧化钠 D.硫酸钠和氯化钡
6、推理是学习化学的重要方法,下列推理正确的是( )
?A.?分子可以构成物质,所以物质都是由分子构成
B.?碱溶液显碱性,所以显碱性的溶液都是碱溶液
C.?中和反应生成盐和水,所以生成盐和水的反应都是中和反应
D.?单质是由同种元素组成,所以同种元素组成的纯净物都是单质
7、下列实验中有化学反应发生,且能观察到明显现象的是(
)
A.
向氯化钾溶液中滴入稀硫酸
B.
向硫酸钠溶液中滴入氯化锌溶液
C.
向氧化铜粉末中滴入氢氧化钠溶液
D.
高温下向氧化铁粉末中通入一氧化碳
8、有关“粗盐中难溶性杂质的去除”实验中说法不正确的是(
)
A.多加水,让粗盐加速溶解
B.玻璃棒用了4次,但作用各不相同
C.粗盐经过溶解、过滤、蒸发、结晶可以得到初步提纯
D.当蒸发皿中出现较多量固体时,停止加热,利用余热使滤液蒸干
9、学习了物质分类与转化规律后,某同学绘制了部分物质间相互反应的关系图。图中阴影部分表示相邻两类物质的反应,其中不能用于制取ZnCl2的是( )
A.①
B.②
C.③
D.④
10、把HCl、Na2CO3、H2SO4、NaOH、NaNO3五种无色溶液鉴别开来,实验方案中所加试剂和先后顺序最合理的是( )
A.?石蕊试液、稀HNO3、AgNO3溶液???????????????????????????B.?BaCl2溶液、稀HNO3、石蕊试液????
C.?稀HNO3、石蕊试液、AgNO3溶液????????????????????????????D.?稀HNO3、酚酞试液、BaCl2溶液
11、去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是
(
)
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用题35图装置加热蒸发,至水分完全蒸干时停止加热
12、下列各组物质的溶液,不用其他试剂,仅通过观察和用组内溶液相互混合的方法,不能将其逐一鉴别出来的是( )
A.?NaOH??Ca(OH)2??HCl???Na2CO3
B.?KCl??Ba(NO3)2????CuSO4??NaOH
C.?AgNO3???HCl???Na2CO3???CaCl2
D.?Ba(OH)2???KCl???Na2SO4???Na2CO3
13、如图,将胶头滴管中的物质X滴入装有物质Y的试管中,两物质充分反应。下列说法错误的是( )
A.X为稀硫酸,若反应有气泡产生,则生成的气体一定是H2
B.X为AgNO3溶液,Y为Cu片,根据现象可判断金属活动性:Cu>Ag
C.X为BaCl2溶液,Y为Na2SO4溶液,反应产生白色沉淀
D.X为稀盐酸,Y为Al(OH)3,该反应可应用于治疗胃酸过多症
14、某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
A.图中b点所示溶液中,溶质是NaCl
B.向图中c点所示溶液中滴加无色酚酞,溶液不变色
C.该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
15、(多选)某同学从网上获悉:高温灼烤下,沙粒中含有的少量碳酸钙会发生反应:CaCO3=CaO+CO2↑,含有这类沙粒的“沙尘暴”可中和酸雨。该“沙尘暴”中能中和酸雨的物质是(??
)
A.?氧化钙????????????????????????????B.?二氧化碳????????????????????????????C.?氢氧化钙????????????????????????????D.?热的沙粒
二、解答题:
16、“了解漳州,爱我家乡”.请结合所学化学知识回答问题:
(1)花果之乡﹣﹣漳州水仙、云霄枇杷、平和蜜柚、长泰芦柑、龙海荔枝、天宝香蕉闻名遐迩.甜美的水果中富含的果糖(C6H12O6)是由________?种元素组成,其中碳、氢原子的个数比是________? ;硝酸钾(KNO3)是花卉、果树的重要肥料,它属于________肥(填“氮”、“钾”或“复合”).
(2)旅游圣地﹣﹣东山风动石、龙文云洞岩、漳浦天福园是游览观光、品尝美食的好去处.海鲜﹣﹣鱼、虾主要富含________(填“维生素”或“蛋白质”);云洞岩盐鸡的制作需要用到食盐,食盐的主要成分是________?.
(3)文明之城﹣﹣诏安书画之乡、南靖云水谣、田螺坑土楼、华安二宜楼等享誉国内外.用墨写的字可以长时间保存,是因为碳在常温下化学性质________(填“活泼”或“不活泼”);碳点燃能与氧气反应,其完全燃烧的化学方程式是________?;土楼里常设有水井,便于取水灭火,用水灭火的原理是________?,石灰浆是修建土楼的主要材料之一,它与二氧化碳反应的化学方程式是 ________? .
17、下图是某实验中各物质间的变化关系:
请回答:
①写出氧化铜与稀硫酸反应的化学方程式:______.
②气体C的化学式是______,溶液D中一定含有的溶质是______.
③固体B和固体E中都含有的物质是______,固体B中该物质的质量______(填“<”或“>”或“=”)固体E中该物质的质量.
18、2020
年
6
月
8
日是第
12
个“世界海洋日”,海洋是巨大的资源宝库。某课题小组模拟工业海水提镁的流程,在实验室制取生产镁的原料——氯化镁,设计方案如下:
【信息】①海水和苦卤中都含有
NaCl、Na2SO4、MgCl2、CaCl2、KCl
等。
②苦卤是海水晒盐后剩余的溶液。
③右表是某品牌不同碱的价格。
试剂
NaOH
Ca(OH)2
Ba(OH)2
KOH
价格(元/吨)
2400
850
5300
5500
请分析与计算。
(1)海水和苦卤都可以作为制取氯化镁的原料,甲同学提出选择苦卤更好,小组同学一致同意他的观点,理由是
。
(2)在工业生产中为了降低成本,试剂
X
最好选择表格中的_____________。
(3)该方案制取氯化镁时,要经历步骤
I
和步骤
II
两步转化,其主要目的是
。
(4)小组同学按上述方案进行了实验,并制得
19.0g
干燥纯净的氯化镁固体。若步骤Ⅱ中溶质质量分数为
10%的稀盐酸与氢氧化镁恰好完全反应,且步骤
III
中氯化镁没有损失,求步骤
II
中消耗稀盐酸的质量。(写出计算步骤)
参考答案
一、选择题:
1、D
2、A
3、
B
4、C
5、B
6、
D
7、D
8、A
9、
C
10、B
11、C
12、D
13、A
14、
B
15、AC
二、解答题:
16、3;1:2;复合;蛋白质;氯化钠;不活泼;C+O2CO2;降低温度至可燃物的着火点以下;
Ca(OH)2+CO2═CaCO3↓+H2O
17、CuO+H2SO4=CuSO4+H2O;H2、CO2;FeSO4;Cu(或铜);<?????
18、(1)镁离子富集浓度高,成本低
(2)Ca
(OH)2
(3)富集镁
(4)
消耗盐酸的质量为146g。
