2.5 表示元素的符号 一课一练 (含解析)
文档属性
| 名称 | 2.5 表示元素的符号 一课一练 (含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 212.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-02-27 00:00:00 | ||
图片预览



文档简介
浙教版八年级下册2.5
表示元素的符号
一、选择题
1.(2019·浙江九年级期末)下列元素周期表中全部是金属元素的是( )
A.甲
B.乙
C.丙
D.丁
2.(2020·浙江湖州市·八年级期末)元素周期表是学习和研究科学的重要工具.表是元素周期表的一部分,A﹣F代表六种不同短周期元素。下列说法不正确的是(
)
A.A,B同周期
B.A,D同族
C.原子核中质子数D>B
D.D,F化学性质相似
3.(2020·浙江温州市·九年级月考)X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的的最低价离子分别为和,Y+和具有相同的电子层结构。下列说法正确的是( )
A.原子序数:X>Y>Z
B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z-
D.原子的最外层电子数:X>Y>Z
4.(2020·浙江八年级月考)铱-192是一种放射性物质,对人体有严重辐射伤害。如图所示是元素周期表中铱元素的有关信息,下列说法错误的是( )
A.铱元素原子的原子核内有77个质子
B.铱元素是金属元素
C.铱元素原子的核外有77个电子
D.铱元素的相对原子质量为192.2g
5.(2020·浙江八年级月考)下列不属于“Fe”表示的意义是( )
A.铁锈
B.铁元素
C.铁
D.一个铁原子
6.(2020·温州市中通国际学校九年级月考)近期,英国自然杂志刊发了材料领域的最新研究成果,科学家找到了接近常温的超导材料“超氢化镧”,下列有关镧的说法,正确的是( )
A.元素符号是La
B.镧是非金属元素
C.中子数是57
D.相对原子质量是138.9克
7.(2014·广东深圳市·中考真题)如图,下列说法正确的是(
)
A.铱元素的核外电子数是77
B.铱元素的相对原子质量是192g
C.铱元素的质子数是115
D.铱元素不是金属元素
8.(2017·全国八年级课时练习)如图为元素周期表的一部分,下列说法错误的是
A.碳元素只能形成一种单质
B.氮原子的核外电子数为7
C.氧原子的相对原子质量为16.00
D.C、N、O的原子序数依次增加
9.(2020·浙江省瑞安市瑞祥实验学校八年级月考)如图为元素周期表的一部分,A~E
代表五种不同元素。下列说法正确的是( )
A.原子序数:CB.核内质子数:A=D
C.A,B,C
同周期
D.D、E
同族
10.(2020·浙江温州市·九年级其他模拟)国际通用的元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写。镍元素的拉丁文名称为Niccolum,则镍的元素符号为( )
A.Ni
B.NI
C.N
D.Na
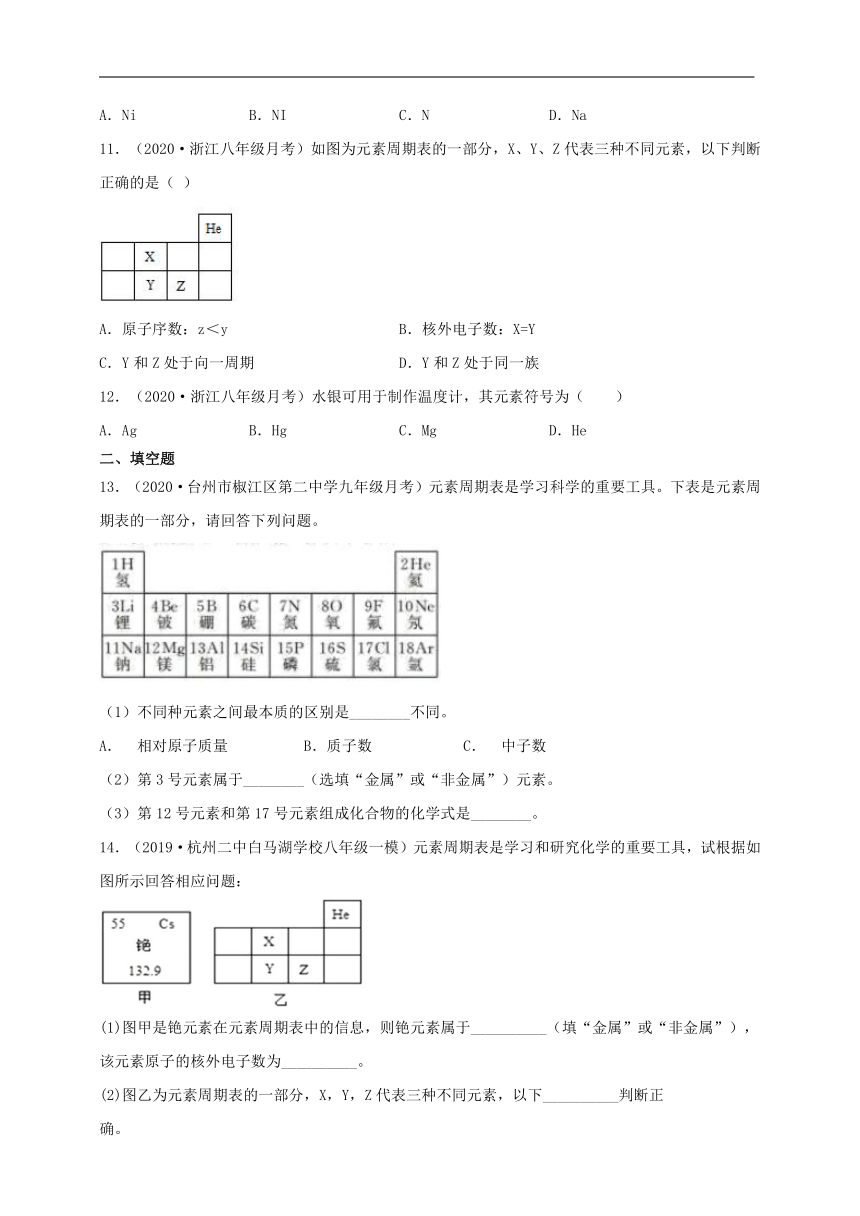
11.(2020·浙江八年级月考)如图为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是(
)
A.原子序数:z<y
B.核外电子数:X=Y
C.Y和Z处于向一周期
D.Y和Z处于同一族
12.(2020·浙江八年级月考)水银可用于制作温度计,其元素符号为(
)
A.Ag
B.Hg
C.Mg
D.He
二、填空题
13.(2020·台州市椒江区第二中学九年级月考)元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题。
(1)不同种元素之间最本质的区别是________不同。
A.?相对原子质量?????B.质子数??????C.?中子数
(2)第3号元素属于________(选填“金属”或“非金属”)元素。
(3)第12号元素和第17号元素组成化合物的化学式是________。
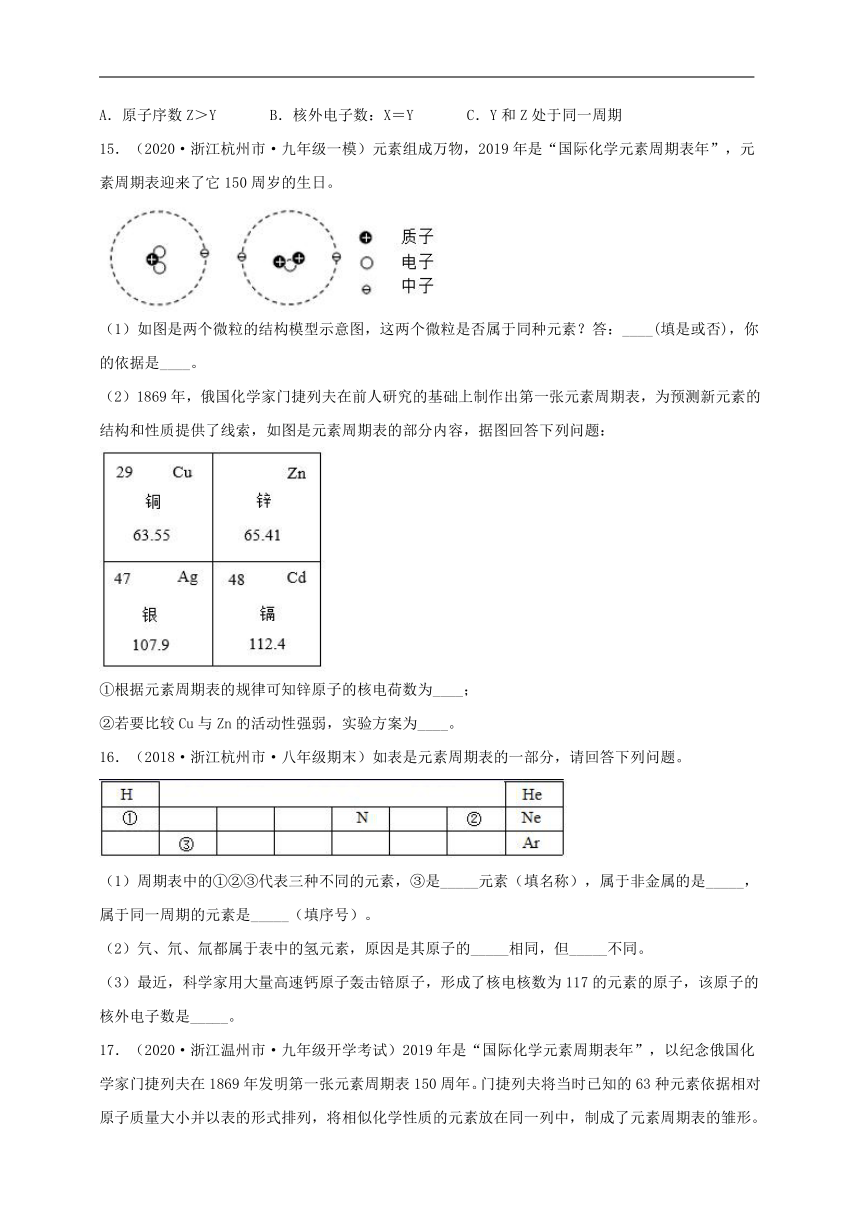
14.(2019·杭州二中白马湖学校八年级一模)元素周期表是学习和研究化学的重要工具,试根据如图所示回答相应问题:
(1)图甲是铯元素在元素周期表中的信息,则铯元素属于__________(填“金属”或“非金属”),该元素原子的核外电子数为__________。????
(2)图乙为元素周期表的一部分,X,Y,Z代表三种不同元素,以下__________判断正确。????????????
A.原子序数Z>Y???
B.核外电子数:X=Y???
C.Y和Z处于同一周期
15.(2020·浙江杭州市·九年级一模)元素组成万物,2019年是“国际化学元素周期表年”,元素周期表迎来了它150周岁的生日。
(1)如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?答:____(填是或否),你的依据是____。
(2)1869年,俄国化学家门捷列夫在前人研究的基础上制作出第一张元素周期表,为预测新元素的结构和性质提供了线索,如图是元素周期表的部分内容,据图回答下列问题:
①根据元素周期表的规律可知锌原子的核电荷数为____;
②若要比较Cu与Zn的活动性强弱,实验方案为____。
16.(2018·浙江杭州市·八年级期末)如表是元素周期表的一部分,请回答下列问题。
(1)周期表中的①②③代表三种不同的元素,③是_____元素(填名称),属于非金属的是_____,属于同一周期的元素是_____(填序号)。
(2)氕、氘、氚都属于表中的氢元素,原因是其原子的_____相同,但_____不同。
(3)最近,科学家用大量高速钙原子轰击锫原子,形成了核电核数为117的元素的原子,该原子的核外电子数是_____。
17.(2020·浙江温州市·九年级开学考试)2019年是“国际化学元素周期表年”,以纪念俄国化学家门捷列夫在1869年发明第一张元素周期表150周年。门捷列夫将当时已知的63种元素依据相对原子质量大小并以表的形式排列,将相似化学性质的元素放在同一列中,制成了元素周期表的雏形。
(1)钔的质子数为101,中子数为157,相对原子质量为258,则其核外电子数为______;
(2)在1869年之前,许多化学家就对当时己知的元素进行排列。但国际上公认把发明元素周期律的桂冠戴在了门捷列夫的头上,你推测可能的原因是______。
A.门捷列夫按照相对原子质量排列元素,这也是现在元素周期表元素排列的标准
B.门捷列夫以“相似化学性质的元素放同一列”原则修正一些元素的相对原子质量
C.门捷列夫发明的元素周期表完全是他的独创,并不需要吸收别人的研究成果
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实
E.门捷列夫当时在科学界威望极高,他的发明成果更能让人信服
18.(2019·浙江温州市·八年级一模)用元素符号表示或说出符号的意义:
(1)镁元素________?
(2)钠原子________?
(3)3Hg________
(4)H2________.
19.(2020·浙江丽水市·八年级期末)元素周期表是我们学习和研究科学的重要工具,请根据如图所示部分周期表回答问题。
(1)每一周期结尾的是稀有气体元素,它们的化学性质______(填“活泼”或“稳定”);
(2)根据周期表的元素排列规律,锂与钠、碳与硅的化学性质相似,则氟与______化学性质相似。
三、简答题
20.(2020·浙江八年级月考)如图为元素周期表的一部分,请按要求填空:
(1)表中元素②形成单质的化学式为_____.
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的_____相同.
(3)表中9号和17号元素最外层电子数相同,都易_____(填“得到”或“失去”)电子。
(4)表中不同种元素最本质的区别是_____.
A.质子数不同
B.中子数不同
C.相对原子质量不同
D.最外层电子数不同.
答案部分
1.B
【分析】
根据甲区含有氢元素丙区包含ⅢA~ⅦA元素,含有金属元素与非金属性元素,过渡元素区全部为金属元素。
【详解】
甲区包含ⅠA族、ⅡA族元素,含有氢元素,丙区ⅢA~ⅦA元素,含有金属元素与非金属性元素,丁区包含零族元素都是惰性气体,属于非金属,过渡元素区包含乙区,金属元素原子最外层电子数小于电子层数全部为金属元素,故选B。
2.D
【详解】
A.根据图片可知,A和B在同一行,因此为同一周期,故A正确但不合题意;
B.A和D在同一列,因此为同一族,故B正确但不合题意;
C.D比B多一行,那么D比B多一个电子层,因此D的核电荷数肯定大于B的核电荷数,即D的质子数大于B的质子数,故C正确但不合题意;
D.D和F在同一周期,但是最外层电子数不同,所以它们的化学性质不同,故D错误但符合题意。
故选D。
3.A
【分析】
原子的化学性质主要由最外层电子数决定,当最外层电子数小于4时,反应中易失去电子成为阳离子,阳离子带的正电荷数等于失电子数;当最外层电子数大于4时,反应中易得到电子成为阴离子,阴离子带负电荷数等于得电子数。X、Z的最低价离子分别为x2-和Z-,则X为第VIA族元素,Z为VIIA族元素;Y+和Z-具有相同的电子层结构,则Y在的下一周期,则为Na元素,Z为F元素,X、Y同周期,则X为S元素。
【详解】
A、X、Y、Z分别为S、Na、F,原子序数分别为16、11、9,故A正确;
B、常温下Na、S为固体,F2为气体,Na的熔点较低,但钠的沸点高于硫,顺序应为Na>S>F2,故B错误;
C、Na+、F具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为F>Na+,故C错误;
D、
X、Y、Z分别为S、Na、F,原子最外层电子数分别为6、1、7,故D错误。
故选A。
4.D
【详解】
A、元素信息图左上角的数字是元素的原子序数,原子序数等于原子核内的质子数,由图可知,铱元素原子的原子核内有77个质子,选项正确;
B、由图可知,铱元素的名称带有金字旁,所以铱元素是金属元素,选项正确;
C、元素信息图左上角的数字是元素的原子序数,原子序数等于原子核内的质子数等于核外电子数,由图可知,铱元素原子的核外有77个电子,选项正确;
D、元素信息图中正下方的数字就是元素的相对原子质量,由图可知,铱元素的相对原子质量为192.2,g是质量的单位符号,不是相对原子质量的单位符号,选项错误,故选D。
5.A
【详解】
Fe可以表示铁元素;表示一个铁原子;还可以表示铁这种物质。不能表示铁锈,故选:A。
6.A
【详解】
A、元素信息图中右上角的符号就是元素符号,所以镧的元素符号是La,选项正确;
B、由图可知,镧元素的名称带有“钅”字旁,属于金属元素,选项错误;
C、元素信息图中左上角的数字是元素的原子序数,与原子核内的质子数和核外电子数相同,即镧原子核内质子数为57,不是中子数,选项错误;
D、元素信息图最下方的数值是元素原子的相对原子质量,所以镧原子的相对原子质量是138.9,相对原子质量的单位是“1”,不是“g”,常省略不写,选项错误。
故选A。
7.A
【分析】
元素周期表信息内容的分析。
【详解】
根据元素周期表的信息可知:
A、铱元素的原子序数为77,则铱元素的原子核外电子数是77,A选项正确,符合题意;
B、铱元素的相对原子质量是192.0,B选项错误,不符合题意;
C、铱元素的原子序数为77,铱元素的质子数是77,C选项错误,不符合题意;
D、铱元素是金属元素,D选项错误,不符合题意。故选A。
8.A
【详解】
A、金刚石、石墨都是碳元素形成的单质,A选项错误,符合题意;
B、由氮元素元素周期表信息图可知,氮原子原子序数为7,核外电子数等于原子序数,也为7,B选项正确,不符合题意;
C、由氧元素元素周期表信息图可知,氧原子的相对原子质量为16.00,C选项正确,不符合题意;
D、由元素周期表信息图可知C、N、O的原子序数分别为6、7、8,依次增加,D选项正确,不符合题意。故选A。
9.C
【详解】
根据,A~E五种不同元素在元素周期表中的位置可知:
A、同一周期(横行)从左往右原子序数逐渐增大,因此原子序数:C>B,A选项说法不正确,不符合题意;
B、A、D位于同一纵行,D在A的下一周期,D的核内质子数大于A,B选项说法不正确,不符合题意;
C、A、B、C位于同一横行,则A、B、C
同周期,C选项说法正确,符合题意;
D、D、E位于同一横行,则D、E同周期,D选项说法不正确,不符合题意。故选C。
10.A
【详解】
A、因为元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写,所以镍的元素符号为:Ni,选项A正确;
B、“NI”中第二个字母是大写,不符合书写原则,选项B不正确;
C、“N”是氮的元素符号,选项C不正确;
D、“Na”是钠的元素符号,选项D不正确。故选A。
11.C
【详解】
A、元素周期表原子序数自左向右依次增大,原子序数:z>y,A错误;
B、元素周期表中同一族原子最外层电子数相等,B错误;
C、元素周期表中同一行表示同一周期,同一列表示同一族;Y和Z属于同一周期,C正确;
D、元素周期表中同一行表示同一周期,同一列表示同一族,Y和Z属于同一周期,D错误;
故选C。
12.B
【详解】
水银是金属汞的俗称,其组成元素是汞元素,汞元素的符号是Hg,故选B。
13.B
金属
MgCl2
【详解】
(1)不同种元素之间最本质的区别是核内质子数不同。
故填:B。
(2)第3号元素是锂元素,属于金属元素。
故填:金属。
(3)第12号元素(镁元素)和第17号元素(氯元素)组成化合物是氯化镁,氯化镁中镁元素化合价是+2,氯元素化合价是-1,根据化合物中元素化合价代数和为零可知,氯化镁的化学式是MgCl2。
故填:MgCl2。
14.金属
55
AC
【解析】
(1)金属元素一般都带有“钅”字旁,所以铯元素属于金属元素;又因为在原子内,质子数等于核外电子数,所铯元素原子的核外电子数为55.故答案为金属;55;
(2)A、根据元素周期律:同一周期原子的原子序数从左到右逐渐增加.所以原子序数:Z>Y,故A说法正确;
B、根据不同种元素之间的本质区别是质子数不同,A,D不是同种元素,所以质子数不相等,即电子数不想等;故B说法错误;
C、根据元素周期律:同一撗行的元素属于同一周期,所以Y和Z同周期,故C说法正确;
故选AC.
15.否
它们具有不同的质子数(或核电荷数)
30
方案一:将铜和锌分别投入稀硫酸中,有大量气泡产生的是锌,无现象的为铜。方案二:锌片插入硫酸铜溶液中,锌片表面产生一层红色物质
【分析】
元素是质子数相同的一类原子的总称,锌和稀硫酸反应生成硫酸锌和氢气,锌和硫酸铜反应生成硫酸锌和铜。
【详解】
(1)由两个微粒的结构模型示意图可知,第一个微粒含有1个质子,第二个微粒含有2个质子,元素是质子数相同的一类原子的总称,故这两个微粒不属于同种元素,依据是它们具有不同的质子数(或核电荷数)。
(2)①元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量,同一周期,原子序数逐渐增大,则锌的原子序数为30,原子中,核电荷数=核内质子数=核外电子数=原子序数,故根据元素周期表的规律可知锌原子的核电荷数为30。
②在金属活动性顺序表中,金属活动性Zn>H>Cu,铜和稀硫酸不反应,锌和稀硫酸反应生成硫酸锌和氢气,锌和硫酸铜反应生成硫酸锌和铜,故若要比较Cu与Zn的活动性强弱,实验方案为方案一:将铜和锌分别投入稀硫酸中,有大量气泡产生的是锌,无现象的为铜。方案二:锌片插入硫酸铜溶液中,锌片表面产生一层红色物质。
【点睛】
在金属活动性顺序中,金属的位置越靠前,它的活动性越强,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来。
16.镁
②
①②
质子数
中子数
117
【分析】
【详解】
(1)根据元素周期表中的元素排序,①号元素是锂元素,②号元素是氟元素,③号元素是镁元素,其中①③是金属元素,②是非金属元素,①②位于同一周期。
(2)元素是指据有相同质子数(或核电荷数)的同一类原子的总称,因此氕、氘、氚的质子数相同,中子数不同;
(3)在原子中,质子数=核电荷数=核外电子数,则原子的核外电子数是117。
17.101
BD
【详解】
(1)在原子中,质子数=核电荷数=原子序数=核外电子数,钔的质子数为101,根据核外电子数等于质子数可知,它的核外电子数为101。
(2)A.元素周期表是按照原子序数,也就是原子里面的质子数的大小进行排列的,故A错误;
B.门捷列夫发现了“相似化学性质的元素放同一列”原则,据此对已经发现的元素的相对原子质量进行了修正,故B正确;
C.门捷列夫得到的元素周期表并不是他独创的,而是在前面大量科学家的研究结果之上,再加上自己的仔细研究才得到的,故C错误;
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实,故D正确;
D.在科学界,科学家的荣誉都是建立在实实在在的研究成果之上的,和他本身的威望没有多大关系,故D错误。
故选BD。
18.Mg
Na
3个汞原子
氢气或一个氢分子
【详解】
(1)镁元素用元素符号Mg表示,故填Mg;
(2)钠原子用元素符号Na代表钠原子,故填Na;
(3)3Hg代表对汞原子有个数描述,故填3个汞原子;
(4)可以代表氢气,同时也可以代表代表一个氢分子,故填氢气或一个氢分子。
19.稳定
氯
【分析】
元素发生化学变化的难易程度,与该元素最外层的电子个数有关,另外最外层电子个数相同的元素,其化学性质会具备一定的相似性。
【详解】
(1)每一周期结尾的是稀有气体元素,其最外层是最稳定的2个或者8个电子结构所以它们的化学性质稳定,答案:稳定;
(2)根据周期表的元素排列规律,锂与钠、碳与硅的化学性质相似,是因为它们的最外层电子个数相同,那么与氟化学性质相似的元素其最外层电子个数要与其一样,从图中可以看出,该元素为氯(Cl),答案:氯。
【点睛】
化学元素周期表的规律特点。
20.N2
核外电子层数
得到
A
【详解】
(1)表中元素②为氮元素,氮元素形成的单质为氮气,化学式为N2。
(2)分析元素原子的核外电子排布可知,3至10号元素的原子核外均有2个电子层,11至18号元素的原子核外均有3个电子层,可以得到的规律是每个周期元素的原子核外电子层数相同。
(3)表中9号和17号元素的最外层电子数均为7,都易得到1个电子形成稳定结构。
(4)元素是具有相同核电荷数(即质子数)的一类原子的总称,所以不同种元素间最本质的区别是核电荷数(即质子数)不同,故选A。
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
表示元素的符号
一、选择题
1.(2019·浙江九年级期末)下列元素周期表中全部是金属元素的是( )
A.甲
B.乙
C.丙
D.丁
2.(2020·浙江湖州市·八年级期末)元素周期表是学习和研究科学的重要工具.表是元素周期表的一部分,A﹣F代表六种不同短周期元素。下列说法不正确的是(
)
A.A,B同周期
B.A,D同族
C.原子核中质子数D>B
D.D,F化学性质相似
3.(2020·浙江温州市·九年级月考)X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的的最低价离子分别为和,Y+和具有相同的电子层结构。下列说法正确的是( )
A.原子序数:X>Y>Z
B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z-
D.原子的最外层电子数:X>Y>Z
4.(2020·浙江八年级月考)铱-192是一种放射性物质,对人体有严重辐射伤害。如图所示是元素周期表中铱元素的有关信息,下列说法错误的是( )
A.铱元素原子的原子核内有77个质子
B.铱元素是金属元素
C.铱元素原子的核外有77个电子
D.铱元素的相对原子质量为192.2g
5.(2020·浙江八年级月考)下列不属于“Fe”表示的意义是( )
A.铁锈
B.铁元素
C.铁
D.一个铁原子
6.(2020·温州市中通国际学校九年级月考)近期,英国自然杂志刊发了材料领域的最新研究成果,科学家找到了接近常温的超导材料“超氢化镧”,下列有关镧的说法,正确的是( )
A.元素符号是La
B.镧是非金属元素
C.中子数是57
D.相对原子质量是138.9克
7.(2014·广东深圳市·中考真题)如图,下列说法正确的是(
)
A.铱元素的核外电子数是77
B.铱元素的相对原子质量是192g
C.铱元素的质子数是115
D.铱元素不是金属元素
8.(2017·全国八年级课时练习)如图为元素周期表的一部分,下列说法错误的是
A.碳元素只能形成一种单质
B.氮原子的核外电子数为7
C.氧原子的相对原子质量为16.00
D.C、N、O的原子序数依次增加
9.(2020·浙江省瑞安市瑞祥实验学校八年级月考)如图为元素周期表的一部分,A~E
代表五种不同元素。下列说法正确的是( )
A.原子序数:C
C.A,B,C
同周期
D.D、E
同族
10.(2020·浙江温州市·九年级其他模拟)国际通用的元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写。镍元素的拉丁文名称为Niccolum,则镍的元素符号为( )
A.Ni
B.NI
C.N
D.Na
11.(2020·浙江八年级月考)如图为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是(
)
A.原子序数:z<y
B.核外电子数:X=Y
C.Y和Z处于向一周期
D.Y和Z处于同一族
12.(2020·浙江八年级月考)水银可用于制作温度计,其元素符号为(
)
A.Ag
B.Hg
C.Mg
D.He
二、填空题
13.(2020·台州市椒江区第二中学九年级月考)元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题。
(1)不同种元素之间最本质的区别是________不同。
A.?相对原子质量?????B.质子数??????C.?中子数
(2)第3号元素属于________(选填“金属”或“非金属”)元素。
(3)第12号元素和第17号元素组成化合物的化学式是________。
14.(2019·杭州二中白马湖学校八年级一模)元素周期表是学习和研究化学的重要工具,试根据如图所示回答相应问题:
(1)图甲是铯元素在元素周期表中的信息,则铯元素属于__________(填“金属”或“非金属”),该元素原子的核外电子数为__________。????
(2)图乙为元素周期表的一部分,X,Y,Z代表三种不同元素,以下__________判断正确。????????????
A.原子序数Z>Y???
B.核外电子数:X=Y???
C.Y和Z处于同一周期
15.(2020·浙江杭州市·九年级一模)元素组成万物,2019年是“国际化学元素周期表年”,元素周期表迎来了它150周岁的生日。
(1)如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?答:____(填是或否),你的依据是____。
(2)1869年,俄国化学家门捷列夫在前人研究的基础上制作出第一张元素周期表,为预测新元素的结构和性质提供了线索,如图是元素周期表的部分内容,据图回答下列问题:
①根据元素周期表的规律可知锌原子的核电荷数为____;
②若要比较Cu与Zn的活动性强弱,实验方案为____。
16.(2018·浙江杭州市·八年级期末)如表是元素周期表的一部分,请回答下列问题。
(1)周期表中的①②③代表三种不同的元素,③是_____元素(填名称),属于非金属的是_____,属于同一周期的元素是_____(填序号)。
(2)氕、氘、氚都属于表中的氢元素,原因是其原子的_____相同,但_____不同。
(3)最近,科学家用大量高速钙原子轰击锫原子,形成了核电核数为117的元素的原子,该原子的核外电子数是_____。
17.(2020·浙江温州市·九年级开学考试)2019年是“国际化学元素周期表年”,以纪念俄国化学家门捷列夫在1869年发明第一张元素周期表150周年。门捷列夫将当时已知的63种元素依据相对原子质量大小并以表的形式排列,将相似化学性质的元素放在同一列中,制成了元素周期表的雏形。
(1)钔的质子数为101,中子数为157,相对原子质量为258,则其核外电子数为______;
(2)在1869年之前,许多化学家就对当时己知的元素进行排列。但国际上公认把发明元素周期律的桂冠戴在了门捷列夫的头上,你推测可能的原因是______。
A.门捷列夫按照相对原子质量排列元素,这也是现在元素周期表元素排列的标准
B.门捷列夫以“相似化学性质的元素放同一列”原则修正一些元素的相对原子质量
C.门捷列夫发明的元素周期表完全是他的独创,并不需要吸收别人的研究成果
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实
E.门捷列夫当时在科学界威望极高,他的发明成果更能让人信服
18.(2019·浙江温州市·八年级一模)用元素符号表示或说出符号的意义:
(1)镁元素________?
(2)钠原子________?
(3)3Hg________
(4)H2________.
19.(2020·浙江丽水市·八年级期末)元素周期表是我们学习和研究科学的重要工具,请根据如图所示部分周期表回答问题。
(1)每一周期结尾的是稀有气体元素,它们的化学性质______(填“活泼”或“稳定”);
(2)根据周期表的元素排列规律,锂与钠、碳与硅的化学性质相似,则氟与______化学性质相似。
三、简答题
20.(2020·浙江八年级月考)如图为元素周期表的一部分,请按要求填空:
(1)表中元素②形成单质的化学式为_____.
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的_____相同.
(3)表中9号和17号元素最外层电子数相同,都易_____(填“得到”或“失去”)电子。
(4)表中不同种元素最本质的区别是_____.
A.质子数不同
B.中子数不同
C.相对原子质量不同
D.最外层电子数不同.
答案部分
1.B
【分析】
根据甲区含有氢元素丙区包含ⅢA~ⅦA元素,含有金属元素与非金属性元素,过渡元素区全部为金属元素。
【详解】
甲区包含ⅠA族、ⅡA族元素,含有氢元素,丙区ⅢA~ⅦA元素,含有金属元素与非金属性元素,丁区包含零族元素都是惰性气体,属于非金属,过渡元素区包含乙区,金属元素原子最外层电子数小于电子层数全部为金属元素,故选B。
2.D
【详解】
A.根据图片可知,A和B在同一行,因此为同一周期,故A正确但不合题意;
B.A和D在同一列,因此为同一族,故B正确但不合题意;
C.D比B多一行,那么D比B多一个电子层,因此D的核电荷数肯定大于B的核电荷数,即D的质子数大于B的质子数,故C正确但不合题意;
D.D和F在同一周期,但是最外层电子数不同,所以它们的化学性质不同,故D错误但符合题意。
故选D。
3.A
【分析】
原子的化学性质主要由最外层电子数决定,当最外层电子数小于4时,反应中易失去电子成为阳离子,阳离子带的正电荷数等于失电子数;当最外层电子数大于4时,反应中易得到电子成为阴离子,阴离子带负电荷数等于得电子数。X、Z的最低价离子分别为x2-和Z-,则X为第VIA族元素,Z为VIIA族元素;Y+和Z-具有相同的电子层结构,则Y在的下一周期,则为Na元素,Z为F元素,X、Y同周期,则X为S元素。
【详解】
A、X、Y、Z分别为S、Na、F,原子序数分别为16、11、9,故A正确;
B、常温下Na、S为固体,F2为气体,Na的熔点较低,但钠的沸点高于硫,顺序应为Na>S>F2,故B错误;
C、Na+、F具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为F>Na+,故C错误;
D、
X、Y、Z分别为S、Na、F,原子最外层电子数分别为6、1、7,故D错误。
故选A。
4.D
【详解】
A、元素信息图左上角的数字是元素的原子序数,原子序数等于原子核内的质子数,由图可知,铱元素原子的原子核内有77个质子,选项正确;
B、由图可知,铱元素的名称带有金字旁,所以铱元素是金属元素,选项正确;
C、元素信息图左上角的数字是元素的原子序数,原子序数等于原子核内的质子数等于核外电子数,由图可知,铱元素原子的核外有77个电子,选项正确;
D、元素信息图中正下方的数字就是元素的相对原子质量,由图可知,铱元素的相对原子质量为192.2,g是质量的单位符号,不是相对原子质量的单位符号,选项错误,故选D。
5.A
【详解】
Fe可以表示铁元素;表示一个铁原子;还可以表示铁这种物质。不能表示铁锈,故选:A。
6.A
【详解】
A、元素信息图中右上角的符号就是元素符号,所以镧的元素符号是La,选项正确;
B、由图可知,镧元素的名称带有“钅”字旁,属于金属元素,选项错误;
C、元素信息图中左上角的数字是元素的原子序数,与原子核内的质子数和核外电子数相同,即镧原子核内质子数为57,不是中子数,选项错误;
D、元素信息图最下方的数值是元素原子的相对原子质量,所以镧原子的相对原子质量是138.9,相对原子质量的单位是“1”,不是“g”,常省略不写,选项错误。
故选A。
7.A
【分析】
元素周期表信息内容的分析。
【详解】
根据元素周期表的信息可知:
A、铱元素的原子序数为77,则铱元素的原子核外电子数是77,A选项正确,符合题意;
B、铱元素的相对原子质量是192.0,B选项错误,不符合题意;
C、铱元素的原子序数为77,铱元素的质子数是77,C选项错误,不符合题意;
D、铱元素是金属元素,D选项错误,不符合题意。故选A。
8.A
【详解】
A、金刚石、石墨都是碳元素形成的单质,A选项错误,符合题意;
B、由氮元素元素周期表信息图可知,氮原子原子序数为7,核外电子数等于原子序数,也为7,B选项正确,不符合题意;
C、由氧元素元素周期表信息图可知,氧原子的相对原子质量为16.00,C选项正确,不符合题意;
D、由元素周期表信息图可知C、N、O的原子序数分别为6、7、8,依次增加,D选项正确,不符合题意。故选A。
9.C
【详解】
根据,A~E五种不同元素在元素周期表中的位置可知:
A、同一周期(横行)从左往右原子序数逐渐增大,因此原子序数:C>B,A选项说法不正确,不符合题意;
B、A、D位于同一纵行,D在A的下一周期,D的核内质子数大于A,B选项说法不正确,不符合题意;
C、A、B、C位于同一横行,则A、B、C
同周期,C选项说法正确,符合题意;
D、D、E位于同一横行,则D、E同周期,D选项说法不正确,不符合题意。故选C。
10.A
【详解】
A、因为元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写,所以镍的元素符号为:Ni,选项A正确;
B、“NI”中第二个字母是大写,不符合书写原则,选项B不正确;
C、“N”是氮的元素符号,选项C不正确;
D、“Na”是钠的元素符号,选项D不正确。故选A。
11.C
【详解】
A、元素周期表原子序数自左向右依次增大,原子序数:z>y,A错误;
B、元素周期表中同一族原子最外层电子数相等,B错误;
C、元素周期表中同一行表示同一周期,同一列表示同一族;Y和Z属于同一周期,C正确;
D、元素周期表中同一行表示同一周期,同一列表示同一族,Y和Z属于同一周期,D错误;
故选C。
12.B
【详解】
水银是金属汞的俗称,其组成元素是汞元素,汞元素的符号是Hg,故选B。
13.B
金属
MgCl2
【详解】
(1)不同种元素之间最本质的区别是核内质子数不同。
故填:B。
(2)第3号元素是锂元素,属于金属元素。
故填:金属。
(3)第12号元素(镁元素)和第17号元素(氯元素)组成化合物是氯化镁,氯化镁中镁元素化合价是+2,氯元素化合价是-1,根据化合物中元素化合价代数和为零可知,氯化镁的化学式是MgCl2。
故填:MgCl2。
14.金属
55
AC
【解析】
(1)金属元素一般都带有“钅”字旁,所以铯元素属于金属元素;又因为在原子内,质子数等于核外电子数,所铯元素原子的核外电子数为55.故答案为金属;55;
(2)A、根据元素周期律:同一周期原子的原子序数从左到右逐渐增加.所以原子序数:Z>Y,故A说法正确;
B、根据不同种元素之间的本质区别是质子数不同,A,D不是同种元素,所以质子数不相等,即电子数不想等;故B说法错误;
C、根据元素周期律:同一撗行的元素属于同一周期,所以Y和Z同周期,故C说法正确;
故选AC.
15.否
它们具有不同的质子数(或核电荷数)
30
方案一:将铜和锌分别投入稀硫酸中,有大量气泡产生的是锌,无现象的为铜。方案二:锌片插入硫酸铜溶液中,锌片表面产生一层红色物质
【分析】
元素是质子数相同的一类原子的总称,锌和稀硫酸反应生成硫酸锌和氢气,锌和硫酸铜反应生成硫酸锌和铜。
【详解】
(1)由两个微粒的结构模型示意图可知,第一个微粒含有1个质子,第二个微粒含有2个质子,元素是质子数相同的一类原子的总称,故这两个微粒不属于同种元素,依据是它们具有不同的质子数(或核电荷数)。
(2)①元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量,同一周期,原子序数逐渐增大,则锌的原子序数为30,原子中,核电荷数=核内质子数=核外电子数=原子序数,故根据元素周期表的规律可知锌原子的核电荷数为30。
②在金属活动性顺序表中,金属活动性Zn>H>Cu,铜和稀硫酸不反应,锌和稀硫酸反应生成硫酸锌和氢气,锌和硫酸铜反应生成硫酸锌和铜,故若要比较Cu与Zn的活动性强弱,实验方案为方案一:将铜和锌分别投入稀硫酸中,有大量气泡产生的是锌,无现象的为铜。方案二:锌片插入硫酸铜溶液中,锌片表面产生一层红色物质。
【点睛】
在金属活动性顺序中,金属的位置越靠前,它的活动性越强,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来。
16.镁
②
①②
质子数
中子数
117
【分析】
【详解】
(1)根据元素周期表中的元素排序,①号元素是锂元素,②号元素是氟元素,③号元素是镁元素,其中①③是金属元素,②是非金属元素,①②位于同一周期。
(2)元素是指据有相同质子数(或核电荷数)的同一类原子的总称,因此氕、氘、氚的质子数相同,中子数不同;
(3)在原子中,质子数=核电荷数=核外电子数,则原子的核外电子数是117。
17.101
BD
【详解】
(1)在原子中,质子数=核电荷数=原子序数=核外电子数,钔的质子数为101,根据核外电子数等于质子数可知,它的核外电子数为101。
(2)A.元素周期表是按照原子序数,也就是原子里面的质子数的大小进行排列的,故A错误;
B.门捷列夫发现了“相似化学性质的元素放同一列”原则,据此对已经发现的元素的相对原子质量进行了修正,故B正确;
C.门捷列夫得到的元素周期表并不是他独创的,而是在前面大量科学家的研究结果之上,再加上自己的仔细研究才得到的,故C错误;
D.门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实,故D正确;
D.在科学界,科学家的荣誉都是建立在实实在在的研究成果之上的,和他本身的威望没有多大关系,故D错误。
故选BD。
18.Mg
Na
3个汞原子
氢气或一个氢分子
【详解】
(1)镁元素用元素符号Mg表示,故填Mg;
(2)钠原子用元素符号Na代表钠原子,故填Na;
(3)3Hg代表对汞原子有个数描述,故填3个汞原子;
(4)可以代表氢气,同时也可以代表代表一个氢分子,故填氢气或一个氢分子。
19.稳定
氯
【分析】
元素发生化学变化的难易程度,与该元素最外层的电子个数有关,另外最外层电子个数相同的元素,其化学性质会具备一定的相似性。
【详解】
(1)每一周期结尾的是稀有气体元素,其最外层是最稳定的2个或者8个电子结构所以它们的化学性质稳定,答案:稳定;
(2)根据周期表的元素排列规律,锂与钠、碳与硅的化学性质相似,是因为它们的最外层电子个数相同,那么与氟化学性质相似的元素其最外层电子个数要与其一样,从图中可以看出,该元素为氯(Cl),答案:氯。
【点睛】
化学元素周期表的规律特点。
20.N2
核外电子层数
得到
A
【详解】
(1)表中元素②为氮元素,氮元素形成的单质为氮气,化学式为N2。
(2)分析元素原子的核外电子排布可知,3至10号元素的原子核外均有2个电子层,11至18号元素的原子核外均有3个电子层,可以得到的规律是每个周期元素的原子核外电子层数相同。
(3)表中9号和17号元素的最外层电子数均为7,都易得到1个电子形成稳定结构。
(4)元素是具有相同核电荷数(即质子数)的一类原子的总称,所以不同种元素间最本质的区别是核电荷数(即质子数)不同,故选A。
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
