2020—2021学年浙教版科学八年级下册阶段滚动检测试卷(七)测试范围 第3章 空气与生命 3.1~3.4
文档属性
| 名称 | 2020—2021学年浙教版科学八年级下册阶段滚动检测试卷(七)测试范围 第3章 空气与生命 3.1~3.4 |
|
|
| 格式 | docx | ||
| 文件大小 | 733.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-04-06 00:00:00 | ||
图片预览


文档简介
阶段滚动检测(七)
[测试范围:3.1~3.4 时间:30分钟 分值:100分]
一、选择题(每题5分,共45分)
1.节日期间商场里顾客很多,有人感觉到闷热缺氧,测定此时商场内空气中氧气的体积分数,其结果可能是( )
A.1%
B.19%
C.25%
D.78%
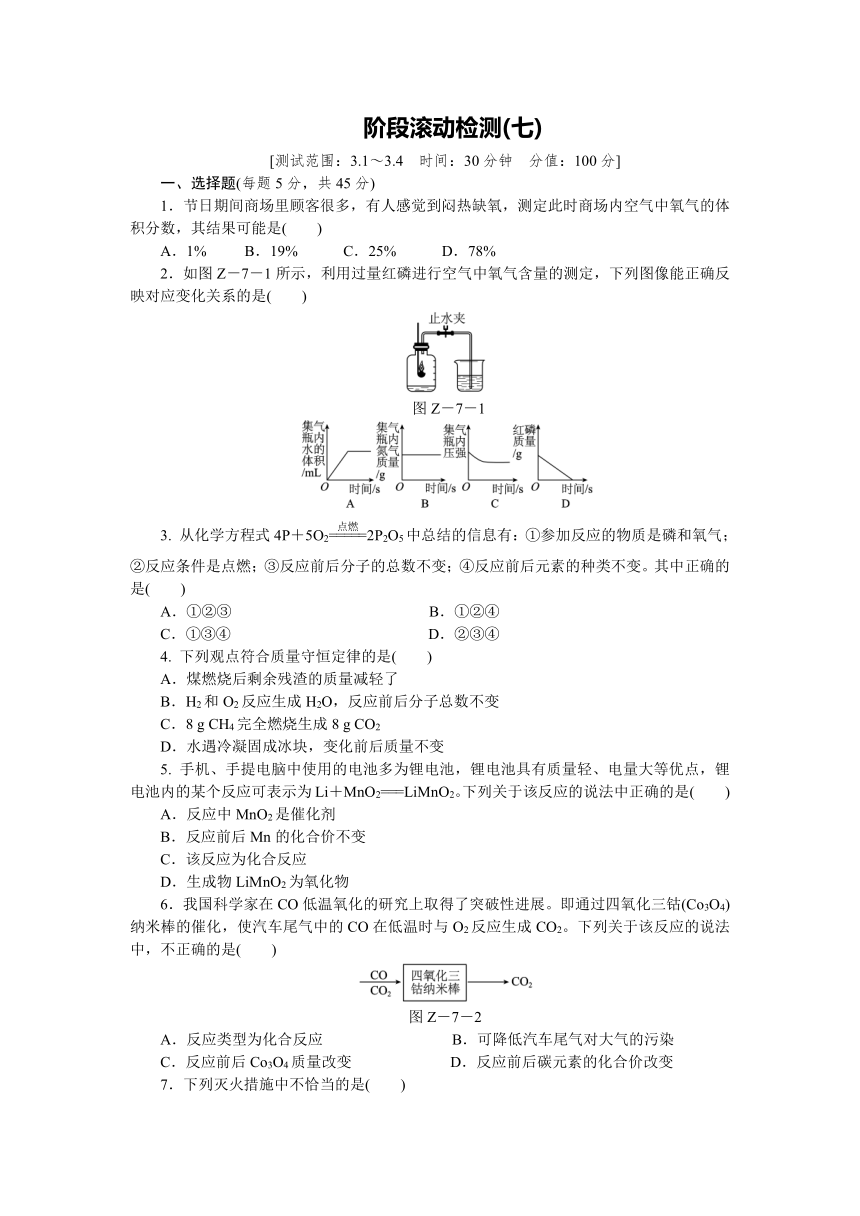
2.如图Z-7-1所示,利用过量红磷进行空气中氧气含量的测定,下列图像能正确反映对应变化关系的是( )
图Z-7-1
3.
从化学方程式4P+5O22P2O5中总结的信息有:①参加反应的物质是磷和氧气;②反应条件是点燃;③反应前后分子的总数不变;④反应前后元素的种类不变。其中正确的是( )
A.①②③
B.①②④
C.①③④
D.②③④
4.
下列观点符合质量守恒定律的是( )
A.煤燃烧后剩余残渣的质量减轻了
B.H2和O2反应生成H2O,反应前后分子总数不变
C.8
g
CH4完全燃烧生成8
g
CO2
D.水遇冷凝固成冰块,变化前后质量不变
5.
手机、手提电脑中使用的电池多为锂电池,锂电池具有质量轻、电量大等优点,锂电池内的某个反应可表示为Li+MnO2===LiMnO2。下列关于该反应的说法中正确的是( )
A.反应中MnO2是催化剂
B.反应前后Mn的化合价不变
C.该反应为化合反应
D.生成物LiMnO2为氧化物
6.我国科学家在CO低温氧化的研究上取得了突破性进展。即通过四氧化三钴(Co3O4)纳米棒的催化,使汽车尾气中的CO在低温时与O2反应生成CO2。下列关于该反应的说法中,不正确的是( )
图Z-7-2
A.反应类型为化合反应
B.可降低汽车尾气对大气的污染
C.反应前后Co3O4质量改变
D.反应前后碳元素的化合价改变
7.下列灭火措施中不恰当的是( )
①炒菜时,锅里的油起火应采取的最佳灭火措施是端下油锅
②秸秆、柴草着火,用水泼灭
③熄灭酒精灯最好用嘴吹灭
④电器着火,最先应当切断电源,再用干粉灭火器灭火
⑤汽油着火,应该立即用水浇灭
⑥洒在实验桌上的酒精着火,应用湿抹布盖灭
A.①③⑤
B.②④⑥
C.①③⑥
D.②③⑤
8.15%的H2O2溶液在二氧化锰的催化作用下会剧烈反应产生O2。实验室欲利用15%的H2O2溶液制取O2,则下列装置中,仪器选择和药品放置最合理的是( )
9.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法中不正确的是( )
物质
甲
乙
丙
丁
反应前物质质量/g
8
32
5
4
反应后物质质量/g
16
4
x
24
A.该反应为分解反应
B.丙可能是该反应的催化剂
C.甲、乙两种物质的质量变化之比为1∶4
D.乙、丁两种物质的质量变化之比为7∶5
二、填空题(共34分)
10.(16分)下列事实说明空气中含有哪些成分。
(1)空气是制造氮肥的原料:________。
(2)长期放在空气中的澄清石灰水表面有一层白色固体:________,其反应的化学方程式为______________________________________。
11.(18分)小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见下表。
收集方法
向上排空气法
排水法
氧气浓度/%
79.6
79.7
79.9
90.0
89.8
89.3
氧气平均浓度/%
79.7
89.7
(1)小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星的木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到____________________为氧气集满的标准。
(2)以上两种方法中,__________法收集到的氧气更纯净。
(3)向上排空气法收集到的氧气浓度只有80%左右的原因有________。
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星的木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
三、实验探究题(共21分)
12.某科学兴趣小组对“测定空气中氧气含量”的实验进行了改进:将数显设备、气体压强传感器和空气中氧气含量测量装置按图Z-7-3连接。装置气密性良好,调节右边敞口容器和集气瓶里的水面相平,此时集气瓶内气体的体积为V1。关闭止水夹,点燃燃烧匙内的红磷,立即塞紧瓶塞,待火焰熄灭后,过一段时间打开止水夹,观察到集气瓶中的水位上升。待集气瓶内的水面不再上升时,集气瓶内的气体体积为V2。然后向右边容器内加入一定量的水至两边水面再次相平,此时集气瓶内的气体体积为V3。在点燃红磷至打开止水夹这一过程中,观察到数显设备显示集气瓶内的气体压强先上升后下降,再趋于稳定。
图Z-7-3
(1)数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的气压变化量________(填“大于”“等于”或“小于”)氧气量减少导致的气压变化量。
(2)基于数显设备显示的气压变化,“过一段时间打开止水夹”中的“一段时间”指的是火焰熄灭后到____________________所经历的时间。
(3)在整个实验过程中,集气瓶中减少的氧气体积为__________(填“V1-V2”“V1-V3”或“V2-V3”)。
详解详析
1.B
2.B [解析]
集气瓶内反应前已有少量水,故集气瓶内水的体积不能从0开始;集气瓶内氮气的质量不变;将燃着的红磷放入装置中,瞬间由于温度升高而使装置中的气体压强增大,随着红磷的燃烧,被消耗的氧气也随之增加,从而使瓶中压强降低,至氧气被消耗尽并且装置冷却后瓶中的压强不再改变;因为红磷是过量的,所以最终红磷质量不能为0。
3.B [解析]
由化学方程式4P+5O22P2O5可知,参加反应的物质是磷和氧气,反应条件是点燃,反应前后元素的种类不变。
4.A 5.C
6.C [解析]
根据题意可以知道反应物为一氧化碳和氧气,而生成物为二氧化碳,故该反应为化合反应;通过Co3O4纳米棒的催化可以将一氧化碳转化为二氧化碳,所以可以减少对空气的污染;催化剂在反应前后质量和化学性质不变,所以反应前后Co3O4的质量不变;反应前一氧化碳中碳元素的化合价为+2,而反应后二氧化碳中碳元素的化合价为+4。
7.A 8.D
9.C [解析]
根据质量守恒定律可知,在化学反应中,参加反应的各物质的质量总和等于反应后生成的各物质的质量总和,反应后质量增加的是生成物,减少的是反应物。由表格信息可知反应后甲质量增加了16
g-8
g=8
g,是生成物;丁质量增加了24
g-4
g=20
g,是生成物;乙质量减少了32
g-4
g=28
g,为反应物,故可知丙反应后质量为5
g,可能是催化剂。反应符合“一变多”的特点,为分解反应。
10.(1)氮气(或N2)
(2)二氧化碳(或CO2)
CO2+Ca(OH)2===CaCO3↓+H2O
[解析]
(1)含有氮元素的肥料称为氮肥,空气是制造氮肥的原料,说明空气中含有氮气。
(2)二氧化碳能使澄清石灰水变浑浊,石灰水长期放在空气中会变浑浊,说明空气中含有二氧化碳。
11.(1)集气瓶口有气泡冒出(或瓶中的水排尽)
(2)排水 (3)ACD
12.(1)大于
(2)集气瓶内的温度恢复到室温(或数显设备的示数不再改变或集气瓶内的气压保持稳定)
(3)V1-V3
[测试范围:3.1~3.4 时间:30分钟 分值:100分]
一、选择题(每题5分,共45分)
1.节日期间商场里顾客很多,有人感觉到闷热缺氧,测定此时商场内空气中氧气的体积分数,其结果可能是( )
A.1%
B.19%
C.25%
D.78%
2.如图Z-7-1所示,利用过量红磷进行空气中氧气含量的测定,下列图像能正确反映对应变化关系的是( )
图Z-7-1
3.
从化学方程式4P+5O22P2O5中总结的信息有:①参加反应的物质是磷和氧气;②反应条件是点燃;③反应前后分子的总数不变;④反应前后元素的种类不变。其中正确的是( )
A.①②③
B.①②④
C.①③④
D.②③④
4.
下列观点符合质量守恒定律的是( )
A.煤燃烧后剩余残渣的质量减轻了
B.H2和O2反应生成H2O,反应前后分子总数不变
C.8
g
CH4完全燃烧生成8
g
CO2
D.水遇冷凝固成冰块,变化前后质量不变
5.
手机、手提电脑中使用的电池多为锂电池,锂电池具有质量轻、电量大等优点,锂电池内的某个反应可表示为Li+MnO2===LiMnO2。下列关于该反应的说法中正确的是( )
A.反应中MnO2是催化剂
B.反应前后Mn的化合价不变
C.该反应为化合反应
D.生成物LiMnO2为氧化物
6.我国科学家在CO低温氧化的研究上取得了突破性进展。即通过四氧化三钴(Co3O4)纳米棒的催化,使汽车尾气中的CO在低温时与O2反应生成CO2。下列关于该反应的说法中,不正确的是( )
图Z-7-2
A.反应类型为化合反应
B.可降低汽车尾气对大气的污染
C.反应前后Co3O4质量改变
D.反应前后碳元素的化合价改变
7.下列灭火措施中不恰当的是( )
①炒菜时,锅里的油起火应采取的最佳灭火措施是端下油锅
②秸秆、柴草着火,用水泼灭
③熄灭酒精灯最好用嘴吹灭
④电器着火,最先应当切断电源,再用干粉灭火器灭火
⑤汽油着火,应该立即用水浇灭
⑥洒在实验桌上的酒精着火,应用湿抹布盖灭
A.①③⑤
B.②④⑥
C.①③⑥
D.②③⑤
8.15%的H2O2溶液在二氧化锰的催化作用下会剧烈反应产生O2。实验室欲利用15%的H2O2溶液制取O2,则下列装置中,仪器选择和药品放置最合理的是( )
9.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法中不正确的是( )
物质
甲
乙
丙
丁
反应前物质质量/g
8
32
5
4
反应后物质质量/g
16
4
x
24
A.该反应为分解反应
B.丙可能是该反应的催化剂
C.甲、乙两种物质的质量变化之比为1∶4
D.乙、丁两种物质的质量变化之比为7∶5
二、填空题(共34分)
10.(16分)下列事实说明空气中含有哪些成分。
(1)空气是制造氮肥的原料:________。
(2)长期放在空气中的澄清石灰水表面有一层白色固体:________,其反应的化学方程式为______________________________________。
11.(18分)小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见下表。
收集方法
向上排空气法
排水法
氧气浓度/%
79.6
79.7
79.9
90.0
89.8
89.3
氧气平均浓度/%
79.7
89.7
(1)小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星的木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到____________________为氧气集满的标准。
(2)以上两种方法中,__________法收集到的氧气更纯净。
(3)向上排空气法收集到的氧气浓度只有80%左右的原因有________。
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星的木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
三、实验探究题(共21分)
12.某科学兴趣小组对“测定空气中氧气含量”的实验进行了改进:将数显设备、气体压强传感器和空气中氧气含量测量装置按图Z-7-3连接。装置气密性良好,调节右边敞口容器和集气瓶里的水面相平,此时集气瓶内气体的体积为V1。关闭止水夹,点燃燃烧匙内的红磷,立即塞紧瓶塞,待火焰熄灭后,过一段时间打开止水夹,观察到集气瓶中的水位上升。待集气瓶内的水面不再上升时,集气瓶内的气体体积为V2。然后向右边容器内加入一定量的水至两边水面再次相平,此时集气瓶内的气体体积为V3。在点燃红磷至打开止水夹这一过程中,观察到数显设备显示集气瓶内的气体压强先上升后下降,再趋于稳定。
图Z-7-3
(1)数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的气压变化量________(填“大于”“等于”或“小于”)氧气量减少导致的气压变化量。
(2)基于数显设备显示的气压变化,“过一段时间打开止水夹”中的“一段时间”指的是火焰熄灭后到____________________所经历的时间。
(3)在整个实验过程中,集气瓶中减少的氧气体积为__________(填“V1-V2”“V1-V3”或“V2-V3”)。
详解详析
1.B
2.B [解析]
集气瓶内反应前已有少量水,故集气瓶内水的体积不能从0开始;集气瓶内氮气的质量不变;将燃着的红磷放入装置中,瞬间由于温度升高而使装置中的气体压强增大,随着红磷的燃烧,被消耗的氧气也随之增加,从而使瓶中压强降低,至氧气被消耗尽并且装置冷却后瓶中的压强不再改变;因为红磷是过量的,所以最终红磷质量不能为0。
3.B [解析]
由化学方程式4P+5O22P2O5可知,参加反应的物质是磷和氧气,反应条件是点燃,反应前后元素的种类不变。
4.A 5.C
6.C [解析]
根据题意可以知道反应物为一氧化碳和氧气,而生成物为二氧化碳,故该反应为化合反应;通过Co3O4纳米棒的催化可以将一氧化碳转化为二氧化碳,所以可以减少对空气的污染;催化剂在反应前后质量和化学性质不变,所以反应前后Co3O4的质量不变;反应前一氧化碳中碳元素的化合价为+2,而反应后二氧化碳中碳元素的化合价为+4。
7.A 8.D
9.C [解析]
根据质量守恒定律可知,在化学反应中,参加反应的各物质的质量总和等于反应后生成的各物质的质量总和,反应后质量增加的是生成物,减少的是反应物。由表格信息可知反应后甲质量增加了16
g-8
g=8
g,是生成物;丁质量增加了24
g-4
g=20
g,是生成物;乙质量减少了32
g-4
g=28
g,为反应物,故可知丙反应后质量为5
g,可能是催化剂。反应符合“一变多”的特点,为分解反应。
10.(1)氮气(或N2)
(2)二氧化碳(或CO2)
CO2+Ca(OH)2===CaCO3↓+H2O
[解析]
(1)含有氮元素的肥料称为氮肥,空气是制造氮肥的原料,说明空气中含有氮气。
(2)二氧化碳能使澄清石灰水变浑浊,石灰水长期放在空气中会变浑浊,说明空气中含有二氧化碳。
11.(1)集气瓶口有气泡冒出(或瓶中的水排尽)
(2)排水 (3)ACD
12.(1)大于
(2)集气瓶内的温度恢复到室温(或数显设备的示数不再改变或集气瓶内的气压保持稳定)
(3)V1-V3
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
