沪教版九年级下册化学课件 第六章 6.2.2 溶质质量分数的综合计算(ppt 共28张)
文档属性
| 名称 | 沪教版九年级下册化学课件 第六章 6.2.2 溶质质量分数的综合计算(ppt 共28张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 725.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-14 00:00:00 | ||
图片预览






文档简介
第2节 溶液组成的表示
第2课时
溶质质量分数的综合计算
第6章 溶解现象
提示:点击 进入习题
答案呈现
见习题
见习题
见习题
1
2
3
4
见习题
5
见习题
见习题
见习题
见习题
6
7
8
1.【中考·重庆B改编】84消毒液的有效成分是次氯酸钠(NaClO),次氯酸钠工业制法的反应原理是Cl2+2NaOH===NaClO+NaCl+H2O。某同学将Cl2通入185.8 g NaOH溶液中(NaOH过量),充分反应后得到混合溶液200 g。计算:
(1)参加反应的氯气质量是多少克。
(2)混合溶液中次氯酸钠的质量分数。
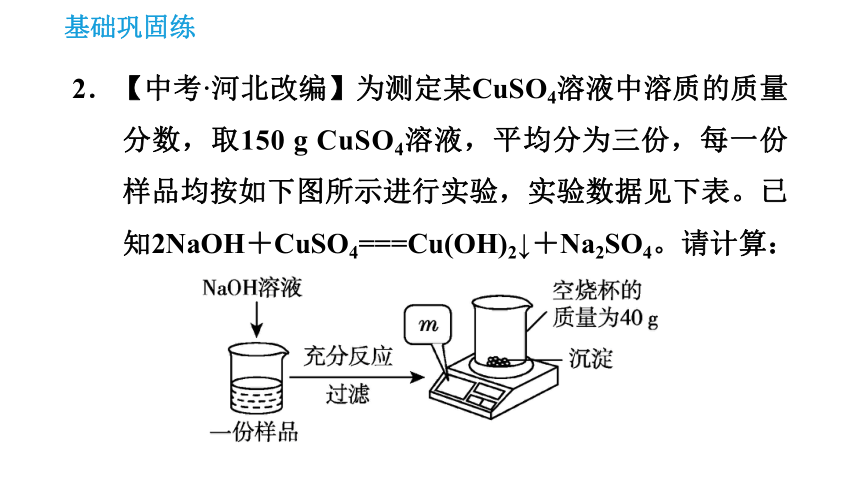
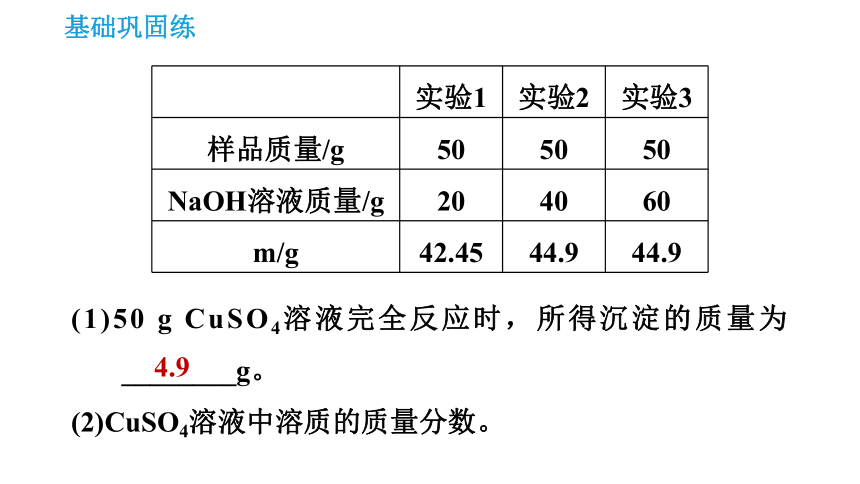
2.【中考·河北改编】为测定某CuSO4溶液中溶质的质量分数,取150 g CuSO4溶液,平均分为三份,每一份样品均按如下图所示进行实验,实验数据见下表。已知2NaOH+CuSO4===Cu(OH)2↓+Na2SO4。请计算:
(1)50 g CuSO4溶液完全反应时,所得沉淀的质量为________g。
(2)CuSO4溶液中溶质的质量分数。
4.9
?
实验1
实验2
实验3
样品质量/g
50
50
50
NaOH溶液质量/g
20
40
60
m/g
42.45
44.9
44.9
3.【中考·河北改编】小明用某纯碱样品(含少量氯化钠)进行了如图所示的实验,请计算:
?
?
已知反应的化学方程式为
Na2CO3+2HCl===2NaCl+H2O+CO2↑。
(1) 生成二氧化碳的总质量为________g。
(2) 所用稀盐酸的溶质质量分数。
4.4
4.实验室用68 g过氧化氢溶液和2 g二氧
化锰制取氧气,实验的相关数据如图。
请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的________________都没有发生变化。
(2)反应生成氧气的质量为________g。
(3)参加反应的过氧化氢溶液的质量分数是多少?
化学性质和质量
1.6
5.【中考·宜昌】实验室常用大理石和稀盐酸制取二氧化碳,现取25 g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与酸
反应),剩余固体质量与加入稀盐
酸的质量关系如图。求:
(1)25 g大理石中碳酸钙的质量。
(2)恰好完全反应时所得溶液中溶质的质量分数。
6.【中考·齐齐哈尔】合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了如图所示实验:
请计算:
(1)生成氢气的质量为多少克,黄铜中锌的质量为多少克;
(2)过滤后所得溶液的溶质质量分数。
7.【中考·益阳】某研究性学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品 5 g,把 60 g 稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。根据实验数据计算:
实验次数
1
2
3
4
加入稀盐酸的质量/g
15
15
15
15
剩余固体的质量/g
3.50
2.00
0.75
0.75
(1)石灰石样品中碳酸钙的质量分数为________。
85%
(2)求原 60 g 稀盐酸中溶质质量分数(要求书写计算过程)。
8.【中考·滨州改编】将1.17 g氯化钠固体放入烧杯中,加入51.7 g水充分溶解后得到常温下的氯化钠溶液,再向所得溶液中逐滴滴入100 g一定溶质质量分数的硝酸银溶液。实验过程中生成沉淀的质量与滴入硝酸银溶液的质量关系如图所示。
已知:NaCl+AgNO3===
NaNO3+AgCl↓。
(1)B点时,溶液中所含硝酸银的质量为多少克?
(2)A点时,所得溶液中溶质质量分数为多少?(计算结果精确到0.1%)
第2课时
溶质质量分数的综合计算
第6章 溶解现象
提示:点击 进入习题
答案呈现
见习题
见习题
见习题
1
2
3
4
见习题
5
见习题
见习题
见习题
见习题
6
7
8
1.【中考·重庆B改编】84消毒液的有效成分是次氯酸钠(NaClO),次氯酸钠工业制法的反应原理是Cl2+2NaOH===NaClO+NaCl+H2O。某同学将Cl2通入185.8 g NaOH溶液中(NaOH过量),充分反应后得到混合溶液200 g。计算:
(1)参加反应的氯气质量是多少克。
(2)混合溶液中次氯酸钠的质量分数。
2.【中考·河北改编】为测定某CuSO4溶液中溶质的质量分数,取150 g CuSO4溶液,平均分为三份,每一份样品均按如下图所示进行实验,实验数据见下表。已知2NaOH+CuSO4===Cu(OH)2↓+Na2SO4。请计算:
(1)50 g CuSO4溶液完全反应时,所得沉淀的质量为________g。
(2)CuSO4溶液中溶质的质量分数。
4.9
?
实验1
实验2
实验3
样品质量/g
50
50
50
NaOH溶液质量/g
20
40
60
m/g
42.45
44.9
44.9
3.【中考·河北改编】小明用某纯碱样品(含少量氯化钠)进行了如图所示的实验,请计算:
?
?
已知反应的化学方程式为
Na2CO3+2HCl===2NaCl+H2O+CO2↑。
(1) 生成二氧化碳的总质量为________g。
(2) 所用稀盐酸的溶质质量分数。
4.4
4.实验室用68 g过氧化氢溶液和2 g二氧
化锰制取氧气,实验的相关数据如图。
请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的________________都没有发生变化。
(2)反应生成氧气的质量为________g。
(3)参加反应的过氧化氢溶液的质量分数是多少?
化学性质和质量
1.6
5.【中考·宜昌】实验室常用大理石和稀盐酸制取二氧化碳,现取25 g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与酸
反应),剩余固体质量与加入稀盐
酸的质量关系如图。求:
(1)25 g大理石中碳酸钙的质量。
(2)恰好完全反应时所得溶液中溶质的质量分数。
6.【中考·齐齐哈尔】合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了如图所示实验:
请计算:
(1)生成氢气的质量为多少克,黄铜中锌的质量为多少克;
(2)过滤后所得溶液的溶质质量分数。
7.【中考·益阳】某研究性学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品 5 g,把 60 g 稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。根据实验数据计算:
实验次数
1
2
3
4
加入稀盐酸的质量/g
15
15
15
15
剩余固体的质量/g
3.50
2.00
0.75
0.75
(1)石灰石样品中碳酸钙的质量分数为________。
85%
(2)求原 60 g 稀盐酸中溶质质量分数(要求书写计算过程)。
8.【中考·滨州改编】将1.17 g氯化钠固体放入烧杯中,加入51.7 g水充分溶解后得到常温下的氯化钠溶液,再向所得溶液中逐滴滴入100 g一定溶质质量分数的硝酸银溶液。实验过程中生成沉淀的质量与滴入硝酸银溶液的质量关系如图所示。
已知:NaCl+AgNO3===
NaNO3+AgCl↓。
(1)B点时,溶液中所含硝酸银的质量为多少克?
(2)A点时,所得溶液中溶质质量分数为多少?(计算结果精确到0.1%)
