沪教版九年级下册化学课件 第六章 基础实验5 配制一定溶质质量分数的氯化钠溶液(ppt 共25张)
文档属性
| 名称 | 沪教版九年级下册化学课件 第六章 基础实验5 配制一定溶质质量分数的氯化钠溶液(ppt 共25张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 644.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-14 00:00:00 | ||
图片预览








文档简介
基础实验5
配制一定溶质质量分数的氯化钠溶液
第6章 溶解现象
提示:点击 进入习题
答案呈现
B
C
D
1
2
3
4
C
5
B
B
B
A
6
7
8
9
见习题
10
见习题
B
60;400
见习题
11
12
13
14
(1)玻璃棒 (2)溶解 (3)75 (4)>
15
(1)量筒 (2)溶质 (3)B
1.要配制100 g 5%的NaCl溶液,除了需要托盘天平和量筒外,还需要用到的一组仪器是( )
A.烧杯、试管、玻璃棒
B.烧杯、胶头滴管、玻璃棒
C.烧杯、胶头滴管、漏斗
D.烧杯、酒精灯、玻璃棒
B
2.用硝酸钾固体配制溶质质量分数为10%的硝酸钾溶液50 g,下列做法不正确的是( )
A.称量:用天平称量硝酸钾5 g
B.量取:用量筒量取蒸馏水45 mL
C.溶解:将硝酸钾倒入量筒中溶解
D.转移:将配好的溶液转移至试剂瓶
C
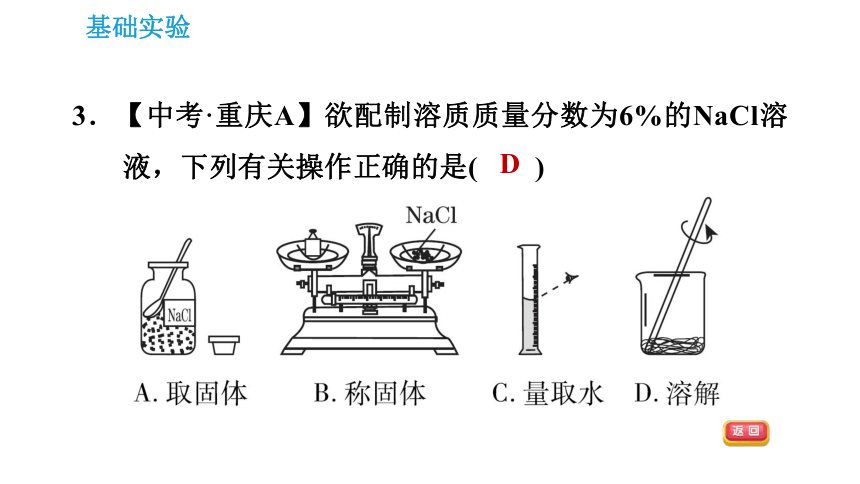
3.【中考·重庆A】欲配制溶质质量分数为6%的NaCl溶液,下列有关操作正确的是( )
D
4.【中考·常德】某同学欲配制50 g 5%的氯化钠溶液,下列说法中正确的是( )
A.用蒸馏水洗涤试剂瓶后立即盛装配好的氯化钠溶液
B.用500 mL的量筒量取所需要的水
C.用托盘天平准确称取氯化钠固体2.5 g
D.氯化钠固体溶解时,用玻璃棒搅拌的目的是增大其在水中的溶解度
C
5.【中考·宁夏】在配制100 g溶质质量分数为10%的氢氧化钠溶液的过程中,下列操作正确的是( )
A.用量筒量取90 mL水时俯视读数
B.氢氧化钠易潮解,且腐蚀性强,应放在玻璃器皿中称量
C.用蒸馏水洗涤烧杯后,立即溶解氢氧化钠
D.实验过程中,用到的玻璃仪器只有烧杯和量筒
B
6.【中考·山西】配制50 g质量分数为5%的硝酸钾溶液,作为无土栽培所需的营养液。溶解过程中硝酸钾的质量分数随时间的变化关系如图所示,观察图像,分析形成这种结果的原因是( )
A.所用硝酸钾固体中含有水分
B.用量筒量取水时俯视刻度线
C.硝酸钾固体溶解前所用的烧杯内有水
D.配好的溶液装瓶时部分液体洒落到试剂瓶外
【点拨】配制50 g质量分数为5%的硝酸钾溶液时,根据图示可知,实际所配得溶液的溶质质量分数大于5%,若硝酸钾固体中含有水分,则实际所配得的溶液溶质质量分数应小于5%;若用量筒量取水时俯视刻度线,则量取的液体体积偏小,配制溶液的溶质质量分数偏大;若硝酸钾固体溶解前所用的烧杯内有水,则所配制的溶液的溶质质量分数应该偏小;配好的溶液装瓶时部分液体洒落到试剂瓶外,不影响所得溶液的溶质质量分数。
【答案】B
7.【中考·无锡】泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%。在配制4%的食盐水时,会导致溶液浓度偏小的是( )
①将称量好的食盐倒入烧杯时,有少许撒出
②量取水的体积时,俯视量筒刻度线
③溶解食盐的烧杯内壁是潮湿的
④用4 g食盐和100 g水配制溶液
A.②③ B.①③④ C.①②③ D.①②③④
【答案】B
8.【中考·滨州】小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳
的操作,其他操作均正确)。
小芳实际配制的氯化钠溶
液的溶质质量分数约为(水
的密度为1 g/cm3)( )
? A.12.4% B.17.2%
C.16.9% D.12.5%
【答案】A
9.【中考·北京】从下图选择仪器,配制60 g溶质质量分数为10%的NaCl溶液。
?
(1)需要称量NaCl的质量为______g。
(2)量取水用到的仪器有_______________________(写名称)。
(3)从配好的溶液中倒出10g,其中溶质和溶剂的质量比为_____。
6
100 mL量筒、胶头滴管
1∶9
10.【中考·邵阳】某同学配制50 g 6%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
?
?
(1)配制溶液的正确操作顺序为__________________(填序号,下同),其中操作错误的是____________。
②①⑤③④
①
(2)图②中盛放氯化钠固体的仪器名称是________,需称取氯化钠________g。
(3)量取水时选用的量筒的量程最合适的是_____(填序号),读数时视线要与量筒内_________________保持水平。
A.10 mL B.25 mL
C.50 mL D.100 mL
广口瓶
3
C
凹液面的最低处
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是________(填序号)。
A.氯化钠固体不纯
B.用生锈砝码称量
C.装瓶时有少量溶液洒出
D.溶解时烧杯内壁有水珠
A、D
11.【中考·兰州】实验室用质量分数为6%的氯化钠溶液(密度约为1.04 g/cm3)配制50 g质量分数为3%的氯化钠溶液。下列说法正确的是( )
A.需要加水的质量是50 g
B.量取水时俯视读数会使所配溶液的浓度偏大
C.玻璃棒的作用是加速水挥发
D.量取6%的氯化钠溶液时选用100 mL的量筒
B
12.过氧化氢溶液因产物没有污染而被称为绿色消毒剂,可用于家庭消毒。如图为某品牌过氧化氢溶液说明书,用该品牌过氧化氢溶液
配制600 g 10%的过
氧化氢溶液用于消
毒,请回答下列问
题:
600 g 10%的过氧化氢溶液中含有________g溶质,配制该溶液时需要在原溶液中加入________g水进行稀释。
60
400
13.已知市售浓盐酸的溶质质量分数为37%,密度为1.18 g/mL。进行实验室制取二氧化碳的分组实验需要溶质质量分数为4%的稀盐酸500 g,请帮老师完成该稀盐酸的配制。
(1)在实验室用浓盐酸配制稀盐酸的主要步骤有:计算、________、混匀、冷却至室温装瓶并贴上标签。
(2)用浓溶液配制稀溶液时,计算的依据是___________________________________。
量取
溶液稀释前后,溶质的质量不变
(3)计算:所需浓盐酸的体积为________mL,水的体积为________mL。(结果保留整数)
(4)量取:所需仪器是____________、_____________、____________。(注明量筒的规格)
(5)配制:将水沿容器壁缓缓倒入盛浓盐酸的烧杯中,并用________不断搅拌。
(6)装瓶贴标签。
46
446
50 mL量筒
500 mL量筒
胶头滴管
玻璃棒
14.【中考·丹东】小莉、小晶两位同学用如下两种不同的方法,配制100 g溶质质量分数为5%的氯化钠溶液。
【小莉用固体氯化钠和水配制溶液】
(1)小莉用到的玻璃仪器有量筒、胶头滴管、烧杯、______________和试剂瓶。
(2)小莉实验时应进行的步骤是计算、称量、量取、________、装瓶并贴标签。
玻璃棒
溶解
【小晶用溶质质量分数为20%的氯化钠溶液加水稀释】
(3)小晶实验时应量取水的体积是________mL。(水的密度可近似看作1 g/cm3)
(4)若小晶量取水时俯视读数,则所配溶液的溶质质量分数________(填“>”“<”或“=”)5%。
75
>
15.【中考·长春改编】在实验室里配制100 g溶质的质量分数为10%的NaCl溶液。
(1)用NaCl固体和蒸馏水配制溶液时,用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和________。
(2)用浓溶液配制稀溶液时,计算的依据是稀释前后的________质量保持不变。
(3)下列配制方法可以达到上述实验目的的是___________。
A.将10 g NaCl固体与100 g水混合溶解
B.向50 g溶质的质量分数为20%的NaCl溶液中加入50 g水
量筒
溶质
B
配制一定溶质质量分数的氯化钠溶液
第6章 溶解现象
提示:点击 进入习题
答案呈现
B
C
D
1
2
3
4
C
5
B
B
B
A
6
7
8
9
见习题
10
见习题
B
60;400
见习题
11
12
13
14
(1)玻璃棒 (2)溶解 (3)75 (4)>
15
(1)量筒 (2)溶质 (3)B
1.要配制100 g 5%的NaCl溶液,除了需要托盘天平和量筒外,还需要用到的一组仪器是( )
A.烧杯、试管、玻璃棒
B.烧杯、胶头滴管、玻璃棒
C.烧杯、胶头滴管、漏斗
D.烧杯、酒精灯、玻璃棒
B
2.用硝酸钾固体配制溶质质量分数为10%的硝酸钾溶液50 g,下列做法不正确的是( )
A.称量:用天平称量硝酸钾5 g
B.量取:用量筒量取蒸馏水45 mL
C.溶解:将硝酸钾倒入量筒中溶解
D.转移:将配好的溶液转移至试剂瓶
C
3.【中考·重庆A】欲配制溶质质量分数为6%的NaCl溶液,下列有关操作正确的是( )
D
4.【中考·常德】某同学欲配制50 g 5%的氯化钠溶液,下列说法中正确的是( )
A.用蒸馏水洗涤试剂瓶后立即盛装配好的氯化钠溶液
B.用500 mL的量筒量取所需要的水
C.用托盘天平准确称取氯化钠固体2.5 g
D.氯化钠固体溶解时,用玻璃棒搅拌的目的是增大其在水中的溶解度
C
5.【中考·宁夏】在配制100 g溶质质量分数为10%的氢氧化钠溶液的过程中,下列操作正确的是( )
A.用量筒量取90 mL水时俯视读数
B.氢氧化钠易潮解,且腐蚀性强,应放在玻璃器皿中称量
C.用蒸馏水洗涤烧杯后,立即溶解氢氧化钠
D.实验过程中,用到的玻璃仪器只有烧杯和量筒
B
6.【中考·山西】配制50 g质量分数为5%的硝酸钾溶液,作为无土栽培所需的营养液。溶解过程中硝酸钾的质量分数随时间的变化关系如图所示,观察图像,分析形成这种结果的原因是( )
A.所用硝酸钾固体中含有水分
B.用量筒量取水时俯视刻度线
C.硝酸钾固体溶解前所用的烧杯内有水
D.配好的溶液装瓶时部分液体洒落到试剂瓶外
【点拨】配制50 g质量分数为5%的硝酸钾溶液时,根据图示可知,实际所配得溶液的溶质质量分数大于5%,若硝酸钾固体中含有水分,则实际所配得的溶液溶质质量分数应小于5%;若用量筒量取水时俯视刻度线,则量取的液体体积偏小,配制溶液的溶质质量分数偏大;若硝酸钾固体溶解前所用的烧杯内有水,则所配制的溶液的溶质质量分数应该偏小;配好的溶液装瓶时部分液体洒落到试剂瓶外,不影响所得溶液的溶质质量分数。
【答案】B
7.【中考·无锡】泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%。在配制4%的食盐水时,会导致溶液浓度偏小的是( )
①将称量好的食盐倒入烧杯时,有少许撒出
②量取水的体积时,俯视量筒刻度线
③溶解食盐的烧杯内壁是潮湿的
④用4 g食盐和100 g水配制溶液
A.②③ B.①③④ C.①②③ D.①②③④
【答案】B
8.【中考·滨州】小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳
的操作,其他操作均正确)。
小芳实际配制的氯化钠溶
液的溶质质量分数约为(水
的密度为1 g/cm3)( )
? A.12.4% B.17.2%
C.16.9% D.12.5%
【答案】A
9.【中考·北京】从下图选择仪器,配制60 g溶质质量分数为10%的NaCl溶液。
?
(1)需要称量NaCl的质量为______g。
(2)量取水用到的仪器有_______________________(写名称)。
(3)从配好的溶液中倒出10g,其中溶质和溶剂的质量比为_____。
6
100 mL量筒、胶头滴管
1∶9
10.【中考·邵阳】某同学配制50 g 6%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
?
?
(1)配制溶液的正确操作顺序为__________________(填序号,下同),其中操作错误的是____________。
②①⑤③④
①
(2)图②中盛放氯化钠固体的仪器名称是________,需称取氯化钠________g。
(3)量取水时选用的量筒的量程最合适的是_____(填序号),读数时视线要与量筒内_________________保持水平。
A.10 mL B.25 mL
C.50 mL D.100 mL
广口瓶
3
C
凹液面的最低处
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是________(填序号)。
A.氯化钠固体不纯
B.用生锈砝码称量
C.装瓶时有少量溶液洒出
D.溶解时烧杯内壁有水珠
A、D
11.【中考·兰州】实验室用质量分数为6%的氯化钠溶液(密度约为1.04 g/cm3)配制50 g质量分数为3%的氯化钠溶液。下列说法正确的是( )
A.需要加水的质量是50 g
B.量取水时俯视读数会使所配溶液的浓度偏大
C.玻璃棒的作用是加速水挥发
D.量取6%的氯化钠溶液时选用100 mL的量筒
B
12.过氧化氢溶液因产物没有污染而被称为绿色消毒剂,可用于家庭消毒。如图为某品牌过氧化氢溶液说明书,用该品牌过氧化氢溶液
配制600 g 10%的过
氧化氢溶液用于消
毒,请回答下列问
题:
600 g 10%的过氧化氢溶液中含有________g溶质,配制该溶液时需要在原溶液中加入________g水进行稀释。
60
400
13.已知市售浓盐酸的溶质质量分数为37%,密度为1.18 g/mL。进行实验室制取二氧化碳的分组实验需要溶质质量分数为4%的稀盐酸500 g,请帮老师完成该稀盐酸的配制。
(1)在实验室用浓盐酸配制稀盐酸的主要步骤有:计算、________、混匀、冷却至室温装瓶并贴上标签。
(2)用浓溶液配制稀溶液时,计算的依据是___________________________________。
量取
溶液稀释前后,溶质的质量不变
(3)计算:所需浓盐酸的体积为________mL,水的体积为________mL。(结果保留整数)
(4)量取:所需仪器是____________、_____________、____________。(注明量筒的规格)
(5)配制:将水沿容器壁缓缓倒入盛浓盐酸的烧杯中,并用________不断搅拌。
(6)装瓶贴标签。
46
446
50 mL量筒
500 mL量筒
胶头滴管
玻璃棒
14.【中考·丹东】小莉、小晶两位同学用如下两种不同的方法,配制100 g溶质质量分数为5%的氯化钠溶液。
【小莉用固体氯化钠和水配制溶液】
(1)小莉用到的玻璃仪器有量筒、胶头滴管、烧杯、______________和试剂瓶。
(2)小莉实验时应进行的步骤是计算、称量、量取、________、装瓶并贴标签。
玻璃棒
溶解
【小晶用溶质质量分数为20%的氯化钠溶液加水稀释】
(3)小晶实验时应量取水的体积是________mL。(水的密度可近似看作1 g/cm3)
(4)若小晶量取水时俯视读数,则所配溶液的溶质质量分数________(填“>”“<”或“=”)5%。
75
>
15.【中考·长春改编】在实验室里配制100 g溶质的质量分数为10%的NaCl溶液。
(1)用NaCl固体和蒸馏水配制溶液时,用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和________。
(2)用浓溶液配制稀溶液时,计算的依据是稀释前后的________质量保持不变。
(3)下列配制方法可以达到上述实验目的的是___________。
A.将10 g NaCl固体与100 g水混合溶解
B.向50 g溶质的质量分数为20%的NaCl溶液中加入50 g水
量筒
溶质
B
