浙教版科学八年级下第2章第三节化学反应与质量守恒(讲义附练习)
文档属性
| 名称 | 浙教版科学八年级下第2章第三节化学反应与质量守恒(讲义附练习) |

|
|
| 格式 | zip | ||
| 文件大小 | 963.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2012-03-29 00:00:00 | ||
图片预览

文档简介
学生辅导讲义
时间:_________ 学生:_________ 教师:__________
课题 质量守恒定律
重点 质量守恒定律定义2.质量守恒定律运用
难点 探究质量守恒定律的实验
知识点梳理:
化学反应与质量守恒
化合反应和分解反应
(1)化合反应:A+B C
(2)分解反应:A B+C
质量守恒定律
定义:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,这个定律叫质量守恒定律。
质量守恒定律的解释
原子种类没有变化
反应前后 原子数目没有增减
(3)化学反应前后一定不变的量: ①原子种类 ② 元素种类 ③ 原子数目
④物质总质量
基础练习:
一、选择题(本题包括10小题,每小题2分,共20分。每小题只有1个选项符合题意)
1、化学反应遵守质量守恒定律的原因是( )
A、物质的种类没有变化 B、分子的种类不会发生变化
C、分子的数目不会改变 D、原子的种类、数目和质量都没有改变
2、下列变化中,属于化学变化,并且能用质量守恒定律解释是( )
木炭燃烧质量减少
B、5g水受热变成5g水蒸气
C、5g蔗糖溶解在95g水中,成为100g的蔗糖的水溶液
D、100mL水加入100mL酒精,成为体积小于200mL的溶液
3、关于质量守恒定律,下列叙述中正确的是( )
A、煤燃烧化为灰烬,该反应不符合质量守恒定律
B、24g镁在空气中完全燃烧生成40g氧化镁,实际消耗空气的质量为16g
C、一切化学反应都遵守质量守恒定律
D、质量守恒定律只适用于有气体或固体生成的化学反应
4、2003年10月16日,“神舟五号”安全返航,标志着我国载人航天技术取得历史性突破。火箭所用的燃料为偏二甲肼[(CH3)2N2H2],其主要反应为(CH3)2N2H2+N2O4→X+CO2+H2O,由此可知X中一定含有的元素是( )
A、碳 B、氢 C、氧 D、氮
5、已知A物质与B物质反应生成C物质,现有12gA与32gB恰好完全反应,则生成C物质的质量是( )
A、44g B、32g C、22g D、12g
6、已知A物质发生分解反应生成B物质和C物质,当一定量的A反应片刻后,生成56gB和44gC;则实际发生分解的A物质的质量为( )
A、12g B、44g C、56g D、100g
7、氯酸钾和二氧化锰的混合物共Ag,加热完全反应后得到Bg氧气和Cg氯化钾,则混和物中二氧化锰的质量为( )
A、(A+B-C)g B、(A-B-C)g C、(A+B+C)g D、(A+C)g
8、已知化学反应: ,a克Mg在b克O2中燃烧,生成MgO的质量为 ( )
A、(a+b)克B、小于(a+b)克 C、小于或等于(a+b)克D、大于(a+b)克
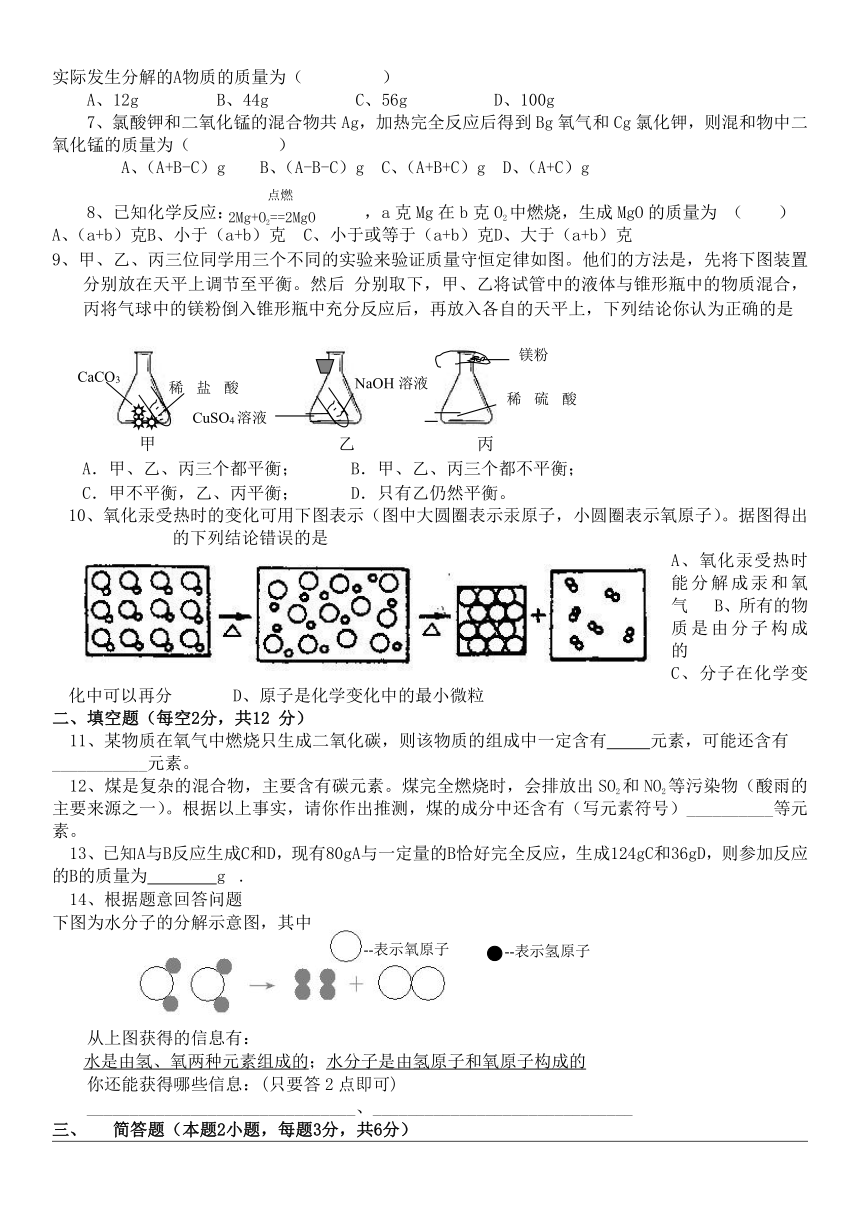
9、甲、乙、丙三位同学用三个不同的实验来验证质量守恒定律如图。他们的方法是,先将下图装置分别放在天平上调节至平衡。然后 分别取下,甲、乙将试管中的液体与锥形瓶中的物质混合,丙将气球中的镁粉倒入锥形瓶中充分反应后,再放入各自的天平上,下列结论你认为正确的是
甲 乙 丙
A.甲、乙、丙三个都平衡; B.甲、乙、丙三个都不平衡;
C.甲不平衡,乙、丙平衡; D.只有乙仍然平衡。
10、氧化汞受热时的变化可用下图表示(图中大圆圈表示汞原子,小圆圈表示氧原子)。据图得出的下列结论错误的是
A、氧化汞受热时能分解成汞和氧气 B、所有的物质是由分子构成的
C、分子在化学变化中可以再分 D、原子是化学变化中的最小微粒
二、填空题(每空2分,共12 分)
11、某物质在氧气中燃烧只生成二氧化碳,则该物质的组成中一定含有 元素,可能还含有___________元素。
12、煤是复杂的混合物,主要含有碳元素。煤完全燃烧时,会排放出SO2和NO2等污染物(酸雨的主要来源之一)。根据以上事实,请你作出推测,煤的成分中还含有(写元素符号)__________等元素。
13、已知A与B反应生成C和D,现有80gA与一定量的B恰好完全反应,生成124gC和36gD,则参加反应的B的质量为 g.
14、根据题意回答问题
下图为水分子的分解示意图,其中
从上图获得的信息有:
水是由氢、氧两种元素组成的;水分子是由氢原子和氧原子构成的
你还能获得哪些信息:(只要答2点即可)
_______________________________、______________________________
简答题(本题2小题,每题3分,共6分)
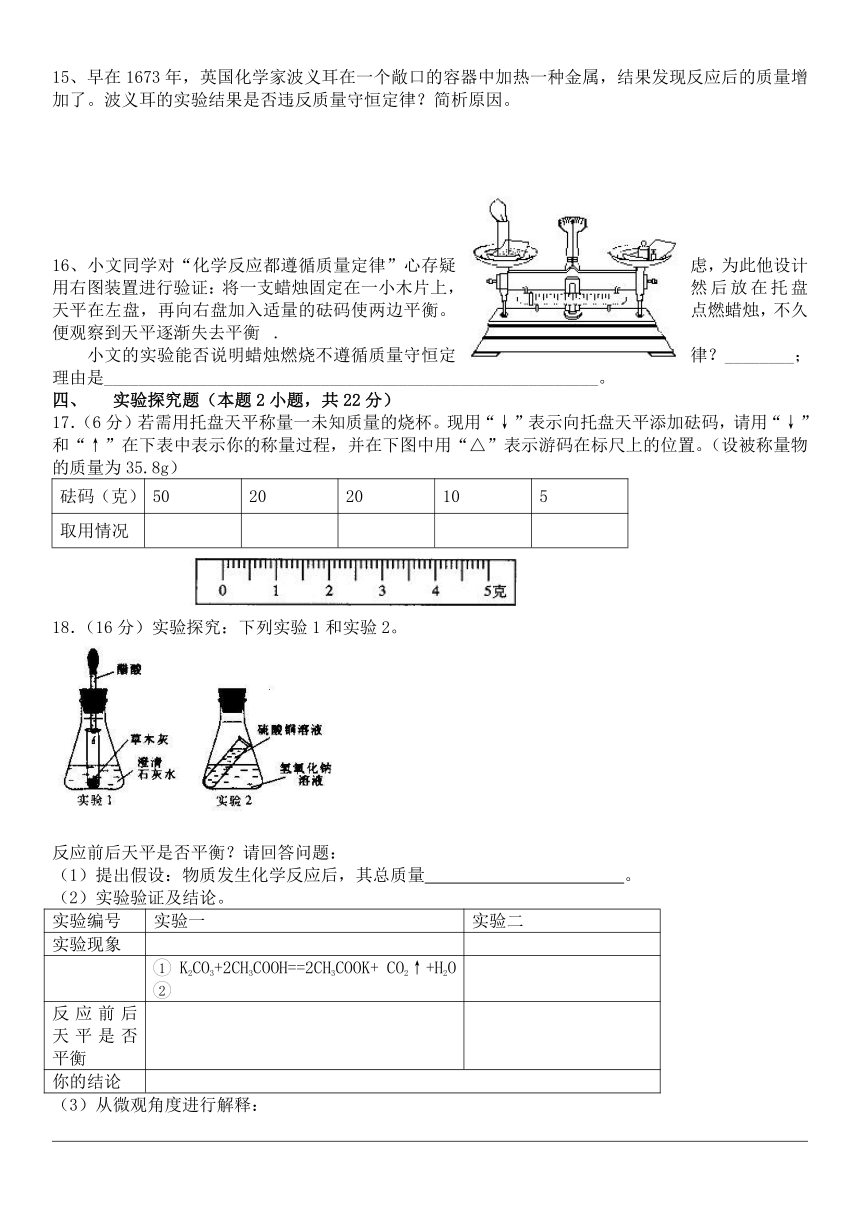
15、早在1673年,英国化学家波义耳在一个敞口的容器中加热一种金属,结果发现反应后的质量增加了。波义耳的实验结果是否违反质量守恒定律?简析原因。
16、小文同学对“化学反应都遵循质量定律”心存疑虑,为此他设计用右图装置进行验证:将一支蜡烛固定在一小木片上,然后放在托盘天平在左盘,再向右盘加入适量的砝码使两边平衡。点燃蜡烛,不久便观察到天平逐渐失去平衡.
小文的实验能否说明蜡烛燃烧不遵循质量守恒定律?________;理由是_________________________________________________________。
实验探究题(本题2小题,共22分)
17.(6分)若需用托盘天平称量一未知质量的烧杯。现用“↓”表示向托盘天平添加砝码,请用“↓”和“↑”在下表中表示你的称量过程,并在下图中用“△”表示游码在标尺上的位置。(设被称量物的质量为35.8g)
砝码(克) 50 20 20 10 5
取用情况
18.(16分)实验探究:下列实验1和实验2。
反应前后天平是否平衡?请回答问题:
(1)提出假设:物质发生化学反应后,其总质量 。
(2)实验验证及结论。
实验编号 实验一 实验二
实验现象
K2CO3+2CH3COOH==2CH3COOK+ CO2↑+H2O
反应前后天平是否平衡
你的结论
(3)从微观角度进行解释:
————————————————————————————————。
巩固提高:
一、选择
1.根据质量守恒定律,镁带在空气中完全燃烧后,生成物的质量应( )
A. 小于镁带的质量 B.大于镁带的质量
C.等于镁带的质量 D.无法比较
2.“化学反应的绿色化”要求原料物质中所有的原子完全被利用,且全部转化到期望的产品中,下列反应类型,一定符合“化学反应的绿色化”要求的是( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应
3.光合作用的实质是:二氧化碳+水 淀粉+氧气,由此可以判断出( )
A淀粉中一定含有碳、氢、氧三种元素
B淀粉中一定含有碳、氢两种元素,可能含有氧元素
C 淀粉中可能含有氮元素 D淀粉中含有水
4.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下反应一段时间后,测得反应前后各物质的质量如下:
物 质 X Y Z Q
反应前质量/g 20 20 20 20
反应后质量/g 20 30 1 6 1 4
试推断该密闭容器中发生化学反应的基本类型可能为( )。
(A) 置换反应 (B) 分解反应
(C) 化合反应 (D)以上都不对
5.把A、B、C、D四种物质各10克放入一密封容器内完全反应后,C比D多10克,B比A多10克,A和C相等,则该该容器内发生的反应为( )
A.A+B=C+D B.D=A+B C.A+B=D D.D=B
6、如图所示探究质量守恒定律,随着蜡烛的燃烧,天平反映的信息是( )
A、指针逐渐向右倾斜
B、指针逐渐向左倾斜
C、指针不动
D、蜡烛燃烧不符合质量守恒定律
7.手机使用的锂电池板是新型的高能电池,以质量轻、电容量大而受到重视。某种锂电池的总反应可表示为Li+MnO2=LiMnO2 。下列说法中正确的是( )
A.LiMnO2为新型的氧化物 B.LiMnO2为锂、锰、氧的合金
C.该反应属于化合反应 D.该反应中Mn的化合价没有变化
8.绿色化学又称环境友好化学,它的主要特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”。下列反应符合绿色化学这一特点的是( )
A.工业冶铁 Fe2O3+3CO 2Fe+3CO2
B.用生石灰制熟石灰 CaO+H2O==Ca(OH)2
C.实验室制取二氧化碳 CaCO3+2HCl==CaCl2+H2O+CO2 ↑
D.实验室制取氢气 Zn+H2SO4==ZnSO4+H2 ↑
9. 生活在密闭狭小的特殊环境(如潜艇、太空舱)里,O2会越来越少,CO2越来越多,因此将CO2 转化为O2,不仅有科学意义也有重要的实用价值。据科学文献报道,NiFe2O4在一定条件下既能促进CO2的分解又可重复使用。NiFe2O4在此反应中是( )
A. 粘合剂 B. 致冷剂 C. 催化剂 D. 防腐剂
10.目前生产自来水常用到氯气,氯气与水发生了如下反应:Cl2+H2O==HCl+HClO,HClO能消毒杀菌。下列说法正确的是( )。
A.消毒杀菌后的自来水是纯净物 B.氯气与水的反应属于化合反应
C.HClO中氯元素的化合价为+2 D.HCl中元素的化合价为-1
填空题(每空1分,共16分)
11、(3分)在一切化学反应中,反应前后原子 没有改变,原子的 没有增减,原子的 也没有变化.
12.(6分)将AgKClO3和BgMnO2的混合物加热到不再放出O2为止,得到固体剩余物Cg,则生成的KCl和O2的质量总和是 g,其中KCl的质量是______g,氧气的质量是 g.
13、(7分)通电分解水的简易装置如右图所示。
(1)在水中加入少量硫酸或氢氧化钠的目的是为了__________________。
(2)试管甲中生成的是___________气,则B极为___________极(填正或负),甲、乙两试管内气体的质量比为___________。
(3)电解水的实验说明水是由___________组成的。这个实验还验证了在化学反应里___________,可以分成原子,而___________不能再分。
14、 (6分)旧版初中化学教材“绪言”中,描述了有关物质的变化和性质:①潺潺的流水能蒸发成水蒸气②水蒸气变成天空中的白云③白云变成了雨滴或雪花降落到地面④铁矿石冶炼成钢铁⑤钢铁可能变成铁锈⑥煤着火燃烧,残余一堆灰烬。
请你分析,其中属于物理性质的是_______ (填序号,下同),属于化学性质的是_______,变化过程中一定遵守质量守恒定律的是_______________。
简答题(本题2小题,每题3分,共6分)
15、简答题:成语“点石成金”,本意为古代方士的一种法术,即能使石头变成黄金;现比喻能化腐朽为神奇。有人说他能把石灰石变成黄金,请你用化学知识说明石灰石不能变成黄金的道理。
16.小冰发现,铁钉生锈后质量会增加,蜡烛燃烧后质量会减少。据此他推断:质量守恒定律也有例外,你认为小冰的推断对吗 为什么?
实验探究题(本题共2小题,共18分)
17、(6分)某学生为了证明甲烷中含有碳、氢元素,设计并完成了如下实验方案。请你帮他完成下面的实验报告。
实验目的:证明甲烷中含有碳、氢元素。
实验用品:火柴、盛有甲烷的贮气瓶、一个光洁干燥的小烧杯、澄清的石灰水
实验步骤 实验现象 结论
(1)点燃甲烷(2)将_________的烧杯罩在甲烷的火焰上方 现象____________
(3)将蘸有_________的小烧杯罩在甲烷燃烧的火焰上方 现象____________ 证明含有__________元素
18.(12分,每空2分) 小刚和小洁以“化学反应中,反应物与生成物的质量关系”为课题进行科学探究。请填写以下探究过程中的空格:
【提出假设】化学反应中,反应物与生成物的质量
【确定研究方法】分析推理、查阅资料、实验探究。
【设计并进行实验】小刚设计的实验装置和选用药品如A图所示,小洁设计的实验装置和选用药品如B图所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。
【实验结论】
小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等。
你认为 的结论正确;请谈谈导致另一结论错误的原因:
。
【结论分析】请从原子的角度,简要分析你认为正确的结论。
。
【查阅资料】小刚和小洁通过查阅资料了解到:法国伟大的科学家拉瓦锡,早在18世纪就围绕这个问题,进行了准确、周密的研究,并做出了科学结论。
【交流表达】请简要谈一下,你认为这条结论有什么重大意义?(不超过30字)
。
【结论应用】环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式为:I2O5+5CO=I2+5X,根据生成X的多少,可以判断CO的含量,X的化学式是 。
点燃
2Mg+O2==2MgO
CaCO3
稀盐酸fhsg
CuSO4溶液
NaOH溶液
稀硫酸fhsg
镁粉
--表示氧原子
--表示氢原子
光叶绿素
1
时间:_________ 学生:_________ 教师:__________
课题 质量守恒定律
重点 质量守恒定律定义2.质量守恒定律运用
难点 探究质量守恒定律的实验
知识点梳理:
化学反应与质量守恒
化合反应和分解反应
(1)化合反应:A+B C
(2)分解反应:A B+C
质量守恒定律
定义:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,这个定律叫质量守恒定律。
质量守恒定律的解释
原子种类没有变化
反应前后 原子数目没有增减
(3)化学反应前后一定不变的量: ①原子种类 ② 元素种类 ③ 原子数目
④物质总质量
基础练习:
一、选择题(本题包括10小题,每小题2分,共20分。每小题只有1个选项符合题意)
1、化学反应遵守质量守恒定律的原因是( )
A、物质的种类没有变化 B、分子的种类不会发生变化
C、分子的数目不会改变 D、原子的种类、数目和质量都没有改变
2、下列变化中,属于化学变化,并且能用质量守恒定律解释是( )
木炭燃烧质量减少
B、5g水受热变成5g水蒸气
C、5g蔗糖溶解在95g水中,成为100g的蔗糖的水溶液
D、100mL水加入100mL酒精,成为体积小于200mL的溶液
3、关于质量守恒定律,下列叙述中正确的是( )
A、煤燃烧化为灰烬,该反应不符合质量守恒定律
B、24g镁在空气中完全燃烧生成40g氧化镁,实际消耗空气的质量为16g
C、一切化学反应都遵守质量守恒定律
D、质量守恒定律只适用于有气体或固体生成的化学反应
4、2003年10月16日,“神舟五号”安全返航,标志着我国载人航天技术取得历史性突破。火箭所用的燃料为偏二甲肼[(CH3)2N2H2],其主要反应为(CH3)2N2H2+N2O4→X+CO2+H2O,由此可知X中一定含有的元素是( )
A、碳 B、氢 C、氧 D、氮
5、已知A物质与B物质反应生成C物质,现有12gA与32gB恰好完全反应,则生成C物质的质量是( )
A、44g B、32g C、22g D、12g
6、已知A物质发生分解反应生成B物质和C物质,当一定量的A反应片刻后,生成56gB和44gC;则实际发生分解的A物质的质量为( )
A、12g B、44g C、56g D、100g
7、氯酸钾和二氧化锰的混合物共Ag,加热完全反应后得到Bg氧气和Cg氯化钾,则混和物中二氧化锰的质量为( )
A、(A+B-C)g B、(A-B-C)g C、(A+B+C)g D、(A+C)g
8、已知化学反应: ,a克Mg在b克O2中燃烧,生成MgO的质量为 ( )
A、(a+b)克B、小于(a+b)克 C、小于或等于(a+b)克D、大于(a+b)克
9、甲、乙、丙三位同学用三个不同的实验来验证质量守恒定律如图。他们的方法是,先将下图装置分别放在天平上调节至平衡。然后 分别取下,甲、乙将试管中的液体与锥形瓶中的物质混合,丙将气球中的镁粉倒入锥形瓶中充分反应后,再放入各自的天平上,下列结论你认为正确的是
甲 乙 丙
A.甲、乙、丙三个都平衡; B.甲、乙、丙三个都不平衡;
C.甲不平衡,乙、丙平衡; D.只有乙仍然平衡。
10、氧化汞受热时的变化可用下图表示(图中大圆圈表示汞原子,小圆圈表示氧原子)。据图得出的下列结论错误的是
A、氧化汞受热时能分解成汞和氧气 B、所有的物质是由分子构成的
C、分子在化学变化中可以再分 D、原子是化学变化中的最小微粒
二、填空题(每空2分,共12 分)
11、某物质在氧气中燃烧只生成二氧化碳,则该物质的组成中一定含有 元素,可能还含有___________元素。
12、煤是复杂的混合物,主要含有碳元素。煤完全燃烧时,会排放出SO2和NO2等污染物(酸雨的主要来源之一)。根据以上事实,请你作出推测,煤的成分中还含有(写元素符号)__________等元素。
13、已知A与B反应生成C和D,现有80gA与一定量的B恰好完全反应,生成124gC和36gD,则参加反应的B的质量为 g.
14、根据题意回答问题
下图为水分子的分解示意图,其中
从上图获得的信息有:
水是由氢、氧两种元素组成的;水分子是由氢原子和氧原子构成的
你还能获得哪些信息:(只要答2点即可)
_______________________________、______________________________
简答题(本题2小题,每题3分,共6分)
15、早在1673年,英国化学家波义耳在一个敞口的容器中加热一种金属,结果发现反应后的质量增加了。波义耳的实验结果是否违反质量守恒定律?简析原因。
16、小文同学对“化学反应都遵循质量定律”心存疑虑,为此他设计用右图装置进行验证:将一支蜡烛固定在一小木片上,然后放在托盘天平在左盘,再向右盘加入适量的砝码使两边平衡。点燃蜡烛,不久便观察到天平逐渐失去平衡.
小文的实验能否说明蜡烛燃烧不遵循质量守恒定律?________;理由是_________________________________________________________。
实验探究题(本题2小题,共22分)
17.(6分)若需用托盘天平称量一未知质量的烧杯。现用“↓”表示向托盘天平添加砝码,请用“↓”和“↑”在下表中表示你的称量过程,并在下图中用“△”表示游码在标尺上的位置。(设被称量物的质量为35.8g)
砝码(克) 50 20 20 10 5
取用情况
18.(16分)实验探究:下列实验1和实验2。
反应前后天平是否平衡?请回答问题:
(1)提出假设:物质发生化学反应后,其总质量 。
(2)实验验证及结论。
实验编号 实验一 实验二
实验现象
K2CO3+2CH3COOH==2CH3COOK+ CO2↑+H2O
反应前后天平是否平衡
你的结论
(3)从微观角度进行解释:
————————————————————————————————。
巩固提高:
一、选择
1.根据质量守恒定律,镁带在空气中完全燃烧后,生成物的质量应( )
A. 小于镁带的质量 B.大于镁带的质量
C.等于镁带的质量 D.无法比较
2.“化学反应的绿色化”要求原料物质中所有的原子完全被利用,且全部转化到期望的产品中,下列反应类型,一定符合“化学反应的绿色化”要求的是( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应
3.光合作用的实质是:二氧化碳+水 淀粉+氧气,由此可以判断出( )
A淀粉中一定含有碳、氢、氧三种元素
B淀粉中一定含有碳、氢两种元素,可能含有氧元素
C 淀粉中可能含有氮元素 D淀粉中含有水
4.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下反应一段时间后,测得反应前后各物质的质量如下:
物 质 X Y Z Q
反应前质量/g 20 20 20 20
反应后质量/g 20 30 1 6 1 4
试推断该密闭容器中发生化学反应的基本类型可能为( )。
(A) 置换反应 (B) 分解反应
(C) 化合反应 (D)以上都不对
5.把A、B、C、D四种物质各10克放入一密封容器内完全反应后,C比D多10克,B比A多10克,A和C相等,则该该容器内发生的反应为( )
A.A+B=C+D B.D=A+B C.A+B=D D.D=B
6、如图所示探究质量守恒定律,随着蜡烛的燃烧,天平反映的信息是( )
A、指针逐渐向右倾斜
B、指针逐渐向左倾斜
C、指针不动
D、蜡烛燃烧不符合质量守恒定律
7.手机使用的锂电池板是新型的高能电池,以质量轻、电容量大而受到重视。某种锂电池的总反应可表示为Li+MnO2=LiMnO2 。下列说法中正确的是( )
A.LiMnO2为新型的氧化物 B.LiMnO2为锂、锰、氧的合金
C.该反应属于化合反应 D.该反应中Mn的化合价没有变化
8.绿色化学又称环境友好化学,它的主要特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”。下列反应符合绿色化学这一特点的是( )
A.工业冶铁 Fe2O3+3CO 2Fe+3CO2
B.用生石灰制熟石灰 CaO+H2O==Ca(OH)2
C.实验室制取二氧化碳 CaCO3+2HCl==CaCl2+H2O+CO2 ↑
D.实验室制取氢气 Zn+H2SO4==ZnSO4+H2 ↑
9. 生活在密闭狭小的特殊环境(如潜艇、太空舱)里,O2会越来越少,CO2越来越多,因此将CO2 转化为O2,不仅有科学意义也有重要的实用价值。据科学文献报道,NiFe2O4在一定条件下既能促进CO2的分解又可重复使用。NiFe2O4在此反应中是( )
A. 粘合剂 B. 致冷剂 C. 催化剂 D. 防腐剂
10.目前生产自来水常用到氯气,氯气与水发生了如下反应:Cl2+H2O==HCl+HClO,HClO能消毒杀菌。下列说法正确的是( )。
A.消毒杀菌后的自来水是纯净物 B.氯气与水的反应属于化合反应
C.HClO中氯元素的化合价为+2 D.HCl中元素的化合价为-1
填空题(每空1分,共16分)
11、(3分)在一切化学反应中,反应前后原子 没有改变,原子的 没有增减,原子的 也没有变化.
12.(6分)将AgKClO3和BgMnO2的混合物加热到不再放出O2为止,得到固体剩余物Cg,则生成的KCl和O2的质量总和是 g,其中KCl的质量是______g,氧气的质量是 g.
13、(7分)通电分解水的简易装置如右图所示。
(1)在水中加入少量硫酸或氢氧化钠的目的是为了__________________。
(2)试管甲中生成的是___________气,则B极为___________极(填正或负),甲、乙两试管内气体的质量比为___________。
(3)电解水的实验说明水是由___________组成的。这个实验还验证了在化学反应里___________,可以分成原子,而___________不能再分。
14、 (6分)旧版初中化学教材“绪言”中,描述了有关物质的变化和性质:①潺潺的流水能蒸发成水蒸气②水蒸气变成天空中的白云③白云变成了雨滴或雪花降落到地面④铁矿石冶炼成钢铁⑤钢铁可能变成铁锈⑥煤着火燃烧,残余一堆灰烬。
请你分析,其中属于物理性质的是_______ (填序号,下同),属于化学性质的是_______,变化过程中一定遵守质量守恒定律的是_______________。
简答题(本题2小题,每题3分,共6分)
15、简答题:成语“点石成金”,本意为古代方士的一种法术,即能使石头变成黄金;现比喻能化腐朽为神奇。有人说他能把石灰石变成黄金,请你用化学知识说明石灰石不能变成黄金的道理。
16.小冰发现,铁钉生锈后质量会增加,蜡烛燃烧后质量会减少。据此他推断:质量守恒定律也有例外,你认为小冰的推断对吗 为什么?
实验探究题(本题共2小题,共18分)
17、(6分)某学生为了证明甲烷中含有碳、氢元素,设计并完成了如下实验方案。请你帮他完成下面的实验报告。
实验目的:证明甲烷中含有碳、氢元素。
实验用品:火柴、盛有甲烷的贮气瓶、一个光洁干燥的小烧杯、澄清的石灰水
实验步骤 实验现象 结论
(1)点燃甲烷(2)将_________的烧杯罩在甲烷的火焰上方 现象____________
(3)将蘸有_________的小烧杯罩在甲烷燃烧的火焰上方 现象____________ 证明含有__________元素
18.(12分,每空2分) 小刚和小洁以“化学反应中,反应物与生成物的质量关系”为课题进行科学探究。请填写以下探究过程中的空格:
【提出假设】化学反应中,反应物与生成物的质量
【确定研究方法】分析推理、查阅资料、实验探究。
【设计并进行实验】小刚设计的实验装置和选用药品如A图所示,小洁设计的实验装置和选用药品如B图所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。
【实验结论】
小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等。
你认为 的结论正确;请谈谈导致另一结论错误的原因:
。
【结论分析】请从原子的角度,简要分析你认为正确的结论。
。
【查阅资料】小刚和小洁通过查阅资料了解到:法国伟大的科学家拉瓦锡,早在18世纪就围绕这个问题,进行了准确、周密的研究,并做出了科学结论。
【交流表达】请简要谈一下,你认为这条结论有什么重大意义?(不超过30字)
。
【结论应用】环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式为:I2O5+5CO=I2+5X,根据生成X的多少,可以判断CO的含量,X的化学式是 。
点燃
2Mg+O2==2MgO
CaCO3
稀盐酸fhsg
CuSO4溶液
NaOH溶液
稀硫酸fhsg
镁粉
--表示氧原子
--表示氢原子
光叶绿素
1
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
