人教高中化学选修二3.2金属材料 课件(31张ppt)
文档属性
| 名称 | 人教高中化学选修二3.2金属材料 课件(31张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 546.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-03 00:00:00 | ||
图片预览






文档简介
(共31张PPT)
第三章
化学与材料的发展
第二节
金属材料
新课标人教版高中化学课件系列
选修2
化学与技术
一、从矿石中获得金属
获得金属材料经过探矿、采矿、选矿等工序,之后进入冶炼阶段。金属冶炼所依据的原理是利用氧化还原反应将金属从其化合物中还原出来。
我们知道,只有少数化学性质不活泼的金属,如金、铂以及少量的银和铜在自然界中能以游离态存在,大多数金属是与氧、硫等非金属单质和化合物而存在。
金属冶炼的方法:由于金属的活动性不同,金属离子得到电子被还原成金属原子的能力也就不同,因此必须采用不同的冶炼方法。
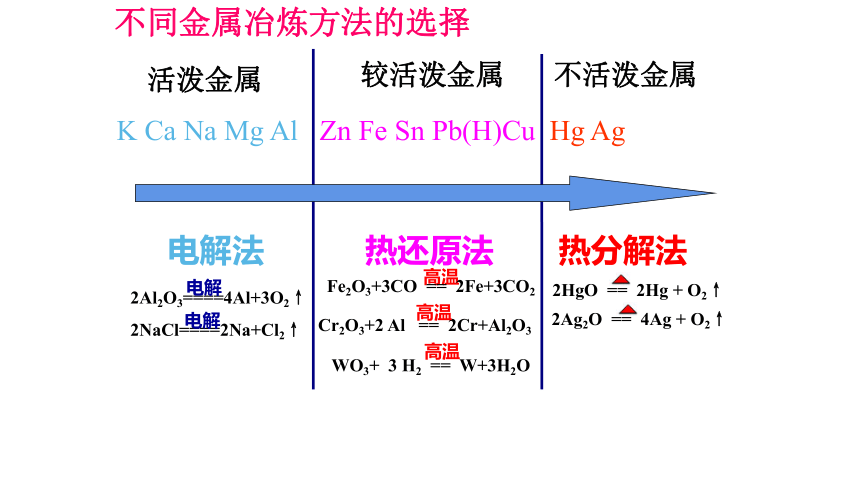
(1)热分解法;(2)热还原法;(3)电解法。
电解法
热还原法
热分解法
不同金属冶炼方法的选择
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb(H)Cu
Hg
Ag
2HgO
==
2Hg
+
O2↑
2Ag2O
==
4Ag
+
O2↑
活泼金属
较活泼金属
不活泼金属
高温
Fe2O3+3CO
==
2Fe+3CO2
2Al2O3====4Al+3O2↑
2NaCl====2Na+Cl2↑
电解
电解
Cr2O3+2
Al
==
2Cr+Al2O3
高温
WO3+
3
H2
==
W+3H2O
高温
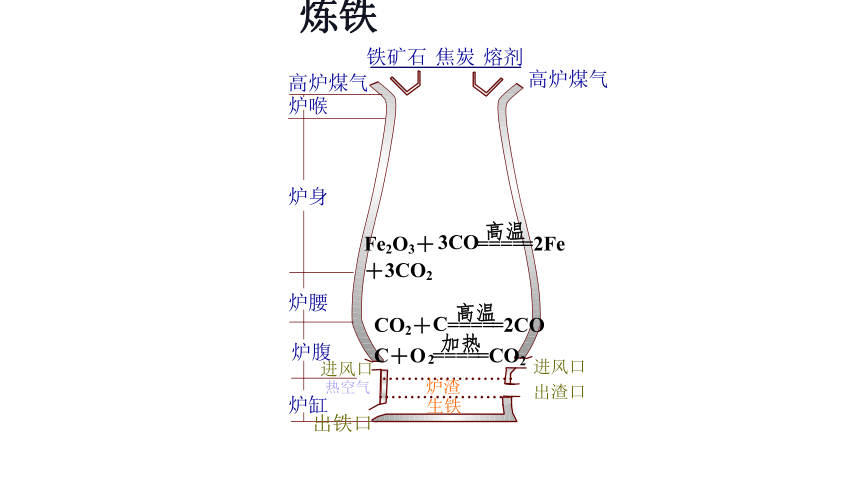
(1)炼铁
原理:
原料:
在高温下用还原剂把铁从其氧化物中还原出来
铁矿石,焦炭,石灰石,空气
1.钢铁的冶炼
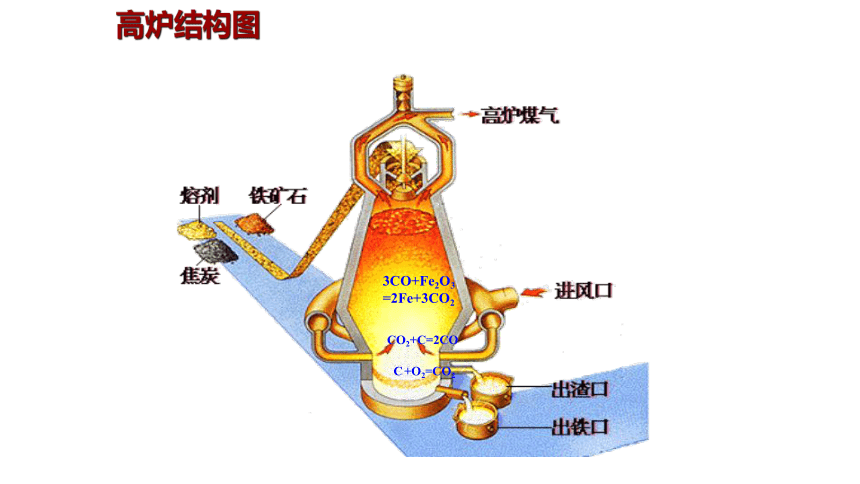
设备:
高炉
主要反应:
Fe2O3+3CO
2Fe+3CO2
高温
高炉结构图
C
+O2=CO2
CO2+C=2CO
3CO+Fe2O3
=2Fe+3CO2
C
+
O
2
====
=
加热
CO
2
CO
2
+
C
====
=
高温
2CO
Fe
2
O
3
+
3CO
====
=
高温
2Fe
+
3CO
2
炼铁
从氧化物、碳酸盐、硫化物中冶炼金属有哪些不同?为什么?
以氧化物形式存在的金属矿石可直接用还原剂还原,如生铁的冶炼;以碳酸盐形式存在的金属矿则可通过煅烧(在缺少空气条件下加热至高温但不使炉料熔化)分解生成金属氧化物或金属,然后再将金属氧化物还原;以硫化物形式存在的金属矿,由于低价硫的存在,所以先要焙烧(在有空气条件下加热至高温但不使炉料熔化)生成金属氧化物或金属,然后再将金属氧化物还原。
炼铁
高炉炼铁产生的废气、废渣的成分是什么?
高炉炼铁中产生的废气、废渣的主要成分:废气有CO、CO2、SO2、NO2,炉渣有CaSiO3、少量含C、P、S、Si、Mn的化合物及SiO2等。
炼铁
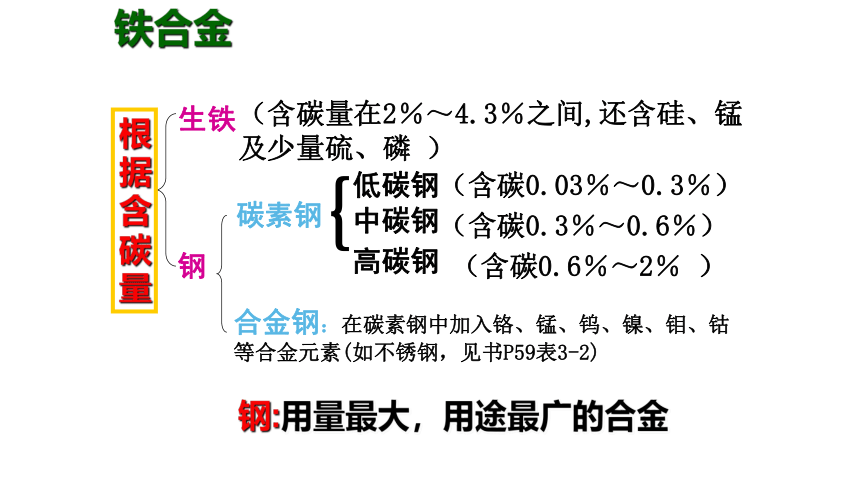
铁合金
生铁
钢
(含碳量在2%~4.3%之间,还含硅、锰及少量硫、磷
)
碳素钢
{
低碳钢
(含碳0.3%~0.6%)
高碳钢
(含碳0.03%~0.3%)
中碳钢
(含碳0.6%~2%
)
合金钢:在碳素钢中加入铬、锰、钨、镍、钼、钴等合金元素(如不锈钢,见书P59表3-2)
钢:用量最大,用途最广的合金
根据含碳量
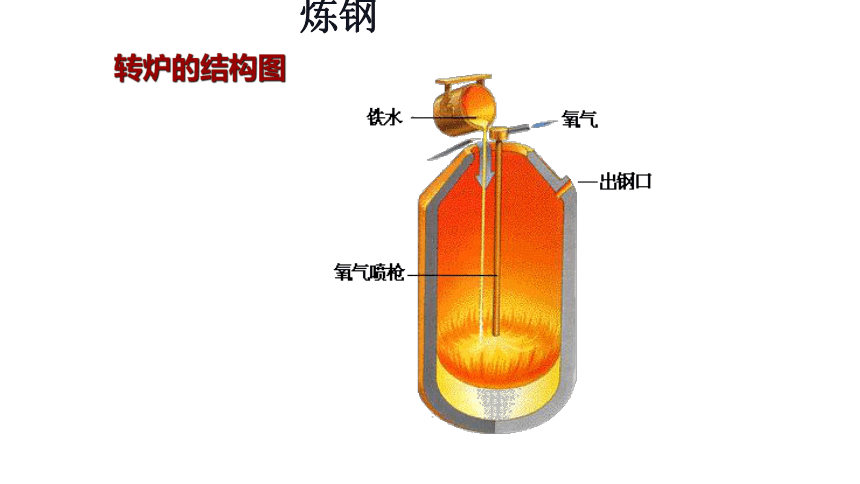
(2)炼钢
原理:
原料:
在高温下用氧化剂把生铁里过多的碳和S、P等其他杂质氧化成气体或炉渣除去,再添加硅、锰、铝等其他合金作为脱氧剂,以调整钢水的成分制成符合规格的钢材。
生铁(液态),氧气(或空气),生石灰(造渣材料),脱氧剂(硅铁、锰铁、铝等)
设备:
平炉、转炉、电炉
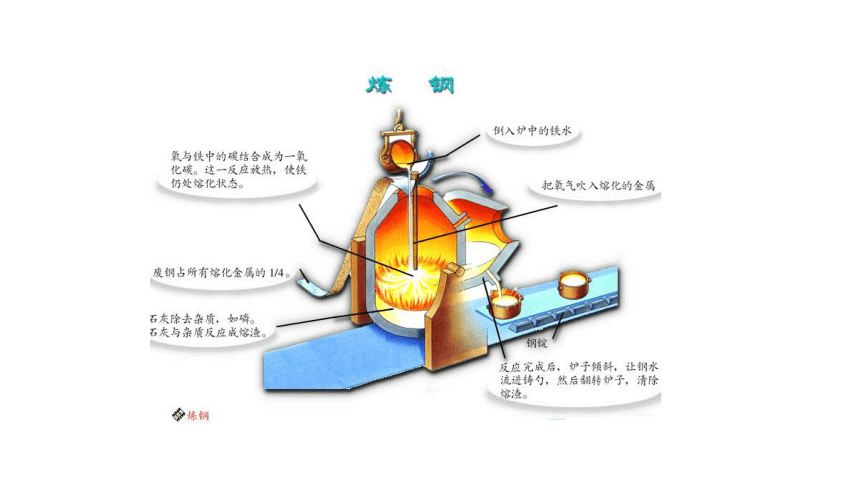
转炉的结构图
炼钢
炼铁和炼钢的主要反应原理有何异同?
炼铁和炼钢的主要反应原理的比较:
相同点:都是利用氧化还原反应。
不同点:炼铁主要是用还原剂把铁从铁矿石中还原出来(侧重还原),而炼钢主要是用氧化剂把生铁中过多的碳和其他杂质氧化而除去(侧重氧化)。
炼钢
炼铁和炼钢的对比:
炼
铁
炼
钢
原料及其作用
主要反应原理
异
同
设备
主要化学反应
尾
气
铁矿石:铁来源
焦炭、空气:产生热量及还原剂CO
石灰石:熔剂(除脉石)
生铁或废钢铁
氧化剂:O2、富氧空气、空气
生石灰:造渣、除Si、P
Si
Mn
Al:还原剂,除FeO,调整钢的成分
高温下,用还原剂(CO)将铁矿石中的铁还原出来
高温下,用氧化剂把生铁中过多的碳和其它杂质氧化成气体或炉渣除去
都是利用氧化还原反应
高
炉
平炉、转炉、电炉
①还原剂CO的生成:
C+O2→CO2
CO2+C→2CO
点燃
高温
②铁的还原:
Fe2O3+3CO
→2Fe+3CO2
高温
③炉渣的生成:CaCO3→CaO+CO2↑
CaO+SiO2→CaSiO3
高温
①氧化造渣(降C,调Si、Mn,除S、P):
2Fe+O2→2FeO(Fe过量)FeO+C→Fe+CO↑
2FeO+Si→2Fe+SiO2
FeO+Mn→Fe+MnO
FeS+CaO→FeO+CaS
2P+5FeO+3CaO→5Fe+Ca3(PO4)3
②还原FeO(脱氧),调节钢的成分:
2FeO+Si→2Fe+SiO2
FeO+Mn→Fe+MnO
高温
高温
高温
高温
高温
高温
高温
高温
高炉煤气(CO、CO2、N2等)
棕色烟气(Fe2O3尘粒、CO等)
电解铝的原料主要来自铝土矿(主要成分Al2O3),其中氧化铝的含量约为50%~70%,而电解时,要求氧化铝的纯度不能低于98.5%,因此,工业上需要先从铝土矿中获得符合要求的氧化铝。这一过程包括三个环节,主要利用了氢氧化铝的两性:
a.将铝土矿中的氧化铝溶解在NaOH溶液中:
Al2O3+2NaOH==2NaAlO2+H2O
b.向偏铝酸钠溶液中通入CO2,析出氢氧化铝:
NaAlO2+CO2+2H2O==Al(OH)3↓+NaHCO3
c.使氢氧化铝脱水生成氧化铝:
2Al(OH)3==Al2O3+3H2O
铝的冶炼
阳极:6O2--12
e-
=3O2↑
阴极:4Al3+
+
12e-
=4Al
通电
总式:2Al2O3
4Al+3O2
↑
冶炼铝的原理:
助熔剂:冰晶石(Na3AlF6
六氟合铝酸钠)
阳极材料(碳)和熔融氧化铝需要定期补充
思考:工业上为什么用电解熔融氧化铝的方法冶炼铝而不用AlCl3?
铝的冶炼
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为__________________
______;加入硅、锰和铝的目的是___________________。
(3)不锈钢含有的Cr元素是在炼钢过程的氧________(填“前”或“后”)加入,原因是___________________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_______
炉身
炉腰
P+5FeO+3CaO==Ca3(PO4)2+5Fe
脱氧和调整钢的成分
后
避免Cr被氧化
CO
燃料(或还原剂)
高温
从矿石中获得金属
在炼铁、炼钢过程中都有碳参加反应。下列有关碳参加反应的叙述正确的是( )
A.两个过程中碳原子都被氧化,都只起着提供热源的作用
B.炼铁过程中碳被氧化,既起产生热量的作用,又起产生CO的作用
C.炼钢过程中碳被还原,从而达到降低含碳量的目的
D.炼铁过程中碳参加反应,只起产生CO的作用
B
从矿石中获得金属
降低Al2O3的熔化温度
下层
(3)阴极和阳极均由________材料做成;电解时不断消耗的电极是________(填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成______(填代号)。
a.冰晶石
b.氧化铝
c.铝锭
d.硫酸铝
碳素(或石墨)
阳极
C
从矿石中获得金属
金属阳离子
失e-
氧化反应
3、金属腐蚀的类型
化学腐蚀(温度的影响很大)
电化腐蚀
析氢腐蚀
吸氧腐蚀
(常见、普遍)
(一)、金属的腐蚀
金属原子
2、金属腐蚀的本质:
1、金属腐蚀:
是指金属或合金跟接触的气体或液体发生氧化还原反应而腐蚀损耗的过程。
M
–
ne-→Mn+
化学腐蚀与电化腐蚀的比较:
化学腐蚀
电化腐蚀
条件
现象
本质
联系
金属跟非金属单质直接接触
不纯金属或合金
跟电解质溶液接触
无电流产生
有微弱电流产生
金属被氧化
较活泼金属被氧化
两者往往同时发生,电化腐蚀更普遍
中性溶液或酸性很弱——吸氧腐蚀(钢铁腐蚀的主要情况)
2H2O+O2+4e-=4OH-
Fe-2e-
=Fe2+
正极:得电子
负极:失电子
金属的腐蚀
2H+
+
2e-=H2↑
酸性较强——析氢腐蚀
Fe-2e-=Fe2+
正极:
负极:
金属的腐蚀
钢铁的析氢腐蚀和吸氧腐蚀比较
Fe2O3
·
nH2O
(铁锈)
通常两种腐蚀同时存在,但以后者更普遍。
析氢腐蚀
吸氧腐蚀
条件
水膜呈酸性。
水膜呈中性或酸性很弱或碱性
电极反应
负极Fe(-
)
Fe-2e-=Fe2+
2Fe-4e-=2Fe2+
正极C(+)
2H++2e-=H2↑
O2+2H2O+4e-=4OH-
总反应:
Fe
+
2H+
=
Fe2+
+
H2
↑
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
联系
(二)、金属腐蚀的防止和利用
金属腐蚀的防护方法
1.金属表面覆盖保护层
如油漆、油脂等,在金属表面氧化形成致密的氧化物薄膜作保护层。
原理:隔绝金属与外界空气、电解质溶液的接触。
2.电镀
如电镀一些在空气或溶液里不易发生化学变化的金属(如Cr、Zn、Ni等)或合金作保护层。
原理:应用电解原理,镀件作阴极镀层金属作阳极。
3.改变金属的内部结构
4.电化学保护法
原理:形成原电池反应时,让被保护金属做正极,
不反应,起到保护作用,而活泼金属发生氧化反应被腐蚀或让被保护金属做电解池的阴极而受到保护。
如将Cr、Ni等金属加进钢里制成不锈钢。
金属防腐的方法还有很多,例如,可以根据不同的设计条件选用不同的金属或非金属材料;也可以控制和改善环境气体、液体介质(如选用缓蚀剂)。实际上,金属防腐包括生产设计、选材、防腐措施、施工、监测、管理、维护等环节,常常需要进行综合评价和决策等等。
金属腐蚀的利用
金属腐蚀的会带来严重危害和损失,但也可被利用来进行材料加工。
例如:化学蚀刻就是利用腐蚀原理进行金属定域“切削”的加工方法(如书图3-28所示)
化学蚀刻不仅适用于难切削的不锈钢、钛合金、铜合金等,更广泛地用于印刷电路的铜布线腐蚀、半导体器件与集成电路制造中的精细加工等。
1、埋在地下的自来水铁管,在下列情况被腐蚀的速率最慢的是(
)
A.在含有铁元素较多的酸性土壤中
B.在潮湿、疏松的土壤中
C.在自来水的铁管上用导线连接一块锌块后,再埋入不透气的土壤中
D.在自来水铁管上用导线连接铜块后,再埋入潮湿、松的土壤中
课堂练习
C
2、下列现象与电化学腐蚀无关的是(
)
A.黄铜(铜锌合金)制作的铜锣不容易生锈
B.生铁比软铁芯(几乎是纯铁)容易生锈
C.铁质器件附有铜质配件,在接触处容易生锈
D.银质奖牌久置表面变暗
D
3、下列几种铁板,在镀层被破坏后,最耐腐蚀的是(
)
A.镀锌铁板 B.镀铜铁板
C.镀锡铁板 D.镀铅铁板
A
4、下列方法可用于金属防护的是(
)
①原电池原理 ②涂油漆 ③电镀
④置于干燥环境
A.②③④ B.①②
C.②③ D.全部
D
第三章
化学与材料的发展
第二节
金属材料
新课标人教版高中化学课件系列
选修2
化学与技术
一、从矿石中获得金属
获得金属材料经过探矿、采矿、选矿等工序,之后进入冶炼阶段。金属冶炼所依据的原理是利用氧化还原反应将金属从其化合物中还原出来。
我们知道,只有少数化学性质不活泼的金属,如金、铂以及少量的银和铜在自然界中能以游离态存在,大多数金属是与氧、硫等非金属单质和化合物而存在。
金属冶炼的方法:由于金属的活动性不同,金属离子得到电子被还原成金属原子的能力也就不同,因此必须采用不同的冶炼方法。
(1)热分解法;(2)热还原法;(3)电解法。
电解法
热还原法
热分解法
不同金属冶炼方法的选择
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb(H)Cu
Hg
Ag
2HgO
==
2Hg
+
O2↑
2Ag2O
==
4Ag
+
O2↑
活泼金属
较活泼金属
不活泼金属
高温
Fe2O3+3CO
==
2Fe+3CO2
2Al2O3====4Al+3O2↑
2NaCl====2Na+Cl2↑
电解
电解
Cr2O3+2
Al
==
2Cr+Al2O3
高温
WO3+
3
H2
==
W+3H2O
高温
(1)炼铁
原理:
原料:
在高温下用还原剂把铁从其氧化物中还原出来
铁矿石,焦炭,石灰石,空气
1.钢铁的冶炼
设备:
高炉
主要反应:
Fe2O3+3CO
2Fe+3CO2
高温
高炉结构图
C
+O2=CO2
CO2+C=2CO
3CO+Fe2O3
=2Fe+3CO2
C
+
O
2
====
=
加热
CO
2
CO
2
+
C
====
=
高温
2CO
Fe
2
O
3
+
3CO
====
=
高温
2Fe
+
3CO
2
炼铁
从氧化物、碳酸盐、硫化物中冶炼金属有哪些不同?为什么?
以氧化物形式存在的金属矿石可直接用还原剂还原,如生铁的冶炼;以碳酸盐形式存在的金属矿则可通过煅烧(在缺少空气条件下加热至高温但不使炉料熔化)分解生成金属氧化物或金属,然后再将金属氧化物还原;以硫化物形式存在的金属矿,由于低价硫的存在,所以先要焙烧(在有空气条件下加热至高温但不使炉料熔化)生成金属氧化物或金属,然后再将金属氧化物还原。
炼铁
高炉炼铁产生的废气、废渣的成分是什么?
高炉炼铁中产生的废气、废渣的主要成分:废气有CO、CO2、SO2、NO2,炉渣有CaSiO3、少量含C、P、S、Si、Mn的化合物及SiO2等。
炼铁
铁合金
生铁
钢
(含碳量在2%~4.3%之间,还含硅、锰及少量硫、磷
)
碳素钢
{
低碳钢
(含碳0.3%~0.6%)
高碳钢
(含碳0.03%~0.3%)
中碳钢
(含碳0.6%~2%
)
合金钢:在碳素钢中加入铬、锰、钨、镍、钼、钴等合金元素(如不锈钢,见书P59表3-2)
钢:用量最大,用途最广的合金
根据含碳量
(2)炼钢
原理:
原料:
在高温下用氧化剂把生铁里过多的碳和S、P等其他杂质氧化成气体或炉渣除去,再添加硅、锰、铝等其他合金作为脱氧剂,以调整钢水的成分制成符合规格的钢材。
生铁(液态),氧气(或空气),生石灰(造渣材料),脱氧剂(硅铁、锰铁、铝等)
设备:
平炉、转炉、电炉
转炉的结构图
炼钢
炼铁和炼钢的主要反应原理有何异同?
炼铁和炼钢的主要反应原理的比较:
相同点:都是利用氧化还原反应。
不同点:炼铁主要是用还原剂把铁从铁矿石中还原出来(侧重还原),而炼钢主要是用氧化剂把生铁中过多的碳和其他杂质氧化而除去(侧重氧化)。
炼钢
炼铁和炼钢的对比:
炼
铁
炼
钢
原料及其作用
主要反应原理
异
同
设备
主要化学反应
尾
气
铁矿石:铁来源
焦炭、空气:产生热量及还原剂CO
石灰石:熔剂(除脉石)
生铁或废钢铁
氧化剂:O2、富氧空气、空气
生石灰:造渣、除Si、P
Si
Mn
Al:还原剂,除FeO,调整钢的成分
高温下,用还原剂(CO)将铁矿石中的铁还原出来
高温下,用氧化剂把生铁中过多的碳和其它杂质氧化成气体或炉渣除去
都是利用氧化还原反应
高
炉
平炉、转炉、电炉
①还原剂CO的生成:
C+O2→CO2
CO2+C→2CO
点燃
高温
②铁的还原:
Fe2O3+3CO
→2Fe+3CO2
高温
③炉渣的生成:CaCO3→CaO+CO2↑
CaO+SiO2→CaSiO3
高温
①氧化造渣(降C,调Si、Mn,除S、P):
2Fe+O2→2FeO(Fe过量)FeO+C→Fe+CO↑
2FeO+Si→2Fe+SiO2
FeO+Mn→Fe+MnO
FeS+CaO→FeO+CaS
2P+5FeO+3CaO→5Fe+Ca3(PO4)3
②还原FeO(脱氧),调节钢的成分:
2FeO+Si→2Fe+SiO2
FeO+Mn→Fe+MnO
高温
高温
高温
高温
高温
高温
高温
高温
高炉煤气(CO、CO2、N2等)
棕色烟气(Fe2O3尘粒、CO等)
电解铝的原料主要来自铝土矿(主要成分Al2O3),其中氧化铝的含量约为50%~70%,而电解时,要求氧化铝的纯度不能低于98.5%,因此,工业上需要先从铝土矿中获得符合要求的氧化铝。这一过程包括三个环节,主要利用了氢氧化铝的两性:
a.将铝土矿中的氧化铝溶解在NaOH溶液中:
Al2O3+2NaOH==2NaAlO2+H2O
b.向偏铝酸钠溶液中通入CO2,析出氢氧化铝:
NaAlO2+CO2+2H2O==Al(OH)3↓+NaHCO3
c.使氢氧化铝脱水生成氧化铝:
2Al(OH)3==Al2O3+3H2O
铝的冶炼
阳极:6O2--12
e-
=3O2↑
阴极:4Al3+
+
12e-
=4Al
通电
总式:2Al2O3
4Al+3O2
↑
冶炼铝的原理:
助熔剂:冰晶石(Na3AlF6
六氟合铝酸钠)
阳极材料(碳)和熔融氧化铝需要定期补充
思考:工业上为什么用电解熔融氧化铝的方法冶炼铝而不用AlCl3?
铝的冶炼
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为__________________
______;加入硅、锰和铝的目的是___________________。
(3)不锈钢含有的Cr元素是在炼钢过程的氧________(填“前”或“后”)加入,原因是___________________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_______
炉身
炉腰
P+5FeO+3CaO==Ca3(PO4)2+5Fe
脱氧和调整钢的成分
后
避免Cr被氧化
CO
燃料(或还原剂)
高温
从矿石中获得金属
在炼铁、炼钢过程中都有碳参加反应。下列有关碳参加反应的叙述正确的是( )
A.两个过程中碳原子都被氧化,都只起着提供热源的作用
B.炼铁过程中碳被氧化,既起产生热量的作用,又起产生CO的作用
C.炼钢过程中碳被还原,从而达到降低含碳量的目的
D.炼铁过程中碳参加反应,只起产生CO的作用
B
从矿石中获得金属
降低Al2O3的熔化温度
下层
(3)阴极和阳极均由________材料做成;电解时不断消耗的电极是________(填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成______(填代号)。
a.冰晶石
b.氧化铝
c.铝锭
d.硫酸铝
碳素(或石墨)
阳极
C
从矿石中获得金属
金属阳离子
失e-
氧化反应
3、金属腐蚀的类型
化学腐蚀(温度的影响很大)
电化腐蚀
析氢腐蚀
吸氧腐蚀
(常见、普遍)
(一)、金属的腐蚀
金属原子
2、金属腐蚀的本质:
1、金属腐蚀:
是指金属或合金跟接触的气体或液体发生氧化还原反应而腐蚀损耗的过程。
M
–
ne-→Mn+
化学腐蚀与电化腐蚀的比较:
化学腐蚀
电化腐蚀
条件
现象
本质
联系
金属跟非金属单质直接接触
不纯金属或合金
跟电解质溶液接触
无电流产生
有微弱电流产生
金属被氧化
较活泼金属被氧化
两者往往同时发生,电化腐蚀更普遍
中性溶液或酸性很弱——吸氧腐蚀(钢铁腐蚀的主要情况)
2H2O+O2+4e-=4OH-
Fe-2e-
=Fe2+
正极:得电子
负极:失电子
金属的腐蚀
2H+
+
2e-=H2↑
酸性较强——析氢腐蚀
Fe-2e-=Fe2+
正极:
负极:
金属的腐蚀
钢铁的析氢腐蚀和吸氧腐蚀比较
Fe2O3
·
nH2O
(铁锈)
通常两种腐蚀同时存在,但以后者更普遍。
析氢腐蚀
吸氧腐蚀
条件
水膜呈酸性。
水膜呈中性或酸性很弱或碱性
电极反应
负极Fe(-
)
Fe-2e-=Fe2+
2Fe-4e-=2Fe2+
正极C(+)
2H++2e-=H2↑
O2+2H2O+4e-=4OH-
总反应:
Fe
+
2H+
=
Fe2+
+
H2
↑
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
联系
(二)、金属腐蚀的防止和利用
金属腐蚀的防护方法
1.金属表面覆盖保护层
如油漆、油脂等,在金属表面氧化形成致密的氧化物薄膜作保护层。
原理:隔绝金属与外界空气、电解质溶液的接触。
2.电镀
如电镀一些在空气或溶液里不易发生化学变化的金属(如Cr、Zn、Ni等)或合金作保护层。
原理:应用电解原理,镀件作阴极镀层金属作阳极。
3.改变金属的内部结构
4.电化学保护法
原理:形成原电池反应时,让被保护金属做正极,
不反应,起到保护作用,而活泼金属发生氧化反应被腐蚀或让被保护金属做电解池的阴极而受到保护。
如将Cr、Ni等金属加进钢里制成不锈钢。
金属防腐的方法还有很多,例如,可以根据不同的设计条件选用不同的金属或非金属材料;也可以控制和改善环境气体、液体介质(如选用缓蚀剂)。实际上,金属防腐包括生产设计、选材、防腐措施、施工、监测、管理、维护等环节,常常需要进行综合评价和决策等等。
金属腐蚀的利用
金属腐蚀的会带来严重危害和损失,但也可被利用来进行材料加工。
例如:化学蚀刻就是利用腐蚀原理进行金属定域“切削”的加工方法(如书图3-28所示)
化学蚀刻不仅适用于难切削的不锈钢、钛合金、铜合金等,更广泛地用于印刷电路的铜布线腐蚀、半导体器件与集成电路制造中的精细加工等。
1、埋在地下的自来水铁管,在下列情况被腐蚀的速率最慢的是(
)
A.在含有铁元素较多的酸性土壤中
B.在潮湿、疏松的土壤中
C.在自来水的铁管上用导线连接一块锌块后,再埋入不透气的土壤中
D.在自来水铁管上用导线连接铜块后,再埋入潮湿、松的土壤中
课堂练习
C
2、下列现象与电化学腐蚀无关的是(
)
A.黄铜(铜锌合金)制作的铜锣不容易生锈
B.生铁比软铁芯(几乎是纯铁)容易生锈
C.铁质器件附有铜质配件,在接触处容易生锈
D.银质奖牌久置表面变暗
D
3、下列几种铁板,在镀层被破坏后,最耐腐蚀的是(
)
A.镀锌铁板 B.镀铜铁板
C.镀锡铁板 D.镀铅铁板
A
4、下列方法可用于金属防护的是(
)
①原电池原理 ②涂油漆 ③电镀
④置于干燥环境
A.②③④ B.①②
C.②③ D.全部
D
