八下科学 第二单元 微粒的模型与符号 知识点梳理(pdf版)
文档属性
| 名称 | 八下科学 第二单元 微粒的模型与符号 知识点梳理(pdf版) |

|
|
| 格式 | zip | ||
| 文件大小 | 7.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-06-18 00:00:00 | ||
图片预览



文档简介
物质的微观构成
符号与单
电学元件符号等
某物体放大或缩小的复制
张图
表
变化过程示意图
公式、表达式等
数
①分子是由原
发
成原
原
组合形
粒
坑点1分子的种类由原子的种类和数量共同决定。例:一氧化碳、二氧化碳
坑点2同种原子可构成不同种物质。例:金刚石、石墨
坑点3原子是化学变化中的最小微粒。化学变化:分子分解→原子重组
坑点4在由分子构成的物质中,分子是保持物质化学性质的最小微粒。例:水水分子
石墨碳原子
坑点5原子的质量不一定小于分子
氧原子质量>氢分子质量
四、卢瑟福实
粒子
说明两个问题
1、大多数ω粒子方向不变
原子中有一个很大的空间,原子不是①原子中含有带正
电的原子核
原子核实心球体
少数o粒子较大角度偏转极少数甚至②原子核体积很小
被反弹
但质量相对较大
注意:a粒
原
吸引的轨
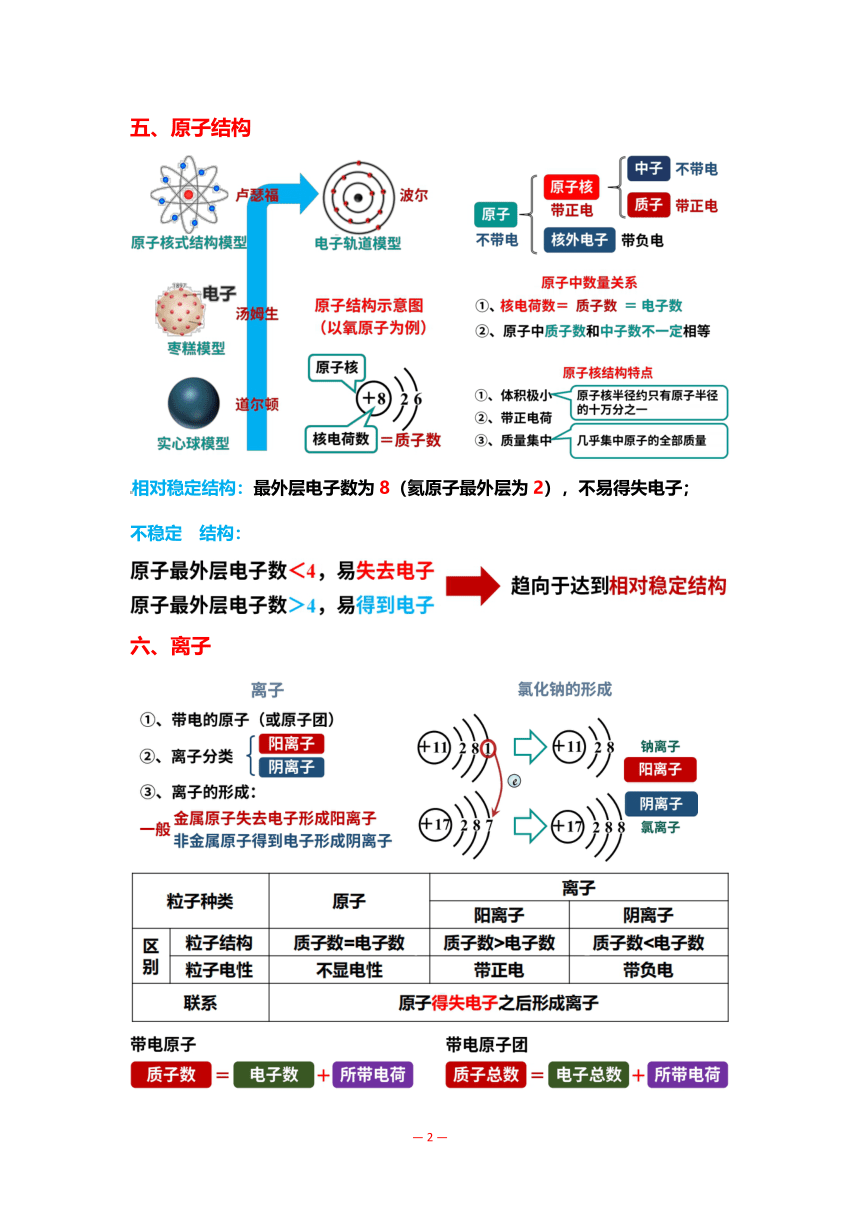
五、原子结构
中子不带电
波尔
带正电
质
子带正电
原子核式结构模
电子轨道模型
不带电核外电子带负电
电子
原子中数量关系
汤姆生
原子结构示意图
①、核电荷数=质子数=电子数
(以氧原子为例)
②2、原子中质子数和中子数不一定相等
枣糕模型
原子核
、带正电荷的+欣多
、体积极
实心球模型
核电荷数=质子数③、质量集中一几乎集中原子的全部质量
对稳定结构:最外层电
不稳定结构
原子最外层电子数<4,易失去电子
趋向于达到相对稳定结构
原子最外层电子数>4,易得到电子
离子
氯化钠的形成
带电的原子(或原子团
阳离子
离子分类
)中沙
钠离子
阳日离子
③、离子的形成
阴离子
般金属原子失去电子形成阳离子
氯离子
非金属原子得到电子形成阴离子
离子
粒子种类
原子
阳离子
阴离子
区粒子结构质子数=电子数质子数>电子数质子数<电子数
别粒子电性
不显电性
带正电
带负电
联系
原子得失电子之后形成离子
带电原子
带电原子团
质子数=【电子数+[所带电荷[质子总数=电子总数+[所带电荷
例题:原子
位的负电有
组成物疯的元素
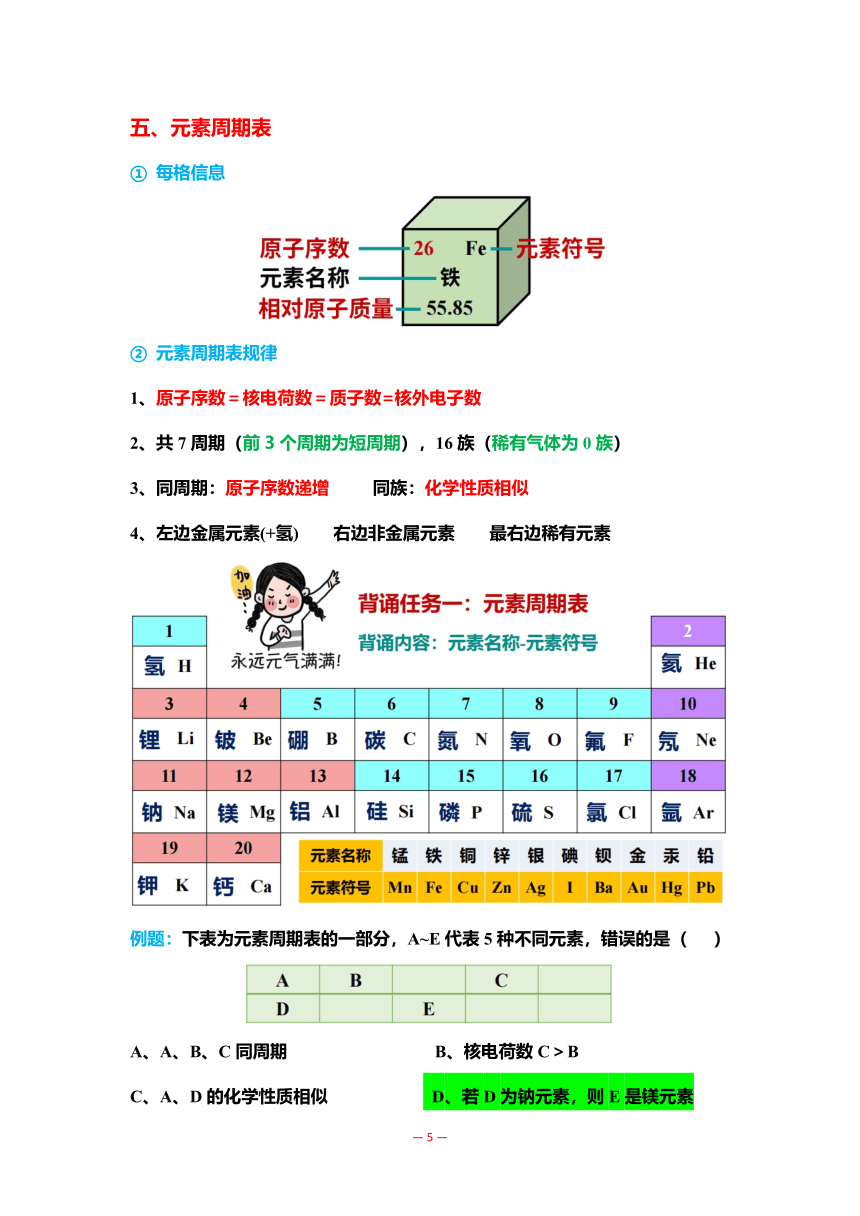
元素定义
元素:核电荷数/质
素
数
数
元素
原子
区别宏观概念,只讲种类,不讲个数微观概念,既讲种类,又讲个数
适用范围
描述物质的宏观组成
描述物质的微观构成
联系
①核电荷数相同的原子同属于一种元素
②原子是元素的最小单位,元素则是原子的一个“集体
水是由元和氧元素构成元素是宏观讲组成不是构
数
数
分子构成
个水分子是由2个氢原子
构成
氧原子构成(x
子构成
质子数相同的微
微粒≠原子
素×微粒≠原子比如
种元素的微
比如:钠原子和钠离
符号与单
电学元件符号等
某物体放大或缩小的复制
张图
表
变化过程示意图
公式、表达式等
数
①分子是由原
发
成原
原
组合形
粒
坑点1分子的种类由原子的种类和数量共同决定。例:一氧化碳、二氧化碳
坑点2同种原子可构成不同种物质。例:金刚石、石墨
坑点3原子是化学变化中的最小微粒。化学变化:分子分解→原子重组
坑点4在由分子构成的物质中,分子是保持物质化学性质的最小微粒。例:水水分子
石墨碳原子
坑点5原子的质量不一定小于分子
氧原子质量>氢分子质量
四、卢瑟福实
粒子
说明两个问题
1、大多数ω粒子方向不变
原子中有一个很大的空间,原子不是①原子中含有带正
电的原子核
原子核实心球体
少数o粒子较大角度偏转极少数甚至②原子核体积很小
被反弹
但质量相对较大
注意:a粒
原
吸引的轨
五、原子结构
中子不带电
波尔
带正电
质
子带正电
原子核式结构模
电子轨道模型
不带电核外电子带负电
电子
原子中数量关系
汤姆生
原子结构示意图
①、核电荷数=质子数=电子数
(以氧原子为例)
②2、原子中质子数和中子数不一定相等
枣糕模型
原子核
、带正电荷的+欣多
、体积极
实心球模型
核电荷数=质子数③、质量集中一几乎集中原子的全部质量
对稳定结构:最外层电
不稳定结构
原子最外层电子数<4,易失去电子
趋向于达到相对稳定结构
原子最外层电子数>4,易得到电子
离子
氯化钠的形成
带电的原子(或原子团
阳离子
离子分类
)中沙
钠离子
阳日离子
③、离子的形成
阴离子
般金属原子失去电子形成阳离子
氯离子
非金属原子得到电子形成阴离子
离子
粒子种类
原子
阳离子
阴离子
区粒子结构质子数=电子数质子数>电子数质子数<电子数
别粒子电性
不显电性
带正电
带负电
联系
原子得失电子之后形成离子
带电原子
带电原子团
质子数=【电子数+[所带电荷[质子总数=电子总数+[所带电荷
例题:原子
位的负电有
组成物疯的元素
元素定义
元素:核电荷数/质
素
数
数
元素
原子
区别宏观概念,只讲种类,不讲个数微观概念,既讲种类,又讲个数
适用范围
描述物质的宏观组成
描述物质的微观构成
联系
①核电荷数相同的原子同属于一种元素
②原子是元素的最小单位,元素则是原子的一个“集体
水是由元和氧元素构成元素是宏观讲组成不是构
数
数
分子构成
个水分子是由2个氢原子
构成
氧原子构成(x
子构成
质子数相同的微
微粒≠原子
素×微粒≠原子比如
种元素的微
比如:钠原子和钠离
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
