科学 第三单元 空气与生命 知识点梳理(pdf版)
文档属性
| 名称 | 科学 第三单元 空气与生命 知识点梳理(pdf版) |
|
|
| 格式 | zip | ||
| 文件大小 | 3.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-06-18 00:00:00 | ||
图片预览



文档简介
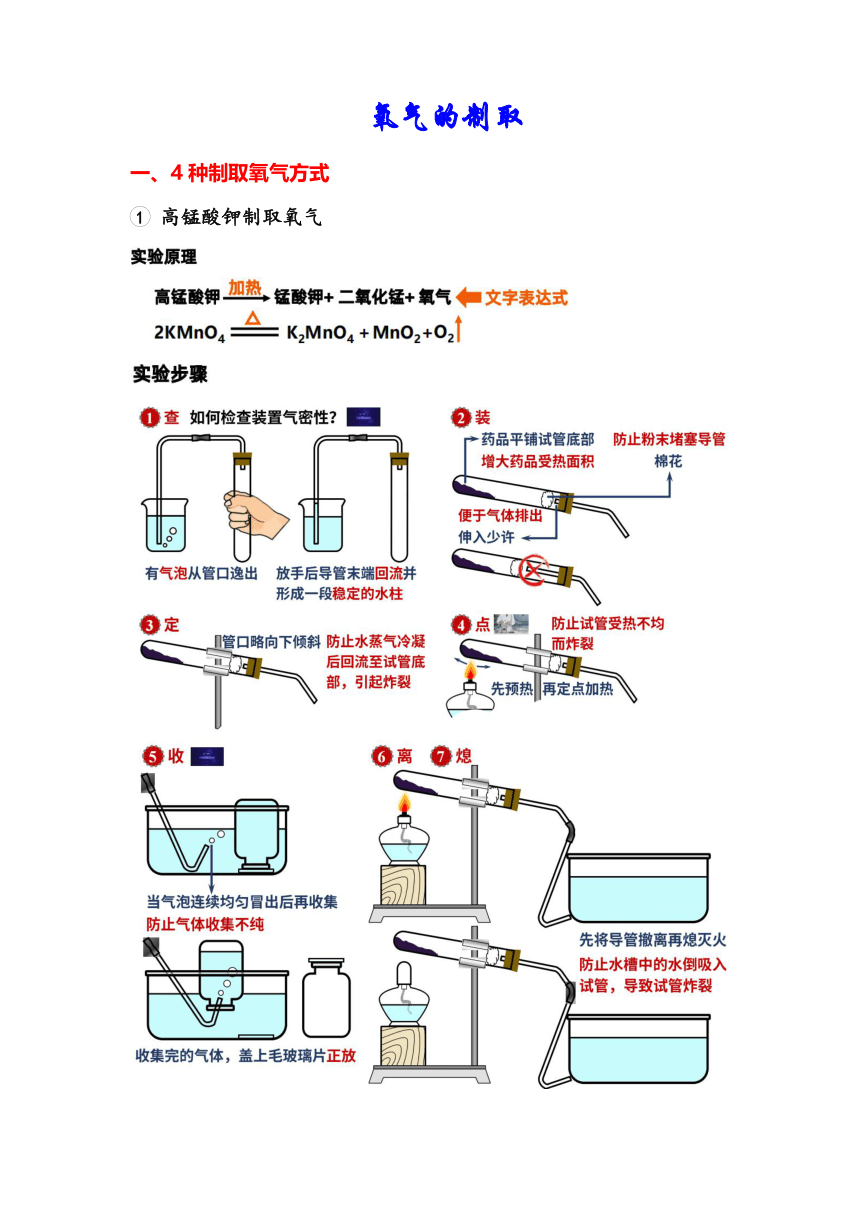
氧气的制取
到
高锰酸钾制取氧气
实验原理
高锰酸钾二热锰酸钾+二氧化锰十氯气‘文字表达式
2KMnO4
K,MnO4
+
Mno2+O2
实验步骤
①查如何检查装置气密性?
装
品平铺试管底部防止粉末堵塞导管
增大药品受热面积
棉花
便于气体排出
伸入少许
有气泡从管口逸出放手后导管末端回流并
形成一段稳定的水柱
④点通防止试管受热不均
∏管口略向下倾斜防止水蒸气冷凝
炸裂
后回流至试管底
部,引起炸裂
点先预热再定点加热
6收
⑥离熄
当气泡连续均匀冒出后再收集
防止气体收集不纯
先将导管撤离再熄灭火
防止水槽中的水倒吸入
试管,导致试管炸裂
收集完的气体,盖上毛玻璃片正放
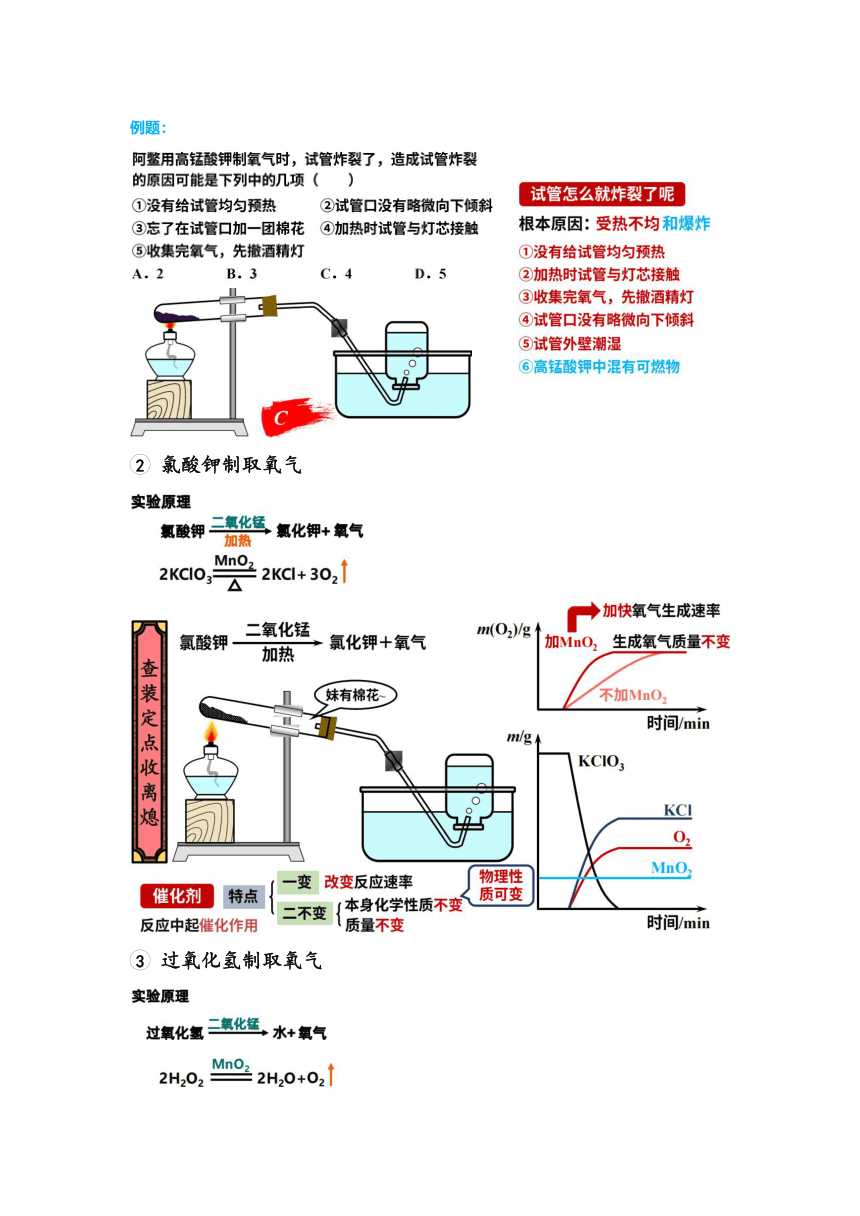
例题
阿鳖用高锰酸钾制氧气时,试管炸裂了,造成试管炸裂
①没有给试管均匀预热②2试管口没有略微向下傾斜
试管怎么就炸裂了呢
③忘了在试管口加一团棉花④加热时试管与灯芯接触根本原因:受热不均和爆炸
⑤收集完氧气,先撤酒精灯
①没有给试管均匀预热
②2加热时试管与灯芯接触
③3收集完氧气,先撤酒精灯
④试管口没有略微向下倾斜
试管外壁潮湿
⑤高锰酸钾中混有可燃物
氟酸钾制取氧气
实验原理
氯酸钾二化氯化钾+氯气
Mno
2K03=天
2KC|+30
加快氧气生成速率
二氧化锰
(O2)g
∥氯酸钾一二北→氯化钾十氧气
加MnO2生成氧气质量不变
妹有棉花
不加MnO
时间
KCiO3
KCI
Mno
变改变反应速率
物理性
催化剂」特点
质可变
不变{本身化学性质不变
反应中起催化作用
质量不变
时间/min
过氧化氢制取氧气
实验原理
过氧化氯二氧化气水+氧气
2H2o2=2H2o+02↑
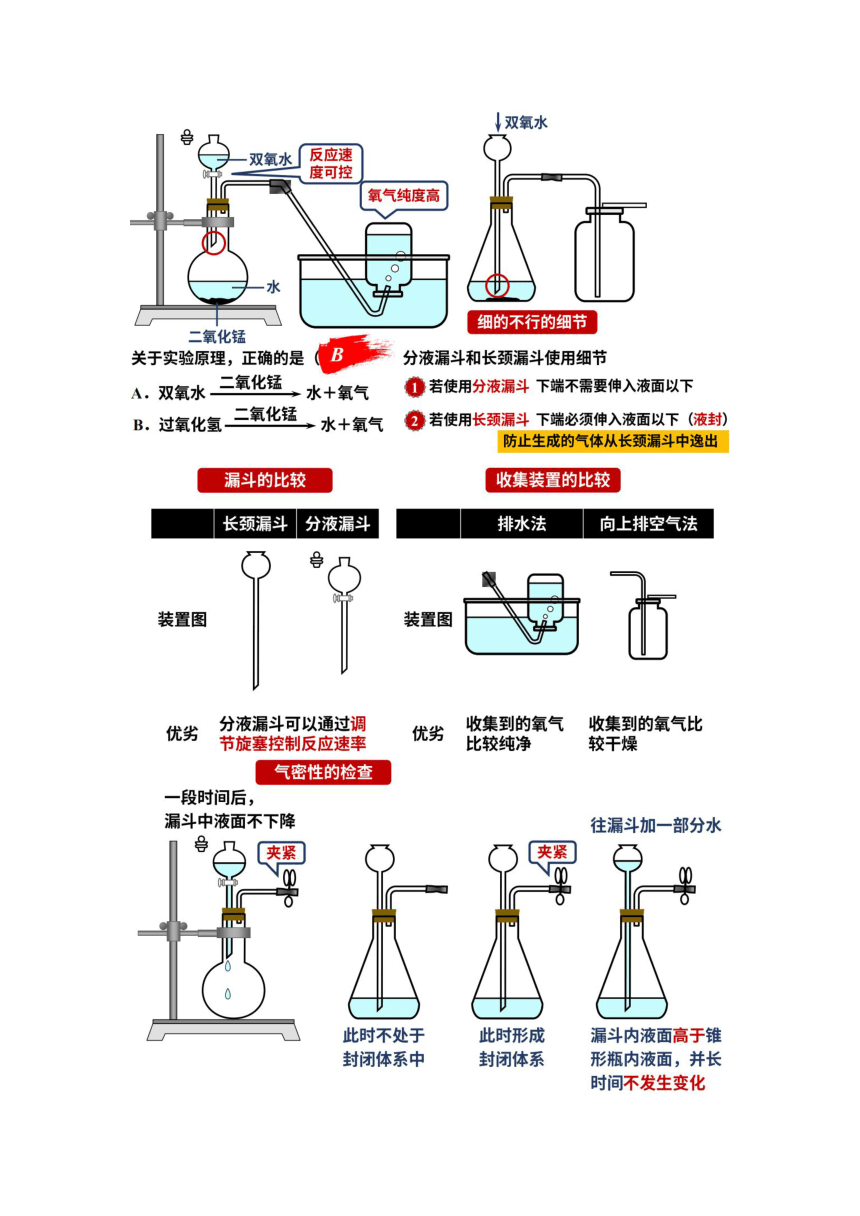
↓双氧水
双氧水「反应速
度可控
氧气纯度高
细的不行的细节
氧化锰
关于实验原理,正确的是(B
分液漏斗和长颈漏斗使用细节
A.双氧水一二氧化锰
水+氧气O若使用分液漏斗下端不需要伸入液面以下
B.过氧化氢二三氧化猛,水十氧气色若使用长颈漏斗下端必须伸入液面以下(液封)
防止生成的气体从长颈漏斗中逸出
漏斗的比较
收集装置的比较
长颈漏斗分液漏
向上排空气
装置图
装置图
优劣分液漏斗可以通过调优劣收集到的氧气收集到的氧气比
气密性的检查
段时间后,
漏斗中液面不下降
往漏斗加一部分水
矿男
此时不处于
此时形成漏斗内液面高于锥
封闭体系中
封闭体系形瓶内液面,并长
时间不发生变化
氧气的工业制法
实验原理
空气中不同种类气体
(主要为氮气和氧气)沸点不同
气体制取装置
发生装置收集装置
发生装置收集装置
向上排空气法向下排空气法
密度比空气大密度比空气小
固体加热型
排水法
固液不需加热型排空气法
排水法
对气体要求:气体不溶于水,不与水反应
优点:收集的气体纯度高,直观判断是否收集满
对气体要求:无毒无污染;不与空气反应;密度与空气有差距
非空气
优点:仪器简单、操作方便;可以制取干燥气体
气体收集装置变形唯一目标:「排水法:把水排出,气体留下
排空气法:把空气排出,气体留下
进气管可长可短
进气管可长可短
排水管需长
排水管需短
P空气
长进短出
p短进长出「排气法收集
Psp空气在它该在的地方!
短进长出
勿,长进短出
到
高锰酸钾制取氧气
实验原理
高锰酸钾二热锰酸钾+二氧化锰十氯气‘文字表达式
2KMnO4
K,MnO4
+
Mno2+O2
实验步骤
①查如何检查装置气密性?
装
品平铺试管底部防止粉末堵塞导管
增大药品受热面积
棉花
便于气体排出
伸入少许
有气泡从管口逸出放手后导管末端回流并
形成一段稳定的水柱
④点通防止试管受热不均
∏管口略向下倾斜防止水蒸气冷凝
炸裂
后回流至试管底
部,引起炸裂
点先预热再定点加热
6收
⑥离熄
当气泡连续均匀冒出后再收集
防止气体收集不纯
先将导管撤离再熄灭火
防止水槽中的水倒吸入
试管,导致试管炸裂
收集完的气体,盖上毛玻璃片正放
例题
阿鳖用高锰酸钾制氧气时,试管炸裂了,造成试管炸裂
①没有给试管均匀预热②2试管口没有略微向下傾斜
试管怎么就炸裂了呢
③忘了在试管口加一团棉花④加热时试管与灯芯接触根本原因:受热不均和爆炸
⑤收集完氧气,先撤酒精灯
①没有给试管均匀预热
②2加热时试管与灯芯接触
③3收集完氧气,先撤酒精灯
④试管口没有略微向下倾斜
试管外壁潮湿
⑤高锰酸钾中混有可燃物
氟酸钾制取氧气
实验原理
氯酸钾二化氯化钾+氯气
Mno
2K03=天
2KC|+30
加快氧气生成速率
二氧化锰
(O2)g
∥氯酸钾一二北→氯化钾十氧气
加MnO2生成氧气质量不变
妹有棉花
不加MnO
时间
KCiO3
KCI
Mno
变改变反应速率
物理性
催化剂」特点
质可变
不变{本身化学性质不变
反应中起催化作用
质量不变
时间/min
过氧化氢制取氧气
实验原理
过氧化氯二氧化气水+氧气
2H2o2=2H2o+02↑
↓双氧水
双氧水「反应速
度可控
氧气纯度高
细的不行的细节
氧化锰
关于实验原理,正确的是(B
分液漏斗和长颈漏斗使用细节
A.双氧水一二氧化锰
水+氧气O若使用分液漏斗下端不需要伸入液面以下
B.过氧化氢二三氧化猛,水十氧气色若使用长颈漏斗下端必须伸入液面以下(液封)
防止生成的气体从长颈漏斗中逸出
漏斗的比较
收集装置的比较
长颈漏斗分液漏
向上排空气
装置图
装置图
优劣分液漏斗可以通过调优劣收集到的氧气收集到的氧气比
气密性的检查
段时间后,
漏斗中液面不下降
往漏斗加一部分水
矿男
此时不处于
此时形成漏斗内液面高于锥
封闭体系中
封闭体系形瓶内液面,并长
时间不发生变化
氧气的工业制法
实验原理
空气中不同种类气体
(主要为氮气和氧气)沸点不同
气体制取装置
发生装置收集装置
发生装置收集装置
向上排空气法向下排空气法
密度比空气大密度比空气小
固体加热型
排水法
固液不需加热型排空气法
排水法
对气体要求:气体不溶于水,不与水反应
优点:收集的气体纯度高,直观判断是否收集满
对气体要求:无毒无污染;不与空气反应;密度与空气有差距
非空气
优点:仪器简单、操作方便;可以制取干燥气体
气体收集装置变形唯一目标:「排水法:把水排出,气体留下
排空气法:把空气排出,气体留下
进气管可长可短
进气管可长可短
排水管需长
排水管需短
P空气
长进短出
p
Psp空气在它该在的地方!
短进长出
勿,长进短出
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
