浙教版科学八年级下册周末一练第九周 第2章空气与生命单元检测
文档属性
| 名称 | 浙教版科学八年级下册周末一练第九周 第2章空气与生命单元检测 |
|
|
| 格式 | zip | ||
| 文件大小 | 338.3KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2012-04-30 00:00:00 | ||
图片预览


文档简介
浙教版科学八年级下册周末一练
第九周 第2章空气与生命单元检测
一、选择题(每小题2分,共40分)
1.空气中含量较多且性质比较活泼的气体是 ( )
A.氮气 B.氧气 C.二氧化碳 D.水蒸气
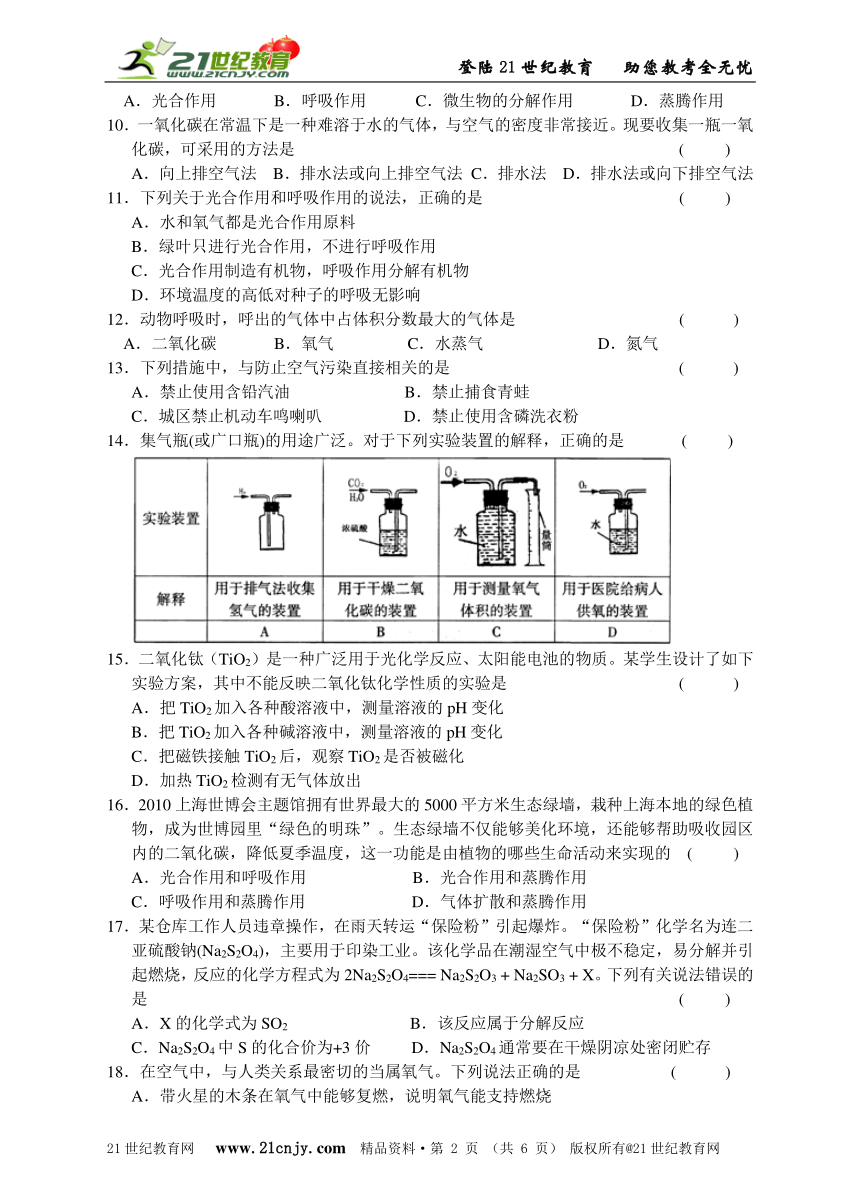
2.下列各图所示的实验操作中,正确的是 ( )
3.下列关于O2和CO2的“自述”中,属于物理性质的是 ( )
4.下列属于化合反应的正确化学方程式是 ( )
A.2H2O 2H2↑+O2↑ B.4P + 5O2 燃烧 2P2O5
C.Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O D.CO2 + H2O === H2CO3
5.下图表示物质A()与B()在一定条件下反应生成C( )的微观不意图(和表示两种质子数不同的原子)。下列说法正确的是 ( )
A.该反应在反应前后其原子种类没有发生变化,但原子数目减少
B.A、B、C三种物质在分类上均属于化合物
C.该反应的化学方程式中,A、B、C的化学计量数之比为2:l:2
D.该反应属于复分解反应
6.最近,科学家研发出一种廉价的合成氨技术,在常温常压下便能合成氨,其化学反应方程式为N2+3H2 2NH3。该化学反应属于 ( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
7.对下列反应的判断:①2KMnO4 加 热 K2MnO4 + MnO2 + O2↑是分解反应;②CO2 + H2O === H2CO3是化合反应;③4P + 5O2 点 燃 2P2O5是氧化反应。其中正确的是 ( )
A.只有① B.只有①② C.只有①③ D.①②③
8.某同学欲鉴别分别装在三个集气瓶中的氧气、氮气、空气,请你帮他确定一个最简便的方法 ( )
A.分别倒人少量的澄清石灰水 B.分别测量它们的密度
C.分别测量它们的溶解度 D.分别伸人燃烧的木条
9.下列与自然界的碳循环没有直接关系的是 ( )
A.光合作用 B.呼吸作用 C.微生物的分解作用 D.蒸腾作用
10.一氧化碳在常温下是一种难溶于水的气体,与空气的密度非常接近。现要收集一瓶一氧化碳,可采用的方法是 ( )
A.向上排空气法 B.排水法或向上排空气法 C.排水法 D.排水法或向下排空气法
11.下列关于光合作用和呼吸作用的说法,正确的是 ( )
A.水和氧气都是光合作用原料
B.绿叶只进行光合作用,不进行呼吸作用
C.光合作用制造有机物,呼吸作用分解有机物
D.环境温度的高低对种子的呼吸无影响
12.动物呼吸时,呼出的气体中占体积分数最大的气体是 ( )
A.二氧化碳 B.氧气 C.水蒸气 D.氮气
13.下列措施中,与防止空气污染直接相关的是 ( )
A.禁止使用含铅汽油 B.禁止捕食青蛙
C.城区禁止机动车鸣喇叭 D.禁止使用含磷洗衣粉
14.集气瓶(或广口瓶)的用途广泛。对于下列实验装置的解释,正确的是 ( )
15.二氧化钛(TiO2)是一种广泛用于光化学反应、太阳能电池的物质。某学生设计了如下实验方案,其中不能反映二氧化钛化学性质的实验是 ( )
A.把TiO2加入各种酸溶液中,测量溶液的pH变化
B.把TiO2加入各种碱溶液中,测量溶液的pH变化
C.把磁铁接触TiO2后,观察TiO2是否被磁化
D.加热TiO2检测有无气体放出
16.2010上海世博会主题馆拥有世界最大的5000平方米生态绿墙,栽种上海本地的绿色植物,成为世博园里“绿色的明珠”。生态绿墙不仅能够美化环境,还能够帮助吸收园区内的二氧化碳,降低夏季温度,这一功能是由植物的哪些生命活动来实现的 ( )
A.光合作用和呼吸作用 B.光合作用和蒸腾作用
C.呼吸作用和蒸腾作用 D.气体扩散和蒸腾作用
17.某仓库工作人员违章操作,在雨天转运“保险粉”引起爆炸。“保险粉”化学名为连二亚硫酸钠(Na2S2O4),主要用于印染工业。该化学品在潮湿空气中极不稳定,易分解并引起燃烧,反应的化学方程式为2Na2S2O4=== Na2S2O3 + Na2SO3 + X。下列有关说法错误的是 ( )
A.X的化学式为SO2 B.该反应属于分解反应
C.Na2S2O4中S的化合价为+3价 D.Na2S2O4通常要在干燥阴凉处密闭贮存
18.在空气中,与人类关系最密切的当属氧气。下列说法正确的是 ( )
A.带火星的木条在氧气中能够复燃,说明氧气能支持燃烧
B.铁丝在空气中剧烈燃烧.火星四射,说明氧气具有可燃性
C.氧气的化学性质非常活泼,能与所有的物质发生化学反应
D.用高锰酸钾制取氧气的反应中,锰元素、氧元素的化合价都没有变化
19.研究物质的变化时可使用具有放射性的18O作为“示踪原子”。科学家希尔和尼尔研究证明,光合作用的通式更合理地表达为: 6CO2 + 12H2O ?? C6H12O6 + 6H2O + 618O2
??? 在光照充分的环境里,将一种植物——黑藻放入含有“示踪原子”18O的水中,一段时间后分析“示踪原子”,最有可能是 ( )
A.在植物体周围的空气中发现 B.在植物体内的葡萄糖(C6H12O6)中发现
C.在植物体内的淀粉和蛋白质中发现 D.无法确定示踪原子在什么地方出现
20.鱼苗在长途运输中,通常将鱼苗养在相对密闭的容器内,加入某种药品,使容器内满足下列条件才能保持鱼苗的存活:充足的氧气、及时除去鱼苗呼出的CO2水的pH调节在8左右,碱性不能太强。现有以下四种物质供选择:双氧水、过氧化钙(CaO2) .过氧化钠(Na2O2)、氯酸钾。它们的有关化学性质如下:
(1) 2H2O===2H2O+O2↑ (2)2Na2O2+2H2O==4NaOH十O2↑
(3)2Na2 O2+2CO2== 2Na2CO3+O2↑ (4)2CaO2+2H2O== 2Ca(OH)2+O2↑
(5)2CaO2+2CO2 ==2CaCO3↓+O2↑ (6) KC1O3不与H2 O、CO2反应
在鱼苗长途运输中你认为最适合加入的物质是 ( )
A.双氧水 B.过氧化钙 C.过氧化钠 D.氯酸钾
二、填空题(每空2分,共30分)
21.写出下列物质变化过程的化学方程式,并在(2)题后的括号内写上反应类型。
⑴细铁丝在纯氧中燃烧: ;
⑵实验室用过氧化氢溶液和二氧化锰制取氧气: ( );
⑶二氧化碳使澄清石灰水变浑浊: 。
22.铁生锈是一种 氧化反应,铁在氧气中燃烧是一种 氧化反应,自燃是由而引起的自发燃烧,白磷可以在空气中发生自燃,生成白色固体P2O5,该反应的化学方程式为 。
23.碱石灰是由氢氧化钠和生石灰组成的,实验时常用来吸收二氧化碳和水。在实验室中还可以用它和无水醋酸钠反应来制取某种气体,反应的化学方程式为:
CH3COONa+NaOH X↑+Na2CO3
⑴请写出X的化学式为 。
⑵根据物质分类,碱石灰属于 (选填 “单质”、“化合物”或“混合物”)。
24.实验室关于液溴贮藏时,经常在液溴上方放一层水,如图所示,请回答:
⑴液溴上方放少量水的目的是 。
⑵分析图中信息,可得出液溴的物理性质有 。
25.右图是自然界碳循环简图.请回答:
(1)植物光合作用时,二氧化碳和水在光的作用下生成葡萄糖(C6H12O6)和氧气.其化学方程式为 。
(2)人类降低空气中二氧化碳含量的研究有两个方向:一个是减少二氧化碳的排放,另一个是 。
(3)二氧化碳是导致温室效应的主要气体.但也是一种宝贵的碳氧资源。在高温高压下以CO2和NH3为原料合成尿素[CO(NH2)2],同时有水生成。这是固定和利用二氧化碳的成功范例。请写出反应的化学方程式 。
三、实验探究题(每空2分,共18分)
26.通过一个学期的化学学习.你已经掌握了实验室制取气体的有关规律.右边是老师提供的一些实验装置。请结合右图回答问题:
(1)写出图中标号的仪器名称a ;b 。
(2)写出实验室用A装置制取氧气的化学方程式 。
(3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。小芳同学加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应的发生装置是 ,收集装置是 。(填字母编号)
27.某同学看到装有薯片的包装袋总是鼓鼓的,里面充有气体。他进行了如下探究:
⑴他提出的问题是 。
⑵其他同学一致认为该实验方案是不合理的,正确的实验方案是:将收集的该气体 ,观察现象。
28.小科很爱动脑筋,在实验中,他认为装置D可以代替装置A、B、C收集气体,欲收集具备下面性质的气体,应如何使用装置D?
(1)收集比空气密度大的气体:进气口为(填“a” 或“b”,下同) ;
(2)收集难溶于水的气体:试剂瓶中应装满水,进气口为 。
四、分析计算题(每小题6分,共12分)
反应前
鸡蛋壳的质量
16克
装置和稀盐酸的总质量
220克
反应后
装置及其内容物的总质量
231.6克
29.鸡蛋壳的主要成分是碳酸钙.为测定鸡蛋壳中的碳酸钙含量。某同学将鸡蛋壳洗净、充分干燥并捣碎,将鸡蛋壳置于如图所示的锥形瓶中,打开分液漏斗的活塞,使其充分反应,直到不再产生气泡为止(假设装置中的稀盐酸足量,鸡蛋壳中的其他物质不与稀盐酸反应)。实验数据记录如右表:
编号
1
2
3
4
加水的质量(g)
10
10
10
10
剩余固体的质量(g)
7.25
4.05
m
3
请计算该鸡蛋壳中碳酸钙的质量分数。
30.在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气。某科学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出。加水的质量与剩余固体的质量见表:(MnO2是不溶于水的固体粉末)。试求:
(1)表中m值为 。 (2)所制得氧气的质量。
参考答案
一.选择题(每小题2分,40分)
题号
1
2
3
4
5
6
7
8
9
10
答案
B
C
B
D
C
B
D
D
D
C
题号
11
12
13
14
15
16
17
18
19
20
答案
C
D
A
C
C
B
C
A
A
B
二、填空题(每空2分,共30分)
21.(1) 3Fe + 2O2 点 燃 Fe3O4
(2)2H2O2MnO2 2H2O +O2↑ 分解反应
(3) Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O
22.缓慢 剧烈 缓慢氧化 4P + 5O2 点 燃 2P2O5
23.(1)CH4 (2)混合物
24.(1)液封(防止液溴与空气接触、隔绝空气) (2)液溴不易溶于水,液溴的密度比水大
25.(1) 6 CO2 +6H2O C6H12 O6 +6O2
(2)增加空气中的CO2的消耗,如植树造林
(3)CO2 + 2NH3高温 高压CO(NH2)2 + H2O
三、实验探究题(每空2分,共18分)
26.(1)分液漏斗 试管
(2) 2H2O2MnO2 2H2O +O2↑
(3)B E
27.(1)袋内是什么气体(合理即可)
(2)通入澄清石灰水
28.(1)a (2)b
四、分析计算题(每小题6分,共12分)
29.解:mCO2=16克+220克-231.6克=4.4克
设该鸡蛋壳中碳酸钙的质量为x
CaCO3 + 2HCl=== CaCl2 + H2O + CO2↑
100 44
x 4.4克
CaCO3%=
答:该鸡蛋壳中碳酸钙的质量分数为62.5%
30.(1)3
(2)方法一:
设所制得氧气的质量为x
mKClO3=15.25克-3克=12.25克
2KClO3 2KCl + 3O2↑
245 96
12.25克 x
方法二:m残余物=7.25克+(7.25克-4.05克)=10.45克
M氧气=15.25克-10.45克=4.8克
答:所制得氧气的质量为4.8克。
第九周 第2章空气与生命单元检测
一、选择题(每小题2分,共40分)
1.空气中含量较多且性质比较活泼的气体是 ( )
A.氮气 B.氧气 C.二氧化碳 D.水蒸气
2.下列各图所示的实验操作中,正确的是 ( )
3.下列关于O2和CO2的“自述”中,属于物理性质的是 ( )
4.下列属于化合反应的正确化学方程式是 ( )
A.2H2O 2H2↑+O2↑ B.4P + 5O2 燃烧 2P2O5
C.Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O D.CO2 + H2O === H2CO3
5.下图表示物质A()与B()在一定条件下反应生成C( )的微观不意图(和表示两种质子数不同的原子)。下列说法正确的是 ( )
A.该反应在反应前后其原子种类没有发生变化,但原子数目减少
B.A、B、C三种物质在分类上均属于化合物
C.该反应的化学方程式中,A、B、C的化学计量数之比为2:l:2
D.该反应属于复分解反应
6.最近,科学家研发出一种廉价的合成氨技术,在常温常压下便能合成氨,其化学反应方程式为N2+3H2 2NH3。该化学反应属于 ( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
7.对下列反应的判断:①2KMnO4 加 热 K2MnO4 + MnO2 + O2↑是分解反应;②CO2 + H2O === H2CO3是化合反应;③4P + 5O2 点 燃 2P2O5是氧化反应。其中正确的是 ( )
A.只有① B.只有①② C.只有①③ D.①②③
8.某同学欲鉴别分别装在三个集气瓶中的氧气、氮气、空气,请你帮他确定一个最简便的方法 ( )
A.分别倒人少量的澄清石灰水 B.分别测量它们的密度
C.分别测量它们的溶解度 D.分别伸人燃烧的木条
9.下列与自然界的碳循环没有直接关系的是 ( )
A.光合作用 B.呼吸作用 C.微生物的分解作用 D.蒸腾作用
10.一氧化碳在常温下是一种难溶于水的气体,与空气的密度非常接近。现要收集一瓶一氧化碳,可采用的方法是 ( )
A.向上排空气法 B.排水法或向上排空气法 C.排水法 D.排水法或向下排空气法
11.下列关于光合作用和呼吸作用的说法,正确的是 ( )
A.水和氧气都是光合作用原料
B.绿叶只进行光合作用,不进行呼吸作用
C.光合作用制造有机物,呼吸作用分解有机物
D.环境温度的高低对种子的呼吸无影响
12.动物呼吸时,呼出的气体中占体积分数最大的气体是 ( )
A.二氧化碳 B.氧气 C.水蒸气 D.氮气
13.下列措施中,与防止空气污染直接相关的是 ( )
A.禁止使用含铅汽油 B.禁止捕食青蛙
C.城区禁止机动车鸣喇叭 D.禁止使用含磷洗衣粉
14.集气瓶(或广口瓶)的用途广泛。对于下列实验装置的解释,正确的是 ( )
15.二氧化钛(TiO2)是一种广泛用于光化学反应、太阳能电池的物质。某学生设计了如下实验方案,其中不能反映二氧化钛化学性质的实验是 ( )
A.把TiO2加入各种酸溶液中,测量溶液的pH变化
B.把TiO2加入各种碱溶液中,测量溶液的pH变化
C.把磁铁接触TiO2后,观察TiO2是否被磁化
D.加热TiO2检测有无气体放出
16.2010上海世博会主题馆拥有世界最大的5000平方米生态绿墙,栽种上海本地的绿色植物,成为世博园里“绿色的明珠”。生态绿墙不仅能够美化环境,还能够帮助吸收园区内的二氧化碳,降低夏季温度,这一功能是由植物的哪些生命活动来实现的 ( )
A.光合作用和呼吸作用 B.光合作用和蒸腾作用
C.呼吸作用和蒸腾作用 D.气体扩散和蒸腾作用
17.某仓库工作人员违章操作,在雨天转运“保险粉”引起爆炸。“保险粉”化学名为连二亚硫酸钠(Na2S2O4),主要用于印染工业。该化学品在潮湿空气中极不稳定,易分解并引起燃烧,反应的化学方程式为2Na2S2O4=== Na2S2O3 + Na2SO3 + X。下列有关说法错误的是 ( )
A.X的化学式为SO2 B.该反应属于分解反应
C.Na2S2O4中S的化合价为+3价 D.Na2S2O4通常要在干燥阴凉处密闭贮存
18.在空气中,与人类关系最密切的当属氧气。下列说法正确的是 ( )
A.带火星的木条在氧气中能够复燃,说明氧气能支持燃烧
B.铁丝在空气中剧烈燃烧.火星四射,说明氧气具有可燃性
C.氧气的化学性质非常活泼,能与所有的物质发生化学反应
D.用高锰酸钾制取氧气的反应中,锰元素、氧元素的化合价都没有变化
19.研究物质的变化时可使用具有放射性的18O作为“示踪原子”。科学家希尔和尼尔研究证明,光合作用的通式更合理地表达为: 6CO2 + 12H2O ?? C6H12O6 + 6H2O + 618O2
??? 在光照充分的环境里,将一种植物——黑藻放入含有“示踪原子”18O的水中,一段时间后分析“示踪原子”,最有可能是 ( )
A.在植物体周围的空气中发现 B.在植物体内的葡萄糖(C6H12O6)中发现
C.在植物体内的淀粉和蛋白质中发现 D.无法确定示踪原子在什么地方出现
20.鱼苗在长途运输中,通常将鱼苗养在相对密闭的容器内,加入某种药品,使容器内满足下列条件才能保持鱼苗的存活:充足的氧气、及时除去鱼苗呼出的CO2水的pH调节在8左右,碱性不能太强。现有以下四种物质供选择:双氧水、过氧化钙(CaO2) .过氧化钠(Na2O2)、氯酸钾。它们的有关化学性质如下:
(1) 2H2O===2H2O+O2↑ (2)2Na2O2+2H2O==4NaOH十O2↑
(3)2Na2 O2+2CO2== 2Na2CO3+O2↑ (4)2CaO2+2H2O== 2Ca(OH)2+O2↑
(5)2CaO2+2CO2 ==2CaCO3↓+O2↑ (6) KC1O3不与H2 O、CO2反应
在鱼苗长途运输中你认为最适合加入的物质是 ( )
A.双氧水 B.过氧化钙 C.过氧化钠 D.氯酸钾
二、填空题(每空2分,共30分)
21.写出下列物质变化过程的化学方程式,并在(2)题后的括号内写上反应类型。
⑴细铁丝在纯氧中燃烧: ;
⑵实验室用过氧化氢溶液和二氧化锰制取氧气: ( );
⑶二氧化碳使澄清石灰水变浑浊: 。
22.铁生锈是一种 氧化反应,铁在氧气中燃烧是一种 氧化反应,自燃是由而引起的自发燃烧,白磷可以在空气中发生自燃,生成白色固体P2O5,该反应的化学方程式为 。
23.碱石灰是由氢氧化钠和生石灰组成的,实验时常用来吸收二氧化碳和水。在实验室中还可以用它和无水醋酸钠反应来制取某种气体,反应的化学方程式为:
CH3COONa+NaOH X↑+Na2CO3
⑴请写出X的化学式为 。
⑵根据物质分类,碱石灰属于 (选填 “单质”、“化合物”或“混合物”)。
24.实验室关于液溴贮藏时,经常在液溴上方放一层水,如图所示,请回答:
⑴液溴上方放少量水的目的是 。
⑵分析图中信息,可得出液溴的物理性质有 。
25.右图是自然界碳循环简图.请回答:
(1)植物光合作用时,二氧化碳和水在光的作用下生成葡萄糖(C6H12O6)和氧气.其化学方程式为 。
(2)人类降低空气中二氧化碳含量的研究有两个方向:一个是减少二氧化碳的排放,另一个是 。
(3)二氧化碳是导致温室效应的主要气体.但也是一种宝贵的碳氧资源。在高温高压下以CO2和NH3为原料合成尿素[CO(NH2)2],同时有水生成。这是固定和利用二氧化碳的成功范例。请写出反应的化学方程式 。
三、实验探究题(每空2分,共18分)
26.通过一个学期的化学学习.你已经掌握了实验室制取气体的有关规律.右边是老师提供的一些实验装置。请结合右图回答问题:
(1)写出图中标号的仪器名称a ;b 。
(2)写出实验室用A装置制取氧气的化学方程式 。
(3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。小芳同学加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应的发生装置是 ,收集装置是 。(填字母编号)
27.某同学看到装有薯片的包装袋总是鼓鼓的,里面充有气体。他进行了如下探究:
⑴他提出的问题是 。
⑵其他同学一致认为该实验方案是不合理的,正确的实验方案是:将收集的该气体 ,观察现象。
28.小科很爱动脑筋,在实验中,他认为装置D可以代替装置A、B、C收集气体,欲收集具备下面性质的气体,应如何使用装置D?
(1)收集比空气密度大的气体:进气口为(填“a” 或“b”,下同) ;
(2)收集难溶于水的气体:试剂瓶中应装满水,进气口为 。
四、分析计算题(每小题6分,共12分)
反应前
鸡蛋壳的质量
16克
装置和稀盐酸的总质量
220克
反应后
装置及其内容物的总质量
231.6克
29.鸡蛋壳的主要成分是碳酸钙.为测定鸡蛋壳中的碳酸钙含量。某同学将鸡蛋壳洗净、充分干燥并捣碎,将鸡蛋壳置于如图所示的锥形瓶中,打开分液漏斗的活塞,使其充分反应,直到不再产生气泡为止(假设装置中的稀盐酸足量,鸡蛋壳中的其他物质不与稀盐酸反应)。实验数据记录如右表:
编号
1
2
3
4
加水的质量(g)
10
10
10
10
剩余固体的质量(g)
7.25
4.05
m
3
请计算该鸡蛋壳中碳酸钙的质量分数。
30.在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气。某科学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出。加水的质量与剩余固体的质量见表:(MnO2是不溶于水的固体粉末)。试求:
(1)表中m值为 。 (2)所制得氧气的质量。
参考答案
一.选择题(每小题2分,40分)
题号
1
2
3
4
5
6
7
8
9
10
答案
B
C
B
D
C
B
D
D
D
C
题号
11
12
13
14
15
16
17
18
19
20
答案
C
D
A
C
C
B
C
A
A
B
二、填空题(每空2分,共30分)
21.(1) 3Fe + 2O2 点 燃 Fe3O4
(2)2H2O2MnO2 2H2O +O2↑ 分解反应
(3) Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O
22.缓慢 剧烈 缓慢氧化 4P + 5O2 点 燃 2P2O5
23.(1)CH4 (2)混合物
24.(1)液封(防止液溴与空气接触、隔绝空气) (2)液溴不易溶于水,液溴的密度比水大
25.(1) 6 CO2 +6H2O C6H12 O6 +6O2
(2)增加空气中的CO2的消耗,如植树造林
(3)CO2 + 2NH3高温 高压CO(NH2)2 + H2O
三、实验探究题(每空2分,共18分)
26.(1)分液漏斗 试管
(2) 2H2O2MnO2 2H2O +O2↑
(3)B E
27.(1)袋内是什么气体(合理即可)
(2)通入澄清石灰水
28.(1)a (2)b
四、分析计算题(每小题6分,共12分)
29.解:mCO2=16克+220克-231.6克=4.4克
设该鸡蛋壳中碳酸钙的质量为x
CaCO3 + 2HCl=== CaCl2 + H2O + CO2↑
100 44
x 4.4克
CaCO3%=
答:该鸡蛋壳中碳酸钙的质量分数为62.5%
30.(1)3
(2)方法一:
设所制得氧气的质量为x
mKClO3=15.25克-3克=12.25克
2KClO3 2KCl + 3O2↑
245 96
12.25克 x
方法二:m残余物=7.25克+(7.25克-4.05克)=10.45克
M氧气=15.25克-10.45克=4.8克
答:所制得氧气的质量为4.8克。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
